脂蛋白(a)与心血管疾病风险关系及临床管理的专家科学建议
2022-01-06北京心脏学会
北京心脏学会
动脉粥样硬化性心血管疾病(ASCVD)居全球心血管疾病(CVD)首位,并成为当今全球人类死亡的首要原因[1]。血脂异常是ASCVD 发生、发展的核心机制,并列为可纠正危险因素。 众所周知,低密度脂蛋白胆固醇(LDL-C)作为重要的血脂指标,视为ASCVD 血脂干预的首要靶标已为人们所熟知。但随机对照研究和真实世界研究表明,将LDL-C 水平控制在当今指南的理想范围内仍存在心血管事件(CVE)剩余风险[2];且系列研究发现,尚存新的血脂指标与剩余风险相关,脂蛋白(a) [Lp(a)]便是近年来证据较多且备受关注的血脂干预潜在新靶点之一。
事实上,Lp(a)约于60 年前即被人类发现并为之命名[3]。随后的小样本临床观察性研究提示血浆Lp(a)水平升高可能与CVD 特别是冠心病(CAD)相关,但直到2009 年孟德尔随机研究结果提示,Lp(a)与心肌梗死(MI)风险升高具有相关性[4],Lp(a)的意义才得到重视。近年来,基于Lp(a)的病理生理学[5]、流行病学[6]、孟德尔随机[4]、全基因组分析[7]、随机对照临床研究的事后分析[8]、特殊人群如家族性高胆固醇血症(FH)[9]和荟萃分析[10]等多维度的研究结果,趋同性地发现Lp(a)极可能是独立于LDL-C 以外ASCVD 的致病性危险因素,再次激发了学界对Lp(a)的关注。
现有证据强烈提示,高Lp(a)水平能预测更高的CVE 风险,在一级预防人群亦或已使用他汀类药物或前蛋白转化酶枯草溶菌素9 (PCSK9)抑制剂的二级预防人群中均体现了高度一致性[10]。然而,人类对于Lp(a)的综合认识尚存在一定的困惑。因此,新近多个国家和地区的指南均对Lp(a) 导致CVD 风险增加的切点、检测人群和干预策略进行了相应推荐,但不同国家指南的推荐有所不同。我国现有的CVD 防治指南中关于Lp(a)的描述与推荐尚缺乏全面而系统的建议与指导。据此,本专家组综合全球有关Lp(a)的现有认知,结合中国人群的研究数据,系统概述Lp(a)的相关知识,并提出关于中国人群Lp(a)的管理要点供临床实践参考。
1 Lp(a)的结构与流行病学特点
Lp(a)由低密度脂蛋白(LDL)样颗粒和载脂蛋白a [Apo(a)]组成,两者以二硫键共价结合[11]。电镜下Lp(a)呈圆球型,直径约21 nm,密度约1.05~1.10 g/ml。Lp(a)结构 (图1) 包括[12]:LDL 样颗粒约含有30%~46%的胆固醇及载脂蛋白B100(ApoB100)和氧化磷脂(OxPL)。Apo(a)是一种高度糖化的亲水蛋白质,占Lp(a)总量的25%~40%。Lp(a)具有显著的多态性,源于Apo(a)肽链长度不一。Apo(a)有10 个同源的kringle Ⅳ(K Ⅳ)结构域,K Ⅳ第2 个结构域中的相似环饼从2~40 个拷贝数不等,其他均只有一个拷贝数,从而决定了Lp(a)的分子量大小及血浆Lp(a)水平在不同个体间存在较大差异。此外,Apo(a) 的多态性还取决于其糖化程度。

图1 Lp(a)组成结构示意图:LDL(包括ApoB100) 颗粒、载脂蛋白a 和OxPL
Lp(a)与LDL 不同,不能由极低密度脂蛋白(VLDL)转化而来,也不能转化为其他脂蛋白,是一类独立的由肝脏合成的脂蛋白。Apo(a)几乎完全在肝细胞内合成,但Lp(a)的组装地点尚未明确,可能在肝细胞内、狄氏间隙或血液循环中完成。组装过程包括Apo(a) 对接至 LDL,然后在Apo(a) 的K Ⅳ9和LDL 的ApoB 之间形成共价二硫键,此过程是否可逆尚不清楚。血浆中Lp(a)的清除途径和机制也了解甚少,目前认为大部分Lp(a)在肝脏中经LDL受体清除,小部分也可经肾脏和其他途径清除[11]。但也有研究显示清道夫受体B 型Ⅰ (SR-B Ⅰ)、纤溶酶原受体、LDL 受体相关蛋白1 (LDLRP1)及其他受体也参与了肝脏介导的Lp(a) 清除。
与呈正态分布的LDL-C 水平不同,Lp(a)水平在人群中呈偏态分布,多数个体(约70%)的Lp(a)水平<30 mg/dl。美国大型流行病学调查研究共纳入531 144 例门诊患者,Lp(a)数据采集自全科医生对一般门诊患者的CVD 风险筛查。结果显示,Lp(a)水平呈偏态分布,均值为(34.0±40.0) mg/dl,中位数为17 mg/dl,其中Lp(a) >30 mg/dl 的比例为35%,Lp(a) >50 mg/dl为24%[13]。同样,中国人群的Lp(a)水平也呈偏态分布,第80 百分位值相对更低。来自江苏省健康体检人群9 238 例数据提示,Lp(a)中位数为5.6 mg/dl,其中女性群体第80 百分位值20.7 mg/dl,男性群体第80百分位值14.5 mg/dl[14]。
此外,由于Apo(a)的多态性,导致Lp(a)血浆水平存在一定的种族和地域性差异。一项研究比较中国人、白种人和非裔美国人的Lp(a)水平,结果显示,中国人、白种人和非裔美国人血浆Lp(a)水平的中位数分别为8.0 mg/dl、9.0 mg/dl 和33 mg/dl。中国人和白种人血浆Lp(a)水平的总体分布仅存在细微的统计学差异,但均与非裔美国人存在显著差异(P<0.001)[15]。关于Lp(a)水平升高人群的地域性分布情况,2018 年美国国立健康研究所(NHLBI)工作组指出[16],全球范围内超过14 亿人Lp(a)水平高于50 mg/dl。其中,非洲约为30%,欧洲、北美及大洋洲约20%,南美约15%,除南亚约25%外,其他亚洲地区约为10%,提示不同人种之间Lp(a)水平的分布存在一定差异。
专家意见1
Lp(a)呈偏态分布,且有地域和种族差异,中国人群的Lp(a)水平总体较其他国家与地区低。
2 基因组学研究与引起Lp(a) 升高的因素
基因研究进一步验证了Lp(a)与CAD 和缺血性脑卒中的相关性。孟德尔随机化研究提示,Lp(a)与CAD 具有相关性[4]。PROCARDIS 队列数据与全基因组关联分析显示,两个LPA 单核苷酸(SNP)(SNPrs10455872和rs3798220)多态性与Lp(a)水平升高和CAD 风险增加密切相关[7]。一项GWAS 研究纳入1 403 例接受经皮冠状动脉介入(PCI)治疗的CAD 患者研究结果提示,LPA 基因中的rs7770628、rs73596816和rs6926458,SLC22A2基 因 中 的rs144217738与Lp(a)水平独立相关。其中LPA 基因中的rs7770628和rs73596816与CAD 严重程度显著相关[17]。另一项全基因组研究纳入三个队列的欧洲白种人群包含6 942 例主动脉瓣钙化和3 795 例二尖瓣环钙化患者。基因检测结果发现,LPA 位点 SNP(rs10455872) 对主动脉瓣钙化具有显著意义(每个等位基因的OR=2.05,P=9×10-10),且在其他队列中得到证实[18]。
血浆Lp(a)水平虽主要取决于LPA 基因多态性(约70%~90%),但目前已知部分非遗传因素也会影响其水平。在慢性肾脏病的患者中,血清Lp(a)水平随着肾小球滤过率的下降而升高,推测与大型异构体分解代谢减少有关。此外,血清Lp(a)水平在大多数肝病患者中降低,在显性甲状腺功能减退患者中升高。血清Lp(a)水平与年龄或性别并不一致,但绝经后妇女的激素替代治疗可显著降低血清Lp(a)水平[11]。因此,寻找可能引起Lp(a)水平升高的继发因素也具有一定的临床意义。
专家意见2
Lp(a)水平主要受基因控制,部分非遗传因素也会影响其水平。
3 Lp(a)可能的致病机制
目前,Lp(a)的生理病理功能尚未完全阐明。从生物学结构理解,Lp(a)可能具有比LDL-C 更强的致ASCVD 特性。 首先,Lp(a)可以渗透到动脉内膜,结合细胞外基质的成分,促进巨噬细胞浸润和平滑肌细胞增殖[19]。在动脉粥样硬化病变进展的各个阶段,均可见Lp(a)在斑块中富集。其次,Lp(a)具有独特的Apo(a)结构,而Apo(a)正是Lp(a)发挥其独特致ASCVD 作用的关键之一[20]。由于Apo(a)与纤溶酶原的结构相似,推测Lp(a)可能的生理作用之一是参与伤口早期的修复。组织损伤时,细胞外基质暴露于血液中,Lp(a)被“捕获”至伤口处,促进炎症细胞(如单核细胞)向血管内皮下内流,通过抑制纤溶而发挥促血栓的作用[12]。 最后,在所有脂蛋白中,Lp(a)是OxPL 的最大结合力载体,OxPL具有重要的促炎、促动脉粥样硬化作用,通过诱导内皮细胞、平滑肌细胞和巨噬细胞的促炎信号激活,引发动脉壁的炎症反应[21]。因此,与LDL-C相比,Lp(a)同时还可通过促血栓形成和促炎作用加剧ASCVD 的发生与发展。最后,新近的研究提示Lp(a)尚参与瓣膜与血管钙化的发生与发展,其确切机制尚待阐明。
4 Lp(a)水平与CVD 的关系
基因组学、流行病学、孟德尔随机研究均显示,Lp(a) 升高是多种CVD 包括 CAD、缺血性脑卒中和钙化性主动脉瓣狭窄(CAVS)等疾病的独立危险因素。
CAD:多项观察性研究和基因组学研究证实,Lp(a)升高是CAD 的独立危险因素。AIM-HIGH 试验提示,LDL-C 达到65.2 mg/dl(1.62 mmol/L)及Lp(a) >50 mg/dl 的患者与LDL-C 水平相似,但与Lp(a)水平低于50 mg/dl 的患者相比,主要不良心血管事件(MACE)的风险高90%[12]。一项荟萃分析纳入7 项29 069 例经他汀治疗的随机对照研究,结果显示,即使经他汀治疗后LDL-C 较低情况下,Lp(a)升高仍会增加CVD 风险[10]。哥本哈根城市心脏研究分析7 524 例受试者资料,随访时间长达16 年,结果提示,Lp(a)升高与CVD 风险增加呈显著正相关[6]。中国人群的大型观察性研究表明,Lp(a)是CAD 的独立危险因素。基于CCSSSCC 数据库进行回顾性分析,纳入1 522 例首次急性心肌梗死(AMI)患者和1 691 例无CAD 的对照者,结果提示,与对照组(LDL-C <2.6 mmol/L,Lp(a)第1 个五分位数)相比,Lp(a)升高的AMI 的OR 值根据Lp(a)五分位分层后,首次AMI 的OR 值分别为1.51、1.84、1.86 和2.66[22]。
缺血性脑卒中:无论从观察性研究还是遗传学的分析,Lp(a)均与缺血性脑卒中的高风险相关。哥本哈根一般人口研究及城市心脏研究纳入6 万余例缺血性脑卒中患者,结果显示,高水平的Lp(a)与缺血性脑卒中的风险增加相关。与Lp(a)水平 <10 mg/dl 的个体相比,Lp(a) >93 mg/dl 缺血性脑卒中的多变量校正后危险比为1.60。观察性分析中,对于Lp(a)水平>50 mg/dl,缺血性脑卒中的年龄和性别调整后的危险比为1.20[23]。源于上海市嘉定区于2010 年3 月至8 月随机抽取10 375 名40 岁以上居民入组队列数据,8 500 名受试者纳入最终分析。结果发现,血清Lp(a) 水平与脑卒中发生风险之间存在显著相关性(P<0.05)。多变量校正分析显示,与低Lp(a)水平组相比,高Lp(a)水平组发生脑卒中的HR 为1.34[24]。孟德尔随机化研究近40 万余人数据显示Lp(a)与大动脉闭塞性脑卒中正相关,与小血管闭塞性脑卒中负相关[25]。
CAVS:Lp(a) 也 是CAVS 的 危 险 因 素[26]。ASTRONOMER 研究在220 例轻-中度主动脉狭窄(AS)患者中测量Lp(a),平均随访3.5 年。结果提示,Lp(a)水平的升高与CAVS 疾病进展相关[27]。有研究以Lp(a)=58.5 mg/dl 为切点,发现在Lp(a)升高的患者中,AS 的进展更快,提示Lp(a)可预测轻-中度CAVS 的进展[28]。另外, Liu 及团队测定652 例中国CAVS 患者的血清Lp(a)水平,平均随访(3.16± 2.74)年,临床终点定义为主动脉瓣置换术(AVR)和心脏性死亡的复合终点。结果发现,与Lp(a)第一分位和第二分位组患者相比,Lp(a)第三分位组患者严重动脉粥样硬化比例更高(46.2% vs. 33.9%,P=0.005)。此外,Lp(a) 的最高分位数是严重动脉粥样硬化的独立预测因子(OR =1.78,95% CI:1.18~2.66,P=0.006)。然而,Lp(a)的三分位与临床事件之间没有显著相关性[29]。
值得指出的是,Lp(a)升高也是FH 和2 型糖尿病患者发生CVD 的危险增强因素。SAFEHEART 注册研究纳入2 404 例既往无ASCVD 的FH 患者,中位随访5.5 年,分析显示Lp(a)水平是FH 患者发生ASCVD 的独立预测因素之一[9]。另一项中国研究连续纳入393 例杂合子家族性高胆固醇血症(HeFH)患者,根据基线Lp(a)三分位分组(<19.7、19.8~51.9及≥52.0 mg/dl),平均随访时长为36.5 个月。分析发现,高Lp(a)组无事件存活率显著降低(P=0.004);经对数转化的基线Lp(a)值每增加1 个单位,心血管事件风险约增加一倍[30]。同时,Lp(a)升高与糖尿病前期和糖尿病患者ASCVD 事件增加显著相关[31-32]。 中国医学科学院阜外医院研究团队从2011 年4 月至2017 年3 月,连续纳入2 284 例既往有CVE 病史的2 型糖尿病患者,平均随访3 年。研究结果提示,当CVD 患者合并2 型糖尿病时,Lp(a)带来的相关心血管风险可能会进一步升高[33]。此外,尚有散在报道提示,Lp(a)升高与动脉血管钙化、静脉血栓性疾病相关,但尚需更进一步积累证据。
专家意见3
Lp(a)升高是CAD、缺血性脑卒中和CAVS的独立危险因素。
5 Lp(a)检测人群
个体血浆Lp(a)水平主要由遗传基因决定,因此在一生中保持相对稳定。(1)对一般人群的检测建议,本科学建议中关于至少应测量一次Lp(a)的建议与2019 年欧洲血脂异常指南一致[34]:“在每个成年人的一生中至少应考虑检测一次,以确定那些具有非常高的遗传性Lp(a)水平增高的人群[>180 mg/dl(>430 nmol/L)],这类人群可能具有与HeFH 相同的ASCVD 的终生风险”。(2) 基于第四部分“Lp(a)水平与ASCVD 的关系“的相关证据,本科学建议推荐在以下目标人群进行Lp(a)筛查:
①ASCVD 极高危人群[定义见2019 年欧洲心脏病学会(ESC)/欧洲动脉粥样硬化学会(EAS)指南]。PRIME 研究显示,Lp(a)为冠心病预测因子[35]。另外,Lp(a)水平与复发性CVE 风险独立相关,Lp(a)测定有助于及时干预,从而降低事件复发风险[36]。
②早发 ASCVD 家族史 (男性<55 岁,女性<65 岁) 。 早发ASCVD 家族史的个体CVD 风险增加[37],同时伴有更高的动脉粥样硬化负荷[38]。而Lp(a)的升高会进一步加重这种风险,因而有必要对早发ASCVD 家族史的患者进行Lp(a)的筛查。
③直系亲属血清Lp(a)水平升高>90 mg/dl(>200 nmol/L)。Lp(a)水平属于显性遗传,Lp(a)水平的检测对于Lp(a)>90 mg/dl (>200 nmol/L)病例的直系家庭成员可能具有CVD 风险评估的参考价值。
④FH 和其他遗传性血脂异常。Lp(a)水平是FH 患者发生ASCVD 的独立预测因素之一[9],其为ASCVD 的一个重要“促进”剂,也是FH 家族中Lp(a)级联筛查的一个指标。既往研究结果表明,在ASCVD 的FH 患者中监测Lp(a)是有益的。
⑤CAVS 患者。Lp(a)是CAVS 的潜在危险因素[26],由于Lp(a)升高的患者可能需要更早的干预,了解患者Lp(a)水平可以指导临床治疗和随访间隔时间。
专家意见4
建议在以下人群中检测血清Lp(a)水平:(1)ASCVD 极高危人群;(2)有早发 ASCVD 家族史(男性<55 岁,女性<65 岁);(3)直系亲属血清Lp(a)水平升高>90 mg/dl(200 nmol/L);(4)FH或其他遗传性血脂异常;(5)CAVS 患者。
6 Lp(a) 的风险增高切点
尽管有大量研究提示,Lp(a)水平升高与CAD、脑卒中和 CAVS 相关,并导致MACE 风险升高。遗憾的是,迄今有关Lp(a)增加CVD 风险增高的切点值尚无定论。事实上,Lp(a)的风险增高切点的确定需要大样本人群的系列研究数据。正如前面所述,不同种族Lp(a)浓度存在差异,因此不同种族的Lp(a)风险增高切点亦不同。根据现有研究和荟萃分析,专家组认为Lp(a)导致动脉粥样血栓形成的风险增高的Lp(a) 水平约在30~50 mg/dl (75~125 nmol/L)之间。
此外,关于CVD 风险增高的Lp(a) 切点值,不同国家指南和共识中的推荐也非一致。2016 年加拿大心血管学会(CCS)血脂异常管理指南[39],Lp(a) >30 mg/dl 界定为CVD 风险增高的危险因素,指南建议对Lp(a)进行测量以指导决策,特别是在有早发CAD 家族史的中度风险人群且不符合高风险标准的年轻患者中。2016 中国成人血脂异常防治指南建议[40],在排除各种应激性升高的情况下,Lp(a)升高被认为是ASCVD 的独立危险因素,Lp(a)通常以30 mg/dl 为风险增高切点,高于此水平者患CAD 的危险性明显增高。欧洲动脉粥样硬化学会(EAS)血脂异常管理指南和国家脂质协会(NLA)Lp(a) 在 临 床 实 践 中 的 应 用 共 识 均 提 出[34,41],Lp(a)>50 mg/dl 存在风险显著增加。在治疗管理LDL-C 后,建议对具有中-高度CVD 风险的患者进行Lp(a)筛查。
汇总在中国人群中探究Lp(a) 风险切点的研究[14,24,36,42-44](表1),多数研究结果显示,Lp(a) >30 mg/dl 是CAD 和缺血性脑卒中的独立预测因子。因此,本科学建议基于中国人群的现有数据,倾向于支持将30 mg/dl 作为中国人群Lp(a)的风险增高切点,即Lp(a)超过30 mg/dl 心血管疾病风险可能性增加。
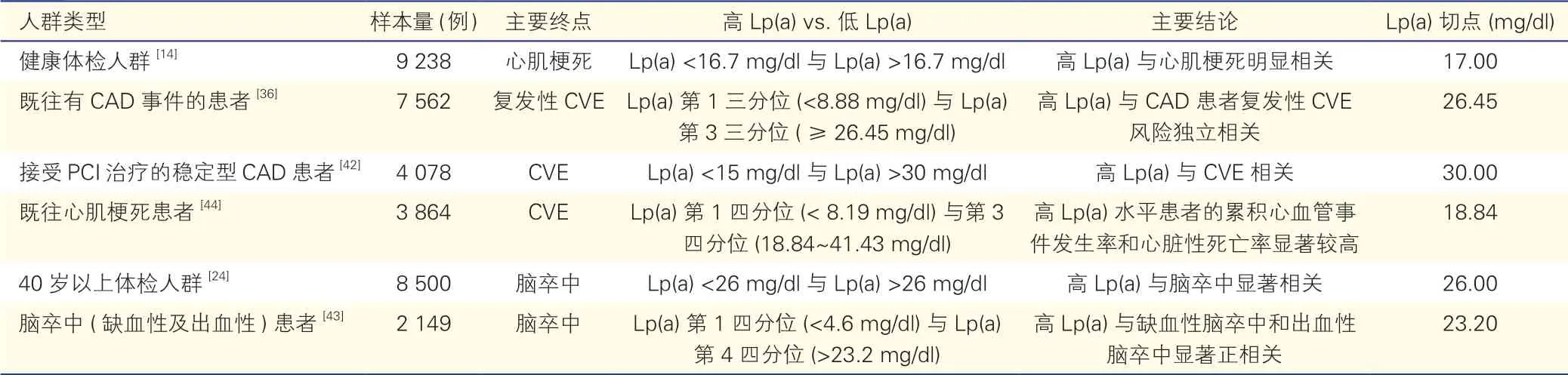
表1 中国人群中探究Lp(a)风险切点的研究
专家意见5
关于Lp(a)致心血管风险增高的切点值,不同国家指南和共识中的推荐并不一致,较多使用的是50 mg/dl。根据中国人群的现有研究数据,本建议倾向于支持将30 mg/dl 作为风险增加的切点。
7 Lp(a)的实验室检测
Lp(a)是ASCVD 的独立风险因素,但缺乏Lp(a)实验室检测的标准化,使得Lp(a)与CVD 的相关性缺乏准确的评估。众多研究表明,Lp(a)的检测不仅有助于对因Lp(a)升高而导致的动脉粥样硬化及血栓风险的患者进行可靠的诊断和分类,其检测方法标准化对于提高CVD 的风险评估准确率,改善患者预后具有重要意义[45]。
Lp(a)的定量检测方法有超速离心法、凝胶电泳法和免疫法,目前临床实验室常用方法主要为双抗体夹心酶联免疫分析法(Sandwich ELISA)和免疫比浊法(包括散射比浊法和透射比浊法),检测抗体包括抗Apo(a)和ApoB100 的单或多克隆抗体。Lp(a)实验室检测目前面临的挑战:(1)Lp(a)的大小、密度呈现非均一性即 Lp(a)的多态性,这是Lp(a)测定标准化的最大困难[45-46]。由于Apo(a)中KⅣ2 的拷贝数存在差异,而免疫检测使用的是单一KⅣ2 拷贝数Apo(a)校准品,当样品中Apo(a)分子小于校准物中Apo(a)浓度时,测定结果易被低估;而当样品中的Apo(a)分子大于校准物中Apo(a)分子时,测定结果易被高估。不同Apo(a)异构体的免疫反应性不同,而产生测量误差;(2)不同检测方法未采用国际公认的统一标准物质和溯源程序为校准品定值;(3)Lp(a)临床常用实验室检测分为“质量浓度法(mg/dl)”和“摩尔浓度法(nmol/L)”。“质量浓度法”局限性在于,由于原始标准物质来源于纯化的天然Lp(a),而大多数个体携带两种不同的Lp(a)颗粒(父源、母源),这两种颗粒的Apo(a)大小、Lp(a)质量和组分上存在差异,因此无法实现对含有差异蛋白、脂质与糖类等组分的Lp(a)进行准确定量。而表示Lp(a)颗粒浓度的“摩尔浓度法”可消除这一误差;因此,国际临床化学和检验医学联合会(IFCC)提倡采用“mmol/L”作为Lp(a)报告单位。需要注意的是,“摩尔浓度法”也应选择识别KⅣ2 可变区以外且不与纤溶酶原交叉的特异性单克隆抗体,以减少结果变异。
Lp(a)实验室检测的标准化已被提到临床实践的重要位置。目前美国华盛顿大学西北脂类研究实验室(NWLRL)使用抗Apo(a) K Ⅳ9 型表面决定簇a-40 和K Ⅳ8 型表面决定簇a1-1 单克隆抗体建立的Sandwich ELISA 方法被认为是现有“金标准”检测法,该方法不受Apo(a)不均一性的影响。2003 年WHO 确定IFCC 的 SRM-2B 为Lp(a)免疫测定二级参考物质(WHO/IFCC SRM-2B),其可溯源到上述一级参考物质,Lp (a)含量为(107.1±8.6) nmol/L。目前多个国家指南推荐临床实验室检测方法应溯源至WHO/IFCC SRM-2B[11,41]。需要注意的是,不可使用固定值作为“质量浓度法(mg/dl)”和“摩尔浓度法(nmol/L)”检测值间的转换因子。但目前临床实践和研究中大多仍然使用“质量浓度法(mg/dl)”单位,因此,在无法完全统一为“摩尔浓度法(nmol/L)”之前,使用质量单位和摩尔单位均可,但溯源至SRM-2B 的摩尔单位法最佳。
专家意见6
Lp(a)的实验室检测:(1)应使用一种对Apo(a)异构体不敏感且与纤溶酶原无交叉的单克隆抗体;(2)选择校准品可溯源到WHO/IFCC SRM-2B 参考物质的检测体系;(3)基于现状,报告结果以质量单位或者摩尔单位表示均可(摩尔单位最佳),但质量单位不推荐固定转换因子直接转换为摩尔单位。
8 Lp(a) 水平升高患者的综合管理
迄今尚缺乏有效降低Lp(a)水平的治疗方法,也无药物获批专用于降低Lp(a)。对于Lp(a)升高的患者,管理原则是:(1)降低总体ASCVD 风险;(2)控制伴随的其他有临床意义的血脂异常。
生活方式干预:尽管健康饮食、运动等生活方式治疗无法直接降低Lp(a)水平,但是通过积极控制其他可改变的心血管危险因素,对于降低Lp(a)升高患者的总体心血管风险仍然具有十分重要的意义。在EPIC-Norfolk 研究中, Lp(a)升高(>50 mg/dl)且心血管健康评分最高(包括体重指数、健康饮食、体力活动、吸烟状况、血压、糖尿病和胆固醇水平)的参与者,与心血管健康评分最低的参与者相比,CVD 风险大大降低(校正后HR=0.33,95% CI:0.17~0.63,P=0.001),提示对Lp(a)升高的患者,保持更积极的健康生活方式的重要意义[47]。对于Lp(a)升高的ASCVD 低危人群,推荐加强生活方式干预。对于ASCVD 中危及以上的人群,除了加强生活方式干预,需要强化降LDL-C 治疗。
他汀治疗:积极降低LDL-C 也可以降低Lp(a)升高带来的CVD 风险[48-49]。2018 年美国心脏病学会(ACC)/美国心脏协会(AHA)血脂指南建议[50]:在ASCVD 中危人群(10 年ASCVD 风险7.5%~19.9%)的一级预防中,Lp(a) ≥50 mg/dl 或≥100 nmol/L 是一个合理的风险增强因子,考虑启动中强度或高强度他汀类药物治疗是必要的。需要注意的是,即使将LDL-C 控制在较低的水平,高Lp(a)患者的MACE 风险仍然显著高于低Lp(a)的患者[51-52],提示Lp(a)水平升高带来的风险并不会因他汀等降脂药物的使用和LDL-C 的达标而完全消除。因此,部分Lp(a)升高的患者可能会从更积极的他汀降LDL-C 治疗中获益。值得指出的是,近期也有研究显示他汀治疗可轻度升高血Lp(a)水平,升高后的Lp(a)差值是否会进一步增加CVE 风险尚需要进一步研究。
烟酸:烟酸可使Lp(a)水平降低约23%[53]。但是,AIM-HIGH 研究和HPS2-THRIVE 研究显示,在他汀的基础上加用烟酸并未降低ASCVD 高危患者包括Lp(a)升高患者的CVE 风险,反而会增加严重不良事件的风险[54-55]。究其原因是否因AIM-HIGH 和HPS2-THRIVE 入选人群中Lp(a)水平并非显著升高有关尚不清楚。因此,专家组认为烟酸降低Lp(a)的临床意义有待进一步探讨。
PCSK9 抑制剂:现有数据显示,PCSK9 单克隆抗体及靶向PCSK9 信使RNA 的小干扰RNA(siRNA)类药物可使Lp(a)水平降低约20%~30%[56-58]。在FOURIER 研究和ODYSSEY 研究的探索性分析中,Lp(a)较高的受试者CVE 风险降幅似乎更大[59-61],但考虑到这部分患者本身的绝对风险也更高,上述探索性研究中显示的更多获益是否完全源于Lp(a)的降低尚需要进一步研究证实。LDL-C 和Lp(a)的降低在上述获益中分别发挥了多大程度的贡献也并不完全清楚。值得指出的是,孟德尔随机研究提示,需要有一个较大的Lp(a)绝对值降幅(65.7~100.0 mg/dl),才可能产生临床上有意义的心血管风险降低[62-63]。据此,专家组建议,对于Lp(a) ≥30 mg/dl的ASCVD 患者,应尽可能使用中等强度的最大可耐受他汀和依折麦布联合治疗使其LDL-C 达标包括加用PCSK9 抑制剂。但考虑药物经济学和现有证据,不论何种人群,本科学建议不推荐以降Lp(a)为首要目的应用PCSK9 抑制剂。
脂蛋白置换术(LA):LA 后即刻对于Lp(a)的降幅可达50%~70%,一周内的平均降幅约为30%~35%[64]。HEART UK 指南建议,对于已经采取最大程度降脂治疗仍有进行性CAD 恶化,且Lp(a)>60 mg/dl,LDL-C 仍在125 mg/dl(3.3 mmol/L)以上的患者,可考虑LA 治疗[65]。自2008 年以来,德国已有约1 500 例Lp(a)水平超过60 mg/dl 的患者接受了LA 治疗[66]。现有两项研究显示,定期接受LA的患者CVD 风险明显降低。相比治疗前,LA 治疗后CVE 平均减少约80%[67-68]。此外,近期的一项随机对照试验显示,对于Lp(a) >60 mg/dl 的难治性心绞痛患者,LA 可显著改善心肌灌注,减轻动脉粥样硬化负荷,并降低心绞痛的发生率[69]。鉴于LA 的局限性(操作复杂、有一定并发症风险,费效比低和国内能开展LA 的中心非常有限等),本专家组不推荐LA 常规用于治疗Lp(a)增高的患者。借鉴国外经验与建议,对于经充分降LDL-C 治疗以及控制其他危险因素后, Lp(a) ≥60 mg/dl,且动脉粥样硬化进行性加重的患者可采用“医生与患者沟通决策模式”酌情选用LA 治疗。
研发中的新型药物: RNA 靶向疗法对目标mRNA 具有高度选择性和亲和力,迄今已被成功应用于多个疾病领域[70],也是目前最有希望获批用于降低Lp(a)的干预措施。靶向肝脏LPARNA的反义寡核苷酸可以通过沉默Apo(a) 基因的表达,阻断Apo(a)蛋白的合成,从而有效降低循环中Lp(a)水平。在已完成的一期和二期临床试验中,反义寡核苷酸疗法对Lp(a)的降幅高达80%以上,且安全耐受性良好[71-72]。目前,旨在评估反义寡核苷酸疗法对Lp(a)升高患者心血管结局影响的全球三期临床试验(HORIZON,NCT04023552)正在进行中,该研究是全球首个针对Lp(a)升高患者的心血管终点研究。此外,针对LPARNA 的siRNA疗法也处于早期开发阶段(NCT03626662)。因此,降Lp(a)的 RNA 靶向治疗能否降低CVE 风险值得期待。
其他药物:有文献报道,血浆胆固醇酯转移蛋白(CETP)抑制剂,米泊美生(Mipomersen)可降血Lp(a)水平达20%~30%[73-74],但缺乏证据支持其治疗的心血管获益。
专家意见7
Lp(a)升高的患者管理的核心原则是降低总体ASCVD 风险,包括控制伴随的各种有临床意义的血脂异常。
9 中国人群Lp(a) 研究的未来方向
近年来,尽管人类对Lp(a)的了解和认识已经取得了长足的进步,但是关于Lp(a)仍然还有很多未知,如Lp(a)的确切合成和代谢途径、病理生理学特征等,都有待于今后的基础研究逐步探索。鉴于Lp(a)水平的分布在全球不同种族人群中存在显著差异,我国仍有待开展高水平、大样本、覆盖不同区域人群的流行病学研究,以进一步明确中国人群的Lp(a)水平分布情况,以及更适合中国人群的Lp(a)风险增加切点。如何提高Lp(a)检测的准确性,并逐步推动Lp(a)检测的标准化,也是未来的研究重点。尽快在随机对照临床试验中检验可以特异性降低Lp(a)的干预措施,如反义寡核苷酸类药物和LA,对Lp(a)升高患者CVD 预后的影响。对于一级和二级预防,以及特定的疾病,如FH 和CAVS,都应考虑进行相应的临床干预试验。
专家委员会成员:李建军(中国医学科学院阜外医院),马长生(首都医科大学附属北京安贞医院),赵冬(首都医科大学附属北京安贞医院),严晓伟(北京协和医院),叶平(解放军总医院第二医学中心),陈红(北京大学人民医院),李勇(复旦大学附属华山医院),袁祖贻(西安交通大学第一附属医院),张瑞岩(上海交通大学医学院附属瑞金医院),赵水平(中南大学湘雅二医院),陆国平(复旦大学附属儿科医院),梁春(海军军医大学附属长征医院),董吁钢(中山大学附属第一医院),陈桢玥(上海交通大学医学院附属瑞金医院),彭道泉(中南大学湘雅二医院),唐熠达(北京大学第三医院),汪芳(北京医院),周洲(中国医学科学院阜外医院),孙艺红(中日友好医院),刘静(首都医科大学附属北京安贞医院),郭远林(中国医学科学院阜外医院),袁慧(首都医科大学附属北京安贞医院),吴娜琼(中国医学科学院阜外医院),祝烨(四川大学华西医院)
利益冲突:本专家科学建议中的所有描述仅代表专家意见,无任何利益冲突
