《2021年亚太肝病学会临床实践指南:与免疫抑制治疗相关的HBV再激活》摘译
2022-01-06冬译陈国凤审校
张 珊,纪 冬译,陈国凤审校
1 北京大学三〇二临床医学院, 北京 100039; 2 解放军总医院第五医学中心, 北京 100039
20世纪70年代,HBV再激活(HBV reactivation,HBVr)在HBsAg阳性和HBsAg阴性但抗-HBs阳性的骨髓增生性和淋巴细胞增生性疾病患者中首见报道。20世纪90年代的前瞻性研究表明,近一半的HBsAg阳性恶性淋巴瘤患者在接受细胞毒治疗时,会出现HBVr导致的肝炎。随着后来更积极的免疫抑制治疗(immunosuppressive therapy,IST)(如异体造血干细胞治疗等技术)的应用,HBsAg阳性的血液恶性肿瘤患者由HBVr导致的死亡逐渐成为一个严重的临床问题。因此,建议对接受细胞毒治疗的HBsAg阳性的恶性肿瘤患者进行密切监测。更有效的免疫抑制疗法和靶向单克隆疗法(如利妥昔单抗,一种人/鼠的嵌合抗CD20单克隆抗体)的使用,使得各医学学科取得了进一步的进展,即使在那些已经从过去的HBV感染中恢复——HBsAg阴性但抗-HBc阳性,并且只有敏感的巢式PCR能检测到HBV DNA的患者,也发现了由HBVr引起的致命性暴发性肝衰竭。在21世纪之交,随着强效核苷(酸)类似物(NAs)的出现,随机对照试验显示,在HBsAg阳性和HBsAg阴性但抗-HBs和抗-HBc阳性并接受细胞毒性化疗的患者中,预先使用拉米夫定、恩替卡韦(ETV)和替诺福韦(TDF)对预防HBVr及相关疾病的发病率和死亡率都非常有效。
截至2020年,许多旨在减少HBVr相关肝炎的临床指南已经制定。尽管如此,HBVr相关肝炎导致的慢加急性肝衰竭在HBV感染流行的亚太地区,仍然是主要的健康威胁,这似乎与其他非肝病学科的医护人员不了解相关知识有关。而各种新的免疫抑制剂,如用于治疗各种癌症的酪氨酸激酶抑制剂(tyrosine-kinase inhibitors,TKI)、免疫检查点抑制剂(immune checkpoint inhibitors,ICI)和用于许多自身免疫性疾病的TNF拮抗剂的使用迅速增多,使情况变得更加复杂。最近,在HBV/HCV共感染的患者中,使用直接作用抗病毒药物(DAA)治疗期间和之后也出现了HBVr的相关报告。
阻碍指南成功实施的因素包括:对HBVr的流行缺乏关注,对于简单易行、成本低廉的预防HBVr的措施认识不足。作者的目标是为所有相关的医学学科制定一个实用方便的临床实践指南,这将有助于减少IST治疗对象中与HBVr有关的发病率和死亡率,特别是在HBV流行的亚太地区。
在亚太肝病学会(APASL)指导委员会的倡议下,来自亚太地区21个不同行政区域/国家的专家被邀请组成一个工作小组,制定IST治疗患者的HBVr临床实践指南。该小组不仅包括肝病专家,还包括肿瘤专家、风湿病专家、移植外科专家、肾病专家和介入放射科专家。本指南涉及以下问题:(1)HBVr的定义是什么?(2)谁应该接受筛查?(3)筛查时应做什么?(4)计划接受IST的患者应如何管理和监测?所有建议均按照GRADE系统进行分级。这些建议是在泰国曼谷举行的第30届APASL年会(2021年2月6日)上提出并采纳的。
1 HBVr诱发肝炎的免疫病理学
HBV是一种嗜肝病毒,进入肝细胞后,含有部分双链HBV DNA(dsDNA)的HBV核衣壳进入细胞核,病毒聚合酶将dsDNA修复成全长、共价封闭的环状DNA(cccDNA),成为HBV的核库。逆转录、病毒复制和壳体化在病毒组装、释放或新生的核衣壳再循环进入细胞核之前就发生在细胞质中,以补充cccDNA池。这些低水平的cccDNA在肝细胞中的持续存在,可能是HBV感染清除、HBsAg血清学阴性患者接受强效IST治疗仍长期存在HBVr风险的原因。HBV感染的临床结局高度依赖于病毒特异性宿主免疫反应之间复杂的相互作用,包括HBV特异性的CD8 细胞毒性T淋巴细胞和自然杀伤(NK)细胞/NK-T淋巴细胞反应、细胞因子介导的非细胞溶解反应以及B淋巴细胞介导的体液免疫。与此相一致的是,无论是否出现抗-HBs,HBsAg缺失的HBV感染都需要CD4辅助T淋巴细胞来促进病毒特异性适应性CD8 T淋巴细胞反应和B淋巴细胞抗体的产生。
迄今为止,除了从病原体的作用机制推断外,对HBVr相关肝炎的发生发展和严重程度的关键生物学途径还没有很好的定义。很少有数据将HBV序列变异与HBVr的风险或严重程度联系起来,联系的前提是假定所有的HBV基因型和变异都可能与再激活有关。尽管如此,基于一系列检测、HBV血清学标志物和肝功能测试,已确定HBVr引起肝炎的过程包含两个阶段。初始阶段的特点是病毒复制增强,伴随着病毒抗原在肝脏的表达明显增加。据推测,HBVr的这一初始阶段是由于药物治疗直接或间接抑制了针对HBV的抗病毒免疫反应而发生的,其中B淋巴细胞耗竭疗法和造血干细胞移植(hematopoietic stem cell transplant,HSCT)的风险最高。在实体器官移植中使用IST、传统化疗(包括经动脉化疗栓塞治疗肝细胞癌)以及最近使用的TKI、TNF拮抗剂和蛋白酶体抑制剂治疗各种恶性肿瘤和自身免疫性疾病时也有HBVr的情况出现。HBV基因组内包含类固醇反应元件,延长皮质类固醇治疗与HBVr中-高度相关。也有报道称,对HBV/HCV或HBV/HDV共感染的患者进行HCV或HDV抗病毒治疗,可以间接导致HBVr。这种现象反映了病毒之间的相互作用,即宿主对一种肝炎病毒的免疫反应抑制了另一种病毒的复制—通常HCV或HDV比HBV占优势—对优势病毒的抗病毒治疗导致了免疫途径的继发性下调,使HBV的复制增加。第二阶段发生在停用IST后的免疫重建期间,如通过DAA持续快速抑制HCV,或通过无抗HBV活性的高效抗逆转录病毒治疗持续快速抑制HIV。对明显增强的HBV抗原肝脏表达的免疫反应导致的肝脏损伤,主要表现为肝炎、黄疸型肝炎和暴发性慢加急性肝衰竭。
2 用免疫抑制剂治疗的HBVr的发病率
2.1 HBsAg阳性患者 来自日本和我国香港的数据显示,接受造血干细胞移植的HBsAg阳性患者在没有进行抗病毒预防的情况下,有45%~100%的HBVr风险和15%的肝衰竭风险。亚太地区的荟萃分析显示,在接受含利妥昔单抗治疗的HBsAg阳性淋巴瘤患者中,HBVr的风险>30%。在亚太地区接受化疗的HBsAg阳性乳腺癌患者中,HBVr和HBV相关肝炎的风险分别为22%(14%~41%)和11%(0~21%)。接受含类固醇方案的HBsAg阳性癌症患者的HBVr风险为26%~72%,而接受不含类固醇方案的患者为13%~36%。来自韩国的数据观察到,对于接受经动脉化疗栓塞的HBV相关HCC患者,HBVr的风险为32%(30%~43%),HBV相关肝炎的风险为18%(16%~31%)。基线HBV DNA水平>2000 IU/mL、基线肝硬化和HCC多方法综合治疗均与较高的HBVr风险相关。
2.2 靶向治疗、单克隆抗体、生物制剂 目前,TKI被广泛用于肺癌和慢性骨髓性白血病(CML)的靶向治疗。在我国台湾和韩国的研究中,接受伊马替尼的CML患者的HBVr风险为26%~38.5%。最近一项我国台湾研究观察到在接受表皮生长因子受体抑制剂的非小细胞肺癌患者中,有9.4%的HBVr风险。
目前,ICI已被批准用于治疗各种癌症。来自我国台湾和我国大陆的病例系列研究显示,在HBsAg阳性的癌症患者中,接受ICI治疗的HBVr及其相关肝炎的风险分别为14%(9.1%~17%)和11.7%(9.1%~17%)。尽管病例数较少,有报道称用于自身免疫性疾病(如风湿性疾病和炎症性肠病)的TNFα抑制剂与14%~63%的HBVr风险有关,美国肝病学会关于免疫增强药物治疗期间预防和治疗HBVr的指南也认为抗TNF治疗为中度风险。
改变病情的抗风湿药物(bDMARD/sDMARD)在HBsAg阳性患者中的HBVr风险约为22%(9%~63%)。在接受托珠单抗(一种IL-6受体单克隆抗体)的HBsAg阳性风湿病患者中,已经观察到HBVr、肝炎上升甚至是暴发性肝衰竭的发生。由于抗IL-6类药物正应用于世界上一些地区的COVID-19大流行中,这一领域还需要进一步的研究。
2.3 HBsAg阴性/抗-HBc阳性患者 来自亚太地区的数据观察到,在接受HSCT而没有进行抗病毒预防的HBV临床治愈患者中,有6%~29%的HBVr风险。一项荟萃分析显示,接受含利妥昔单抗治疗的淋巴瘤患者的HBVr风险明显高于接受不含利妥昔单抗治疗的患者(10% vs 4%)。Kusumoto等在3期GOYA和GALLIUM研究中发现,基于奥比努妥珠单抗和利妥昔单抗的免疫化学疗法之间的HBVr风险没有明显差异(P=0.17)。3项研究328例HBV感染临床治愈的实体瘤患者的荟萃分析显示,中位HBVr风险为3%(0.3%~9%)。最近,我国香港的一项研究数据表明,在接受类固醇治疗的孤立抗-HBc血清阳性患者中,一年的HBsAg血清转换率为1.8%。所有皮质类固醇的剂量和持续时间超过7 d的组合都会增加肝炎的风险。
接受TKI或ICI的HBsAg阴性/抗-HBc阳性患者的HBVr风险数据有限。最近一项泰国研究观察到,在123例接受TKI治疗的HBV临床治愈的CML患者中,没有人出现HBVr。
亚太地区有数据显示,TNFα抑制剂和DAMARD的HBVr相关风险约为3.1%(1.1%~5.2%)。最近的一项我国台湾研究报告称,在64例接受托珠单抗的风湿病患者中,有1例(1.6%)出现了HBVr。这些领域仍需要进一步研究。
2.4 HBV和HCV共感染者的HBVr DAA的使用极大地提高了慢性HCV感染的治疗成功率,使HCV在不久的将来有可能被清除。使用DAA成功根除HCV的比率在HCV感染者和HBV/HCV共同感染者之间是相当的。然而,在进行DAA治疗期间和之后,合并感染的患者有发生HBVr的风险,这比基于干扰素治疗的HBVr发生得更早,在临床上更有意义。亚太地区一项研究显示,HBVr的风险为41.1%(14%~100%),HBV相关肝炎的风险为7.1%(0~30%),HBV相关黄疸型肝炎的风险为2.1%(0~10%),死亡率为2%(0~7%)。HBVr的风险与基线HBV DNA水平没有关系。基线检测不到HBV DNA的患者仍有HBVr风险。在最近的一项研究中,基线HBsAg滴度(qHBsAg)与HBVr有关,基线qHBsAg>10 IU/ml的患者1年累积发病率为42.5%,而基线qHBsAg<10 IU/ml的患者为18.5%。
2.5 风险分层
与HBVr相关的关键风险因素有三个:
(1)宿主因素:男性、年龄较大、存在肝硬化、用IST治疗的疾病类型,如骨髓移植或实体器官移植。
(2)HBV病毒学因素:HBsAg血清阳性、基线HBV DNA水平高、HBeAg血清阳性,以及没有抗-HBs的HBV感染或合并感染HCV、HDV或HIV的患者。
(3)IST的类型和程度:在HBsAg阳性者和HBsAg阴性/抗-HBc阳性患者之间存在一个HBVr的风险梯度。HBsAg阳性的患者比抗HBsAg阴性的患者发生HBVr的风险高5~8倍。在HBsAg阳性的患者中,再激活的最佳预测因子已被证明是基线时的HBV DNA水平。HBsAg阴性和抗-HBc阳性的患者发生HBVr风险较低,据报道,接受B淋巴细胞治疗或HSCT的患者风险较高。在HBsAg阴性/抗-HBc阳性个体中,抗-HBs的存在和滴度与对HBVr的保护有关,然而,数据有限,目前没有足够的证据支持在这种情况下使用抗-HBs滴度进行临床决策。根据IST的类型和持续时间以及HBV感染的状况,HBVr的风险被分为低(<1%)、中(1%~10%)、高(>10%)3层(表1)。
3 预先使用NAs的理论依据
在拉米夫定全球注册后不久,在中国淋巴瘤患者中进行了第一项随机对照试验,比较“早期”预防性治疗(在淋巴瘤细胞毒化疗开始前或开始时开始使用拉米夫定)和“延迟”治疗(仅在监测发现HBVr时开始使用拉米夫定)。该方案基于这样的假设:如果在强烈IST的初始阶段能够抑制HBV复制的增强,那么在撤消IST的免疫重建过程中,HBV抗原携带的肝细胞数量作为目标宿主的免疫力,因此肝脏损伤的发生率应该大大降低。这将与“延迟”的方法形成鲜明对比,因为对HBV抗原的肝细胞免疫反应已经开始,事实上,明显增强的HBV复制已经在减弱。与此相呼应,“早期”使用的方法被发现优于“延迟”使用拉米夫定,从而使接受强细胞毒IST治疗的HBsAg阳性淋巴瘤患者的HBVr和肝炎发病率明显降低。同样,在一项针对中国成人HBV非活动携带者和并发IgA肾病(蛋白尿≥3.5 g/d)的前瞻性、开放式队列研究中,发现“早期”使用拉米夫定在预防HBVr及其相关肝炎方面有很好的效果。随后14项研究的系统回顾和荟萃分析显示,HBVr和HBV相关肝炎的相对风险在0~0.21,支持预先使用拉米夫定治疗。没有预先使用拉米夫定治疗的患者中断化疗的比例明显升高。然而,由于拉米夫定的低耐药性屏障,一些患者可能会出现YMDD突变,阻碍了这种预先治疗的有效性。因此,拉米夫定后来被阿德福韦、ETV和TDF等高耐药屏障的NAs所取代。由于长期使用ETV、TDF和最近的丙酚替诺福韦(TAF)具有较高的安全性,在计划接受IST治疗的患者中预先使用其对HBVr进行预防的效用已在随机对照试验中得到验证。
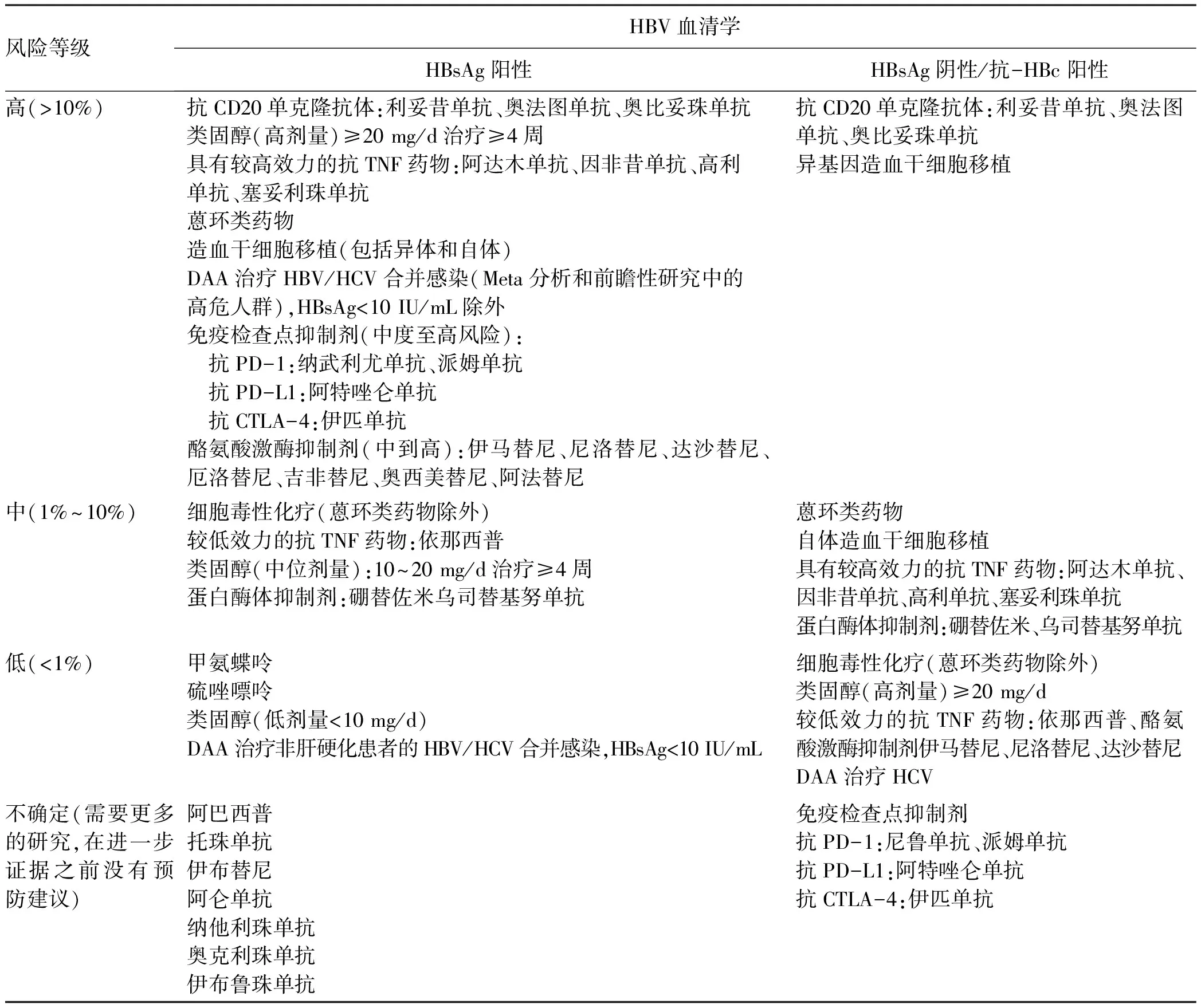
表1 HBsAg阳性、HBsAg阴性/抗-HBc阳性患者HBVr风险分级
4 由肝病专家评估是否终止NAs治疗
所有计划进行IST的患者都应在基线时检测HBsAg、抗-HBs和抗-HBc,并对HBVr的风险进行评估(图1)。对于HBsAg阳性患者,应监测血清HBV DNA,可能还有qHBsAg。目前关于其他生物标志物的数据,如抗-HBs和抗-HBc滴度、HBV核心相关抗原(HBcrAg)、超敏HBsAg评估和HBV RNA,在诊断和监测免疫抑制治疗过程中的HBVr方面,尚无任何额外的实际临床用途。对肝纤维化的评估,无论是有创的还是无创的,都应该在肝病专家的指导下进行。所有HBV治疗指南都建议有显著肝纤维化(F2或更高)的患者应接受NAs治疗,而对于没有显著肝纤维化的患者,可能需要密切监测。因此,使用肝脏纤维化评估对低至中度风险患者的预防性治疗进行分层是一种合理方法。一些国际管理指南已经开发并采用了各种非侵入性评估。瞬时弹性成像的肝脏硬度测量(LSM)得到了最广泛的验证,是预测慢性乙型肝炎患者晚期纤维化或肝硬化(≥F3)的准确可重复的方法。该方法的关键挑战是ALT水平的混杂影响,LSM的下降可能只反映ALT的正常化。因此,在HBVr患者中,LSM应在ALT水平正常后进行评估,以准确诊断纤维化的程度。然而,Jia等一个中国慢性乙型肝炎患者的大队列研究显示,ALT水平达到正常值的5倍并没有明显影响LSM的诊断能力。Li等的研究表明,ALT水平轻度升高的患者在预测F2~F4(6.5kPa vs 6 kPa)和F4(10.2 kPa vs 7.8 kPa)方面,LSM的临界值比ALT水平正常的患者要高。在不考虑ALT水平的情况下使用临界值诊断,LSM对F2~F4的诊断准确度为81%,对F4的诊断准确度为89%。应用以ALT分层的临界值,LSM预测F2~F4的诊断准确度为82%,预测F4的准确度为86%。在不容易获得LSM的地区,基于普通实验室参数的血清模型具有高度适用性的优点,如AST与PLT比率指数(APRI)、Forns指数和Fibrosis-4(FIB-4)评分。
对于HBsAg阳性和HBsAg阴性/抗-HBc阳性的IST患者,如果认为风险较高,应先启动高耐药屏障NAs的治疗。对于中度风险的患者,所有HBsAg阳性和HBsAg阴性/抗-HBc阳性的晚期肝纤维化或肝硬化患者应开始预防性使用高耐药屏障NAs,首选的NAs是ETV、TDF或TAF。对于那些HBsAg阴性/抗-HBc阳性的患者,如果没有晚期肝病或肝硬化,应每3个月监测一次血清ALT。如果监测时发现ALT升高>2×基线,应进行HBsAg和HBV DNA检测,如果两者均为阳性,应开始使用高耐药屏障NAs。对于低危人群,HBsAg阳性和HBsAg阴性/抗-HBc阳性的晚期纤维化或肝硬化患者,应启动预防性NAs。HBsAg阳性和HBsAg阴性/抗-HBc阳性的低风险患者,应每3个月监测一次血清ALT。美国肝病学会、美国胃肠病学会和欧洲肝病学会建议抗病毒治疗应在IST停药后持续应用至少6个月,B淋巴细胞耗竭剂停药后至少12个月。在肝病专家的指导下,本共识小组建议对于没有晚期肝纤维化或肝硬化的HBsAg阳性患者,在开始使用NAs之前,若HBV DNA水平较低(<2000 IU/mL),在IST完成后6个月即考虑终止NAs。对于那些持续HBsAg阴性/抗-HBc阳性的患者,在IST完成后6个月应考虑终止NAs。HBV DNA监测指导下的预防性NAs对于预防这些患者的HBV相关肝炎是有效的。每3个月进行一次密切监测并及时启动NAs可能更具有成本效益。在未来有更可靠的证据后,新的生物标志物,如HBV RNA、HBcrAg,可能有助于决定在IST完成后何时终止NAs。

图1 预防HBVr管理流程
5 与以前的指南比较
《亚洲-太平洋地区乙型肝炎管理临床实践指南:2015年更新版》中,“免疫抑制治疗或化疗前的抗病毒预防措施”被纳入讨论,HBsAg阳性的患者,建议预防性NAs治疗,HBsAg阴性/抗-HBc阳性的患者,需要进一步研究来比较不同预防策略(预防性NAs与监测)的有效性和成本效益。在过去的几年中,有更多的数据可以用来对各种免疫抑制剂的HBVr风险进行更好的分层,即新的生物制剂、靶向治疗、免疫治疗和抗HCV直效抗病毒制剂。本指南对于HBsAg阳性的患者,仍建议及时开始预防性NAs治疗。主要变化在于HBsAg阴性/抗-HBc阳性患者,过去几年不断发展的数据更好地阐明了该类患者的HBVr风险,因此,现在推荐对中度风险和高度风险组的HBsAg阴性/抗-HBc阳性患者进行预防性NAs治疗。此外,对于血清HBV DNA检测不到的HBsAg阴性/抗-HBc阳性的患者,无论抗-HBs状态如何,都应通过LFT(包括或不包括HBV DNA检测)进行仔细随访,并在确认为HBVr后使用NAs治疗。肝纤维化程度也被纳入评估,因为晚期纤维化和肝硬化患者若发生HBVr,其死亡和发病风险更高。此外,还包括使用DAA治疗HBV/HCV共感染者的HBVr的新数据。
6 推荐意见
6.1 HBVr的定义是什么?
6.1.1 HBV再激活
(1)慢性HBV感染恶化(HBsAg阳性)。
·HBV DNA水平较基线水平增加≥2 log。(等级:证据-Ⅱ-2,建议-1)
·在基线时无法检测到HBV DNA的人中检测到>100 IU/mL水平的HBV DNA。(等级:证据-Ⅱ-2,建议-1)
(2)在免疫抑制治疗开始后,既往HBV感染再激活(HBsAg阴性/抗-HBc阳性)。
·HBsAg血清转化,HBsAg阴性转为HBsAg阳性。(等级:证据-Ⅱ-2,建议-1)
·HBsAg阴性时HBV DNA阴性转为HBV DNA阳性。(等级:证据-Ⅱ-2,建议-1)
6.2 谁应该接受筛查?
·所有计划接受免疫抑制治疗的患者都应接受筛查。(等级:证据-Ⅱ-2,建议-1)
6.3 筛查的内容包括什么?
·筛查应包括HBsAg、抗-HBs和抗-HBc。(等级:证据-Ⅱ-2,建议-1)
·对于那些HBsAg阳性的患者,应考虑进行额外的HBV DNA和HBsAg定量检测 (等级:证据-Ⅱ-2,建议-1)
·所有HBsAg阳性和HBsAg阴性/抗-HBc阳性的患者都应该由肝病专家评估肝纤维化的程度。(等级:证据-Ⅲ,建议-2)
6.4 管理
(1)强制性对以下人员及时进行NAs预防性治疗可以拯救生命。
·在高危组中,所有HBsAg阳性或HBsAg阴性/抗-HBc阳性的患者。(等级:证据-I,建议-1)
·在中风险组中,所有HBsAg阳性和抗-HBc阳性的晚期肝纤维化或肝硬化患者。(等级:证据-Ⅱ-2,建议-1)
(2)必须对以下人员实施预防性的NAs。
·在低风险组中,所有HBsAg阳性或HBsAg阴性/抗-HBc阳性的晚期肝病或肝硬化患者。(等级:证据-II-2,建议-1)
(3)首选的NAs包括ETV、TDF和TAF。(等级:证据-I,建议-1)
(4)应在免疫抑制治疗结束后6个月考虑终止NAs。
·HBsAg阳性,没有晚期肝纤维化或肝硬化的患者。(等级:证据-Ⅱ-2,建议-1)
·使用NAs前HBV DNA水平较低(<2000 IU/mL)的HBsAg阳性患者。(等级:证据-Ⅱ-2,建议-1)
·HBsAg阴性抗-HBc阳性患者。(等级:证据-Ⅱ-2,建议-1)
6.5 肝功能检查(ALT、AST、胆红素、白蛋白、球蛋白)应每12周监测一次
·在中度风险组中,HBsAg阴性/抗-HBc阳性、无晚期肝坏死或肝硬化的患者。(等级:证据-Ⅱ-2,建议-1)
·在低风险组中,HBsAg阳性或HBsAg阴性/抗-HBc阳性且无晚期肝坏死或肝硬化的患者。(等级:证据-II-2,建议-2)
·如果ALT>2×基线,监测HBsAg、HBV DNA,并用NAs对HBsAg血清转换和/或HBV DNA进行治疗。(等级:证据-Ⅱ-2,建议-1)
