胆管导管内乳头状黏液性肿瘤的研究现状
2022-01-06何清云吴会超
徐 颖, 唐 加, 何清云, 吴会超
遵义医科大学附属医院 消化内科, 遵义 563000
胆管导管内乳头状黏液性肿瘤(intraductal papillary mucinous neoplasm of the bile tract,IPMN-B)为起源于胆管上皮的一类特殊胆管系统肿瘤,以胆管黏膜上皮乳头样或绒毛样增生、分泌大量黏液导致胆管梗阻、继发胆管广泛性扩张为特征。2000年,Kim等[1]描述了9例分泌大量黏液的胆管肿瘤,并得出其临床、影像学和病理特征与胰腺导管内乳头状黏液性肿瘤(intraductal papillary mucinous neoplasm of the pancreas,IPMN-P)相似。因缺乏统一命名,IPMN-B曾被称为黏蛋白高分泌型肝内胆管肿瘤、黏液性胆管癌、导管扩张性黏液囊腺癌等[2]。直到2008年,Paik等[3]首次提出IPMN-B的概念来总结此类疾病。
IPMN-B是胆管内乳头状肿瘤(intraductal papillary neoplasm of the bile duct,IPNB)的一种亚型,IPNB是指一种具有精细纤维血管核心,以胆管黏膜上皮乳头样或绒毛状增生为特征的罕见肿瘤。2010年,世界卫生组织将IPNB在消化系统肿瘤分类中作为一组独立的疾病列出并对其进行了系统的分类,包括IPNB伴低或中度上皮内瘤变、IPNB伴高级别上皮内瘤变和IPNB伴浸润性癌[4-5],其中28%~37%的IPNB能分泌黏液,即IPMN-B。基于胆管与胰管在组织胚胎学上均发源于胚胎前肠,且这两种疾病具有相同的临床病理特征[6]:(1)肿瘤均发生在导管系统内(宏观上主要表现为导管内生长模式,微观上表现为乳头状增生);(2)均分泌过多黏液;(3)均可能进展为黏液癌,IPMN-B被认为是IPMN-P在胆管的对应物,故将其命名为IPMN-B[7-8]。无黏液分泌的IPNB则称为非黏液性IPNB(IPNB without mucin secretion,IPNB-NM),其临床症状、影像学表现及组织病理学与IPMN-B均有较大差异。由于IPMN-B发病率低,临床表现及影像学均无特异性,术前诊断困难,容易导致临床诊断困难或误诊,近年来,IPMN-B越来越受到业界的关注。本文就IPMN-B进行文献学习,从病因机制、临床表现及诊疗等方面进行综述。
1 IPMN-B的病因和分型
1.1 IPMN-B的病因 IPMN-B的具体病因尚未阐明,目前普遍认为结石、华支睾吸虫以及慢性炎症等导致的长期慢性刺激可能是该病的主要发病原因[9-10]。除此之外,原发性硬化性胆管炎、先天性胆管畸形及加德纳综合征也被认为可能是IPMN-B的高危致病因素。White等[11]认为,p53基因表达异常及 K-ras 基因突变可能是该病发病的关键机制。在我国,IPMN-B主要是由于肝胆管结石反复慢性炎症刺激及胰液反流所致[12]。
1.2 IPMN-B的分型 根据免疫组化上表达黏液核心蛋白(mucin core protein,MUC)的差异,IPMN-B可分为4个亚型(表1)。(1)胰胆管型:柱状细胞含增大深染色的细胞核与中度双染色的细胞质,与胰胆管、肝胆管上皮细胞类似;(2)胃型:由类似胃小弯的柱状上皮细胞组成;(3)肠型:在肠腺瘤及肠腺癌中发现的高柱状细胞及杯状细胞;(4)嗜酸性细胞型:以丰富的嗜酸性细胞质与大圆形细胞核为特征,与IPMN-P组织学类型基本一致[5,13]。其中肠型是最常见的亚型,其次是胰胆管型、胃型和嗜酸细胞型[14]。虽然黏蛋白高分泌是IPMN-P的一个典型和常见特征,但在IPMN-B中分泌黏蛋白更常见于胃和肠型,而不是胰胆管型[15]。根据影像学特点,IPMN-B可分为4个亚型[16](表2)。
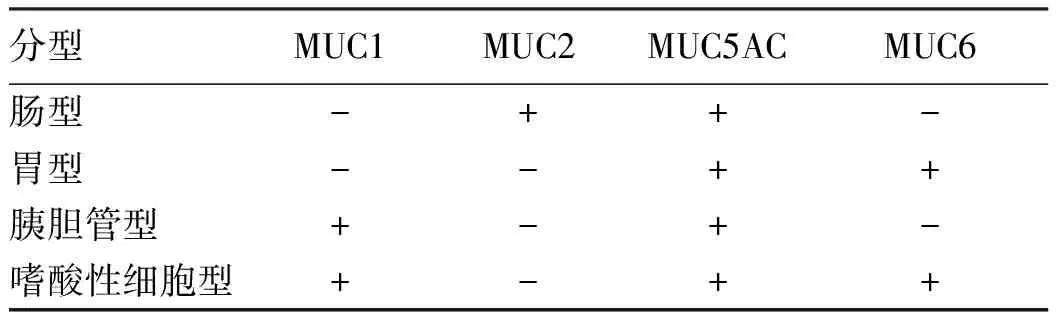
表1 IPMN-B的免疫组化分型

表2 IPMN-B的影像学分型
2 临床表现
IPMN-B的临床表现主要取决于肿瘤发生部位、大小和弥散程度,以及黏液的分泌量和黏稠度。发生于肝内外周胆管的IPMN-B多无明显胆管梗阻症状,而发生于一、二级肝内胆管或肝外胆管的IPMN-B常因胆管内乳头状黏液上皮细胞产生过多黏液,阻碍正常胆汁流经胆管,黏稠的黏液和脱落的肿瘤碎片可导致间歇性部分胆管梗阻,类似于胆管结石[17],引起上腹痛、腹胀、黄疸等无特异性的临床表现。但与胆管结石引起的持续性黄疸不同,因胆管括约肌压力升高后引起十二指肠乳头继发性扩张,可排出黏液使胆管梗阻缓解,故IPMN-B引起的黄疸为波动性。晚期的IPMN-B可发生胆汁性肝硬化,出现腹水、黄疸、脾大及上消化道出血等肝功能失代偿的表现。但有约10%的IPMN-B患者无任何临床症状,而于体检时偶然发现[15,18-19]。
3 实验室检查
主要表现为胆管梗阻后所致的肝功能异常,以血清胆红素、ALP以及GGT升高为主。一项纳入58例IPMN-B的回顾性研究[20]报道,CEA和CA242的检测有助于IPNM-B的良恶性鉴别,也有文献[21]报道CA19-9升高可作为判断黏液性肿瘤恶性程度的指标,但缺乏特异性。急性胆管炎及胆管梗阻也可出现CA19-9的升高,但与胆管癌CA19-9的持续升高不同,胆管炎或胆管梗阻缓解后CA19-9常可回落或出现波动。
4 影像学检查
目前IPMN-B的发现主要是不明原因的肝内外胆管扩张进行手术切除后的偶发病例,术前诊断困难。其典型的影像学表现为胆管内肿块及病灶上下游弥漫胆管扩张,且扩张程度可能与肿瘤的大小及位置并不吻合[22]。目前常用诊断IPMN-B的无创性检查包括超声、CT、MRI、磁共振胰胆管造影(MRCP);有创性检查包括内镜下逆行胰胆管造影(ERCP)、经皮经肝胆道镜(percutaneous transhepatic cholangioscopy,PTCS)、经口胆道镜(peroral cholangioscopy,POCS)、术中胆道镜、肝胆管腔内超声(intraductal ultrasonography,IDUS)。
4.1 超声检查 超声检查因其便捷、无创、经济的优点常作为胆管梗阻及肝脏的首选检查方法。在普通超声检查下IPMN-B典型表现为胆管扩张、胆汁透声差、胆管腔内息肉样病变。当普通超声观察有困难时,可联用超声造影。超声造影可检测到瘤体血流变化,从而鉴别胆管壁息肉及胆管结石。但患者肥胖体型、肠道气体干扰及操作者的经验等因素都可能导致漏诊。
4.2 CT、MRI及MRCP CT及MRI下黏蛋白的密度和信号强度与胆汁相同,使黏蛋白无法检测到,而表现为胆管扩张。同时,这些检测方法也可以检测导管内肿块,但常因黏蛋白过于黏稠影响观察而导致灵敏度不高。其典型表现为胆管扩张、胆管壁上结节或肿块沿胆管黏膜面生长。平扫CT上肿瘤通常表现为低密度病灶(低于肝实质但高于胆汁),增强CT上,与正常肝实质相比,肿瘤在动脉期强化高于门静脉期或延迟期,但肿瘤较小或沿黏膜播散时不宜发现,不典型病灶则可表现为胆管壁增厚或不规则[23-24]。在平扫MRI T1加权成像上,IPMN-B通常表现为低或者等信号,T2上显示为稍高信号(低于胆汁但高于结石),弥散加权成像可更清晰显示IPMN-B且为高信号[10,23,25-26]。T2磁共振成像显示肝内胆管明显“软藤状扩张”被认为是IPMN-B的特征性影像学表现(图1)[20],此外,有报道[27]称Gd-EOB-DTPA增强MRI不仅能显示扩张的胆管及其内增强的肿瘤组织,而且能证实肝胆期胆管充盈缺损是肿瘤分泌的黏液,同时还能区分肿瘤组织和周围炎症以及显示恶性肿瘤肝外胆管的侵犯程度。MRCP能显示扩张的胆管树,可发现管腔内充盈缺损,提示病变可能部位。
4.3 ERCP检查 ERCP曾被认为是诊断IPMN-B的金标准,十二指肠镜下发现十二指肠开口处有黏液流出往往提示胆管或胰管内有产黏液的病变存在,此时结合腹部影像检查可确定病变来源。值得一提的是,有文献[28-29]报道IPMN-B患者十二指肠乳头开口处形态发生改变,呈“鱼眼征”(图2),可能是长期慢性炎症刺激所导致。ERCP下可观察到弥漫扩张的胆管由于充满黏液而形成充盈缺损,但厚重的黏液常挡住了胆管内潜在的相对扁平、体积小的肿物且有诱发胰腺炎的潜在风险。
4.4 PTCS、POCS及术中胆道镜 三者均可直视胆管、获得病灶活检、评估肿瘤范围,对指导下一步治疗策略有重要作用,但因其获得的组织病理学局灶性,往往不能代表肿瘤整体。对于IPMN-B来说, 因分泌大量黏液, PTCS定位肿瘤及确定病灶范围比POCS更有优势;术中胆道镜也可明确胆管病变部位及范围(局灶或弥散性),但对于黏液稠厚的患者无法建立良好的内镜视野,且其对术前诊断IPMN-B并无帮助。


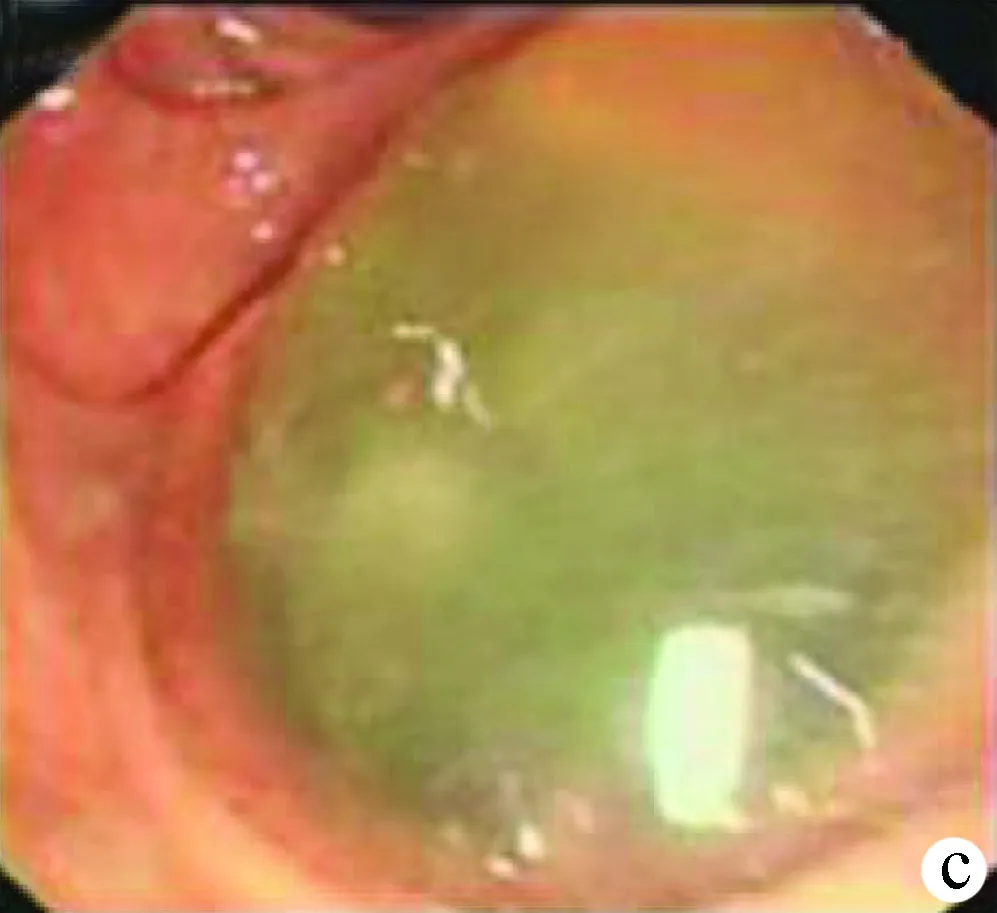
注:a,典型的CT表现为肝内胆管明显的囊性扩张,右肝叶胆管有一小点状高密度病变;b,T2磁共振成像显示肝内胆管明显呈“软藤状”扩张,胆管内有小结节T2信号灶;c,十二指肠镜检查显示乳头上方有一个直径为1.0 cm的十二指肠瘘, 内部充满了胶状黏液。

注:十二指肠乳头开口处呈“鱼眼征”,并伴有黏液流出。图2 ERCP检查
4.5 IDUS检查 IDUS的优势在于既能定位肿物所在胆管位置,又能透过黏液评估肿物是否存在浸润。有研究表明IDUS能发现≥3 mm胰导管内肿物,同时进行超声引导下细针穿刺病理分析。而且,目前的IDUS超声探头可经过肝门到分支胆管,较全面地探查肝内外胆管系统[25]。
5 诊断及鉴别诊断
5.1 诊断 由于IPMN-B临床表现、实验室检查及影像学检查均无特异性,术前诊断IPMN-B异常困难,确诊主要依靠术后病理学检查。当患者出现右上腹痛、黄疸、发热等症状,B超、CT及MRI等影像学检查提示不明原因胆管扩张,无论伴或不伴胆管内肿物,尤其是在此基础上十二指肠镜下发现十二指肠乳头开口处有黏液流出,应高度怀疑IPMN-B。
5.2 鉴别诊断 IPMN-B 需与可引起胆管扩张及十二指肠乳头开口处有黏液流出的疾病进行鉴别。(1)肝内胆管癌:影像学上两者均可见上游胆管扩张,而下游胆管扩张、全胆管扩张为 IPMN-B 特有,且肝内胆管癌主要表现为肝内实质占位或者伴局部胆管梗阻,所引起的CA19-9的升高为持续性。(2)非黏液性 IPNB(IPNB-NM):两者均可出现胆管扩张,但胆管及十二指肠开口处见到胶冻样黏液组织为IPMN-B所特有,IPNB-NM 则无黏液产生。(3)肝黏液性囊性肿瘤:两者在临床表现、影像学及病理学检查方面均有一定重叠,均可产生黏液。但因肝黏液性囊性肿瘤不与胆管相通,它产生的黏液只限制在囊性的肿瘤内而不进入胆管,故影像学上胆管几乎不扩张,且十二指肠开口处无黏液排出,其特征为病理检查可发现卵巢样上皮下间质[30]。(4)IPMN-P:两者均可产生胶冻样胆汁,并由十二指肠乳头开口处排出。但IPMN-B 位于胆管系统,胆管扩张伴或不伴有胆管腔肿瘤是其典型的影像学特征;而IPMN-P 主要为胰导管系统内的占位,影像学图像的异常主要在胰腺部位,主要表现为胰管扩张伴肿物、胰腺炎等。(5)复发性化脓性胆管炎伴胆管扩张:两者症状均可表现为发热、反复的胆管梗阻,影像学均可表现为胆管扩张而不伴有肿物,且复发性化脓性胆管炎伴胆管扩张ERCP图像上也可表现为充盈缺损,IPMN-B的黏液栓与胆管结石影像学图像上亦难鉴别。两者的鉴别要点是复发性化脓性胆管炎伴胆管扩张患者其影像学图像上液性区域不与胆管相通。
6 治疗及预后
6.1 治疗 目前认为IPMN-B为胆管癌的癌前病变,虽其生长缓慢,但随着时间推移最终均会进展为侵袭性肿瘤,故所有IPMN-B患者均应尽早处理。外科手术是治疗IPMN-B的首选方法,由于该病可累及肝内外胆管,因此,明确病变累及范围、确定手术切除范围是决定手术治疗的关键因素。术前充分的影像学评估、术中胆道镜探查以及胆管切缘冰冻病理检查是明确病变累及的重要措施。手术方式取决于肿瘤的位置:肿瘤位于肝内胆管行完整切除病变所在的肝叶、肝段或半肝切除,位于肝门部可行肝门部胆管切除,位于胆管中段行胆管切除+胆肠吻合术,位于胆总管下段可行胰十二指肠切除术,对于门静脉侵犯的患者应联合门静脉切除吻合术[31],对于肝内外胆管广泛受累者,肝移植术是唯一有效的手术方式[9]。经皮经肝胆管穿刺引流、经皮经肝胆囊穿刺引流、内镜下鼻胆管引流和胆管内支架置入可用于术前减黄,但由于胆管内大量黏液存在而无法引流通畅导致疗效较差。常规区域淋巴结清扫尚存在争议,有学者[16]建议对于高度怀疑存在浸润性癌变的患者,加行规范的淋巴结清扫;对于肝门部及胆总管病变的患者,加行肝门部淋巴结清扫[4]。有文献[32]报道即使在吉西他滨为基础的一线化疗中加入表皮生长因子受体单抗,也不会显著提高胆管癌的总生存率和无进展生存率,作为胆管癌的前体,IPMN-B术后是否应行辅助化疗也尚未定论。新的治疗方法例如PTCS激光消融、经胆道镜电凝、铱激光管腔内治疗可用于改善患者生命质量,但目前尚缺乏相关研究[33]。
6.2 预后 总的来说,IPMN-B的预后好于IPMN-NB,且两者的预后均好于传统胆管癌[10,34]。分化程度是影响恶性IPMN-B预后的独立危险因素[21],除此之外,肿瘤位于肝外胆管(包括肝门胆管)、切缘状态阳性、淋巴结转移等可能提示预后不良。亚洲IPMN-B患者根治性切除术后五年生存率为81%[30],但复发率也高至29.3%,故患者术后需长期随访。
7 总结
IPMN-B是一种特殊且少见的胆管肿瘤,与IPMN-P具有同源性。其发病与胆管结石、华支睾吸虫病以及胆管慢性炎症密切相关。临床表现、实验室检查均无特异性,影像学上伴或不伴有肿瘤的广泛性胆管扩张及内镜下十二指肠乳头开口处有黏液流出时应高度警惕该病。手术治疗是首选治疗方式,术前充分的影像学评估、术中胆道镜探查以及胆管切缘冰冻病理检查是评估病变累及范围的重要措施。总的来说,IPMN-B预后比IPMN-NB及胆管癌预后均好,但鉴于其术后有高复发风险,故患者术后需长期随访。
利益冲突声明:所有作者均声明不存在利益冲突。
作者贡献声明:徐颖负责相关文献资料的收集、分析及论文初稿的写作;唐加、何清云参与文献资料的分析和整理;吴会超负责构思并拟定写作思路,指导论文的写作并最终定稿。
