肺淋巴管平滑肌瘤病合并感染性心内膜炎1例
2022-01-06孔晓钰汪心安丁家望
孔晓钰 汪心安 刘 梦 吴 辉 丁家望 李 松 杨 灿
(三峡大学 第一临床医学院[宜昌市中心人民医院] 心血管内科,湖北 宜昌 443003;2.长阳县人民医院 内科,湖北 宜昌 443003)
感染性心内膜炎(infective endocarditis,IE)为心脏内膜表面的微生物感染伴赘生物形成,其发生多与心脏瓣膜病有关。非风湿性心脏瓣膜病已成为IE最常见的基础心脏疾病,尤其是二尖瓣及主动脉瓣病变[1]。本例患者诊断为亚急性IE,追踪其病因,考虑与肺淋巴管平滑肌瘤病(pulmonary lymphangioleiomyomatosis,PLAM)所致肺部血管畸形,进而引起血流动力学改变导致二尖瓣病变相关,现报道如下。
1 病例资料(扫码观看视频,D018192-1)
患者,女,32岁,因“胸闷气喘4月余”于2021年4月3日入院。患者近4月来反复间断性发热,最高体温达38.5℃,伴胸闷、气喘、盗汗、全身酸痛,无头晕头昏、咳嗽咳痰、腹痛腹胀等不适。2020年12月患者因间断发热于我院呼吸与危重症医学科住院治疗,查胸部CT考虑左肺PLAM,左下肺慢性感染,前纵隔及心包左侧占位。予以抗感染、改善气道痉挛、雾化吸入等对症处理后,患者病情好转出院。2021年3月患者至北京世纪坛医院就诊,行上腹部+下腹部MR提示门静脉瘤样扩张、脾大,心脏彩超提示二尖瓣腱索断裂合并赘生物形成,血培养提示托尔豪特菌感染,诊断为亚急性感染性心内膜炎,予以头孢哌酮钠舒巴坦钠抗感染及对症处理,患者体温恢复正常后出院。现患者仍感胸闷气喘来我院就诊,门诊以“亚急性感染性心内膜炎”收入院。既往有慢性阻塞性肺疾病、肺大泡病史。入院查体:体温36.5℃,脉搏90次/min,呼吸20次/min,血压96/60 mmHg,血氧饱和度:84%(未吸氧),神志清楚,双肺呼吸音粗,双下肺可闻及湿性啰音,无胸膜摩擦音;心率90次/min,律齐,心尖部可闻及舒张期隆隆样杂音,无心包摩擦音;脾肋下可触及5 cm;余查体未见明显异常。
入院后完善相关检查:C反应蛋白、心肌酶、凝血功能、血培养、下呼吸道细菌培养、大便常规、肝肾功能等检查均无明显异常;D-二聚体6.33 μg/mL;降钙素原0.140 ng/mL;N端脑钠肽前体9 210 pg/mL。血常规显示白细胞10.93×109/L,血红蛋白82 g/L,淋巴细胞3.97×109/L,单核细胞1.13×109/L,血沉22 mm/h。外送血管内皮生长因子-D(vascular endothelial growth factor-D,VEGF-D):141.34 ng/L。心电图提示:窦性心动过速,R波递增不良,左胸导联低电压,心电轴右偏。床边心脏彩超:二尖瓣前叶脱垂伴赘生物,左房大,二尖瓣大量反流,心包积液。胸部常规增强CT检查:考虑左肺PLAM,前纵隔及心包左侧淋巴管囊肿,部分血管瘤样扩张(见图1),左下肺慢性感染,节段性实变。床边胸片:左肺多发囊状透光影,纵隔增宽,心影增大(见图2)。该患者诊断为“感染性心内膜炎,肺部感染,PLAM可能”,予以抗感染及对症支持治疗。胸心外科会诊认为左肺毁损有明显心脏手术禁忌症,无法耐受手术及麻醉,且患者纵隔及心包左侧占位尚不明确(见图2),于4月21日出院转上级医院治疗,待后续进一步随访。
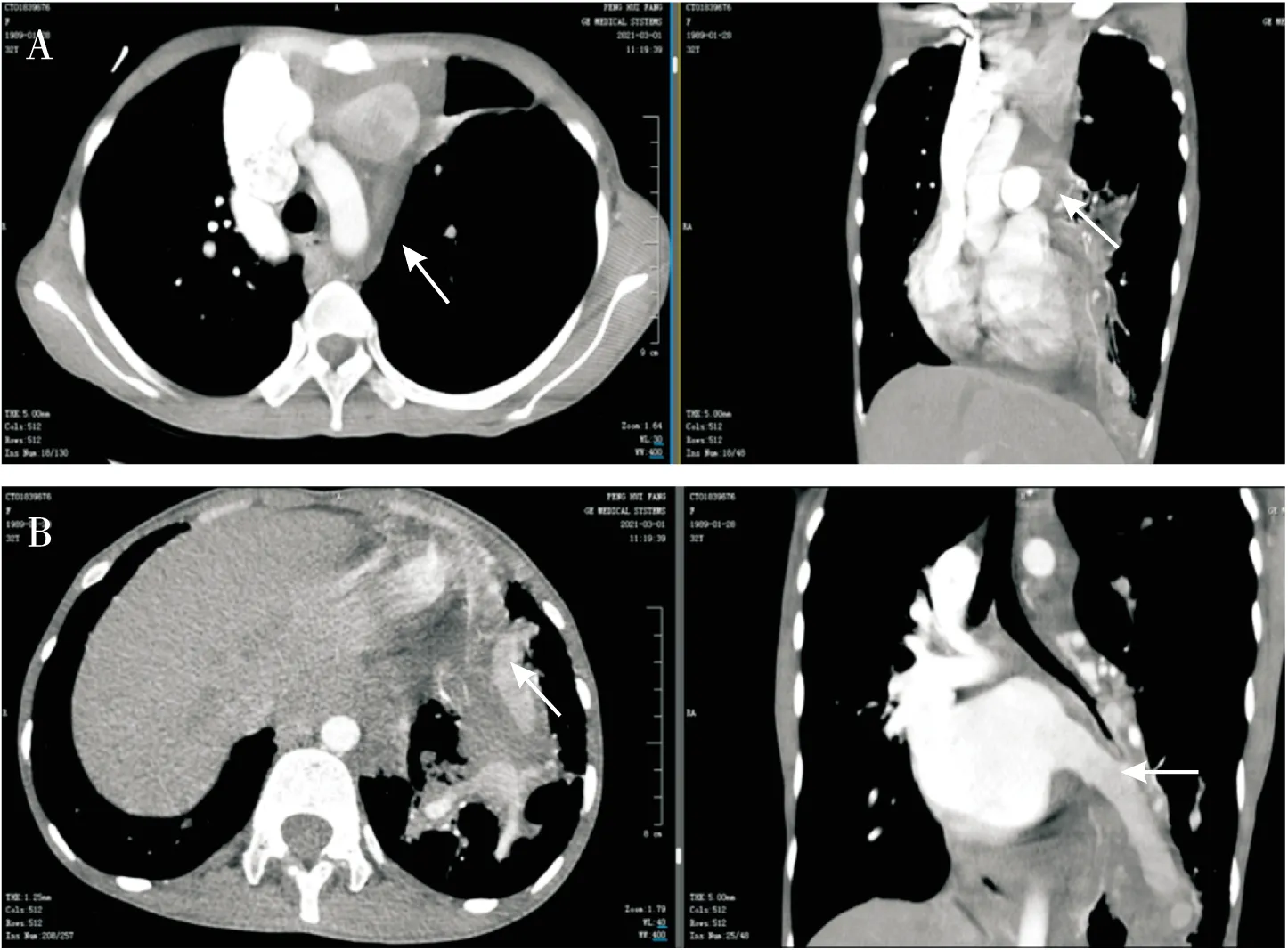
注:A:头臂静脉扩张(白色箭头所示);B:肺静脉扩张(白色箭头所示)图1 患者肺部增强CT结果
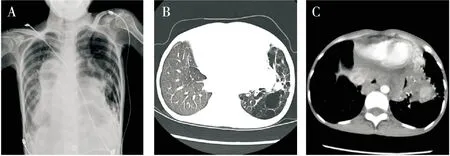
注:A:左肺多发囊状透光影,纵隔增宽,心影增大; B、C:左肺可见多发囊状低密度影,左肺门及下肺见片状实变灶,纵隔及心包左侧可见团片状高密度影图2 患者入院后床边胸片及肺部CT结果
2 讨论
IE指由细菌、真菌和其他微生物直接感染心内膜或心脏瓣膜而产生的炎症,常见于原有心血管器质性损害或畸形,如二尖瓣和主动脉瓣关闭不全、室间隔缺损、动脉导管未闭等[2]。本例患者既往心脏超声检查发现左心扩大,并伴有进行性加重的二尖瓣关闭不全及肺动脉高压。此外,患者肺部CT提示PLAM可能,因患者合并感染性心内膜炎,未能行病理活检。该患者VEGF-D为141.34 ng/L,2017年美国胸科学会和日本呼吸学会将VEGF-D≥800 ng/L纳入PLAM的诊断标准,然而部分散发性PLAM患者血清VEGF-D水平与健康者无差异,人口统计学和功能特征可能有助于解释该患者血清VEGF-D水平较低的原因,因此VEGF-D值正常不能排除该病[3-5]。因本例患者肺部CT表现十分典型,综合考虑为PLAM。
PLAM是一种罕见的以肺弥漫性囊性改变为特征的疾病,主要发生于育龄期女性[6]。临床症状可表现为呼吸困难、气促、咯血、乳糜胸等,常合并肾血管平滑肌脂肪瘤等肺外表现[7]。PLAM特征性CT表现为双肺广泛分布的囊状透亮影[8]。PLAM的最终诊断依赖于组织病理学检查。典型的组织学特征是肺组织结构破坏,肺泡扩张并相互融合形成肺大泡,肺间质中异常平滑肌细胞增生,以梭形、上皮样为主,围绕淋巴管、血管分布,肺部形成多个囊性空洞[9]。随病情进展,患者可出现限制性、阻塞性通气功能障碍和肺弥散功能障碍[8]。此外,部分PLAM患者可出现右心功能不全表现[10]。PLAM引起右心功能不全的机制,主要考虑为肺部血管周围的类平滑肌细胞异常增生导致肺循环障碍,引起肺动脉高压及右心功能不全,而肺循环异常又使左心灌注不足。另一方面,平滑肌细胞在支气管、血管及淋巴管周围异常增生可造成气道阻塞,肺间质平滑肌细胞增生可造成弥散功能障碍和通气血流比例失调,引起低氧血症,加重左心灌注不足,最终导致左心扩大而发生左心衰竭。扩大的左心房使二尖瓣相对关闭不全,二尖瓣大量反流,形成湍流,利于微生物沉积和生长,导致IE发生。因此,PLAM可引起左心和右心结构及功能异常,增加IE的发生几率。
查看本例患者既往病历发现,其2017年8月肺部CT已提示PLAM可能,当时给予患者抗感染及对症处理,并建议患者病情稳定后进一步检查明确诊断,患者未予重视,于病情好转后出院,未行进一步诊治。患者于2021年1月因“腹痛腹胀”就诊,腹部CT检查提示肝脏增大,脾大,腹腔积液等,符合右心功能不全表现,且患者左心扩大、二尖瓣反流、肺动脉高压较前进展,推测其一系列症状与PLAM引起的肺部血管畸形有关。当时外送VEGF-D<800 ng/L,尚不支持PLAM诊断,且患者慢性阻塞性肺疾病伴有急性加重,合并肺部感染,临床医生予以相应抗感染处理,并再次建议患者病情稳定后进一步检查。患者2021年3月查心脏彩超提示二尖瓣反流、肺动脉高压等进一步加重。当患者再次发生肺部感染时,病原菌也趁机侵犯病变的心脏瓣膜,最终导致IE。因此,当患者肺部CT提示PLAM,且心脏彩超提示心脏瓣膜病变时,积极行进一步检查明确PLAM诊断并采取相应措施,可能有助于延缓患者心脏瓣膜病变进行性加重,减少IE的发生。
总之,PLAM是累及多系统的罕见病,胸部CT的改变极具特征性,虽不能作为确诊PLAM的依据,但对于PLAM的诊断具有强烈提示作用。对于疑似或确诊PLAM患者,临床医生应警惕其心血管系统的伴随改变,尤其对于心脏瓣膜结构异常且进行性加重的患者及早诊断并采取相应措施具有重要的临床意义。
