CLSI EP06-Ed2与EP06-A在定量测量程序线性验证应用中的差异
2022-01-05谢轩波刘洋洋单汉明李晓博杭州迪安医学检验中心杭州310030
谢轩波,刘洋洋,单汉明,李晓博(杭州迪安医学检验中心,杭州310030)
线性区间(linear interval)是指使实验系统的最终分析结果为可接受的线性浓度范围,此时非线性结果与理论值之间的误差应低于允许误差[1]。此项对定量测定检测系统尤为重要,是系统性能评价非常重要的一项指标[2-4]。
2003年美国临床和实验室标准协会(CLSI)发布EP06-A[5],引入多项式回归分析,非线性模型与线性模型相比较,进而判断最适非线性模型与线性模型各浓度的差值是否小于该方法允许的偏差。国内发布的WS/T 408—2012[4]以及CNAS-GL037:2019[6]也参考了相关内容。
2020年11月CLSI最新发布了EP06-Ed2[5],在定量测量程序的线性区间确认(validation)和验证(verification)程序、实验数据分析处理、未通过结果处理等方面都做了较大调整。最显著特征是使用WLS回归分析,将偶然因素导致的失败风险降低,根据95%置信区间(confidence interval,CI)与允许线性偏差(allowable deviation from linearity,ADL)比较来评估待验证线性区间是否可接受。
现以几个实验室常见检测项目为例,探讨CLSI EP06-Ed2与EP06-A在定量测量程序线性验证中的差异。
1 材料与方法
1.1样品来源 杭州迪安医学检验中心实验室检测结果靠近线性区间上下限附近的临床样本。
1.2主要仪器和试剂 i3000全自动化学发光免疫分析仪(四川迈克公司)及配套糖类抗原50(CA50)测定试剂盒(直接化学发光法)、糖类抗原19-9(CA19-9)测定试剂盒(直接化学发光法)和校准品;UniCel DxI 800 Access免疫分析系统(美国Beckman Coulter公司)及配套孕酮(Prog)测定试剂盒(化学发光法)和校准品。
CA50试剂说明书声称线性区间为2~200 U/mL,允许偏差±2.5 U/mL;CA19-9声称线性区间为5~2 000 U/mL,允许偏差±6 U/mL;Prog声称线性区间为0.1~40 ng/mL,允许偏差±0.64 ng/mL;参考国家卫生健康委临床检验中心室间质评项目可接受范围将这3个项目的允许总误差(TEa)均设定为±25%。
以上检测项目均已进行精密度和正确度相关验证,结果符合标准。
1.3实验方法
1.3.1样本准备 每个项目分别选取接近线性区间上限和下限的样本,将高浓度样本标记为H,低浓度样本标记为L,按6L、5L+1H、4L+2H、3L+3H、2L+4H、1L+5H、6H比例混合得到7个浓度梯度的样本,最终7个样本按浓度从高到低依次标记为1至7。
1.3.2实验操作 将每个浓度水平的样本重复检测2次。要求所有样本在一次运行中或几次间隔很短的运行中随机测定,在1 d之内完成。
1.3.3数据分析
1.3.3.1按照CLSI EP06-Ed2进行数据分析:
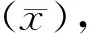
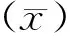
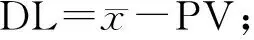
(e)按公式计算线性偏差CI:
其中,
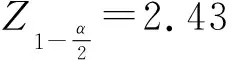
(f)ADL百分比设定为1/2TEa,对应本研究探讨项目皆为±12.5%,根据每个样本预期值,计算ADL:ADL=±(PV×12.5%);
(g)根据预期浓度为X轴,线性偏差为Y轴,然后将DL、CI、ADL绘制成散点图;
(h)按照EP06-Ed2方案判断,有1个浓度线性偏差CI与ADL完全不相交视为线性区间验证不可接受。
1.3.3.2按照CLSI EP06-A进行数据回归分析,计算出最适多项式回归方程,比较各点与理论线性方程结果之间的差异,最适回归方程与理论线性方程之间有1个浓度的差异同时大于1/2TEa和允许偏差视为线性区间验证不可接受。
1.4统计学分析 用Excel 2016进行。数据处理过程中不对中间结果做修约处理。
2 结果
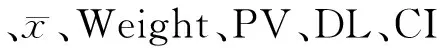
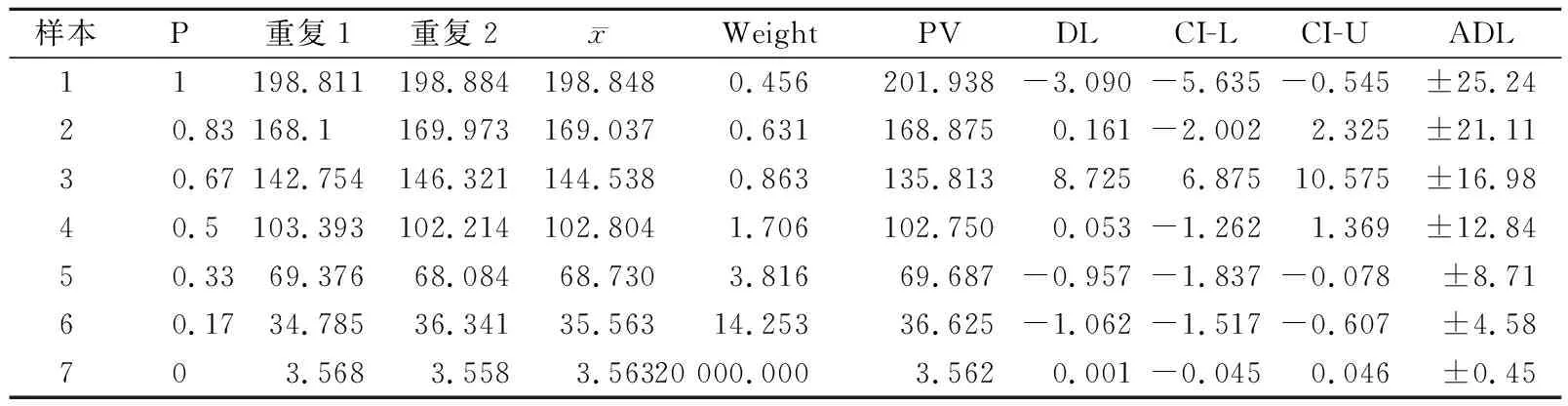
表1 CA50重复检测结果及各样本权重(U/mL)
根据EP06-Ed2绘制图1;根据EP06-A计算出最适回归方程y=-0.388 8x3+4.201 6x2+20.935x-20.931,7个浓度的偏倚或偏差分别为0.013 5 U/mL、-6.3%、-1.3%、1.8%、2.7%、1.4%、-2.3%,均在可接受范围内,根据数据结果绘制图2。
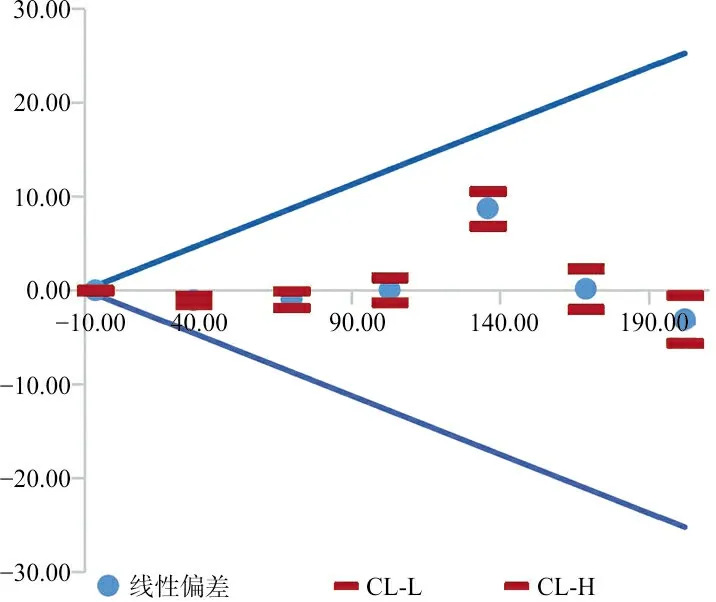
图1 CA50散点图(EP06-Ed2)
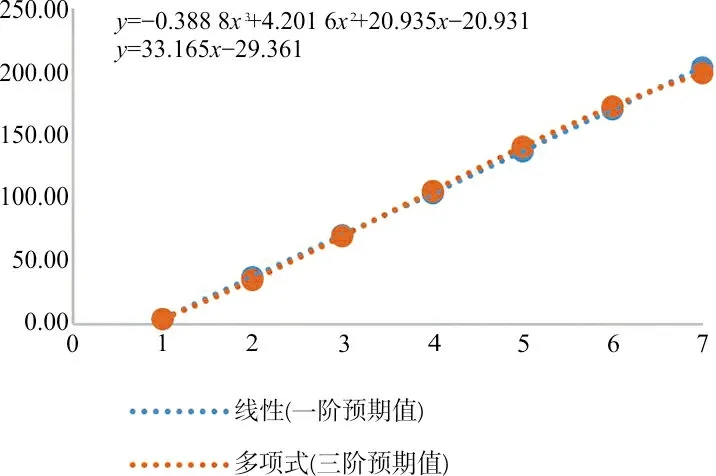
图2 CA50回归分析(EP06-A)
2.2CA19-9相关结果及分析 按照EP06-Ed2分析项目各线性样本重复检测结果、Weight、PV、DL、CI及ADL见表2,加权后线性回归方程为Y=3.82+1 889.55X。
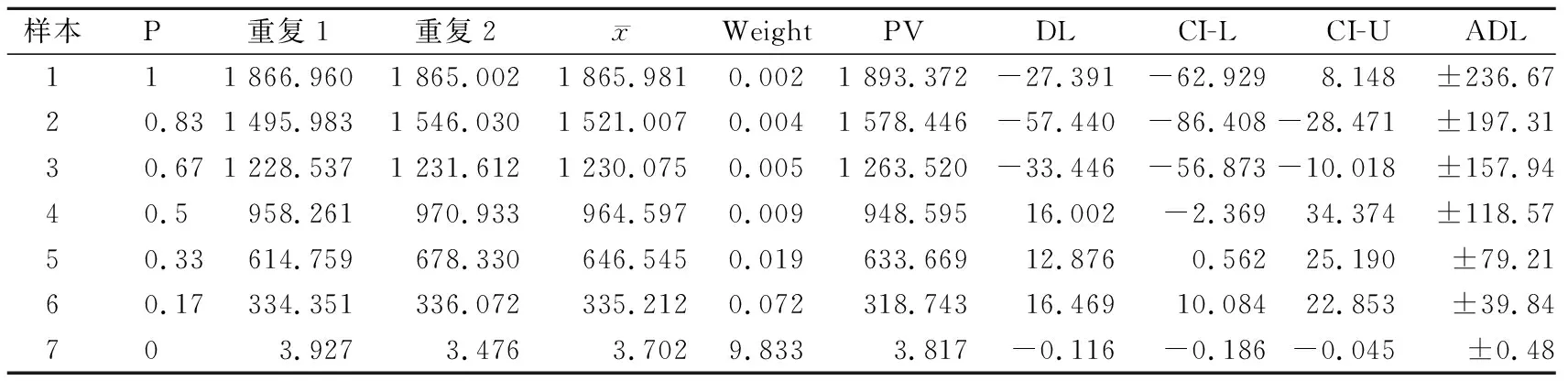
表2 CA19-9重复检测结果及各样本权重(U/mL)
根据EP06-Ed2绘制图3;根据EP06-A计算出最适回归方程y=2.582 1x3-32.65x2+424.25x-395.05,7个浓度的偏倚或偏差分别为-23.815 8 U/mL、4.7%、3.2%、0.7%、-0.8%、-1.0%、0.4%,最低浓度超过允许偏差,其他在可接受范围内,根据数据结果绘制图4。
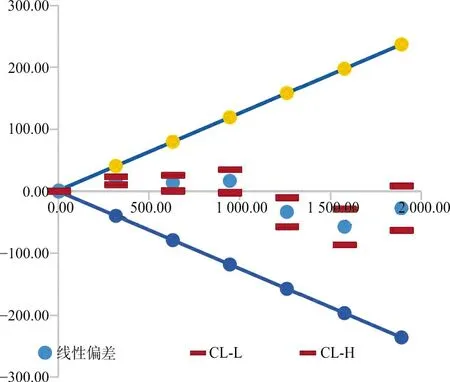
图3 CA19-9散点图(EP06-Ed2)
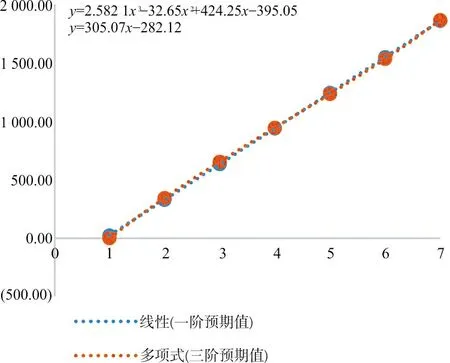
图4 CA19-9回归分析(EP06-A)
2.3Prog相关结果及分析 按照EP06-Ed2分析项目各线性样本重复检测结果、Weight、PV、DL、CI及ADL见表3,加权后线性回归方程为Y=0.14+34.84X。
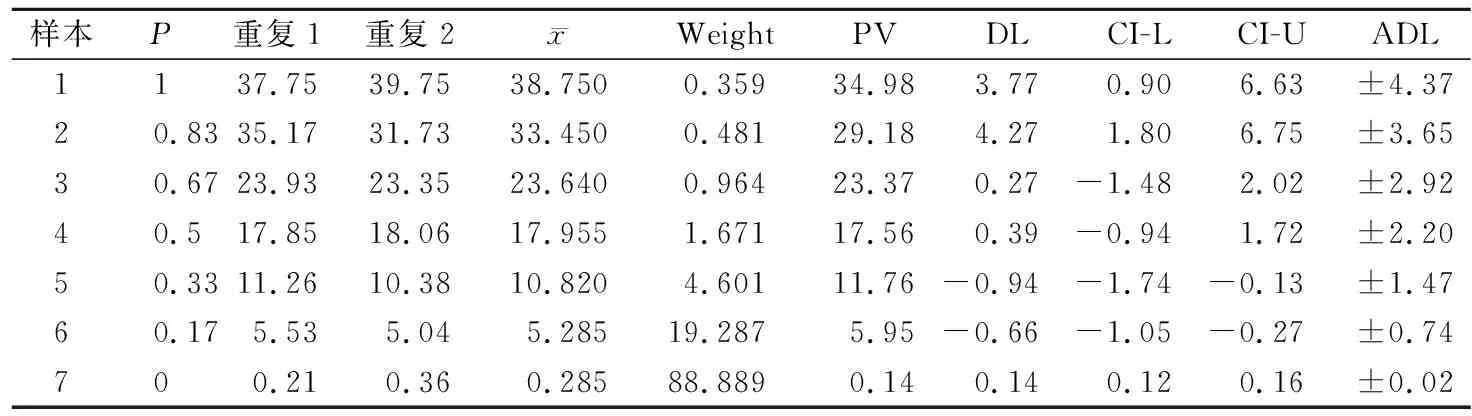
表3 Prog重复检测结果及各样本权重(ng/mL)
根据EP06-Ed2绘制图5。根据EP06-A计算出最适回归方程为y=0.237 8x2+4.688 5x-4.912 1,7个浓度的偏倚或偏差分别为1.189 0 ng/mL、0.0%、-5.9%、-5.1%、-2.8%、0.0%、3.1%,最低浓度超过允许偏差,其他在可接受范围内,根据数据结果绘制图6。
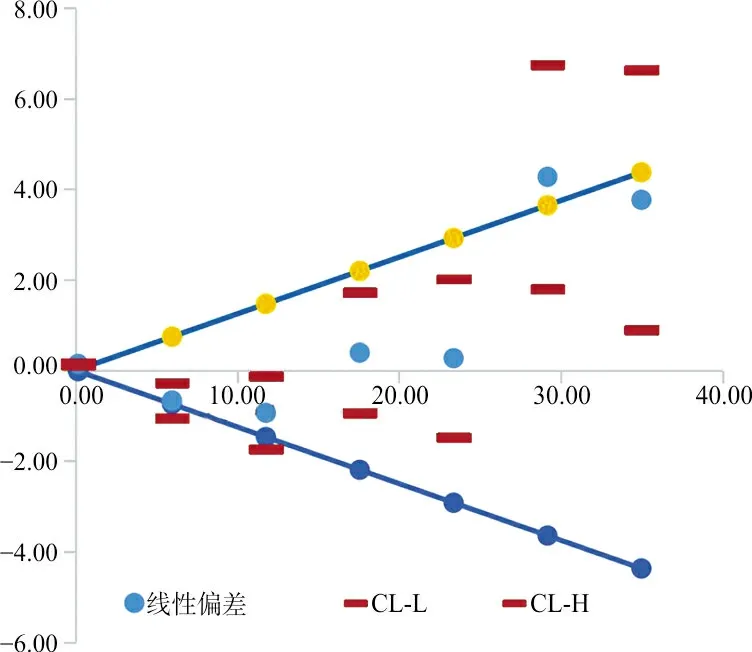
图5 Prog散点图(EP06-Ed2)
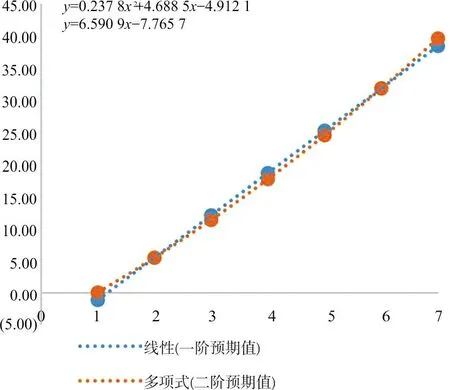
图6 Prog回归分析(EP06-A)
2.4结论差异汇总 CA50项目以EP06-Ed2与EP06-A方案进行线性区间验证均可接受,两者结论一致。
CA19-9项目以EP06-Ed2方案验证线性区间可接受,以EP06-A方案验证线性区间不可接受,两者结论不一致。
Prog项目以EP06-Ed2方案验证线性区间可接受,以EP06-A方案验证线性区间不可接受,两者结论不一致。
3 讨论
同为对线性区间验证的指南,将EP06-Ed2与EP06-A进行比较。在样本选择及实验操作方法上,CLSI EP06-Ed2和CLSI EP06-A无明显差异;数据分析方法以及判断标准选择有较大的差异,因此实验结论也有可能不同。在数据分析上,EP06-Ed2采用WLS回归分析,当测量程序重复性明显与浓度相关,加权可防止高浓度样本对线性拟合产生不成比例的影响。根据ADL评估线性偏差,以95%CI检查与待验证线性区间的一致性。当某浓度结果的线性偏差CI与ADL全部或部分相交视为该浓度验证可接受。EP06-A采用多项式回归计算,当测量程序重复性明显与浓度相关,各浓度权重相同,高浓度样本将对拟合方程的斜率产生较大影响,导致拟合曲线计算出的低值预期值与实际结果差异较大。某浓度最适回归方程与理论线性方程结果差异小于1/2TEa或小于允许偏差视为该浓度线性区间验证可接受。由于数据分析及结果判断标准的差异,可能会造成2种方案结论上的差异:以EP06-A判断,CA50可接受,CA19-9和Prog不可接受;以EP06-Ed2判断,CA50、CA19-9和Prog均可接受。
EP06-A中低值样本测定值与预期值偏差相较EP06-Ed2更易出现验证不可接受的情况,只要1个浓度与理论值的偏差超过允许范围,即判断线性验证不可接受。EP06-A也并未对线性区间验证不可接受的结果有太多解释。EP06-Ed2则对不同结果进行了更为详细的解释。(1)各浓度的测定均值在ADL范围内,CI全部或者部分在ADL范围内,线性可接受。(2)部分浓度测定均值在ADL范围外,但相关CI有部分在ADL范围内,统计学上其线性可被接受。如果整体性能足以满足临床需求,可接受其线性研究结果;如果整体性能不足以满足临床需求,拒绝其线性研究结果。(3)有部分浓度测定均值在ADL范围之外,且相关CI全部在ADL范围外,线性不可接受。
综上,线性区间是性能评价重要指标,CLSI EP06-Ed2相较EP06-A,在数据分析、结果判断及后续解读上更具优势,有助于避免一部分能被临床接受的项目因实验结果而被直接拒绝。建议实验室可根据实际需求选择合适的方案进行线性区间验证。
