对比分析巩膜扣带术与玻璃体切割术治疗孔源性视网膜脱离的疗效及术后并发症
2022-01-04吕婷婷牛彤彤王海林尹蓉实
吕婷婷, 牛彤彤, 王海林, 尹蓉实, 安 燕
(辽宁省沈阳市第四人民医院眼科, 辽宁 沈阳 110031)
视网膜脱离是一类较为严重的致盲性眼部疾病,起病急、发展迅速,当发生视网膜脱离后,若不及时复位则会发生视网膜萎缩及变性,引起视力障碍且不可恢复[1],是致盲的重要原因之一。近年来,视网膜脱离的发病率呈明显上升趋势,已引起社会关注。视网膜脱离可分为孔源性、牵拉性和渗出性三种类型,其中孔源性视网膜脱离(rhegmatogenous retinaldetachment,RRD)最为常见,RRD的发病原因主要与视网膜裂孔、玻璃体牵拉液化有关,玻璃体液化后通过视网膜裂孔进入神经上皮视网膜下,分离视网膜神经上皮层和色素上皮层,脱离的视网膜因无法感知光线导致眼部图像缺失。视网膜脱离与年龄、眼外伤及高度近视等因素存在密切联系,现阶段仍以手术治疗为主,治疗原则为封闭视网膜裂孔和复位脱离视网膜[2]。相关文献[3]记载,随着手术器械的不断改进和医疗水平的提高,通过手术达到视网膜结构复位成功率极高,但都存在术后视功能改善不明显的缺点。1951年,巩膜扣带术(scleral bucking,SB)得以发明和推广,且具有手术简单、术中损伤小、预后好等优点,其发展趋势为减小手术量、提高复位率、减少手术并发症,现已成为治疗非复杂RRD的最好术式;上个世纪70年代,玻璃体切割术(pars plana vitrectomy,PPV)被提出且被证实为治疗复杂性视网膜脱离的有效治疗手段,经过各位学者的不断努力创新,手术技巧和手术器械都得到了改进,现已历经20G、25G、27G玻璃体切割系统[4]。无论是SB还是PPV,都可达到修补裂孔、促进网膜下积液吸收和视网膜复位的治疗目的。为探究最佳临床治疗手段,尽可能的恢复患者最终视力,本研究回顾性分析了93例RRD患者的临床资料,对比观察SB和PPV的临床疗效及术后并发症,具体结果如下。
1 资料与方法
1.1一般资料:回顾性选取2019年6月至2021年1月于本院眼科行手术治疗的93例(93只眼)RRD患者的临床资料,其中41例(41只眼)患者行SB设为SB组,其余52例(52只眼)患者行PPV设为PPV组。纳入标准:①患者均行最佳矫正视力、眼压、裂隙灯显微镜、眼底彩色照相、相干光断层扫描等检查确诊为原发性RRD;②既往未接受过内眼手术治疗;③手术均由同一位经验丰富的医师完成;④视网膜裂孔数≥2个;⑤临床资料完整。排除标准:①合并黄斑裂孔、视神经萎缩、弱势等影响中央视力的疾病;②屈光间质混浊明显者。两组患者一般资料比较无明显统计学意义(P>0.05),见表1。
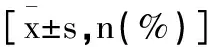
表1 两组患者一般资料比较
1.2方法:术前两组患者均行视力、眼压、裂隙灯检查、眼底照相、OCT等常规检查并绘制视网膜图,对于位于同一象限或同一纬度的多发裂孔以变性孔为主,伴有增生性玻璃体视网膜病变且以视网膜下膜为主的患者及年轻或独眼的特殊患者首选SB进行治疗;对于裂孔分散、裂孔较大、裂孔处玻璃体牵拉且以视网膜前膜为主的患者采用PPV进行治疗。
1.2.1PPV组:给予25G+PPV术进行治疗。全麻或球后神经阻滞后常规消毒铺巾,于颞下、鼻上和颞上方距角巩膜缘3.5~4mm处使用25G玻切套管针穿刺巩膜,进入球内后回抽出针芯,形成3个穿刺口,将套管留置穿刺口,颞下套管装置25G灌注头,其余两个套管放置玻璃体切割头及导光纤维及其他器械,进行全玻璃体切除,术中联合视网膜激光光凝处理视网膜裂孔及变性区,并使用硅油眼内填充。
1.2.2SB组:给予单纯SB进行治疗。全麻后常规消毒铺巾,根据裂孔方位沿角膜缘环形切开球结膜且放射状切开,预置裂孔旁两个方位眼肌牵引线,于视网膜裂孔下方6点钟位置角膜巩膜缘后12~15cm处切口穿刺,排出视网膜下液,并辅以顶压维持眼压,以裂孔为中心行裂孔及变形区冷凝,根据术前裂孔定位放置276或277硅胶带,缝合固定于浅层巩膜上,检查裂孔位于手术嵴上,并根据具体情况决定是否调整预置缝线位置和进行巩膜环扎,若眼压偏高则行前房穿刺,放出少量房水。
1.3观察指标:两组患者术后均进行为期3个月的随访调查。①观察患者视网膜复位情况。复位良好:检查结果显示视网膜平状,黄斑区无视网膜下液;好转:检查结果显示视网膜大部分平伏或局限性视网膜脱离,黄斑区有或无视网膜下液;复位不良:检查结果显示视网膜脱离,黄斑区存在视网膜下液,且病情进一步发展。②最佳矫正视力情况(BCVA)采用标准对数视力表站立位检查,均由同一位经验丰富的验光师验光检查。③并发症发生情况,记录两组患者出现医源性视网膜裂孔、重水残留、黄斑前膜、高眼压、穿刺口出血、并发性白内障等情况。

2 结 果
2.1两组患者术前视网膜脱离情况比较:两组视网膜裂孔数目、位置、类型、视网膜脱离范围及特殊视网膜脱落情况比较具有统计学意义(P<0.05);与SB组相较,PPV组病情更为复杂,见表2。
2.2两组患者术后3个月视网膜复位情况比较:术后3个月,PPV组视网膜复位良好率为90.38%(47/52),略高于SB组78.05%(32/41),但组间比较无统计学意义(χ2=2.728,P>0.05)。
2.3两组患者手术前后BCVA比较:PPV组和SB组患者治疗前后BCVA差值比较无统计学意义(P>0.05),见表3。

表3 两组患者手术前后BCVA比较
2.4两组患者并发症发生情况比较:PPV组并发症发生率为42.31%,SB组并发症发生率为11.90%,组间比较具有统计学意义(χ2=18.309,P<0.05),见表4。

表4 两组患者并发症发生情况比较n(%)
3 讨 论
RRD也被称为原发性视网膜脱离,是一类视网膜神经上皮层和色素层分离的严重的致盲性眼病,RRD的发生主要与视网膜退行性变、玻璃体变形液化后经视网膜裂孔进入视网膜神经上皮层和色素层间有关,因此任何造成视网膜和玻璃体发生病变的因素都会增加RRD的发生概率[5]。目前RRD的发病机制仍在探究之中,但以往研究[6]发现,RRD的发病原因多与年龄、眼部外伤、高度近视及遗传等因素相关。RRD致盲的原因主要是脱离视网膜部分无法感知光线刺激,导致眼部图像缺失,视网膜复位是治疗RRD的主要方法,术前仔细观察患者玻璃体及视网膜脱离情况,评估患者病情,从而选择最佳手术方式也是视网膜复位成功的关键[7]。
SB临床常用来治疗晶状体囊膜完整、裂孔明确、位于赤道前的非复杂性RRD,通过将环扎硅胶带固定于裂孔相应方位直肌下,联合局部加压、放液、冷凝、环扎等操作封闭裂孔及复位视网膜,其发展趋势是减少手术量、提高复位率、尽可能地降低并发症的发生[8]。PPV是后极部视网膜裂孔、增生性玻璃体视网膜病变等复杂性视网膜脱离的最佳选择,切除玻璃体后使用硅油或气体眼内填充,使视网膜复位。硅油填充可恢复眼内容积,分离粘连增殖膜;切除玻璃体可有效解除其对视网膜的牵拉,封闭视网膜裂孔,使视网膜复位[9]。本研究中,术后3个月,PPV组视网膜复位良好率为90.38%,略高于SB组78.05%,但组间比较无统计学意义(P>0.05);PPV组和SB组患者治疗前后BCVA差值比较无统计学意义(P>0.05),表明两种手术方法治疗RRD患者的临床疗效比较无显著差异。两组患者术前视网膜脱离情况显示,两组视网膜裂孔数目、位置、类型、视网膜脱离范围及特殊视网膜脱落情况比较具有统计学意义(P<0.05),表明SB具有且具有手术简单、术中损伤小、预后好、准确性高等优点;随着微创技术和显微镜技术的发展,微创PPV通过应用更为精细的手术器械缩小手术切口,无需缝合巩膜和球结膜切口,具有损伤更小、术后恢复更快等显著进步[10]。但本研究中,PPV组并发症发生率明显高于SB组(42.31%vs11.90%),眼压升高、并发性白内障及医源性视网膜裂孔均为PPV术后常见并发症。眼压升高可能与PPV术刺激眼局部血流动力学改变,血管扩张和通透性增加有关;血流动力改变还会破坏血房水屏障,血浆型房水进入房后导致眼压增高;此外,若术中体位不当,导致硅油进入前房,也会造成瞳孔阻滞型高眼压。PPV术后并发性白内障的发病机制多种多样,主要与晶状体机械性损伤、晶状体物理和化学性变化、PPV术后葡萄膜炎的发生及手术时间等因素相关。手术中光照射会损伤晶状体细胞,使得晶状体内不溶性晶状体蛋白和色素累积,导致其透明度下降;硅油注入玻璃体腔后进入房水循环,并通过该循环与晶状体后表面、虹膜、悬韧带接触,从而改变防水结构,影响晶状体营养代谢;术后发生葡萄膜炎症反应会加重晶状体混浊程度,增加并发性白内障的发生风险。有研究[11]显示,患者年龄和眼部宿疾也与PPV术后并发性白内障有一定联系。医源性视网膜裂孔的发生原因包括:①手术牵拉玻璃体视网膜粘连处;②手术牵拉玻璃体基底部及睫状体导致巨大视网膜裂孔发生;③巩膜切口过小,手术器械强行插入眼内或器械反复进出巩膜切口,引起玻璃体基底部撕脱。由于PPV术技巧难度大、对手术医生技术要求高,且病情复杂多变,尽可能地避免术中和术后并发症的发生是PPV术成功的关键,也是今后需进一步完善的问题。SB的长期稳定性和临床优势确切,并不能被PPV完全取代,尤其对于年轻或独眼患者,意义重大。
综上所述,SB和PPV均有一定的临床疗效,对于复杂的病例多采用PPV,SB因其长期稳定性及安全性多用于年轻患者。但本研究为回顾性研究,病历资料有限,且术后随访时间短,且未分析眼内填充空气及惰性气体的情况,存在一定的局限性,仍需进行前瞻性、随机对照实验以增加研究结果的精确性。
