基于定量视角的电化学解题策略
2021-12-31张英锋
>>>张英锋 于 浩
电化学一般以陌生且复杂的能量转化设备为情境,以原电池、电解池、二次电池(或充放电装置)为载体,以文字叙述加图片的形式呈现,从电化学工作原理、电化学方程式书写和电化学定量计算三个层面对电化学知识进行考查。本文选取离子转移、电极反应物和产物判断及电极反应式书写三个高频考点,从定量视角构建解题模型。
1.离子定量转移问题
例1.微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图装置处理有机废水(以含CH3COO-的溶液为例)。请判断选项C是否正确。
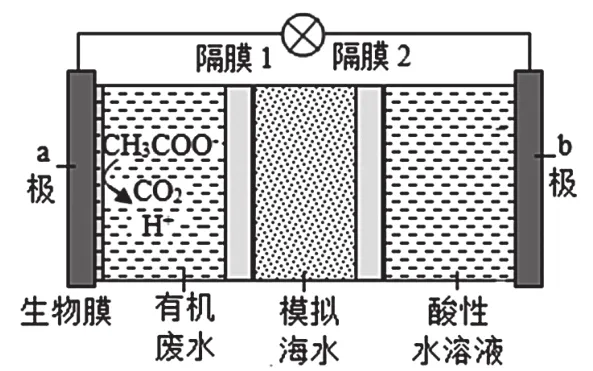
C.当电路中转移1mol电子时,模拟海水理论上除盐58.5g
【解析】此题中Na+、Cl-并不参与放电,但根据原电池的工作原理,可判断出NaCl溶液中的Na+移向正极、Cl-移向负极。其中移动的阴阳离子所带的电荷与移动的电子数量一致,所以电路中转移1mol电子时,通过离子交换膜的Na+为1mol、Cl-为1mol,质量为1mol×58.5g/mol=58.5g,即模拟海水理论上除盐58.5g,故选项C的说法正确。
例2.钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。请判断选项B是否正确。
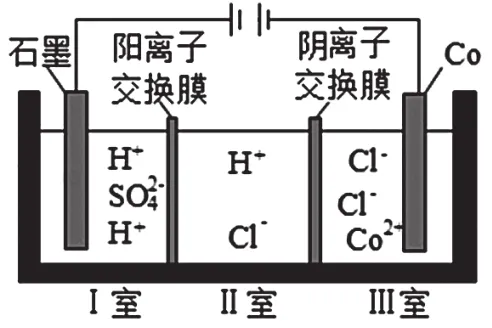
B.生成1mol Co,Ⅰ室溶液质量理论上减少16g
【解析】判断某一电极区溶液质量的变化,一般计算气体逸出或者金属单质、沉淀等固体生成所引起的溶液质量变化,但要注意由于离子移动而可能引起的质量增减。此题中,Ⅰ室实际为电解水2H2O-4e-=O2↑+4H+,逸出O2使溶液质量减少,但Ⅰ室Ⅱ室之间为阳离子交换膜,在Ⅰ室OH-放电的同时,产生的H+通过阳离子交换膜也会导致Ⅰ室溶液质量减少。所以计算时要注意,电解1molCo,由Co2++2e-=Co,转移电子数为2mol,消耗O2为0.5mol,且有2molH+进入Ⅱ室,共减少0.5mol×32g/mol+2mol×1g/mol=18g,故B错误。
解题思路:(1)书写电极反应式时,要根据电极生成物判断溶液中离子的种类;(2)准确判断溶液中各离子移动的方向,注意离子交换膜对离子的选择;(3)结合题目中电子转移的数目,判断离子移动的数目。
2.电极反应物及产物的定量计算问题
例3.K-O2电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电池,请判断选项D是否正确。
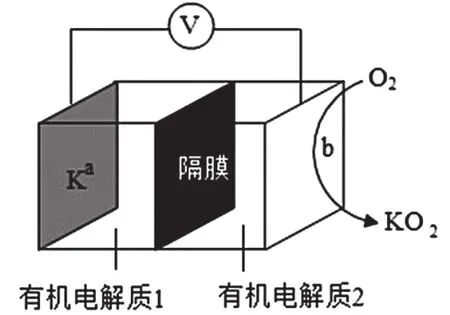
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
【解析】当电池给此装置充电时,两装置中转移电子相同,即根据电子得失守恒的思想进行定量计算。钾为原电池的负极反应物,此电池中负极反应为K-e-=K+,铅酸蓄电池充电时总反应为可知水与电子转移关系2H2O~2e-,即K~e-~H2O,n(H2O)=n(K)=0.1mol,消耗水的质量m(H2O)=nM=0.1mol×18g/mol=1.8g,故D错误。
例4.乙醛酸是一种重要的化工中间体,可采用如图所示的电化学装置合成。图中双极膜中间层中的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移。请判断选项C是否正确。
C.制得2mol乙醛酸,理论上外电路中迁移了1mol电子
【解析】首先分析乙醛酸的来源,其既是阳极区产物又是阴极区产物,根据阳极反应可知HOOC-COOH~2e-~HOH2C-CHO,阴极反应OHC-CHO~2e-~HOH2C-CHO,当制得2mol乙醛酸,根据两极电子得失守恒,阴极阳极各产生1mol乙醛酸,理论上外电路中迁移了2mol电子。故选项C不正确。
解题思路:(1)判断物质是电池哪一电极的反应物或生成物;(2)根据反应物和生成物的化合价变化,找出该物质与电子的定量关系或者直接写出电极反应式;(3)根据电子定量转移,联系两极反应或者两个电池装置进行计算。
3.陌生电池电极反应式的定量分析问题
例5.某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时Li+得电子成为Li嵌入该薄膜材料中;电极B为LiCoO2薄膜;集流体起导电作用。下列说法正确的是( )
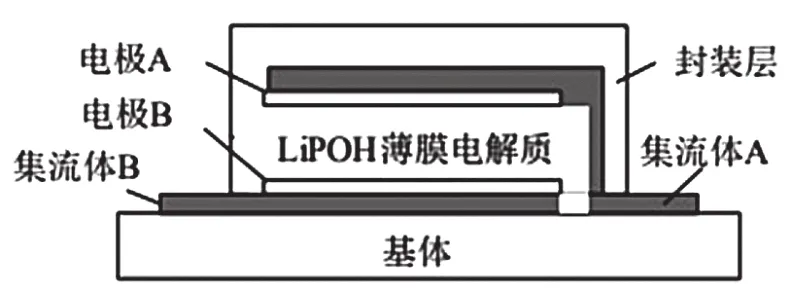
C.放电时,电极B为正极,反应可表示为Li1-xCoO2+xLi++xe-=LiCoO2
【解析】先根据题中信息分析,电极A为非晶硅薄膜,充电时Li+得电子成为Li嵌入该薄膜材料中,则电极A为阴极,反应物为Li+和Si,在书写电极反应式时注意Li元素守恒、电荷守恒,当转移x个电子时,有x个Li+参与反应,电极反应式为:xLi++xe-+Si=LixSi;电极B为阳极,反应物为LiCoO2,在电解质中移动的是Li+,所以电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+。电池总反应可表示为,D项正确。放电时电极B为正极,根据阳极电极反应式可知正极的电极反应式为Li1-xCoO2+xLi++xe-=LiCoO2,C项正确。
解题思路:(1)根据题中信息找出某一电极反应物和生成物;(2)根据电解质判断在电池中移动的离子及移动方向;(3)根据电极反应物和生成物的化合价变化判断电子得失,加入参与的离子实现反应式的电荷守恒或者元素守恒,正确书写电极反应式;(4)对于二次电池,阳极反应式对应正极反应式,阴极反应式对应负极反应式;(5)使两极反应式中得失电子数相等,阴极和阳极反应式相加或者负极和正极反应式相加可得到总反应式。
电化学的解题模型从宏观上,要结合相关现象如电流方向判断电子等微观粒子的运动方向,根据物质相关性质进行推断,如氧化性和还原性的强弱、得失电子的先后顺序等;微观上,要从元素守恒、得失电子守恒、电荷守恒等方面,认识化学反应过程中电子、离子及物质之间的定量关系。
