不同产地白肉灵芝的重金属含量与毒性评价
2021-12-31侯朝祥金鹏程吴昕怡
潘 俊,田 浩,曲 媛,侯朝祥,金鹏程,吴昕怡,李 宏*
(1.云南省农业科学院农产品加工研究所,云南 昆明 650223;2.昆明理工大学生命科学与技术学院,云南 昆明 650091)
【研究意义】灵芝具有滋补强壮、扶正培本的功效,有两千多年的使用历史[1-3]。灵芝作为药材收载于2015年版《中国药典》,其法定中药材为赤芝(Ganodermalucidum) 与紫芝(Ganodermasinensis) 的干燥子实体,而其它品种的灵芝未被收录。白肉灵芝(Ganodermaleucocontextum)为多孔菌科灵芝属大型真菌,是中国西南地区的一个重要灵芝种类[4]。灵芝的安全性是食品开发中面临的首要问题。赤芝和紫芝的安全性使毋庸置疑的,已被国家卫计委列入保健食品名单,但白肉灵芝的安全性尚未见报道,缺乏相关领域的研究。【前人研究进展】白肉灵芝属于灵芝属中的罕见低温型种类,经多年选育,已获得稳定性强、代谢能力高、安全性高的白肉灵芝人工栽培品[5]。目前,针对白肉灵芝的研究主要集中于生物学鉴定[6]、化学成分[7]及药理活性作用[8]等方面,但白肉灵芝安全性研究尚属空白。而对重金属的富集是真菌类食品最大的安全隐患,据报道,灵芝富集重金属能力强,且富集于菌盖、菌柄不同部位,易富集镉、砷等[9-11]。灵芝中重金属的污染及其含量与生长环境密切相关,铅、镉、汞、砷等重金属元素的摄入对人体有毒害作用,甚至引发神经系统疾病[12-13]。目前《中国药典》2020版已对重金属元素进行限量要求,同时灵芝中重金属的含量测定已有文献报道[14-15],灵芝中镉超标率较高[11]。【本研究切入点】灵芝对于重金属的富集存在很大的安全风险,因此,白肉灵芝中重金属含量的测定与评估对其安全性评价十分重要。【拟解决的关键问题】本文以白肉灵芝为研究对象,测定白肉灵芝中铅(Pb)、镉(Cd)、汞(Hg)、砷(As)4种重金属含量,依据国际通用风险评估模式对健康风险进行评估,并对其进行毒理学安全性评价研究,为白肉灵芝的质量安全提供判定依据,为白肉灵芝的进一步开发利用提供科学依据。
1 材料与方法
1.1 实验动物
SPF级昆明种小鼠40只(18~22 g/只,雌雄各半),由昆明医科大学实验动物学部提供,实验动物生产许可证:SCXK(滇)K2015—0002。
1.2 试剂与耗材
云南白肉灵芝(Ganodermaleucocontextum)由云南省农业科学院生物技术与种质资源研究所提供(表1)。汞单元素标准溶液(1000 μg/mL,批号:GBW08617 9041)、铅单元素标准溶液(1000 μg/mL,批号:GBW08619 8061)、镉单元素标准溶液(1000 μg/mL,批号:GBW08612 7063)均购于中国计量科学研究院;砷单元素标准溶液 [1000 μg/mL,GSB G 62028—90(3302),批号:09051132]购于国家钢铁材料测试中心钢铁研究总院。
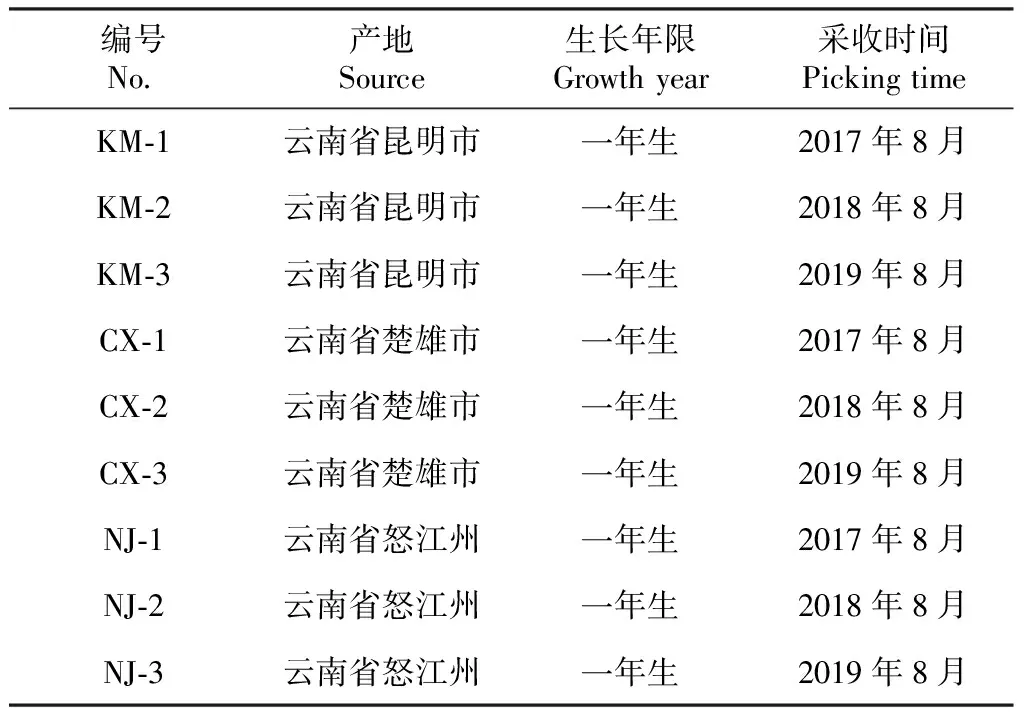
表1 白肉灵芝样品信息
1.3 仪器
PEAA800原子吸收光谱仪(珀金埃尔默股份有限公司);AFS-9230原子荧光光度计(北京吉天仪器有限公司);Mars6 微波消解仪(美国培安公司);BS-280全自动血液生化分析仪(深圳迈瑞生物医疗电子股份有限公司);AUY220电子天平(日本岛津公司);R-200旋转蒸发仪(Buchi 公司);ALPHA 1-4 LSC冷冻干燥机(Christ 公司)。
1.4 方法
1.4.1 对照品制备 按食品安全国家标准的检测方法分别用超纯水将汞(Hg)标准液稀释为0.20、0.50、1.00、1.50、2.00、2.50 ng/mL,镉(Cd)标准液稀释为0.50、1.00、1.50、2.00、3.00 ng/mL,铅(Pb)标准液稀释为5.00、10.00、20.00、30.00、40.00 ng/mL,砷(As)标准液稀释为4.00、10.00、20.00、60.00、120.00 ng/mL系列标准溶液备用。
1.4.2 供试品制备 精密称取0.2 g白肉灵芝样品置于微波消解罐中,加入硝酸5.0 mL混匀,在微波消解仪中进行消解,然后在电热板上于140 ℃赶酸至1 mL左右备用。
1.4.3 线性关系考察 将各重金属元素的系列标准溶液进行测定,以吸光度C为横坐标,浓度A为纵坐标,绘制标准曲线。结果显示各重金属组分线性关系良好,相关系数都大于0.99,符合要求,见表2。
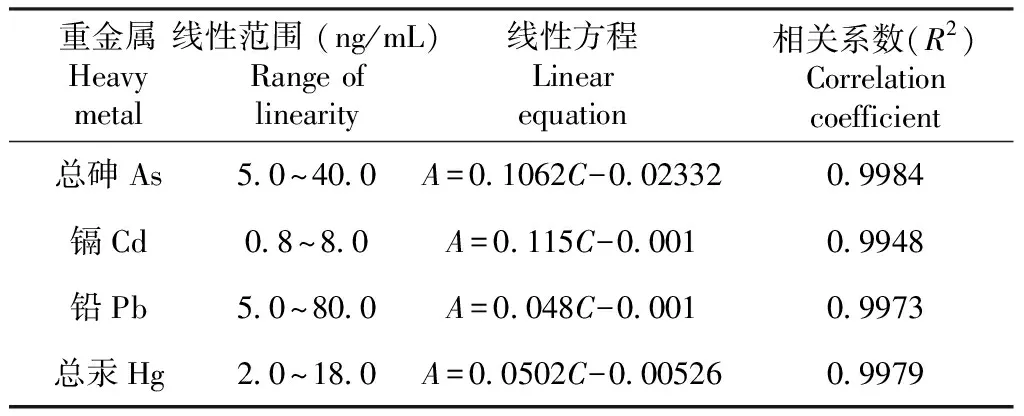
表2 重金属检测线性关系考察
1.4.4 精密度试验 分别取铅标准溶液(80 ng/mL)、砷标准溶液(40 ng/mL)、镉标准溶液(8.0 ng/mL)、汞标准溶液(18 ng/mL)连续进样6次,按其吸光度计算RSD。试验结果显示4种重金属平均吸收度的RSD均不超过1.00%,精密度良好。
1.4.5 回收率试验 制备已知含量的供试品溶液各6份,分别精密加入相应标准品,稀释一定倍数后按相应方法测定,计算回收率。试验结果显示4种重金属平均回收率在96%~103%,RSD值在2%~6%,回收率良好。
1.4.6 含量测定 参照食品安全国家标准进行,其中铅(参照GB 5009.12—2017)、镉(参照GB 5009.15—2014)采用石墨炉原子吸收光谱法进行检测,总砷(参照GB 5009.11—2014)、总汞(参照GB 5009.17—2014)采用原子荧光光谱法进行检测。
1.5 健康风险评估
采用美国环保署(USEPA)提出的人体暴露健康风险评价模型,靶标危害系数法 (Target hazard quotients,THQ),评估人体每日白肉灵芝摄入的重金属所带来的健康风险[16]。
THQ=(EF×ED×M1×CM/RfD×BW×AT)×10-3
(1)
式中,EF为每年暴露于毒物(白肉灵芝)的天数(d/a);ED为暴露于毒物(白肉灵芝)的年数(a);M1为白肉灵芝中重金属含量(mg/kg);CM为白肉灵芝每日摄入量;RfD为口服参考剂量(mg/kg);BW为人体平均体重(kg);AT为平均暴露时间(d)。
采用危害指数HI综合评估多种重金属非致癌风险。
HI=THQPb+THQCd+THQHg+THQAs
(2)
式中,THQPb是Pb的靶标危害系数;THQCd是Cd的靶标危害系数;THQHg是Hg的靶标危害系数;THQAs是As的靶标危害系数。
1.6 小鼠急性经口毒性实验
白肉灵芝样品粉碎后称取100 g置烧瓶中,加入蒸馏水700 mL,回流1 h,提取2次,浓缩后冻干备用,即为白肉灵芝水提物(GLE)。按照GB 15193.3—2014食品安全国家标准急性经口毒性试验中最大耐受量法(MTD)进行实验。分2组,阴性对照组、GLE组,每组20只(雌雄各半),小鼠禁食6 h后,提取物按15.0 g/kg的剂量给药,将样品加水制成400 mg/mL的溶液灌胃2次(间隔4 h),观察14 d,记录动物中毒表现和死亡情况。
1.7 小鼠亚急性毒性实验
1.7.1 分组与给药 将小鼠按体重随机分为阴性对照组、GLE低、中、高剂量组(1.0、2.0、3.0 g/kg),共4组,每组共12只,雌雄各半。阴性对照组灌胃给予相应体积的纯净水,GLE低、中、高剂量组灌胃给予相应浓度的GLE药液,连续给药30 d。
1.7.2 指标测定 给药期间,每天观察记录动物出现的毒性反应,分别于给药当天、给药第7、14、21、28天称取动物体重并记录;末次给药2 h后,眼眶采血分离血清,进行白细胞(WBC)、红细胞(RBC)、血红蛋白(HGB)、谷丙转氨酶(ALT)、谷草转氨酶(AST)、总蛋白(TP)、白蛋白(ALB)、肌酐(CREA)指标测定。眼眶采血后迅速摘取心脏、肝脏、脾脏、肾脏称重尿素(UREA),并计算脏器系数。
脏器指数(%)=脏器质量/小鼠体重×100
(3)
1.8 数据处理
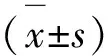
2 结果与分析
2.1 不同产地白肉灵芝的重金属含量
云南3个不同产地(昆明、楚雄、怒江3个地区)白肉灵芝中的砷、镉、铅的含量分别为0.16~0.22、0.15~0.50、0.07~0.18 mg/kg(表3),均符合食品安全国家标准GB 2762—2017关于食用菌及其制品的规定以及国际食品法典委员会关于罐装的蘑菇的规定(表4)。欧盟对食用菌(鲜品)中镉含量的规定为≤0.2 mg/kg,对比检测的9批次白肉灵芝中镉含量超标的有60%,仅有楚雄地区的白肉灵芝符合欧盟标准。此外,汞在白肉灵芝中的含量均小于检测最小值(0.01 mg/kg),未检出,与文献报道的灵芝中汞的含量一致[14]。
2.2 不同产地白肉灵芝的健康风险评估
基于云南白肉灵芝中的铅、镉、汞、砷4种重金属的含量,采用靶标危害系数法(Target hazard quotients,THQ)对经白肉灵芝途径摄入重金属对人体健康产生的危害风险进行分析,依据参考文献对各项参数进行取值,见表5。其中,白肉灵芝摄入率(CM)以最大摄入量(12 g/d)计算。以此为依据,计算通过食用菌途径进入人体重金属Pb、Cd、As和Hg的THQ和综合危险指数(HI)值,见表6。4种重金属的THQ大小为:As>Cd>Pb>Hg,各样品值均<1。从HI平均值来看,不同地区白肉灵芝的HI值,昆明>楚雄>怒江,各样品值均<1。以上数据表明,经白肉灵芝途径的重金属摄入水平在安全限值之内,通过云南白肉灵芝摄入的重金属对人体没有安全风险。

表3 云南不同产地白肉灵芝中重金属含量

表4 不同国家或组织中草药的重金属限量规定
2.3 白肉灵芝的急性毒性
小鼠灌胃给予白肉灵芝提取物(GLE)后,观察14 d,各组动物饮食活动正常,生长良好,未见任何中毒表现,无死亡,见表7。解剖检查,肝脏、脾脏、肾脏、心脏、肺、胃、肠等主要器官,均未见明显异常改变。急性毒性试验中,白肉灵芝水提物对2种性别小鼠的经口最大耐受剂量(MTD)均大于15.00 g/kg。根据急性毒性分级,白肉灵芝提取物属无毒级。按体重60 kg,推荐服用剂量(6 g/d)计,相当于0.1 g/kg的服用量,而生药量MTD远远高于推荐服用量的100倍。
2.4 白肉灵芝的亚急性毒性
2.4.1 体重 以1.00、2.00、3.00 g/kg剂量的白肉灵芝提取物(GLE)分别喂养小鼠,连续30 d,见表8。与阴性对照组相比,给药各剂量组小鼠体重增长无明显变化,无统计学差异(P>0.05),说明白肉灵芝水提物对小鼠生长发育无影响。
2.4.2 脏器系数 脏器系数是毒理实验中的常用指标,可反映毒物对机体的损伤程度。白肉灵芝提取物对小鼠脏器的影响,见表9。白肉灵芝提取物给药组与阴性对照组相比,心、肝、脾、肾的脏器系数无明显变化,与阴性对照组相比无显著性差异(P>0.05),表明小鼠经给药后,脏器未受影响。
2.4.3 血液学指标 白肉灵芝提取物对小鼠血细胞的影响,见表10。白肉灵芝提取物GLE低剂量组对小鼠的红细胞数、白细胞数及血红蛋白含量均未产生不良影响;GLE中、高剂量组小鼠的白细胞、红细胞数量略有降低,血红蛋白略有上升,但与阴性对照组相比均无显著性差异(P>0.05)。

表5 白肉灵芝中重金属对人体健康风险计算参数取值
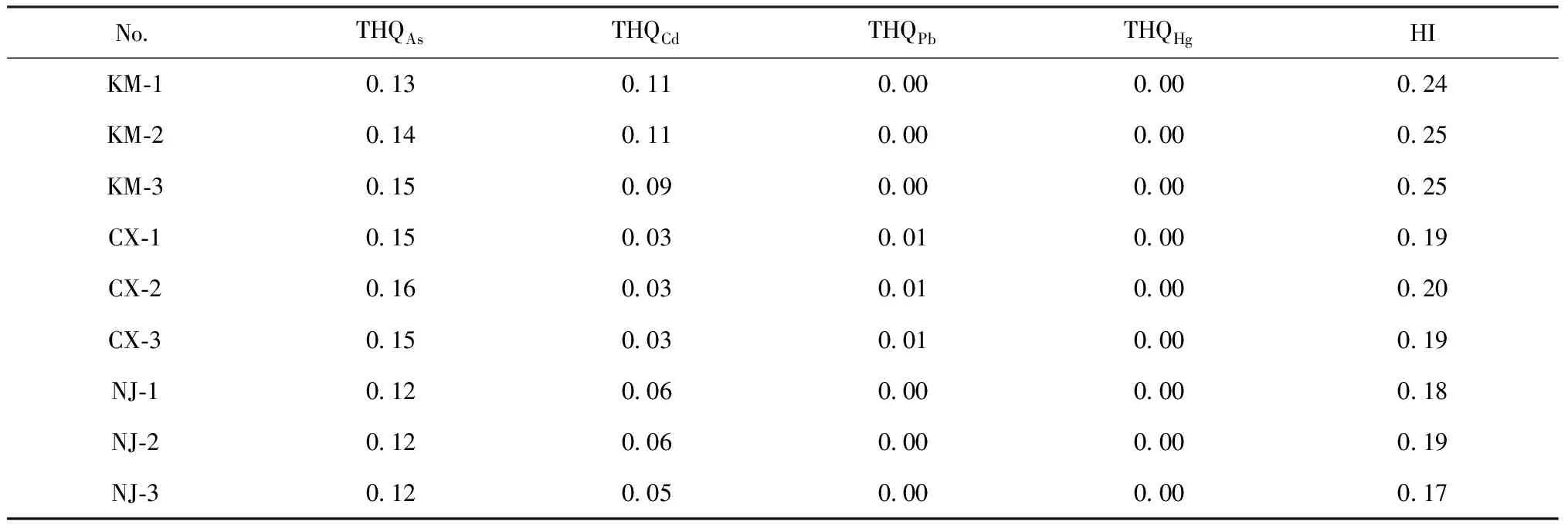
表6 白肉灵芝重金属摄入健康风险评估值
2.4.4 血液生化指标 血液生化指标能够反映机体的健康状况,为疾病诊断提供可靠依据[21]。经连续给药白肉灵芝提取物30 d后,给药组与阴性对照组相比,各剂量组小鼠中谷丙转氨酶(ALT)、谷草转氨酶(AST)、总蛋白(TP)、白蛋白(ALB)、肌酐(CREA)等6项生化指标均无明显差异(P>0.05),见表11,表明白肉灵芝提取物对小鼠机体无明显有害影响。
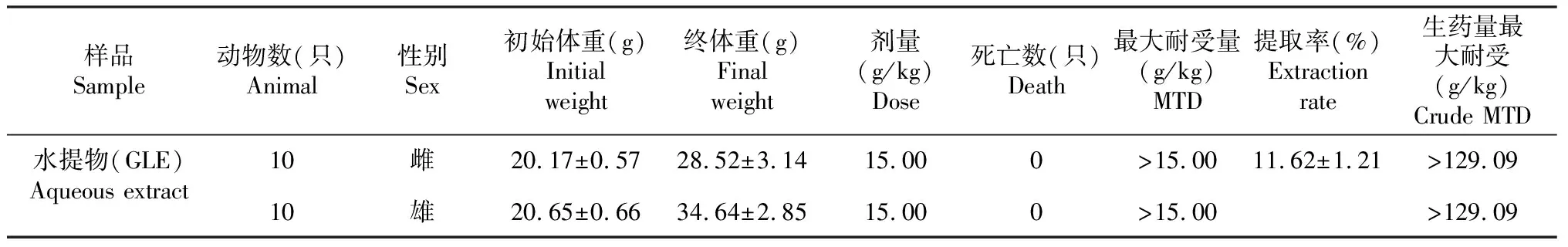
表7 白肉灵芝提取物对小鼠急性经口毒性试验结果
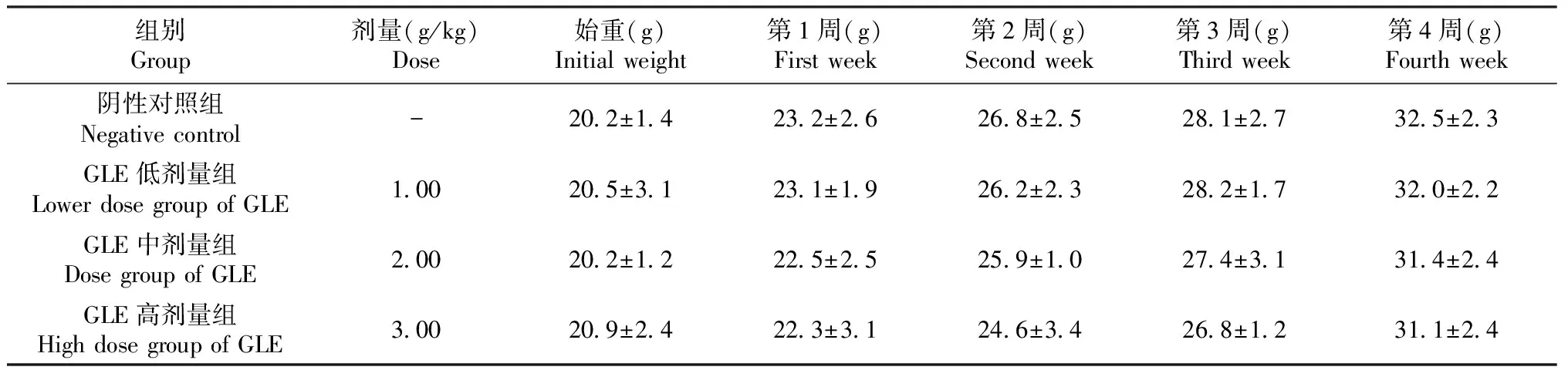
表8 白肉灵芝提取物对小鼠体重的影响

表9 白肉灵芝提取物对小鼠各脏器系数的影响

表10 白肉灵芝提取物对小鼠血细胞的影响
3 讨 论
农产品重金属超标问题已引起全社会的广泛关注。灵芝具有富集重金属的能力,易富集Pb、Cd、Hg、As等元素[9-10]。谢宝贵等[22]发现随着重金属元素浓度增加,其在灵芝菌丝体内的含量显著增加,其富集性能力为Pb>Cd >Hg >As。灵芝[23]在菌丝体阶段对Pb表现出明显的富集作用,而在子实体阶段对Pb的累积作用却不明显。这说明灵芝菌丝体和子实体对重金属具有不同的富集特性。王怀豫等[24]检测不同产地灵芝子实体重金属含量,发现虽检出一定量的有害重金属,但含量较低,未超出国家限量标准,符合《药用植物及制剂进出口绿色行业标准》的有关规定。胡晓等[25]发现不同产地灵芝孢子粉之间的重金属含量均无较大差异,且未破壁与破壁孢子粉之间的重金属含量也无较大差异。云南白肉灵芝中重金属含量研究未见报道。笔者根据食品安全国家标准GB 2762—2017关于食用菌及其制品的规定要求,本研究连续3年对云南省3个产地白肉灵芝中Pb、Cd、Hg、As含量进行监测,均未超标。
灵芝在中国已有2000多年的食用历史,素有“仙草”之誉,在《神农本草经》中灵芝被列为上品(可久服、无毒);明朝时李时珍在《本草纲目》中将灵芝移入菜部(可食用)[26]。2019年国卫食品函(2019)311号文件将灵芝(赤芝和紫芝)列入食药同源试点名单。中国有灵芝属103个种灵芝资源,药用的有23种,如赤芝、薄盖灵芝、菌草灵芝等,但迄今为止未发现灵芝及其制品安全性的负面报道,在日本、韩国、台湾、香港、东南亚等国家和地区灵芝也被广泛用于食品行业[27-30]。目前白肉灵芝的毒理学安全性研究尚未有报道,本研究对小鼠急性、亚急性毒性试验结果表明,白肉灵芝提取物对实验小鼠的活动、体重、白细胞数、红细胞数、血红蛋白含量、脏器系数及肝肾代谢产物均未产生不良影响。可见,白肉灵芝提取物的安全性高,本研究为白肉灵芝的后续开发利用奠定了基础。
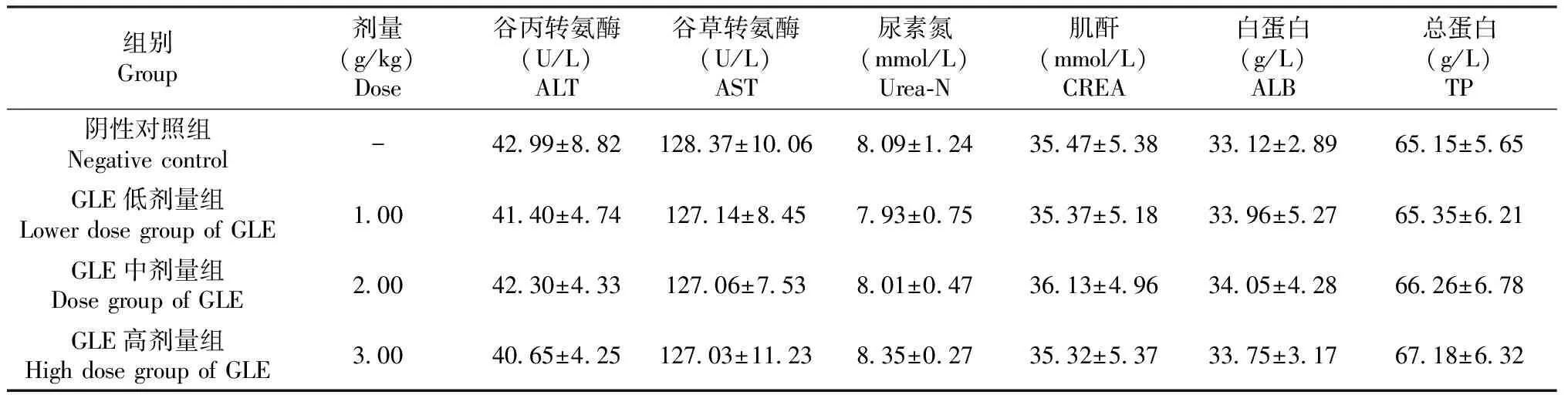
表11 白肉灵芝提取物对小鼠生化指标的影响
4 结 论
云南省3个产地(昆明、楚雄、怒江)的白肉灵芝中的砷、镉、铅的含量分别为0.16~0.22、0.15~0.50、0.07~0.18 mg/kg,均未超标。而汞在白肉灵芝中的含量低于检测限(0.01 mg/kg),未检出。采用靶标危害系数法对重金属研究结果进行评估表明,经白肉灵芝途径的重金属摄入水平在安全限值之内,对人体没有安全风险。根据急性、亚急性毒性试验结果,白肉灵芝提取物对雌雄小鼠经口最大耐受剂量均>15 g/kg,属无毒级物质。
