CC/TiO2/Ag@AgCl复合材料的制备及其光催化性能研究
2021-12-30陈凤华石向东梁娓娓杨茂森凡文蕊陈庆涛姜利英
陈凤华,石向东,梁娓娓,杨茂森,凡文蕊,陈庆涛,姜利英
1.郑州轻工业大学 材料与化学工程学院, 河南 郑州 450001;
2.郑州轻工业大学 电气信息工程学院, 河南 郑州 450002
0 引言
近年来,随着工业的高速发展和人口的快速增长,人类生存环境受到了严重的威胁,特别是水污染问题亟待解决. 光催化降解是指半导体材料吸收光辐射后产生的高活性自由基与废水中的有机物发生氧化还原反应使之降解为无机物的过程,具有清洁、高效、无二次污染等优点,是一种解决水污染问题经济有效的技术[1].
在众多的半导体光催化材料中,二氧化钛(TiO2)因化学性质稳定、催化活性高、价格低廉、无毒无污染等优点而受到广泛关注[2-3]. 但是TiO2属于宽禁带半导体材料,其优异的光催化性能只能在紫外光照射下才能被激发,而电子-空穴对的高复合速率等因素限制了其在可见光能量约占43%的太阳光中的广泛应用[4-5]. 为了改善上述不足,研究者对TiO2进行了多种改性,以达到拓宽其可见光区的吸收范围、抑制光生电子-空穴对的快速复合、提高光催化降解性能的目的. 由已报道文献可知,通过贵金属Au、Ag、Pd等的沉积[6-8],与半导体CdS,ZnO,WO3等的复合[9-11],C、N、P等非金属元素的掺杂[12-14],以及与具有代表性可见光型的Bi基[15-16]、Ag基[17-19]等半导体催化剂形成异质结,均可以不同程度地提高TiO2的光催化效率. 此外,将催化剂负载在特定的基底材料表面,可提高催化剂与污染物的接触面积,改善催化剂的吸附性能,这也是进一步提高光催化效率和解决粉体催化剂难分离回收问题行之有效的方法[20-21].
碳布(Carbon Cloth, CC)耐腐蚀性强,比表面积大,具有优良的导电性和透光率,加之稳定性良好、易分离等特性和有利于半导体原位生长的高孔隙率[22],使CC成为较好的负载吸附剂和光催化剂的基底材料[23],但是目前鲜见关于CC作为光催化材料载体的文献报道.
鉴于此,本研究拟以CC为基底材料,首先通过化学偶联法在其表面负载TiO2纳米粒子,然后依次通过原位沉积法和光致还原法在CC/TiO2复合材料表面进一步负载可见光光催化剂Ag@AgCl,得到CC/TiO2/Ag@AgCl复合光催化材料,并研究其吸附-光催化降解性能、光电性能等,以期获得一种易分离且可循环利用的高效可见光催化降解水中染料的催化材料.
1 材料与方法
1.1 主要材料、试剂与仪器
主要材料与试剂:CC(型号为WOS1002),台湾碳能科技公司产;Ti(C4H9O)4(纯度≥99%)、三乙氧基氨丙基硅烷(APTES, 纯度≥98%)、NH3·H2O(体积分数为25%),上海阿拉丁生化科技公司产;1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDCl, 纯度>98.5%)、C2H2ClNaO2(纯度≥98%)、N-羟基琥珀酰亚胺(NHS, 纯度>98%),上海麦克林生化科技公司产;Na2SO4、KCl、K3[Fe(CN)6]、K4[Fe(CN)6]·3H2O等均为分析纯,均购于国药集团化学试剂有限公司,使用前未做任何处理.
主要仪器:JSM-6490LV型扫描电子显微镜,日本JEOL公司产;D/max 2500型X-射线衍射仪,日本RIGAKU公司产;ESCALAB 250Xi型X-射线光电子能谱仪,美国Thermo公司产;LabRam HR 800型共聚焦显微镜拉曼光谱仪,法国HORIBA Jobin Yvon公司产;Hitachi U-3900H型紫外可见光谱仪、F-4600型荧光光谱仪,日本HITACHI公司产;PLS-SXE300BF型氙灯光源,北京泊菲莱科技有限公司产;CHI 660D型电化学工作站,上海辰华仪器有限公司产.
1.2 CC/TiO2/Ag@AgCl复合光催化材料的制备
1)CC的活化与修饰. 为进一步增加碳纤维表面含氧官能团含量和表面粗糙程度,提高浸润性使复合材料界面紧密连接,本研究利用HNO3的刻蚀扩孔作用[24-25]对CC进行活化处理,具体过程如下:将2 cm×2 cm CC依次置入丙酮、乙醇和去离子水中,分别超声清洗20 min,用去离子水清洗3遍后,将其放入盛有25 mL HNO3溶液(浓度为3 mol/L)的反应釜内,在120 ℃水热条件下反应2 h, 反应结束并冷却至室温后,将CC取出,用蒸馏水冲洗3遍后,再次放入30 mL去离子水中,依次加入2 g NaOH和2 g C2H2CINaO2,超声反应2 h,得到表面羧基化的CC(CC-COOH).
2) TiO2纳米粉末的制备. 首先,将5 mL Ti(C4H9O)4溶于35 mL无水乙醇中,超声处理10 min;然后,加入20 mL乙醇/水混合溶液(体积比为5∶1),于40 ℃条件下磁力搅拌反应1 h后进行离心分离,依次用乙醇和去离子水清洗沉淀2遍,于60 ℃烘箱中烘干;最后将烘干后的物质置于500 ℃马弗炉中煅烧 1 h,即得TiO2纳米粉末.
3) CC/TiO2复合材料的制备. 首先,取20 mg TiO2纳米粉末超声分散于24 mL乙醇/水混合溶液(体积比为5∶1)中,加入1 mL NH3·H2O和100 μL APTES,室温下搅拌反应24 h后进行离心分离,依次用乙醇和去离子水清洗沉淀3遍;然后,将得到的经氨基修饰的TiO2纳米粒子(TiO2-NH2)超声分散于10 mL EDC/NHS混合水溶液(含有20 mg EDCl和16 mg NHS)中,加入一定量的CC-COOH,继续超声反应2.5 h后,于常温下继续搅拌反应48 h;最后,将所得物质依次用乙醇和水清洗3遍,于60 ℃烘箱中烘干,即得CC/TiO2复合材料.
4) CC/TiO2/Ag@AgCl复合材料的制备. 将制备的CC/TiO2复合材料放入20 mL AgNO3/乙醇混合溶液(浓度为0.05 mol/L)中浸泡30 s,取出后再放入20 mL NaCl(浓度为0.02 mol/L)溶液中浸泡30 s. 循环5次后,将生成的CC/TiO2/AgCl复合材料于400 W汞灯下照射1 h, 即得CC/TiO2/Ag@AgCl复合材料,同时收集溶液中的Ag@AgCl纳米粒子沉淀,用于光催化降解性能的对比实验. CC/TiO2/Ag@AgCl复合材料的合成流程如图1所示.
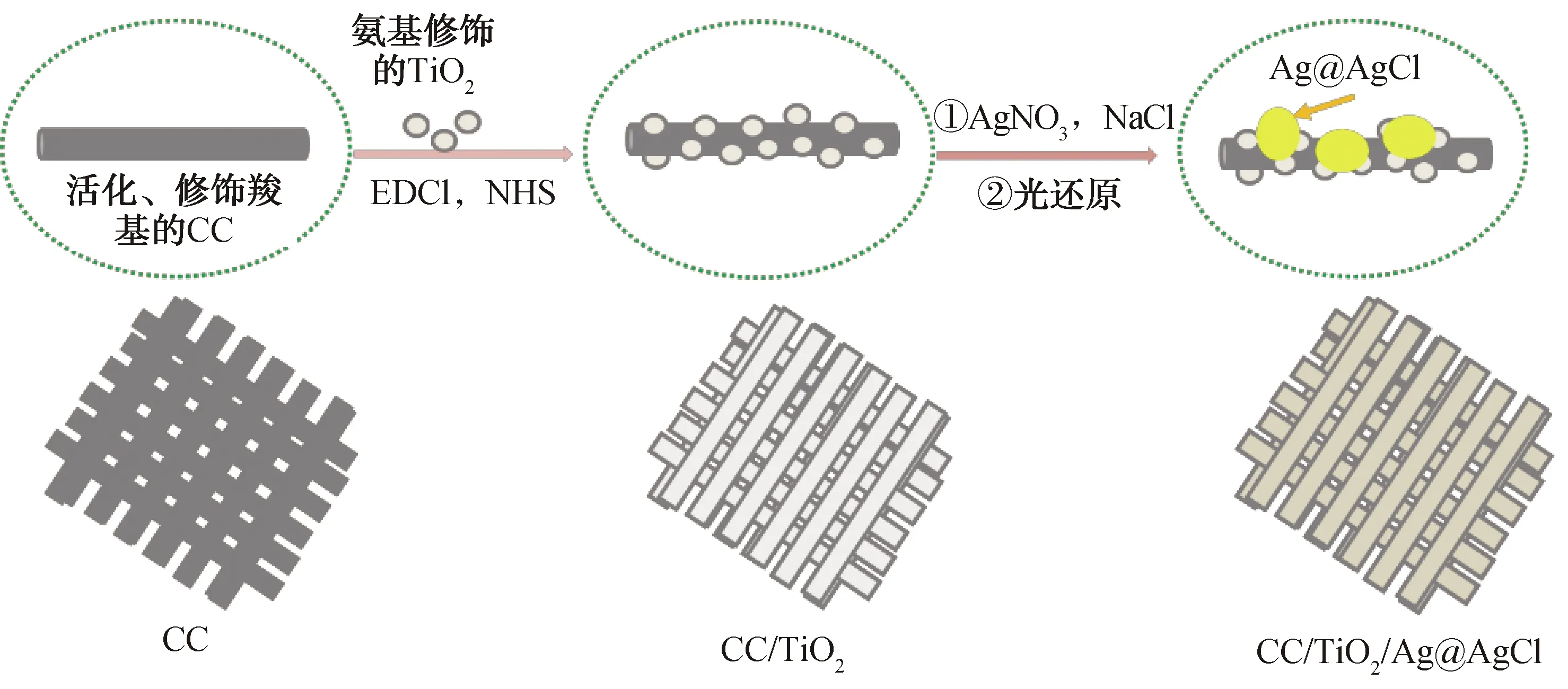
图1 CC/TiO2/Ag@AgCl复合材料的合成流程图Fig.1 Experimental flowchart of the synthesis of CC/TiO2/Ag@AgCl composite material
1.3 CC/TiO2/Ag@AgCl复合材料的形貌和结构表征
采用扫描电子显微镜对复合材料的形貌进行表征,加速电压为0.5~30 kV;利用X-射线衍射仪测试材料的晶型结构,Cu靶Kα辐射线(λ=0.154 05 nm), 测试电压为40 kV,电流为20 mA,扫描速率为2°/min;使用X-射线光电子能谱仪(XPS)分析材料的化学态,单色Al Kα (hv=1 486.6 eV),功率150 W,束斑500 μm,结合能以C1s(284.8 eV)峰进行校准;通过共聚焦显微镜拉曼光谱仪在激发光波长为532 nm的条件下采集样品的拉曼(Raman)光谱;采用紫外可见光光谱仪(波长范围200~800 nm,波长精度0.1 nm)和荧光光谱仪(激发波长为366 nm,激发和发射狭缝为5 nm)进行紫外-可见光(UV-Vis)光谱吸收和荧光(PL)光谱测试.
1.4 CC/TiO2/Ag@AgCl复合材料的光催化性能测试和活性物质的确定
将10 mg CC/TiO2/Ag@AgCl复合材料与50 mL质量浓度为10 mg/L的RhB溶液混合后,将混合液先在暗处磁力搅拌30 min,再将反应液置于500 W氙灯光源下进行光降解反应,光源距离液面约15 cm,每隔一定时间取一次溶液样品并测定UV-Vis光谱,根据溶液样品在553 nm处的吸光度实时评价RhB的光催化降解进程.
以上述方法重复进行6次复合材料的光催化性能测试,以评价其光催化稳定性.
光催化降解反应过程中活性物质的确定实验,是在上述光催化降解实验的基础上,分别于RhB溶液中加入1 mL浓度为2 mmoL/L的自由基清除剂(异丙醇、对苯醌、EDTA-2Na).
1.5 CC/TiO2/Ag@AgCl复合材料的电化学性能测试
以CC/TiO2/Ag@AgCl复合材料为工作电极,铂电极和饱和Ag/AgCl电极分别作为对电极和参比电极,使用传统的三电极电池系统和电化学工作站对该复合光催化材料进行电化学性能测试,外照光源为Phillips 500 W的 Xe灯. 光电流(I-t)在Na2SO4电解质溶液(浓度为0.1 mol/L)中测量;电化学阻抗谱(EIS)在由KCl(0.1 mol/L), K3[Fe(CN)6](5 mmol/L)和K4[Fe(CN)6]·3H2O (5 mmoL/L)组成的电解质溶液中测得.
2 结果与讨论
2.1 复合材料的形貌分析
图2为不同放大倍数下CC/TiO2和CC/TiO2/Ag@AgCl复合材料的SEM图. 从图2可以看出,TiO2纳米粒子成功地负载在了CC表面,并且分布较均匀,进一步负载Ag@AgCl后,CC的表面又出现大量粒径不均匀、衬度比较亮的Ag@AgCl粒子.
图3为CC/TiO2/Ag@AgCl复合材料的EDS能谱图及其各元素面扫描分布图. 由图3可以看出,该复合光催化材料表面由元素C、Ti、O、Ag、Cl组成,结合图2可知,CC/TiO2/Ag@AgCl复合光催化材料已成功制备.

图2 不同放大倍数下CC/TiO2和CC/TiO2/Ag@AgCl复合材料的SEM图Fig.2 SEM images of CC/TiO2 and CC/TiO2/Ag@AgCl composite material with different magnification

图3 CC/TiO2/Ag@AgCl复合材料的EDS能谱图及其各元素面扫描分布图Fig.3 EDS spectra of CC/TiO2/Ag@AgCl composite material and the scanning distribution of each element plane
2.2 复合材料的结构分析
图4为CC/TiO2/Ag@AgCl复合材料的XRD谱图. 由图4可以看出,2θ=25.5°、43.6°处的衍射峰源于CC中石墨化碳的特征峰,2θ=25.9°(与碳布的衍射峰重叠)、 36.9°、48.1°、62.7°处的衍射峰归属于锐钛矿晶型TiO2(JCPDS 21-1272)的特征峰. 除了CC和锐钛矿TiO2的衍射峰外,在2θ=37.7°、 43.7°、64.2°、77.0°处及2θ=29.5°、31.8°、45.8°、57.1°处还出现了分别归属于Ag 和AgCl的特征峰,分别对应于Ag的(111),(200),(220)和(311)晶面和AgCl的(111),(200),(220)和(222)晶面,进一步表明了CC/TiO2/Ag@AgCl复合光催化材料的成功制备.
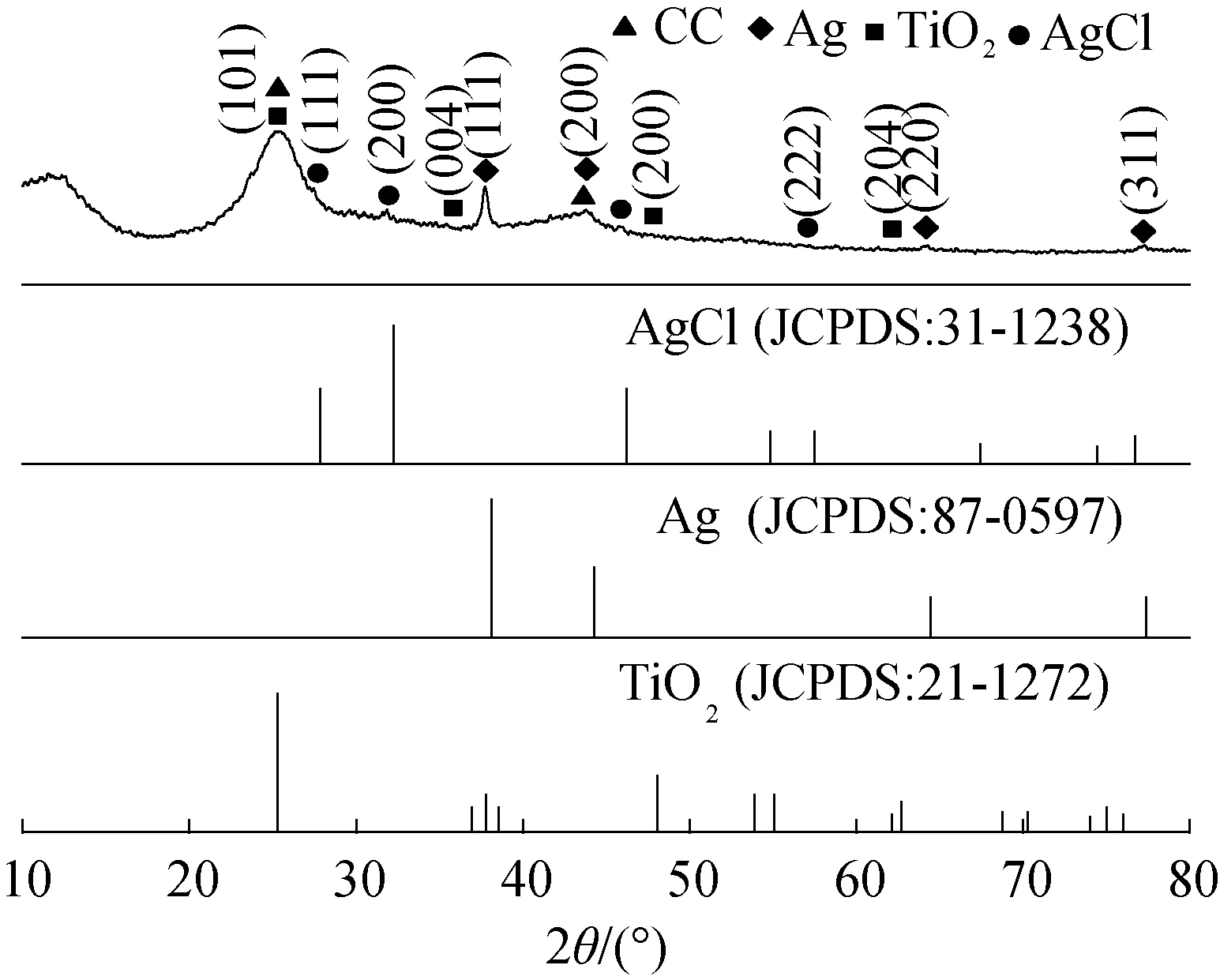
图4 CC/TiO2/Ag@AgCl复合材料的XRD谱图Fig.4 XRD patterns of CC/TiO2/Ag@AgCl composite material
图5为CC,TiO2和CC/TiO2/Ag@AgCl复合材料的Raman谱图. 由图5a)可以看出,位于1345 cm-1与1589 cm-1处的峰分别为CC的D带(A1g)峰和G带(E2g)峰,前者源于C材料中的缺陷结构,后者体现了C材料的石墨化程度,通过计算可得CC的ID/IG=1.03,说明活化后的CC缺陷程度相对较高,有利于电子的传输;位于143 cm-1,396 cm-1,516 cm-1和635 cm-1处的峰分别归属于TiO2的A1g、 B2g、B1g和A1g的拉曼特征峰. 由图5b) 可以看出,CC/TiO2/Ag@AgCl复合材料的Raman谱图中出现明显的CC和TiO2的拉曼特征峰,并且由于Ag的拉曼增强效应,CC/TiO2/Ag@AgCl复合材料中C和TiO2的拉曼特征峰强度明显增大.
2.3 复合材料的化学态分析

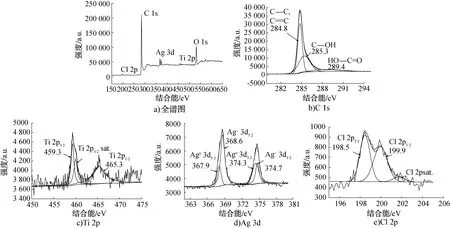
图6 CC/TiO2/Ag@AgCl复合材料的XPS谱图Fig.6 XPS spectra of CC/TiO2/Ag@AgCl composite material
2.4 复合材料的紫外-可见光光谱分析
图7为TiO2、Ag@AgCl和CC/TiO2/Ag@AgCl复合材料的紫外-可见光吸收光谱. 由图7可以看出,TiO2的吸收峰主要集中在紫外光区域,而CC/TiO2/Ag@AgCl复合材料在小于420 nm 的紫外光区域和420~700 nm的可见光区域内都有较强的吸收峰,这主要归因于Ag纳米粒子的等离子体共振效应使AgCl的光响应范围从紫外光区域扩展到了可见光区域,有利于提升CC/TiO2/Ag@AgCl复合材料的可见光光催化降解污染物的性能.
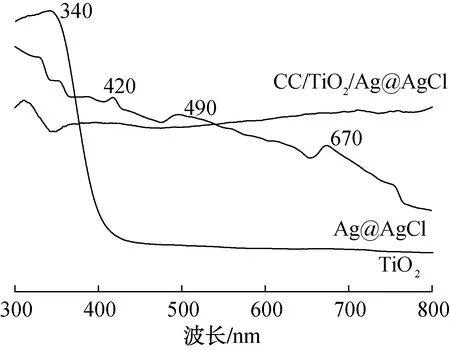
图7 TiO2、Ag@AgCl和CC/TiO2/Ag@AgCl复合材料的紫外-可见光吸收光谱Fig.7 Uv-Vis spectra of TiO2、Ag@AgCl and CC/TiO2/Ag@AgCl composite material
2.5 复合材料的吸附-光催化降解性能分析
图8为CC/TiO2/Ag@AgCl复合材料对有机染料RhB的吸附-光催化降解性能曲线(其中,C0为初始溶液的RhB浓度,Ct为t时刻的RhB浓度). 由图8a)可以看出,在无催化剂的情况下,RhB的光照自降解因素可以忽略不计. 以CC/TiO2/Ag@AgCl复合材料为光催化剂时,120 min内对RhB的紫外-可见光催化降解率可达96.9%,高于TiO2的83.8%和Ag@AgCl的78.6%. 黑暗条件下CC/TiO2/Ag@AgCl复合材料对RhB的吸附实验结果表明,在20 min和120 min内,CC/TiO2/Ag@AgCl复合材料对RhB的吸附量分别为39.5%和53.2%,与其光照条件下的降解过程进行对比可以看出,光照条件下RhB溶液浓度下降的速度比在黑暗条件下快,说明所制备的CC/TiO2/Ag@AgCl复合材料对RhB具有较好的吸附-光催化降解协同效应,有望实现对有机染料的高效去除. 由图8b)可以看出,3种催化剂光催化降解RhB的反应均为一级动力学反应,速率常数分别为0.014 9 min-1、0.013 4 min-1和0.027 4 min-1,以上结果均说明了将TiO2和Ag@AgCl负载在CC上显著提高了其吸附-光催化降解性能, 并且所制备的CC/TiO2/Ag@AgCl复合材料的吸附-光催化降解性能优于文献报道的海藻酸钠负载的TiO2/Ag@AgBr[26],BiVO4/Cu2O/TiO2[27],TiO2/Ag2CrO4[28]等催化剂.
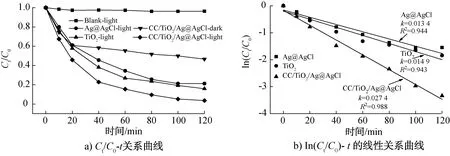
图8 CC/TiO2/Ag@AgCl复合材料对有机染料RhB的吸附-光催化降解性能曲线Fig.8 Adsorption-photocatalytic degradation of RhB by CC/TiO2/Ag@AgCl composite material
2.6 复合材料的光电性能分析
图9为TiO2、Ag@AgCl和CC/TiO2/Ag@AgCl复合材料的PL光谱(λex=366 nm). 由图9可以看出,CC/TiO2/Ag@AgCl复合材料在420~500 nm范围内出现的发射峰强度比TiO2和Ag@AgCl的强度弱很多. 根据文献[29]报道,PL光谱的发射峰强度越低,光生e-和h+的复合速率越低,即光催化剂的光催化活性越高. 由此可知,将TiO2和Ag@AgCl负载在CC上可以加快光生载流子的迁移速率,减缓光生电子-空穴的重组复合,从而提高催化剂的光催化活性.

图9 TiO2、Ag@AgCl和CC/TiO2/Ag@AgCl复合材料的PL光谱Fig.9 Photoluminescence (PL) spectra of TiO2、Ag@AgCl and CC/TiO2/Ag@AgCl composite material
为了进一步探究CC/TiO2/Ag@AgCl复合材料表现出优异光催化活性的原因,使用光电流和电化学阻抗来评估其产生和转移光生载流子的能力. 图10为CC、TiO2、Ag@AgCl和CC/TiO2/Ag@AgCl复合材料的瞬态光电流响应图和电化学阻抗谱图. 由图10a)可以看出,CC/TiO2/Ag@AgCl复合材料的光电流密度明显高于Ag@AgCl、TiO2和CC,说明复合材料可以有效地促使光生电荷的分离和转移,更有利于提高光催化降解反应性能[30]. 由图10b)可以看出,在CC上依次负载TiO2和Ag@AgCl后,圆弧半径与Ag@AgCl, TiO2和CC相比明显减小,而电化学阻抗曲线圆弧半径越小,说明电荷的转移电阻越低且电荷转移速率越快[31],以上结果表明,光生载流子在CC/TiO2/Ag@AgCl复合材料表面的电荷转移电阻较小,能够提高光生载流子的转移速率和传输效率,有助于增强其光催化活性.
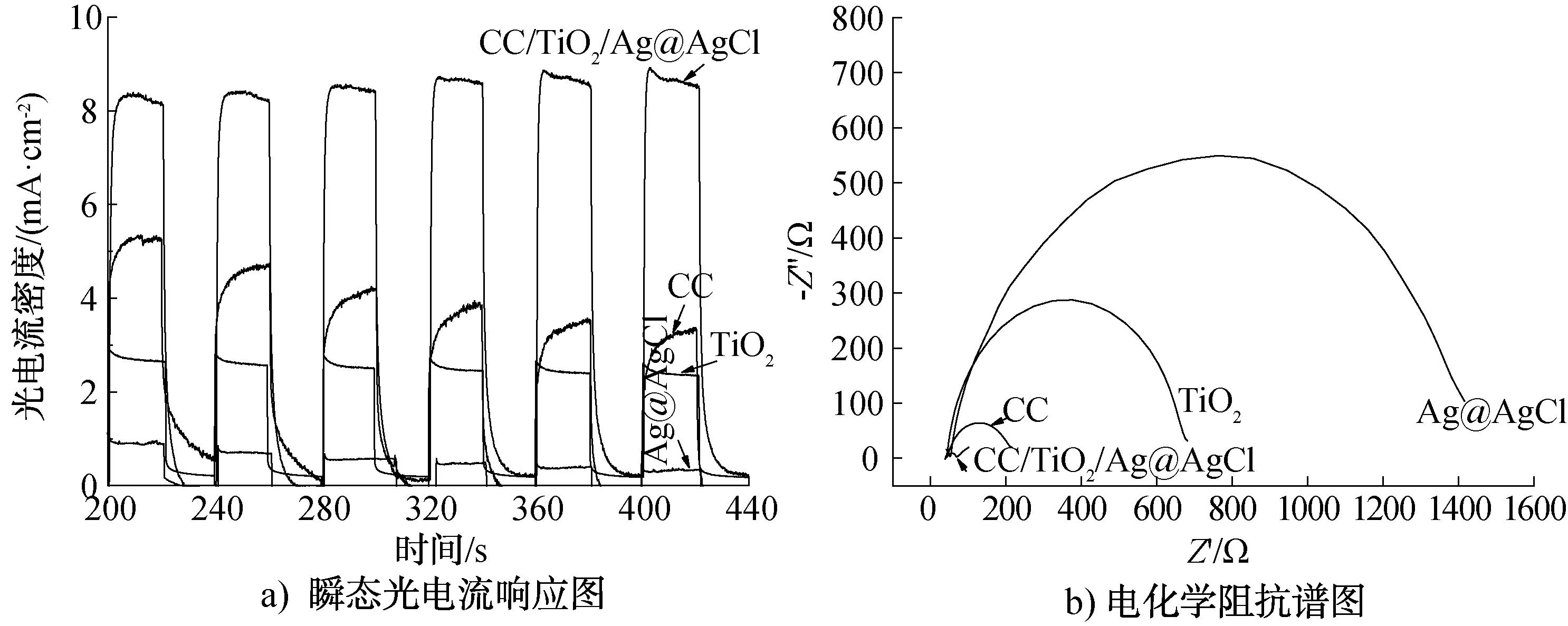
图10 CC、TiO2、Ag@AgCl和CC/TiO2/Ag@AgCl复合材料的瞬态光电流响应图和电化学阻抗谱图Fig.10 The transient photocurrent response and photoelectrochemical impedance spectra of CC、TiO2、Ag@AgCl and CC/TiO2/Ag@AgCl composite material
2.7 光催化降解反应过程中活性物质的确定
将异丙醇、对苯醌和EDTA-2Na分别作为·OH、 ·O2-和h+的自由基清除剂[32-33],测定了CC/TiO2/Ag@AgCl复合材料光催化降解RhB过程中的主要活性物质. 图11为添加不同自由基清除剂时CC/TiO2/Ag@AgCl复合材料对RhB的降解性能曲线. 由图11可以看出,添加对苯醌和异丙醇后,CC/TiO2/Ag@AgCl复合材料光催化降解RhB的性能明显降低,而加入EDTA-2Na对降解RhB过程的影响较小,这说明,·OH和·O2-是CC/ TiO2/Ag@AgCl复合材料光催化降解RhB过程中的主要活性物质.
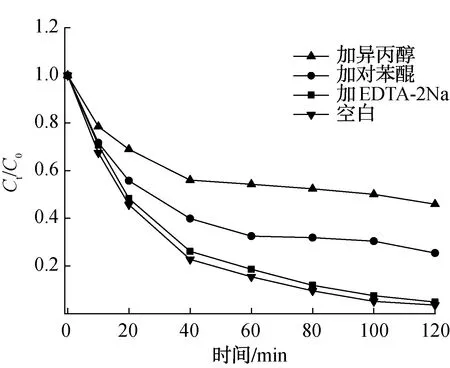
图11 添加不同自由基消除剂时CC/TiO2/Ag@AgCl复合材料对RhB的降解性能曲线Fig.11 Photodegradation of RhB over CC/TiO2/Ag@AgCl composite material in the presence of different free radical eliminators
2.8 复合材料的光催化稳定性分析
图12为CC/TiO2/Ag@AgCl的循环使用次数与光催化降解RhB的关系图. 由图12可以看出,该复合光催化剂循环使用6次后,光催化降解速率由于Ag@AgCl的少量脱落只降低了约9.75%,相对于粉质Ag@AgCl光催化材料,前者在循环过程中更易回收且损耗更少[34]. 图13为CC/TiO2/Ag@AgCl光催化剂循环前和经6次循环后的SEM图. 由图13可以看出,经过6次循环,CC/TiO2/Ag@AgCl复合材料基本没有发生形态上的变化,说明该催化剂具有良好的稳定性和回收再使用能力.
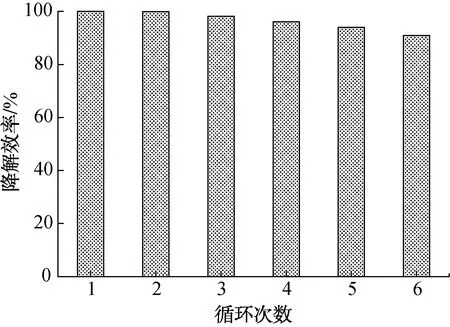
图12 CC/TiO2/Ag@AgCl的循环使用次数与光催化降解RhB的关系图Fig.12 Relationships between cycle numbers and the degradation efficiency of the CC/TiO2/Ag@AgCl catalyst on the RhB solution

图13 CC/TiO2/Ag@AgCl复合材料循环前和经6次循环后的SEM图Fig.13 SEM images of the composites CC/TiO2/Ag@AgCl composite material before and after six cycles
3 结论
本文以活化的CC为基底材料,依次在其表面负载TiO2和Ag@AgCl纳米粒子,成功地制备了CC/TiO2/Ag@AgCl复合材料,对其光催化性能进行研究发现,该复合材料对RhB的吸附-光催化降解性能优于TiO2和Ag@AgCl,这归因于CC/TiO2/Ag@AgCl复合材料增强了光的捕获能力,拓宽了光吸收范围,促进了光生电子-空穴对的分离和电子转移效率,能更有效地抑制光生载流子的复合;·OH和·O2-是CC/TiO2/Ag@AgCl复合材料光催化降解RhB过程中的主要活性物质. 此外,CC/TiO2/Ag@AgCl复合材料制备分离工艺的简便性及其较好的循环使用稳定性都显示了其在污水处理领域中良好的应用前景,为后期设计构建易分离循环使用的可见光驱动光催化剂提供了新思路.
