药物性肝损伤与抗抑郁药物综述*
2021-12-30蔡丽伟司天梅
蔡丽伟 司天梅
自20世纪50年代起,已有十余种抗抑郁药物上市,包括数十种化合物。尤其是90年代以来,新型抗抑郁药物层出不穷,虽然疗效未有突破,但是药物不良反应,尤其是抗胆碱能反应、心血管不良反应变得少而轻[1]。然而,现有的各类抗抑郁药物都要经过肝脏代谢,因此大多数药物都有潜在的肝脏损害风险。近年来,对抗抑郁药物所致肝脏不良反应的报道和关注也有所增加,因此,本文就药物性肝损伤(Drug-induced Liver Injury,DILI),尤其是新型抗抑郁药物上市以来的肝脏相关不良反应报告及研究进行综述,希望为临床实践者提供合理处方和临床处置的循证依据。
1 DILI概述
DILI是最常见和最严重的药物不良反应之一,严重者可致急性肝衰竭甚至死亡,迄今仍缺乏简便、客观、特异的诊断指标和特效治疗手段[2]。我国于2014年发布了HepaTox网站(http://www.hepatox.org/)[3],记录了400余种常见药物的肝损伤信息,为临床医生慎重处方具有潜在肝毒性的药物及评估其风险和收益提供了重要依据。发生DILI的原因主要包括[2]:(1)患者的遗传因素;(2)患者的非遗传因素,例如高龄、女性、妊娠期、有慢性肝病基础以及自身免疫性肝病、糖尿病、肿瘤、心脏病等基础疾病等;(3)药物因素;(4)环境因素,如过量饮酒。关于抗抑郁药物导致DILI的危险因素,一项大型病例对照研究发现,抗抑郁药导致的急性肝损伤患者中,82%为女性,30%有肝病史,47%伴高血压,35%伴血脂异常[4]。不同个体对同一药物的肝毒性反应不同,可能出现耐受、适应或易感性这三种不同的反应[2]。DILI的发病机制非常复杂,一般是多种机制先后作用或共同作用的结果,尚未充分阐明[2]。DILI的临床诊断为排他性诊断,在确定存在肝损伤的基础上,结合用药史、临床特征和肝脏生化学指标动态改变的特点、其他肝损伤病因排除等进行综合分析,肝活检组织学检查有助于诊断和鉴别诊断[2],可使用Roussel Uclaf因果关系评估量表(RUCAM)[5]对DILI进行诊断评估。
在大多数情况下,抗抑郁药引起的肝损伤,患者无明显临床症状,因此,肝功能检测异常结果所确定的生化学改变是唯一可能发现抗抑郁药导致肝损伤的途径,DILI的诊断也通常依赖于检测谷丙转氨酶(ALT)水平的升高。但是,ALT水平存在生理性波动。例如,临床研究中,安慰剂组可能出现20%的肝功能指标异常。此外,饮食的变化,例如碳水化合物或脂肪的摄入增加,只需3 d,ALT的基线水平就会增加3倍。因此,对于正在服用抗抑郁药的患者,如果发现肝功能检查结果异常,医生应谨慎解释,并且注意DILI是一种排他性诊断[2,6]。
2 常见抗抑郁药的肝脏不良反应现况和相关研究
许多抗抑郁药存在肝毒性风险,甚至带来致命的后果。包括1958年推出并于1962年退出市场的单胺氧化酶抑制剂(Monoamine Oxidase Inhibitor, MAOI)类抗抑郁药异烟酰异丙肼,2003年退出市场的萘法唑酮等[7]。包含1 279种药物的DILI严重性和毒性的大型药物清单显示,5类药物(抗抑郁药、抗癫痫药、抗炎和抗风湿药、降糖药)可能发生DILI的比例较高,临床使用该药理品类时需注意肝脏安全性监测[8]。意大利住院患者多中心病例对照研究(病例组为成人急性肝损伤患者,对照组为急性临床疾病-与慢性病和肝脏疾病无关)显示,与不使用抗抑郁药相比,目前使用抗抑郁药会导致肝损伤风险显著增加,急性肝损伤风险增加84%[4]。
一项多中心回顾性研究[9]分析了德国6个医疗中心登记的329例抗抑郁治疗的患者,在抗抑郁治疗期间,5.1%的患者血清转氨酶水平升高,其中3例患者(0.9%)达到了确切DILI指标(ALT>正常值上限5倍);并且,该研究显示,在转氨酶升高的病例中,最常见的抗抑郁药是:米氮平>阿戈美拉汀>西酞普兰=文拉法辛。法国500万病例数据库进行队列研究[10],根据抗抑郁药分类,以选择性5-羟色胺再摄取抑制剂(Selective Serotonin Reuptake Inhibitors, SSRIs)为参照,比较抗抑郁药起效后6个月内严重肝损伤的风险。结果发现,与SSRIs相比,5-羟色胺和去甲肾上腺素再摄取抑制剂(SNRIs)或其他抗抑郁药并未增加严重肝损伤风险。抗抑郁药物与因严重肝损伤住院事件之间的关系见表1。
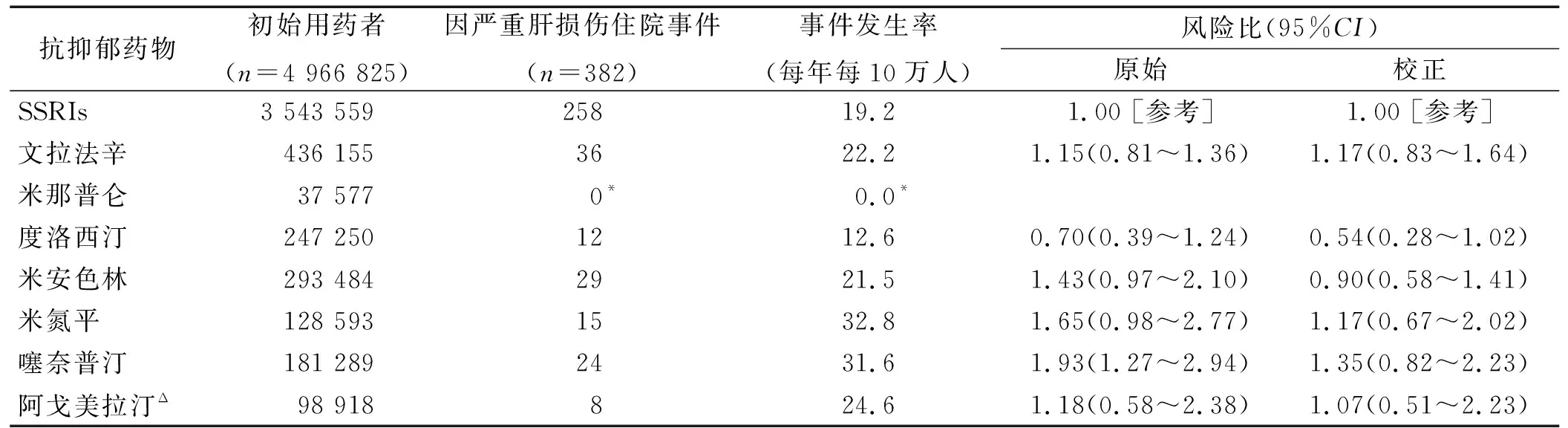
表1 抗抑郁药物与因严重肝损伤住院事件的关系
另一项巢式病例对照队列研究[11]分析了2009~2014年间丹麦、德国、西班牙、瑞典的3 238 495例新始抗抑郁治疗患者,以西酞普兰的急性肝损伤风险为对照,研究结果显示,与西酞普兰相比,阿戈美拉汀没有增加研究人群因急性肝损伤住院的风险。在风险最小化措施的前提下,与西酞普兰相比,阿戈美拉汀风险更低。在其他抗抑郁药中,与西酞普兰相比,舍曲林、艾司西酞普兰、米氮平、文拉法辛、度洛西汀和阿米替林造成急性肝损伤住院风险的趋势较低(统计学显示差异无统计学意义)。欧洲药品管理局(EMA)评估了来自阿戈美拉汀定期安全性报告的新数据,结论为需要强化该药物的肝脏毒性风险最小化措施[12]。
抗抑郁药的代谢特性可能影响其他药物的血药浓度或增加肝脏负担,增加肝毒性。CYP450酶系统负责多种药物的第一阶段氧化反应,有些抗抑郁药物可抑制或诱导CYP450酶活性,在合并用药时,如遇对同种同工酶具有抑制作用或竞争关系的药物,则会增加DILI风险。例如,SSRIs在肝脏经药酶代谢,同时又对这些药酶产生抑制作用[1],若同时服用该药酶的底物,则影响底物代谢,可能增加肝损害风险;又如,合用药物与抗抑郁药竞争相同的CYP450代谢途径,也可能增加肝毒性反应风险[6]。抗抑郁药物潜在的药物相互作用与肝毒性报道见表2。
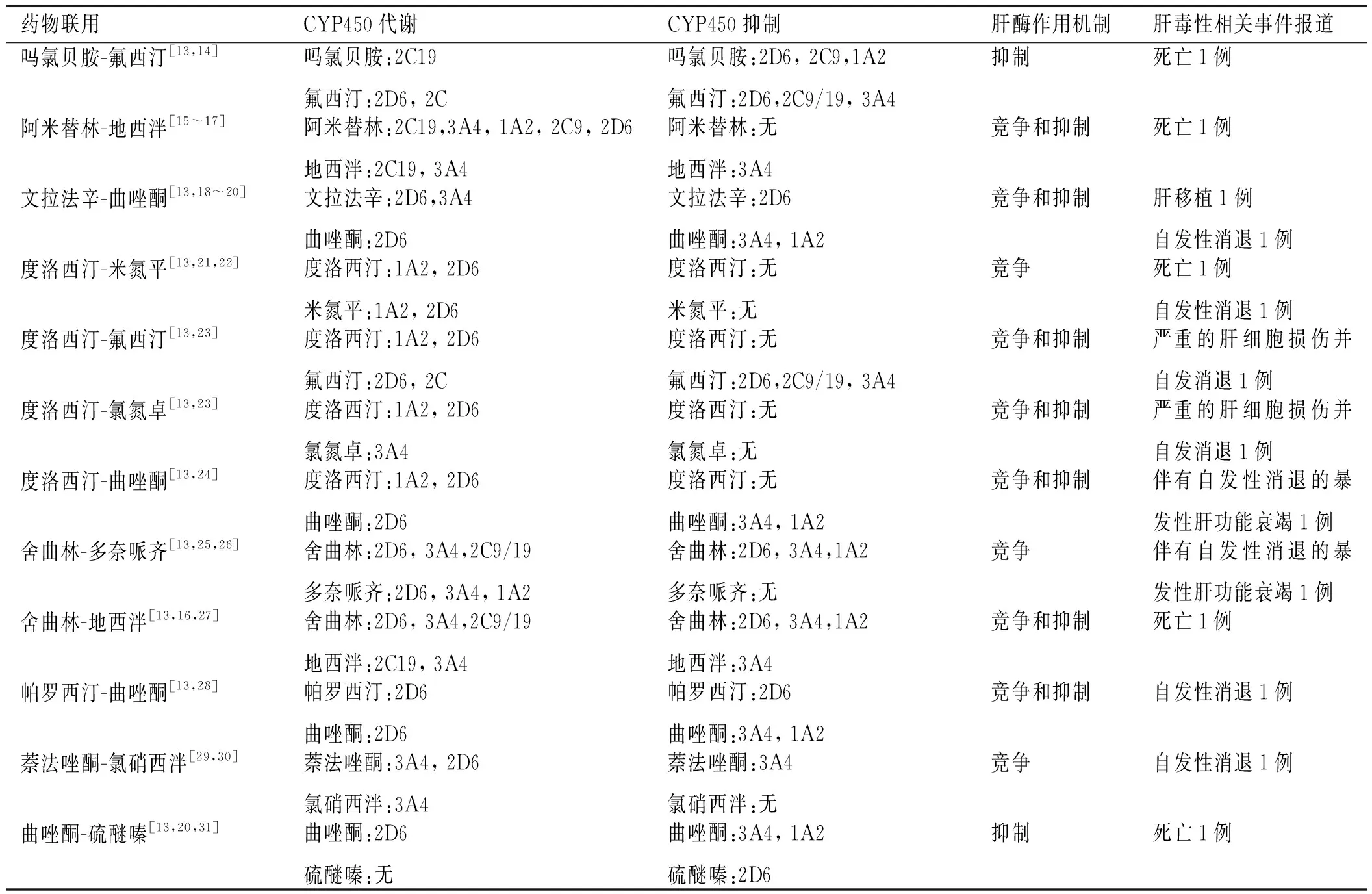
表2 抗抑郁药物潜在的药物相互作用与肝毒性报道
抗抑郁药相关的DILI通常为肝细胞型,一般来说,在肝细胞型DILI中,转氨酶水平会随着停药而迅速恢复正常。在严重的病例中,胆红素浓度的增加与凝血酶原时间的减少有关。在这些罕见的病例中,由于有暴发性肝炎和肝衰竭的危险,必须立即停用该药。对大多数患者来说,在停用抗抑郁药后,肝脏检查结果恢复正常。然而,在某些情况下,可能出现临床症状,发展为严重的DILI,如暴发性肝衰竭,导致死亡或肝移植。妇女和伴有慢性肝病的患者更易发展为更严重的DILI。检索并汇总1965~2014年间Pubmed中DILI相关的发表文献,常见抗抑郁药物肝损伤发生情况及其病理类型和发生机制见表3[6]。

表3 常见抗抑郁药物肝损伤特点
3 抗抑郁药相关肝脏不良反应的管理
为降低抗抑郁药相关肝脏不良反应风险,在临床实践中,应注意以下处方原则[6]:(1)在处方抗抑郁药前,考虑年龄和合并用药的情况,并充分注意配伍禁忌;(2)对于老年患者、共病患者、大量饮酒、违禁药物使用或慢性肝病患者,应谨慎选用抗抑郁药物,抗抑郁治疗前的基线肝功异常会使患者治疗过程中的肝功监测复杂化,具有较高肝毒性风险的抗抑郁药物(萘法唑酮、丙咪嗪、阿米替林、度洛西汀、曲唑酮、阿戈美拉汀等)不应当用于已存在肝衰竭的患者;(3)被怀疑具有较高肝毒性风险的药物应尽量避免合用,以降低DILI的风险,特别是严重DILI的风险;(4)最好避免针对相同CYP450途径的共处方,严格遵守配伍原则;(5)虽然没有明确的剂量-反应关系,但应推荐抗抑郁药的最低有效剂量处方,以降低DILI的风险;(6)在有DILI病史的患者中,建议避免使用同种药物或其他具有类似结构的药物。
医生应该具备抗抑郁药可能导致肝损害的意识,对于明确存在肝损害风险的抗抑郁药物服用者,和存在已知肝损害危险因素的患者,更应该在治疗前进行肝功能实验室检查,了解患者的肝功能基线水平,并在治疗期间定期监测肝功能。基线ALT值有助于解释抗抑郁治疗期间出现的肝功能异常,这些异常可能是潜在相关疾病的表现,也可能是抗抑郁药物导致的肝损害表现。对于已经开具了抗抑郁药物处方的患者,医生与患者进行充分的沟通,并对肝功能实验室指标进行定期的监测,也有助于降低抗抑郁药物相关肝脏不良反应的风险。
对于明确存在肝损害风险的抗抑郁药物服用者,和存在已知肝损害危险因素的患者,医生应当告知他们:(1)抗抑郁药物治疗可能与肝功异常相关,可能没有症状,也可能出现一些肝功能障碍的症状和体征(黄疸、厌食、胃肠道不适、乏力不适等),最严重的情况甚至发生肝衰竭导致死亡或肝移植;(2)饮酒、违禁药物、某些非处方药、中药等可能会增加严重肝脏异常的风险;(3)如果出现任何上述症状,应尽快咨询医生。
肝功能结果异常并不意味着必须停药,抗抑郁药引起的肝酶升高多数呈自限性或出现适应性,真正进展为严重DILI的情况较为少见,因此,无进行性的轻度的肝酶升高一般无需调整剂量或停药[32,33]。如果服用抗抑郁药物的患者出现下述任何一种情况,建议立即停药:(1)任何疑似DILI的患者;(2)ALT>正常值上限3倍(也有人认为是正常值上限5倍);(3)胆红素>正常值上限2倍或凝血酶原时间国际标准化比率(INR)升高,提示肝脏明显受损[2];(4)若患者用药前基线ALT高于正常值上限,则发现ALT>3倍基线水平时应停药;(5)服用阿戈美拉汀者,转氨酶水平超过正常值上限(参考阿戈美拉汀说明书)。
一旦怀疑抗抑郁药导致DILI,在生化学指标正常化或恢复到基线值之前,监测肝功能[ALT、碱性磷酸酶(ALP)、胆红素]是必需的。急性DILI大多预后良好,药物性肝衰竭病死率较高[34]。
4 精神科DILI的治疗和管理
目前尚无确切证据显示预防性应用抗炎保肝药物可减少DILI的发生[35],因此,最为推荐的做法仍是在开始用药后(尤其是用药的前3个月)加强肝功能监测、及时发现肝损伤并给予合理的治疗[2]。
在精神科,一旦怀疑患者可能出现了DILI(参考前述DILI的生化学诊断标准及严重程度分级),应充分权衡停药引起原发病进展和继续用药导致肝损伤加重的风险,及时停用可疑药物且尽量避免再次使用可疑或同类药物,并考虑启动联络会诊程序,与消化科联合处置,或直接转诊至消化科,根据DILI的临床类型选用适当的药物治疗。重型患者可选用N-乙酰半胱氨酸,尽早使用,总疗程不低于3 d,治疗过程中应严格控制给药速度,以防不良反应。糖皮质激素对DILI的疗效证据不甚充分,应严格掌握适应证,并充分权衡治疗收益和潜在的不良反应。异甘草酸镁可用于治疗ALT明显升高的急性肝细胞型或混合型DILI。经验表明,对于轻中度的肝细胞型和混合型DILI,炎症较重者可试用双环醇和甘草酸制剂,炎症较轻者可使用水飞蓟素;胆汁淤积型DILI可用熊去氧胆酸或腺苷蛋氨酸;不过这些药物的确切疗效尚待高级别循证医学证据支持。急性/亚急性肝衰竭等重症患者必要时可考虑紧急肝移植[2,36]。
我国存在临床不规范用药的情况,医护和大众对于DILI的认知和警惕仍然有所欠缺,因此需要采取一系列方法减少风险[2],包括:(1)在药物说明书中对药物肝毒性给予警告,列出预防措施,必要时给予黑框警告;(2)在药物上市后,密切监测药物不良反应,可以在监测和评价过程中充分引入药物警戒理念[37],例如,阿戈美拉汀就采取了风险最小化管理措施,对医生和患者进行充分的警示、告知和教育,在用药前和用药期间定期对肝功能进行实验室监测和记录,如果肝功能出现异常应及时采取相应措施,力图将肝损伤风险降至最低[12];(3)遵循临床指南合理用药,避免药物过量或滥用;(4)用药期间定期进行肝脏生化学检测;(5)加强用药知情同意管理;(6)加强安全用药的公众健康教育。如果未来能够开发出可以预测DILI易感性的生物标志物并转化应用,将会对DILI风险管理提供更加强大的支持[2]。
5 小结
DILI是药物治疗过程中的常见不良反应之一,抗抑郁药物具有不同程度地导致肝损伤的风险,尽管多数程度较轻,无需特殊处理,但偶有严重肝损伤的情况发生,因此临床工作中需要警惕抗抑郁药物导致肝损伤发生的可能,重视抗抑郁药治疗前后的肝功能监测,尤其对明确存在肝损伤风险或存在已知肝损伤危险因素的患者。到目前为止,抗抑郁药物导致肝损伤的发生机制尚未完全明确,因此有待进一步开展相关研究。
