红曲磷虾油软胶囊的毒理安全性评价
2021-12-18张金秋张馨欣侯万萍
张金秋, 江 贺, 张馨欣, 侯万萍, 邹 慧
(长春康彼达科技有限公司, 吉林 长春 130012)
随着物质生活水平的提高和饮食结构的改变,人们摄入高热量、高油脂食物的量增加,长期摄入高脂食物会干扰体内脂质代谢和抗氧化能力。当体内血脂过高后,致使体内形成大量自由基,导致细胞受损,加速细胞凋亡,人体衰老。脂肪在内脏中过多,会导致内脏功能减少;在血管内沉积,形成动脉粥样硬化,易引发心脑血管等疾病。临床研究发现,心脑血管疾病患者血液动力学检查中的总胆固醇(TC)、低密度脂蛋白(LDL-D)均有所升高,表明心脑血管疾病与血脂异常存在一定的关系。全球心脑血管的发病率逐年上升,已严重威胁到人的健康,据不全统计,每年因心脑血管等疾病导致的死亡人数占总死亡人数20%以上[1]。因此,有效控制血脂是预防动脉粥样硬化的有效手段之一。
红曲为药食两用传统中药材,主要含洛伐他汀(Monacolin K)、麦角固醇、γ-氨基丁酸、天然植物激素[2]等,具有调节脂代谢、降低血压、降低血糖、预防和治疗骨质疏松等广泛的药理作用[3-5]。南极磷虾油作为海洋新兴油脂,其含有多种不饱和脂肪酸等活性成分,其中具有代表性的EPA、DHA以磷脂形式存在,活性优于甘油三酯或乙酯,具有调节血脂作用[6-8]。玉米油中含丰富的不饱和脂肪酸、甾醇等成分,其中,亚油酸占油脂总量的50%以上,研究证明玉米油有显著降低血清胆固醇的作用[9]。“红曲磷虾油软胶囊”是由吉林省现代中药工程研究中心有限公司研制,具有辅助降血脂功能的保健食品,以红曲粉、南极磷虾油为原料,玉米油等为辅料制成的软胶囊。为评价红曲磷虾油软胶囊的安全性,依据《保健食品检验与评价技术规范》(2003年版)和《食品安全国家标准 急性经口毒性试验急性毒性剂量分级标准》(GB 15193.3—2014),采用急性毒性试验、遗传毒性试验、28 d喂养试验进行安全性考察。现将试验结果报道如下。
1 材料与方法
1.1 试验材料
1.1.1 红曲磷虾油软胶囊 其是以红曲粉、南极磷虾油为原料,玉米油为辅料,添加一定的蜂蜡作为助悬剂制成。该胶囊由吉林省现代中药工程研究中心有限公司研制(批号:20180701),规格0.5 g/粒,人体推荐用量为2 粒/次、2次/d。供试品为红曲磷虾油软胶囊的内容物。
1.1.2 仪器与设备 电子天平(ME204E、AB135-S型),梅特勒-托利多仪器(上海)有限公司;水浴锅(HH-S114型),金坛市华龙实验仪器厂;血细胞分析仪(BC-280 vet型)、全自动生化分析仪(BS-420型),深圳迈瑞生物医疗电子股份有限公司;尿液分析仪(Uritest-200 B),桂林优利特电子集团有限公司;恒温培养箱(SPX-100B-Z),上海博讯实业有限公司医疗设备厂;超净工作台(SJ-CJ-1FD),苏州苏洁净化设备有限公司。
1.1.3 试验动物 SPF级SD大鼠、昆明小鼠,由西安交通大学医学部动物实验室提供。
1.1.4 药物、试剂等 环磷酰胺、敌克松、秋水仙碱、叠氮化钠(NaN3)、2-氨基芴(2-AF)、1,8-二羟基蒽醌、大鼠肝微粒体酶(S9)、小牛血清、Giemsa染液、伊红染液、磷酸盐缓冲溶液、尿液分析试纸、生化试剂盒(深圳迈瑞生物医疗电子股份有限公司)、TA1535、TA97a、TA98、TA100、TA102菌株,均购自于上海北思生物科技有限公司。
1.2 试验方法
1.2.1 大鼠急性毒性试验 选取SD大鼠20只,雌雄各半,灌胃前禁食16 h,不限饮水,称取供试品100 g,按18.43 mL/kg体重(相当于人体推荐用量的460倍)分2次(间隔6 h)经口灌胃,灌胃后连续14 d观察记录SD大鼠的中毒症状及死亡情况。同时选取20只SD大鼠,雌雄各半,做空白对照试验。试验0 d、7 d和14 d称量大鼠体重,试验结束后处死解剖[10]。
1.2.2 遗传毒性试验
1) 细菌回复突变试验。选择经基因型鉴定符合试验要求的5株组氨酸缺陷型鼠伤寒沙门氏菌(TA1535、TA100、TA97a、TA98、TA102)进行试验。称取1.0 g供试品,加DMSO至20 mL,混合均匀,第1次5个受试物浓度分别为50 μg/皿、158 μg/皿、500 μg/皿、1 581 μg/皿和5 000 μg/皿,第2次分别为8 μg/皿、4 0 μg/皿、200 μg/皿、1 000 μg/皿和5 000 μg/皿,另设阳性对照组、自发回变组和去DMSO对照组,TA1535、TA100:NaN3(1.5 μg,-S9);TA97a、TA98、TA102:敌克松(50.0 μg,-S9),TA102:1,8-二羟基蒽醌(50.0 μg,+S9);TA1535、TA97a、TA98、TA100:2-AF(10.0 μg,+S9)。各组受试物在0.103 MPa下湿热灭菌20 min。各组均设3个平行皿,加入0.1 mL菌株增菌液,0.1 mL受试物(或对照物)和0.5 mL S9混合液(试验组分别设加与不加S9组),加入保温的顶层培养基中混合均匀后用平铺法置于底层培养基平板上,37℃恒温培养48 h后,统计菌落数,试验2次重复。
2) 小鼠骨髓细胞微核试验。取小鼠50只,平均分成5组(每组雌雄各半),分别设供试品0.93 g/kg、1.85 g/kg、3.69 g/kg剂量组,另设阴性对照组(大豆油)及阳性对照组(环磷酰胺40 mg/kg)。采用30 h灌胃法,第2次(与第1次间隔24 h)灌胃后6 h颈椎脱臼处死,取小鼠胸骨挤出骨髓,混合小牛血清,制片,干燥后固定、Giemsa染色,在显微镜下每只小鼠观察1 000个嗜多染红细胞(PCE),计算微核发生率。
3) 小鼠精原细胞畸变试验。取30只雄性小鼠,平均分成6组,分别设供试品0.93 g/kg、1.85 g/kg、3.69 g/kg剂量组,另设溶剂对照组(去离子水)和阳性对照组(环磷酰胺40 mg/kg)。连续灌胃5 d,高剂量组分别于末次给药后24 h和48 h处死,其余剂量组在末次给药后24 h处死,处死前5 h按5 mg/kg剂量给小鼠腹腔注射秋水仙素溶液(注射体积20 mL/kg BW),将所有小鼠颈椎脱臼处死,取双侧附睾尾剪碎,加生理盐水游离出精子,涂片,用1%伊红染色制片,用光学显微镜观察完整精子,每只小鼠观察100个精子,记录各类畸形精子数,计算畸变发生率。
1.2.3 28 d喂养试验 选用68~93 g离乳SD大鼠100只,平均分成5组(每组雌雄各半),分别设供试品0.93 g/kg、1.85 g/kg、3.69 g/kg剂量组,另设阴性对照组(大豆油)。停药后15 d设高剂量组恢复期组和阴性组,每组10只,按4.0 mL/kg每天经口灌胃1次,连续28 d,观察记录大鼠的行为表现、中毒症状及死亡情况。灌胃结束后禁食隔夜,逐只称重,用10%水合氯醛3.5 mL/kg腹腔注射麻醉,腹主动脉取血测定血液学指标和血液生化指标。
1.3 数据分析
对小鼠骨髓细胞微核试验数据进行u检验;小鼠精原细胞畸变试验数据进行二项分布统计;28 d喂养试验数据进行方差齐性检验。
2 结果与分析
2.1 红曲磷虾油软胶囊的急性毒性
从表1看出,用红曲磷虾油软胶囊18.43 g/kg灌胃后大鼠生长良好,未见体重变化,未见有明显中毒症状,14 d观察期内无死亡。心、肝、脾、肺、肾、肠、胃等主要脏器均未发现明显变化。表明,红曲磷虾油软胶囊对大鼠LD50均大于18.43 g/kg,按剂量分级标准,红曲磷虾油软胶囊属于无毒级别。
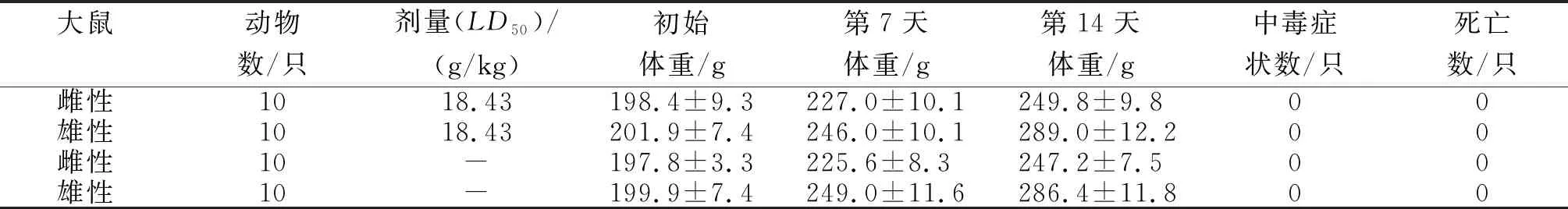
表1 红曲磷虾油软胶囊对大鼠的急性毒性
2.2 红曲磷虾油软胶囊的遗传毒性
2.2.1 细菌回复突变试验 从表2、表3看出,回变菌落数红曲磷虾油软胶囊各剂量组与未处理对照组(自发回变组)相近,且未发现剂量-反应关系,试验结果为阴性,说明红曲磷虾油软胶囊在+S9和―S9情况下,对5种类型菌株均无致突变性。
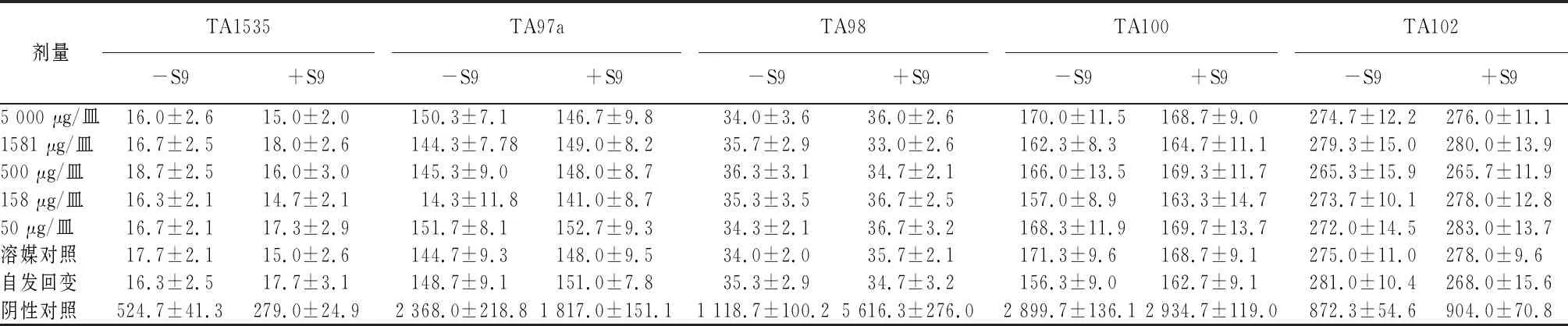
表2 第1次试验的回变菌落数

表3 第2次试验的回变菌落数
2.2.2 小鼠骨髓多染红细胞微核试验 从表4看出,红曲磷虾油软胶囊各剂量组的PCE/NCE与阴性对照组差异均不显著(P>0.05),表明红曲磷虾油软胶囊对骨髓红细胞增殖无明显抑制;雌、雄小鼠阳性对照组的微核率与阴性对照组间差异极显著,表明红曲磷虾油软胶囊小鼠骨髓多染红细胞微核试验结果均为阴性。

表4 红曲磷虾油软胶囊不同剂量下小鼠骨髓多染红细胞微核率(n=5)
2.2.3 小鼠精原细胞畸变试验 染色体畸变类型主要以断裂、断片为主,一般正常小鼠精原细胞畸变率为0.8%~3.4%。从表5看出,红曲磷虾油软胶囊各剂量组与阴性对照组间差异不显著(P>0.05),细胞畸变率阳性对照组与阴性对照组间差异极显著(P<0.01),表明红曲磷虾油软胶囊对小鼠精原畸变试验为阴性。
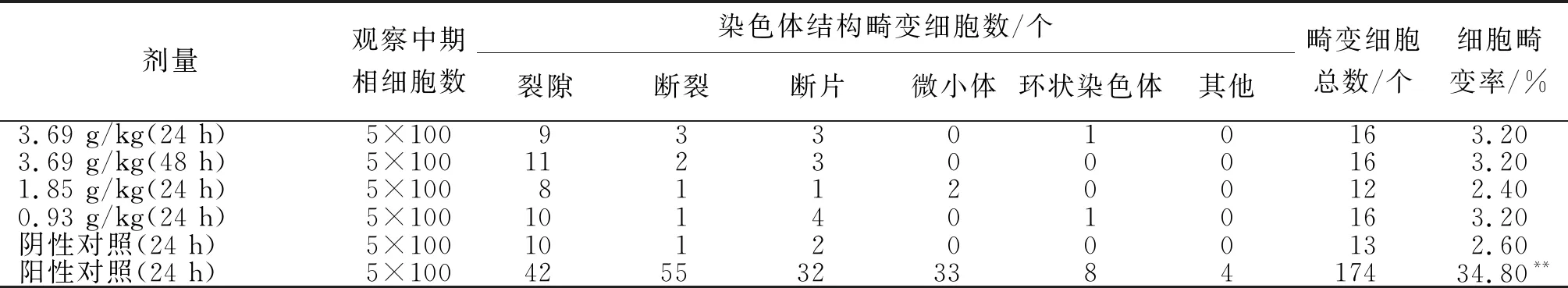
表5 红曲磷虾油软胶囊不同剂量下小鼠的精子畸变情况
2.3 28 d喂养试验
2.3.1 行为体征等 28 d喂养试验期间红曲磷虾油软胶囊各剂量组大鼠的外观形态与对照组无明显差异,生长良好,未发现异常行为和体征,未出现明显中毒症状和死亡。从表6看出,红曲磷虾油软胶囊各剂量组大鼠体重增重、总进食量、总食物利用率与对照组间差异不显著(P>0.05),表明红曲磷虾油软胶囊对大鼠行为特征无影响。
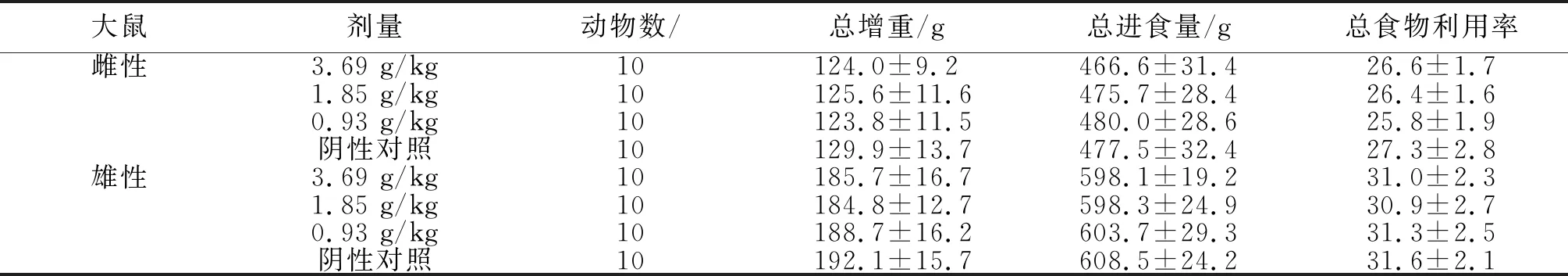
表6 红曲磷虾油软胶囊不同剂量下大鼠的增重、食物总利用率(n=10)
2.3.2 血液学及血液生化指标 红曲磷虾油软胶囊不同剂量灌胃大鼠28 d,血液红细胞计数、血红蛋白水平、白细胞计数及其分类等指标,均满足方差齐要求。从表7、表8看出,红曲磷虾油软胶囊不同剂量组的各项指标与阴性对照间无显著差异(P>0.05),表明红曲磷虾油软胶囊对大鼠血液学及血液生化各项指标无影响。
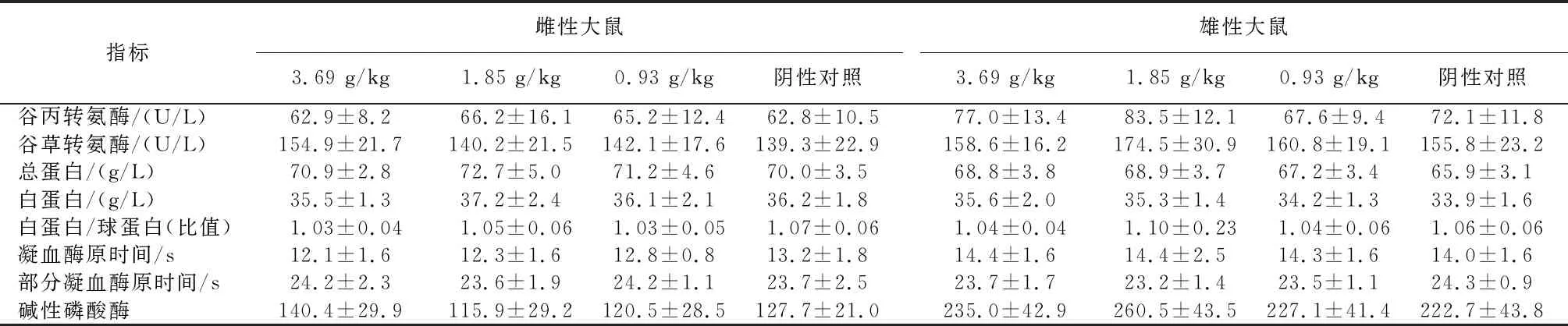
表7 红曲磷虾油软胶囊不同剂量下大鼠的生血液学指标(n=10)

表8 红曲磷虾油软胶囊不同剂量下大鼠的血液指标(n=10)
2.3.3 尿液与脏体指标 从表9、表10看出,红曲磷虾油软胶囊各剂量组大鼠的尿液、禁食后体重、脏体比等指标与阴性对照组间无显著差异(P>0.05),表明红曲磷虾油软胶囊对大鼠尿液、脏体指标无影响。

表9 红曲磷虾油软胶囊不同剂量下大鼠的尿液指标(n=10)
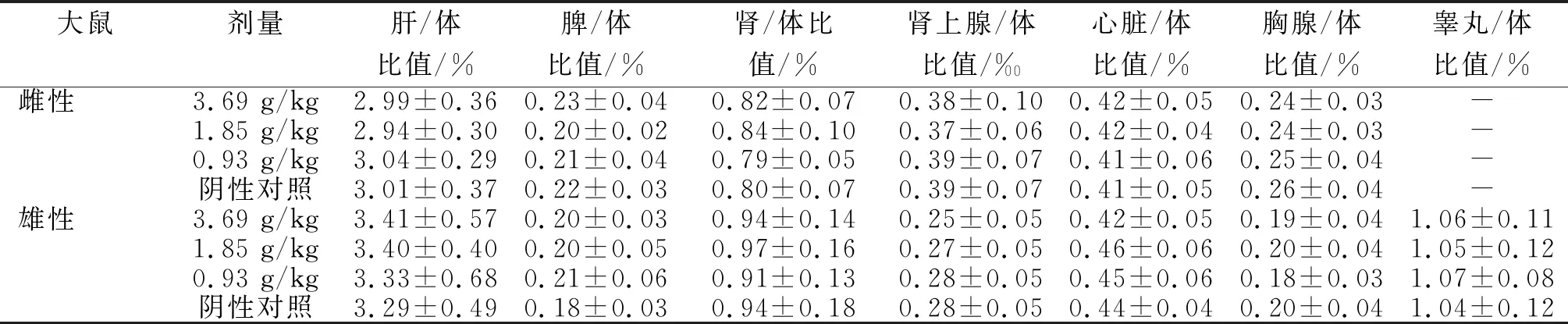
表10 红曲磷虾油软胶囊不同剂量下大鼠的脏体指标(n=10)
2.3.4 病理组织学 大鼠解剖肉眼未见异常。组织病理学检查发现,红曲磷虾油软胶囊高剂量组雌鼠有1例轻度肝小叶空泡变、1例肾轻度淤血、1例胃炎细胞浸润,雄鼠有1例肝小叶炎细胞浸润、1例脾色素沉积,其余组织均未见异常;阴性对照组雌鼠有1例轻度肝小叶空泡变、1例胃黏膜轻度水肿,雄鼠有1例肾皮质部肾小管空泡变、1例胃炎细胞浸润,其余组织均未见异常。红曲磷虾油软胶囊高剂量组(恢复期)雌鼠有1例肝小叶颗粒变性,雄鼠1睾丸间质水肿;阴性对照组(恢复期)雄鼠1例肝少量炎细胞浸润、1例肝小叶空包变、1例肾皮质部肾小管肿胀,雌鼠1例胃少量炎细胞浸润。以上病理学仅在个别大鼠中发生,各组病理变化无明显差异,表明被检脏器未见与红曲磷虾油软胶囊有关的病理学改变。
3 结论
红曲磷虾油软胶囊是由红曲粉、南极磷虾油以及玉米油配比,按照软胶囊工艺制成的一款具有降血脂功能的保健食品。研究结果表明,红曲磷虾油软胶囊以18.43 g/kg体重灌胃大鼠无中毒、死亡症状,表明此产品LD50大于18.43 g/kg,按照《食品安全国家标准 急性经口毒性试验急性毒性剂量分级标准》(GB 15193.3—2014),此胶囊属于无毒级。细菌回复突变试验、小鼠骨髓多染红细胞微核试验、小鼠精原细胞畸变试验结果均为阴性,表明红曲磷虾油软胶囊无遗传毒性。28 d喂养试验的大鼠各项检验指标均未发现明显改变,说明红曲磷虾油软胶囊安全无毒。下一步将对该产品的降血脂功能进行验证,完善该产品的质量控制标准,为产品的开发提供科学依据。
