SrFe0.6Co0.4O3催化降解孔雀石绿的研究
2021-12-15李家飞张永明潘莉莎
李家飞,徐 凯,张永明,潘莉莎
(海南大学,海南省精细化工工程技术研究中心,海口 570228)
0 引 言
随着化纤及染料技术的不断革新,印染行业得到快速的发展,随之而来的印染废水问题也越来越严重[1]。孔雀石绿(malachite green, MG)作为一种常见的三苯甲烷类染料,其含有苯环,双键等复杂结构,常规方法很难降解。未经处理就排放的MG废水会对环境造成严重污染[2]。
物理吸附法、生物处理法等常规废水处理法很难将MG彻底无害化,还可能造成二次污染[3]。芬顿氧化法是一种成熟的印染废水处理方法,但会产生不易回收的氢氧化铁胶体,极易造成二次污染[4-5]。钙钛矿ABO3型复合氧化物的B位离子可以灵活地复合不同特性的变价离子,可制备出不同特性的导电及催化材料[6-9]。经过高温煅烧的ABO3型氧化物催化剂具有陶瓷的耐腐蚀、耐磨及抗压强度高等特性,其金属离子不易溶于水体,用于废水处理时不易造成水体二次污染[10-13]。吴丹等[14]通过溶胶-凝胶法制备了B位复合Ni的LaFeO3,其中LaNi0.9Fe0.1O3对碱性品红的催化活性最高,120 min的降解率可达97%。然而在多数染料降解的研究中,A位元素大部分以La为主,且降解染料所用的时间相对较长。为了快速降解染料废水,同时不造成二次污染,本文选用对人体有益的Sr作为A位元素,Fe为B位元素,并基于对钙钛矿型氧化物ABO3的B位为催化活性中心的认识,拟采用溶胶-凝胶法制备B位复合的钙钛矿ABO3型催化剂SrFe1-xCoxO3,研究其B位离子复合比例及制备条件对MG催化降解活性的影响,并探讨其催化反应机理。
1 实 验
1.1 试剂与仪器
硝酸锶、硝酸铁、硝酸钴、孔雀石绿均为AR级,北京化工厂生产;其余催化剂合成用原辅料试剂均为CP级,上海阿拉丁公司;所有分析用试剂均为AR级,上海麦克林公司。
物相分析采用Rigaku 公司Smart Lab型X射线衍射仪,Cu/Kα射线,2θ=10°~80°;表面原子配位态分析采用Thermo公司Escalab 250Xi型XPS能谱仪,单色Al/Kα射线,电压14.8 kV,电流1.6 A;表面形貌分析采用Hitachi公司S-4800型场发射扫描显微镜,加速电压3.0 kV;比表面积分析采用Micromeritics公司ASAP 2460型吸附仪,脱气温度77 K;MG浓度测定采用分光光度法,使用上海精科721型分光光度计,测定波长为620 nm。
1.2 催化剂的制备
分别配制精确浓度的硝酸锶、硝酸铁、硝酸钴及柠檬酸原料液,金属盐投料比例按分子式SrFe(1-x)CoxO3(x=0.1, 0.2, 0.3, 0.4, 0.5)计量加入溶胶-凝胶制备反应器,柠檬酸的加入量按总金属离子与柠檬酸摩尔比为1 ∶1计,反应混合物在搅拌下于60~100 ℃缓慢浓缩为半固体状凝胶后,置于120 ℃下静态干燥为蓬松状干凝胶,经高温焙烧即得样品。
1.3 催化活性评价
采用静态降解(间歇式降解)法:取50 mL MG溶液(50 mg/L)于催化降解反应器中,计量加入所制备的催化剂,常压常温(27 ℃)进行连续搅拌反应一定时间,取6 mL反应液,离心分离催化剂,以测定MG降解率D:
D=(C0-CT)/C0×100%
(1)
式中:C0为MG初始浓度(mg/L);CT为反应T时间后的MG浓度(mg/L)。催化活性通过催化反应降解率大小来表示。
2 结果与讨论
2.1 催化剂的分子设计
根据钙钛矿型ABO3复合氧化物晶体结构的Goldschmidt半径容差t值规则[15],即:
t=(rA+rO)/(2(rB+rO))
(2)
式中:rA为A位离子半径;rB为B位离子半径;rO为O离子半径。
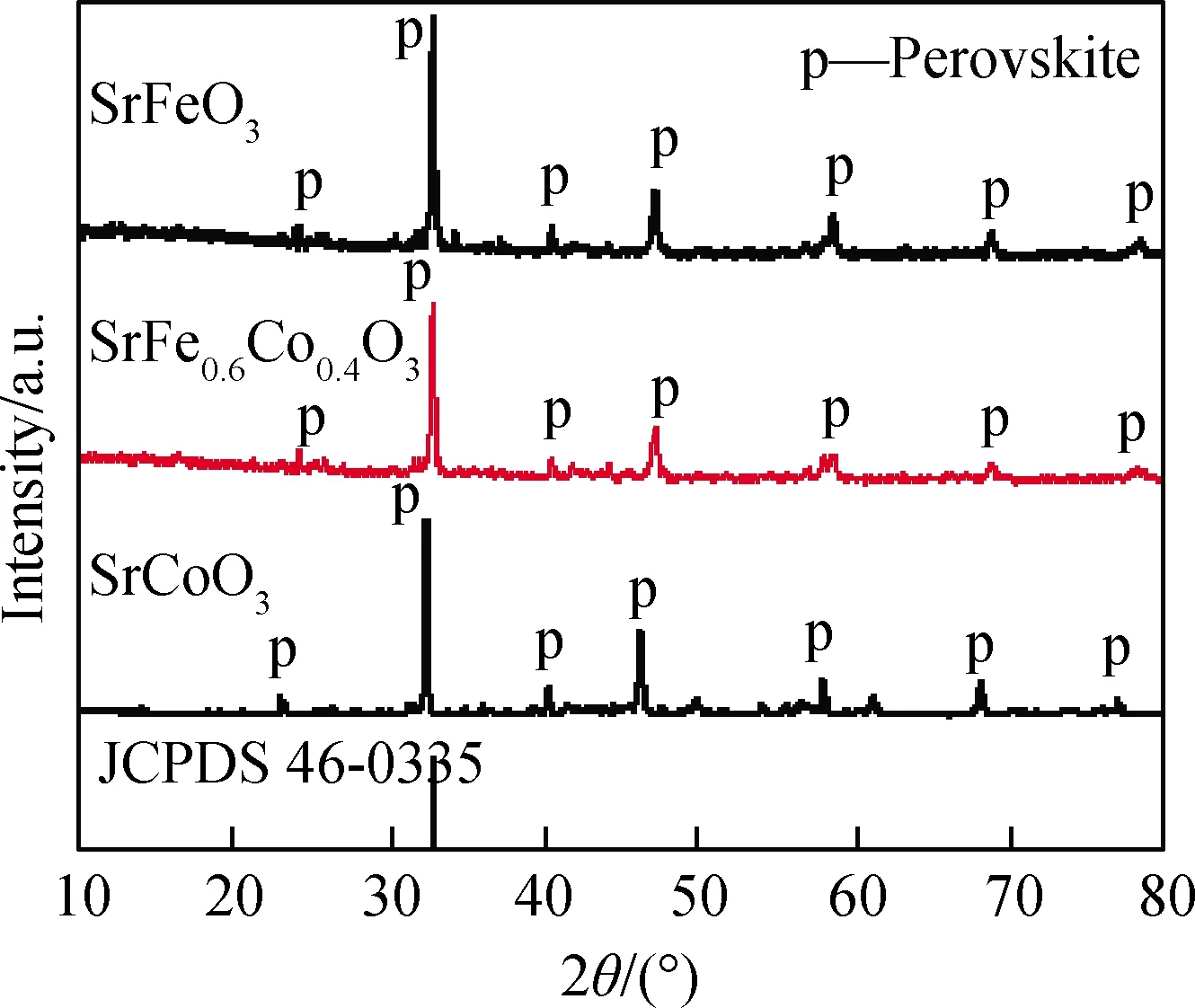
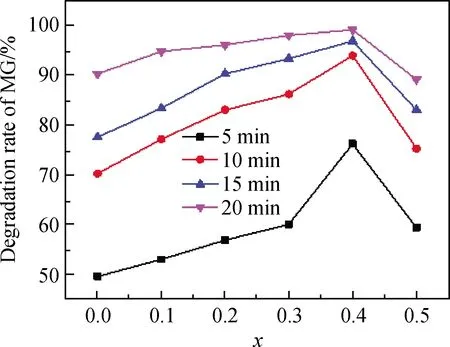
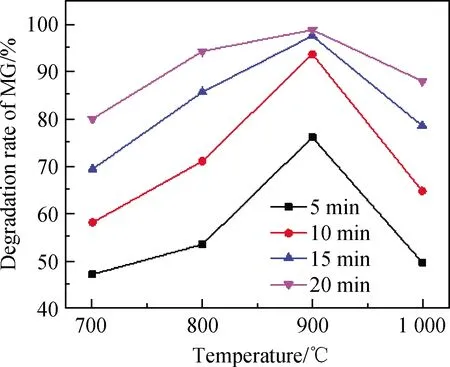
其中t必须满足0.75 表1中rA12、rO6、rB6分别表示12配位的A位离子、6配位的O离子和6配位的B位离子半径。表1的Goldschmidt法计算结果表明,所设计的催化剂SrFe(1-x)CoxO3(x=0~1)的稳定性半径容差t值在0.91~0.97之间,均接近t的理想值1.0,理论上可形成结构稳定性较高的ABO3催化剂[16];从图1可以看出,所制备SrFe(1-x)CoxO3催化剂均为纯净的钙钛矿晶体结构,没有其他杂质相,实验结果达到了催化剂结构设计目标。 表1 基于Goldschmidt计算方法设计催化剂的t值结果Table 1 Results of t value for the designed catalyst based on Goldschmidt-calculating-method ABO3型催化剂中,B位的变价离子是催化反应中的电子传递与循环的活性位置,在B位复合型氧化物SrFe(1-x)CoxO3中,考察了复合B位离子的比例Fe/Co(x值)对催化活性的影响(见图2)。由图2可知,对不同的反应时间都存在这一规律:在x<0.4时,催化活性随x增大而缓慢增大;x=0.4时,达到降解活性最大值;x>0.4时,其活性迅速降低。 这一现象可通过B位离子的容差因子t得到解释:结合表1,Co3+、Fe3+的t值均小于1.0,且Co3+的t值0.91也小于Fe3+的0.97,这意味着Co3+、Fe3+都有吸引电子形成Co3+·e和Fe3+·e的能力,以增大半径而使其结构更趋稳定[17],且形成Co3+·e的倾向大于形成Fe3+·e;相应地,在催化循环中Fe3+·e失去电子的倾向大于Co3+·e。因此要维持整体的催化循环平衡,需要较多的Fe3+·e和较少的Co3+·e满足催化循环时B位离子脱电子的需求。在x<0.4时,B位离子吸引电子能力不足,活性较低;x>0.4时,B位离子脱电子更趋困难,从而使催化剂活性迅速降低。 图1 催化剂XRD谱Fig.1 XRD patterns of catalysts 图2 催化剂SrFe(1-x)CoxO3中x值对活性的影响Fig.2 Effect of x in SrFe(1-x)CoxO3 on catalytic activity 存在不同金属组成时,煅烧温度与钙钛矿结构的完整性密切相关[18]。制备SrFe0.6Co0.4O3催化剂时,考察了制备温度对其晶体结构和催化活性的影响(见图3、图4)。从图3的XRD谱中看出,在700~900 ℃ 范围制备时,都能形成钙钛矿结构。在温度低于900 ℃煅烧时,温度越低,其衍生峰变宽变低,说明其结晶完整度较低;在1 000 ℃煅烧时,除了ABO3型特征峰以外,出现大量杂晶峰,说明ABO3型晶体会出现因高温分解而析出氧化物的趋势。900 ℃煅烧时能够形成衍射峰形尖锐、峰强度最高、且没有杂质峰的钙钛矿型SrFe0.6Co0.4O3纯晶体催化剂。从图3和图4可以看出,晶体结构完整度与催化活性密切相关,采用900 ℃煅烧制备条件可得到晶体结构完整度高、活性高的SrFe0.6Co0.4O3催化剂,900 ℃为最适制备温度。 图3 不同温度制备的SrFe0.6Co0.4O3 XRD谱Fig.3 XRD patterns of SrFe0.6Co0.4O3 prepared at different temperatures 图4 不同温度煅烧对MG降解率的影响Fig.4 Effect of calcination temperature on degradation rate of MG 图5 催化剂量对MG降解率的影响Fig.5 Effect of the catalyst amount on degradation rate of MG 图5是在相同反应原液加入不同量的SrFe0.6Co0.4O3催化剂对MG的降解率的影响。从图5可以看出:在无催化剂情况下,反应液MG不降解;随着催化剂的加入,反应液MG发生降解作用。另外,从曲线e和f看出,当催化剂大于0.04 g、反应时间达到25 min后,MG的降解率可达到100%。 图6是采用900 ℃焙烧制备的SrFe0.6Co0.4O3催化剂的SEM形貌照片,从中看出,该催化剂外观以无规则堆叠的二维“蜂窝”片状结构为主。 图7是N2-BET分析曲线,其形状介于Ⅱ型与Ⅲ型等温线之间,更趋近于Ⅲ型等温线,说明催化剂SrFe0.6Co0.4O3与N2吸附作用很弱;图7中的催化剂吸附支与脱附支几乎重合、回滞环很小,说明催化剂中不存在“墨水瓶”类型孔结构[19],以敞口孔或直孔结构为主;通过BET测试法测定该催化剂比表面积为11.45 m2·g-1,说明其吸附作用很弱[20]。 图6 催化剂SrFe0.6Co0.4O3 的SEM照片Fig.6 SEM image of SrFe0.6Co0.4O3 catalyst 图7 SrFe0.6Co0.4O3催化剂的BET曲线Fig.7 BET curves of SrFe0.6Co0.4O3 catalyst 图8是SrFe0.6Co0.4O3催化剂表面XPS谱,图8(a)为SrFe0.6Co0.4O3进行降解反应前的新鲜催化剂与反应平衡后催化剂的XPS全分析图谱。由图8(a)可知,平衡后催化剂在398 eV附近出现N的峰,说明降解反应过程中产生了含N的化合物;8(b)、(c)为新鲜催化剂与平衡催化剂的Fe2p、Co2p谱,从图8中看出,SrFe0.6Co0.4O3中B位离子同时存在Fe2+/Fe3+和Co2+/Co3+4种价态离子,且反应前后Fe2+/Fe3+含量由1.33增长到1.39,Co2+/Co3+含量由0.55增长到2.35,说明Co3+具有更强的吸引电子的能力,这与本文2.2节的实验结果与机理推测相一致。 图8 SrFe0.6Co0.4O3样品的光电子能谱Fig.8 XPS spectra of catalyst SrFe0.6Co0.4O3 通过上述实验数据和表征分析推测,ABO3型催化剂SrFe0.6Co0.4O3催化降解MG为常规固液催化过程,催化剂的强吸电子能力降低了降解反应的能垒,促使反应快速进行[21]。结合前述实验结果,推测其催化反应机理如下: (3) (4) 随反应进行,当Co2+结构比例偏高时,则在进行Fe2+/Fe3+和Co2+/Co3+之间电子转移,以达到趋向晶格的结构稳定与能量最低: (5) (6) (7) 上面四式相加,总反应式为: (8) 这一机理可简述为:催化剂B位Co3+吸引溶解氧形成活性氧[O2]+及B位离子Co2+;活性氧[O2]+完成对MG的氧化反应后,其正电荷转移到B位Fe2+上形成Fe3+,Fe3+的正电荷再转移到Co2+得到Co3+,完成催化过程的电荷转移与循环。 根据这一反应机理,也能较好地解释2.5节中催化反应前后,催化剂中Fe2+/Fe3+比例由1.33增长到1.39;Co2+/Co3+比例由0.55增加到2.35这一实验现象。新鲜催化剂投入反应体系后,吸附溶解氧,使B位离子的低价态分布数量增加,所以反应后的平衡剂中Fe2+/Fe3+和Co2+/Co3+比例增加。 根据Goldschmidt离子半径容差规则,设计出用于降解孔雀石绿(MG)的钙钛矿ABO3型催化剂SrFe(1-x)CoxO3,当x=0.4时,催化剂SrFe0.6Co0.4O3对MG降解活性最高。催化剂制备温度对其晶体结构完整度和催化活性影响较大,采用900 ℃煅烧制备条件可得到晶体结构完整度高、活性高的SrFe0.6Co0.4O3催化剂。表面形貌与特性研究表明,SrFe0.6Co0.4O3催化剂粒子结构为无规则堆叠的“蜂窝”片状。XPS分析表明,B位离子同时存在Fe2+/Fe3+和Co2+/Co3+4种价态离子,且反应前后,4种离子的分布比例有较大变化。推测该催化反应机理为,催化剂首先使反应体系溶解O2变为活性极高的过渡态[O2]+,[O2]+使MG在常温下被氧化降解,这一机理也能够较好地解释催化剂反应前后B位离子4种价态分布的变化。
2.2 催化剂B位离子复配比例
2.3 催化剂制备温度

2.4 催化剂用量及反应时间

2.5 催化剂SrFe0.6Co0.4O3的形貌与表面特性



3 机理探讨
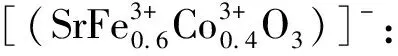
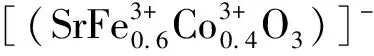
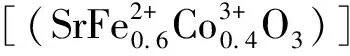
4 结 论
