聚合物微针载药系统研究进展
2021-12-13陈怡宋婷陈雯琳李海梁卢爱玉张峻颖
陈怡,宋婷,陈雯琳,李海梁,卢爱玉,张峻颖
(中国药科大学中药制药系,江苏 南京 211198)
经皮给药是替代口服和注射的有效途径,它不仅可以避免肝脏的首过效应和药物在胃肠道的降解,且给药方便以利于患者的自我管理[1]。自上世纪70年代以来,FDA已批准了多种透皮产品的上市,如Emsam、Daytrana、Secuado、Twirla等[2],这表明了透皮制剂具有广阔的研发前景。然而皮肤的屏障作用使得药物递送到体内的剂量有限,因而提高药物尤其是大分子药物的经皮递送效率已成为研究的热点。目前,研究人员已成功运用了多种手段来提高药物的经皮渗透,如:离子电渗[3]、超声导入[4]、电穿孔[5]、化学促渗[6]、纳米制剂[7]、微针技术[8]等。微针(microneedle)是一种新型的透皮给药制剂,其通过在皮肤表面形成微米级别的孔道,促进药物在体内的递送。目前微针载药系统已应用于疫苗、皮肤病、糖尿病、高血压、眼科等领域,本文将主要从以上热门研究领域综述近些年的研究成果。
1 微针透皮给药的原理
人体皮肤的总厚度为0.5~5 mm,主要分为3个不同的功能层:皮下组织,真皮层和表皮层(见图1)[9]。其中角质层(SC)是表皮层的浅表部分,其厚度约10 μm,为皮肤提供屏障功能[6]。SC由5到20层片状结构的角质细胞组成,角质细胞间充斥着脂质,呈现“砖-泥结构”,SC中角质细胞的致密排布是影响药物透过皮肤进入体内的主要影响因素。真皮层的厚度约为3~5 mm,主要由结缔组织组成,皮下组织由脂肪细胞组成,充当皮肤表皮和真皮层的支撑部分,药物应穿透所有三层才能达到全身循环。

图1 皮肤的结构示意图
微针是经微电子机械技术加工得到的微米级精细针状结构,针部长度一般为25~1 000 μm,通常由金属、玻璃、硅、聚合物等材料制备而成。微针通过在皮肤表面形成微米级别的孔道,使得大分子药物(>500 Da)以最小的侵入方式透过角质层的屏障,增加经皮渗透效率,到达特定的深度发挥局部或者全身作用。
2 微针的分类和特点
目前研究的微针主要如图2,分别为实心微针、涂层微针、中空微针、可溶微针、快速分离微针和水凝胶微针。
2.1 实心微针 实心微针是由金属、硅、玻璃等材质制成,利用微针穿透角质层形成可逆的微通道,随后再配合药液,乳膏或贴剂使用,这种方法显著提高了药物的被动转运。此方法的主要缺点是微通道开放时间有限,有可能过早停止药物的输送[10]。
2.2 涂层微针 涂层微针是对固体微针的表面进行涂层,涂层一般为药物或疫苗[11],该微针插入皮肤后药物或疫苗从涂层表面扩散到更深的表皮层。涂层微针也存在一些限制,如涂层载药量较低;涂层的厚度会影响微针穿透皮肤的能力等。
2.3 中空微针 中空微针的作用与皮下注射制剂相似,在皮肤穿孔后,药物溶液通过微针的中空结构进入体内[12]。由于这些针头的尺寸更短,因此患者对这种方法的接受程度高于传统注射方法。但中空微针的制备复杂且昂贵。
2.4 可溶微针 可溶微针是利用水溶性或可生物降解的载体材料,将药物包封于针部制成的微针[13]。与前几种微针相比,它生物相容性好,药物的释放速率也可以通过改变微针的载体材料而调节,是目前研究的热点。
2.5 快速分离微针 快速分离微针是一种新型微针,由载有药物的水溶性针部与不溶性的聚合物背衬构成[14]。其设计的意义是微针施加到皮肤表面后,针尖与背衬可以快速分离,在短时间内可以去除背衬。
随着微针技术的发展,已经开发了更为复杂的设计。例如在针尖和背衬之间的结构中插入气泡,使插入后的针尖可以轻松快速地从背衬结构中分离,从而使针尖留在皮肤中释放药物[15]。Lopez-Ramirez等[16]制备了一种主动分离的聚合物微针,装载在微针贴片中的镁微粒作为内置引擎,与组织液接触快速反应生成H2,可实现更深更快的皮内药物的递送。Li等[17]使用可生物降解材料制备了泡腾微针,该贴剂在背衬中加入了泡腾剂,在与皮肤接触后针尖和背称层可以快速分离,以缓慢释放左炔诺孕酮。
2.6 水凝胶微针 水凝胶微针在插入皮肤时,吸收皮肤组织液以形成连续的,不可阻塞的微通道,而药物通过网状结构的间隙进入体内,该方法不会在人体内残留针体材料[8]。但是其机械强度与溶胀率和溶胀速率之间的问题影响了其实际的应用[18]。
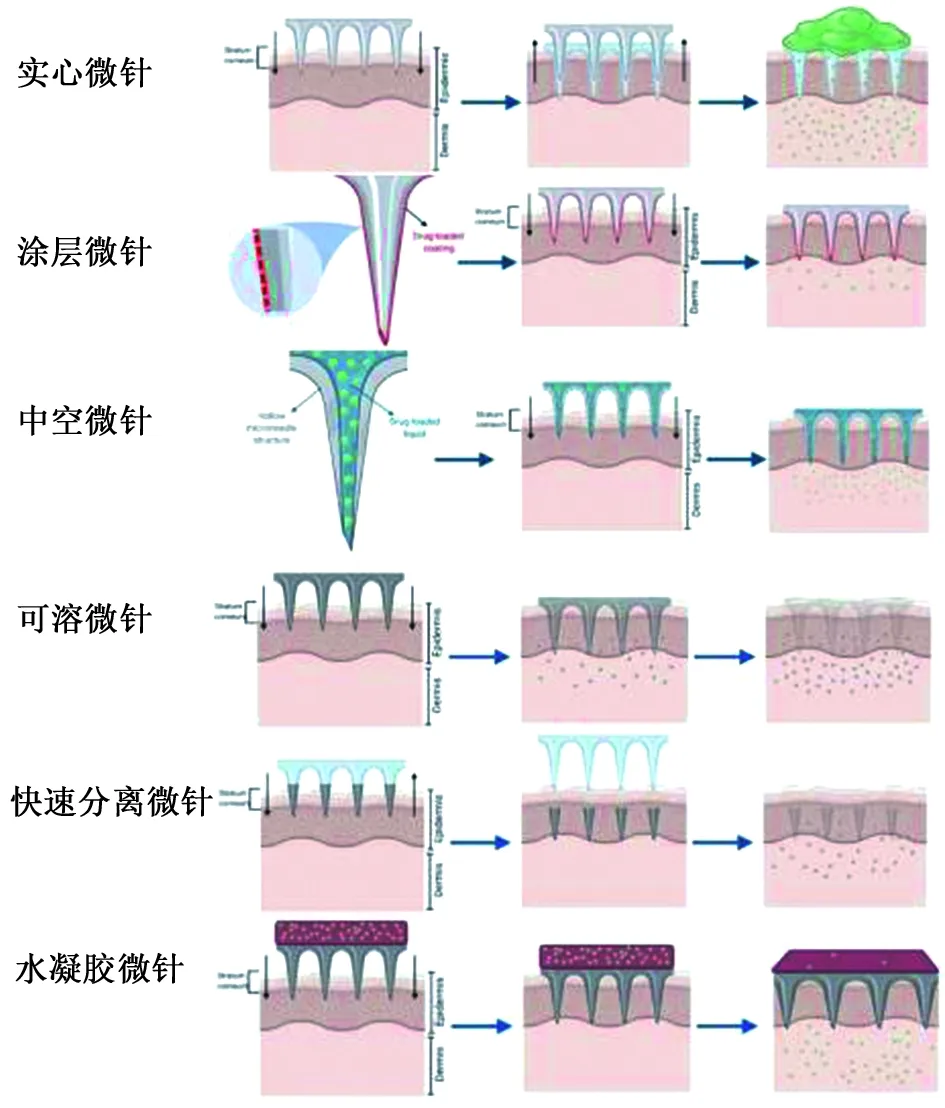
图2 不同类型的微针阵列[19]
3 聚合物微针载药系统的应用
目前聚合物微针的研究方向主要针对的是皮肤类疾病,如黑色素瘤、糖尿病、疫苗、高血压、关节炎等,其主要的施药部位为皮肤,但随着研究的更加深入,微针的研究部位也逐渐扩大为眼部、口腔黏膜等。下文通过不同的给药部位总结了聚合物微针近5年来的应用研究。
3.1 经皮给药的聚合物微针载药系统
3.1.1 免疫接种 皮肤是人体重要的屏障,具有高密度的抗原呈递细胞和具有免疫活性的辅助细胞,可以调节先天免疫反应[20],长期以来一直被认为是疫苗递送的高度免疫原性靶标[21]。目前,市面上绝大多数疫苗采用皮下注射的方式进行给药,冷链储存和运输成本过高,患者依从性差。目前许多研究已表明微针是一种十分有潜力的接种方式。McCrudden等[22]以聚(甲基乙烯基醚-马来酸)为载体材料制备了可溶微针,在鼠模型中递送模型抗原卵清蛋白。结果表明,免疫球蛋白和细胞因子显著增加,从而激活了体液和细胞反应。Rouphael等[23]制备了可溶解的微针贴片用于流感疫苗接种,可产生强大的免疫反应,已进入临床研究。Yan等[24]使用透明质酸微针加载针对肺结核的Ag85B DNA疫苗在皮肤上进行了免疫接种,结果表明免疫剂量低(4.2 μg)时,微针贴片(MNP)和注射(IM)免疫之间没有显著差异,但剂量较高(12.6 μg)时,MNP免疫比IM更好地引起抗体应答。
微针也给新冠病毒候选疫苗提供一种全新的接种方式,Kim等[25]以羧甲基纤维素为载体材料制备了含有MERS-CoV-S1和SARS-CoV-S2疫苗的可溶微针,证实其能够产生有效的抗原特异性IgG反应,并且微针疫苗递送产生的免疫应答比传统皮下注射产生的免疫应答要强,此项研究为针对COVID-19和其他新兴传染病的微针蛋白亚基疫苗的临床开发提供了依据。
3.1.2 糖尿病治疗 近些年胰岛素微针的开发也取得了巨大的进展,多款中空胰岛素微针也已进入临床试验阶段[26]。Chen等[27]用γ-PGA为针部材料制备了胰岛素微针,大鼠实验结果表明,负载胰岛素的微针降血糖作用与常规皮下胰岛素注射所观察到的效果相当,生物利用度高达90%~97%,且连续给药血浆胰岛素浓度曲线无明显差异。顾臻团队开发了血糖响应智能胰岛素/胰高血糖素复合贴片,通过动态释放胰岛素或胰高血糖素来模仿β细胞和α细胞对血糖控制的固有反调节作用,以“同时响应”高血糖和低血糖情况[28]。Tong等[29]设计了将葡萄糖和H2O2反应性聚合物囊泡与聚合物微针结合而成的双反应胰岛素递送装置,与皮下注射或仅加载胰岛素的微针相比,该微针表现出更有效的降血糖作用,这表明该胰岛素传递系统对于糖尿病的治疗具有重要的意义。
3.1.3 皮肤病治疗 微针在皮肤病的治疗及美容方面研究很多,目前针对的皮肤病主要有:瘢痕、皮肤恶性黑色素瘤、牛皮癣、色素性疾病、脱发等[30]。Fakhraei等[31]制备了戊二酸可溶微针(DMN-VPA),并通过体外和体内实验证明DMN-VPA比局部VPA更有效地诱导头发再生。Huang等[32]制备的水凝胶微针同时加载阿霉素和曲美替尼,在B16细胞异种移植裸鼠模型中实现了协同作用。Zhao等[33]使用尖端加载5-氨基乙酰丙酸(ALA)的快速溶解微针与光动力疗法(PDT)结合,在皮下小鼠肿瘤模型中,证实ALA微针组的PDT疗效远高于注射组。另外,Du等[34]制备了氨甲蝶啶(MTX)可溶微针来治疗牛皮癣,从皮肤厚度和Ki67表达水平上可知,MTX微针比口服MTX更为有效。Lin等[35]用HP-β-CD和HA的复合材料制备了曲安奈德的可溶微针,以新西兰兔耳朵为模型,使用微针后瘢痕升高指数值降低,正常值降低,胶原I的mRNA表达下降,TGF-β1下降。
3.1.4 诊断治疗 聚合物微针具有吸收皮肤组织液(ISF)的出色能力,其在刺穿皮肤时,吸收ISF获得机械强度以承受刺穿压力。ISF可用作生物标志物的来源,使聚合物微针成为一种微创的诊断方法[36]。Chang等[37]用交联化甲基丙烯酸透明质酸制成微针贴片可在短时间内提取出足够的ISF,大大促进了及时的代谢分析。He等[38]用PVA和壳聚糖制成水凝胶微针贴片提取ISF以监测血糖,展示了微针的另一潜在用途。
3.2 非经皮给药的聚合物微针载药系统
3.2.1 眼部给药 很多眼部疾病如青光眼、白内障、黄斑病变、糖尿病视网膜疾病等都有很大的失明风险,一般往眼睛区域内进行药物注射治疗。其主要的缺点是依从性差,生物利用度也较低[39]。目前,可溶解聚合物微针的眼部给药是一种新的治疗趋势。Bhatnagar等[40]成功地使用贝西沙星的PVP/PVA微针治疗角膜和眼内的细菌感染。Than等[41]设计了一种可拆卸微针眼罩,这些微针可以穿透眼组织,双层载药结构大大增强了治疗功效,使用角膜新生血管形成作为疾病模型,实验表明该微针使新生血管面积减少约90%。
3.2.2 口腔黏膜给药 口腔是黏膜疫苗接种的十分有潜力的途径,口腔包含丰富的淋巴组织,其pH值比胃肠道更温和,有利于对生物制剂有效成分的保护。研究表明[42],口腔黏膜疫苗递送可引起与肌肉内疫苗相当的全身性体液和细胞免疫应答,并增强局部和在远端部位如鼻腔和女性生殖道的粘膜抗体应答水平。Wang等[43]通过乳化冻干法制备了甘露糖-PEG-胆固醇共轭物和负载HBsAg的脂质A双重修饰脂质体(MLL),并成功地构建HBsAg-MLL微针阵列(proHMA),结果表明经由口腔黏膜给予小鼠的proHMAs引起强烈的全身/黏膜反应。此外,微针还可以进行口腔局部治疗,如SEON-WOO等[44]使用HPMC和Carbopol 971为载体材料加载曲安奈德制备了可溶微针治疗口腔黏膜炎,证实微针贴剂比普通口腔粘膜制剂粘附力更强,递送药物效率更高。
4 展望
聚合物微针由于其生物相容性好、机械强度高、患者依从性好、经皮递送效率高等诸多优势在药物递送领域具有巨大的潜力,其未来在儿科用药的开发中也具有很大的前景。然而其存在的一些问题对其实际应用也提出了重大挑战:如载药能力不足;或载药量大时其机械强度降低;微针几何形状也极易发生断裂或变形等。我们相信,随着对微针递药系统的进一步研究,人们可以逐渐克服这些挑战,聚合物微针或许将来可成为首选的经皮递送途径。
