基于整合药理学策略的黄芪-丹参抗心肌梗死作用机制研究❋
2021-12-10刘志超陈金红高晟玮王治中陆安民王保和谷旭放
刘志超,陈金红,高晟玮,马 莉,王治中 ,陆安民,王保和,谷旭放△
(1.天津中医药大学,天津 300193;2.天津中医药大学第二附属医院,天津 300150)
随着2018年《心肌梗死全球定义(第四版)》指南的修订和发布,急性心肌梗死的诊断与治疗更加明确[1]。亚洲地区各国的研究也表明,早期出现症状与使用药物介入治疗的死亡率低于直接介入治疗的死亡率有关[2,3],而国内则呈现快速增长态势[4]。抗栓治疗是贯穿整个急性心肌梗死临床治疗的方案,包括经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)术后,患者需要长期服用抗血小板、稳定斑块治疗[5]。尽管指南中指出,以抗栓治疗为主,但存在一定风险,包括出血事件、消化系统不良反应。因而课题组致力于探索出一种新的治疗策略,通过中医药的辅助治疗起到“增效减毒”作用。
急性心肌梗死根据其症状、证候表现,属于中医学“胸痹”“真心痛”范畴,最早可追溯至《黄帝内经》中有所记载。现代中医专家对急性心肌梗死的证候演变规律进行总结并达成共识,即气虚、血瘀、痰浊为常见病因病机,证候组合中,以气虚血瘀证为主[6]。黄芪-丹参是中医临床益气活血常用药对,现代药理学研究也表明[7],黄芪-丹参配伍提取物在缺血性心肌中能够有效延缓心肌重塑的进展。
本研究初步对黄芪-丹参组合的相互作用以及对急性心肌梗死的治疗作用进行分子机制预测性挖掘,建立可信度较高的研究体系,从分子层面筛选丹参黄芪配伍抗心肌梗死气虚血瘀证的关键活性成分及靶点,为课题后续研究把握较为精准的方向。
1 数据库建立与研究方法
1.1 数据库建立
利用整合药理学平台[8](http://www.tcmip.cn /)的中药成分数据库、证候相关分子挖掘,结合2015年版《中国药典》中规范药材命名及成分名称,进行虚拟数据资料建库。检索“黄芪”“丹参”主要生物活性成分,自主命名数据作为备用。
1.2 药物靶标预测
利用TCMIP通过提取黄芪-丹参药物成分的化学分子指纹,并将其与Drug Bank(https://www.drugbank.ca/)数据库中获美国食品药品监督管理局(food and drug administration,FDA)批准的抗冠心病心肌梗死药物指纹进行比对,平台利用Tanimoto系数对结果进行评分,选定评分>0.8的为相似性药物,将相似性药物靶点作为黄芪-丹参药物组合的潜在机制靶点[9]。
1.3 疾病、证候靶标确定
以“myocardial infarction”作为疾病关键词,在GeneCard(https://www.genecards.org/)数据库、TTD数据库(http://bidd.nus.edu.sg/BIDD-Databases/TTD/TTD.asp)、DrugBank数据库(https://www.drugbank.ca/)、OMIM数据库(https://omim.org/)、DIGSEE数据库(http://210.107.182.61/geneSearch/)中进行检索全疾病相关靶标,利用Uniprot数据库(https://www.uniprot.org/uniprot/)转换蛋白名称,获取基因名称。最终利用Microsoft Office Excel文本进行去重,整理疾病靶标,建立疾病数据库。
再以“myocardial infarction”作为疾病关键词录入整合药理学平台疾病/证候靶标数据库中进行检索,证素[10]输入心胸刺痛、胸部闷滞,动则加重,伴乏力、短气、汗出等进行关键词检索,提取相应证候靶点信息。
1.4 PPI网络构建、分析与可视化
通过整合药理学平台的网络分析模块蛋白互相作用网络进行拓扑分析,以“节点连接度”的2倍中位数为卡值,选取中药靶点-疾病基因的关键节点(hubs);在此基础上,以“节点连接度”(degree)“节点紧密度”(closeness)“节点介度”(betweenness)的中位数为截取值,选取同时满足3个卡值的节点为黄芪-丹参的潜在靶点,然后对关键靶标网络进行通路富集分析,选取统计值P值排名前20的通路,构建完整的“中药-活性成分-核心靶标-关键通路”多层次关联网络,并进行可视化数据分析。采用TCMIP构建黄芪-丹参最密切关键靶点的PPI网络;通过TCMIP分析平台对关键靶基因进行GO功能富集分析和KEGG富集分析,利用Jvenn(http://www.bioinformatics.com.cn/static/others/jvenn/example.html)在线绘图[11]获取韦恩图。
2 结果
2.1 黄芪-丹参成分靶标预测及分析
通过TCMIPV2.0平台对黄芪、丹参化学成分的分析结果可知,黄芪共收集了27个化学成分,包括黄芪甲苷(astragaloside IV,AS-IV)、黄芪多糖(astragalus polysaccharides,APS)、异黄芪皂苷等,其中潜在靶标数量为218个。丹参共收集96个化学成分,主要为丹参素、丹酚酸B、丹酚酸A、丹参酮Ⅰ、隐丹参酮、丹参酮ⅡA等,其中潜在靶标数量151个。
对黄芪、丹参后选靶标进行基因功能分析和通路富集分析发现,其功能多与类固醇激素介导的信号通路、离子跨膜转运、神经系统过程通路、细胞内受体信号通路、氨基丁酸信号通路、γ-氨基丁酸信号通路(γ-aminobutyric acid,GABA)、膜电位调节、氧化还原过程通路等相关。这些候选靶标参与通路的信息发现主要在神经递质的调节、心肌能量代谢、脂类代谢等通路。
2.2 心肌梗死疾病靶标及相关基因
研究者对全疾病相关潜在靶标合并去重后共计1062个,其中与黄芪-丹参药对组合密切相关的共同靶向基因共计49个,如韦恩图(见图1)。这些靶点的作用机制主要从调控炎性因子(白介素-2、白介素-6、白介素-8)[12]、凝血因子-2(Recombinant Coagulation Factor II,F2)[13]、基质金属肽酶[14]、过氧化物酶体增殖物激活受体γ(peroxisome proliferative activated receptor gamma,PPARG)[15]、肿瘤坏死因子[16]、磷脂酰肌醇-4-磷酸3-激酶催化亚单位2型α[17]、eNOS[18]、血管内皮生长因子[19]、前列腺素内过氧化物合酶[20]、细胞凋亡蛋白酶[21]、前列腺素内过氧化物合酶[22]等共同作用下发挥作用。
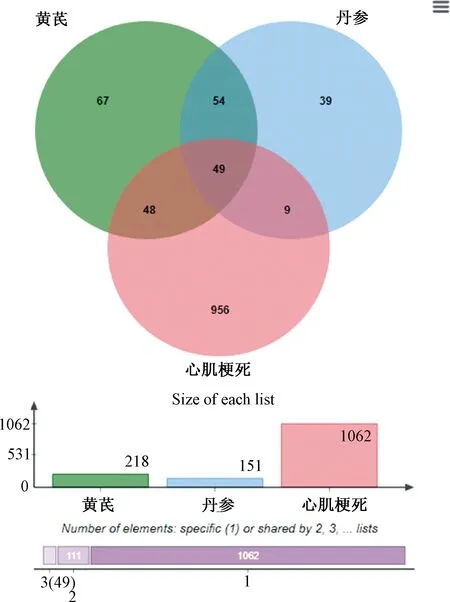
图1 心肌梗死疾病靶标及相关基因韦恩图
2.3 心肌梗死气虚血瘀证素靶标
根据中医学对气虚血瘀证的描述,划分证素包括胸闷、胸痛、乏力、短气、汗出、舌紫暗、脉虚无力等。其中血瘀证素(胸闷胸痛)包含159个相关靶标,气虚证素(乏力短气、汗出)包含143个相关靶标。
2.4 黄芪-丹参抗心肌梗死候选基因的GO富集分析
表1示,通过对黄芪-丹参-心肌梗死候选靶标进行基因功能分析和通路富集分析,罗列出候选作用靶标(P值前20的)所具有的功能。由此可见,黄芪-丹参候选靶标参与的通路,主要涉及在细胞增殖的负调节、细胞凋亡过程的负调控、细胞介导因子、DNA转录、基因表达调控等多方面。

表1 黄芪-丹参抗心肌梗死的候选基因的GO富集分析
2.5 黄芪-丹参抗心肌梗死核心靶标的KEGG富集分析
黄芪-丹参抗心肌梗死关键网络靶标的KEGG通路富集分析结果(见表2),靶标主要涉及白介素、肿瘤域突变体、卵巢肿瘤结构域蛋白酶、eNOS、TGF-β受体信号传导激活Sma和Mad相关蛋白(Sma -and Mad -related protein,Smad)通路、激酶非活性BRAF对加速纤维肉瘤蛋白(rapidly accelerated fibrosarcoma,RAF)信号的异常激活等角度。

表2 黄芪-丹参抗心肌梗死核心靶标的KEGG富集分析
2.6 黄芪-丹参抗心肌梗死的“中药-成分-靶点-通路”多维网络分析
图2示,基于黄芪-丹参药靶与心肌梗死靶标的PPI 网络信息,进行构建黄芪-丹参治抗心肌梗死的“中药-成分-靶标-通路”多维网络图,不同颜色的节点是按照基因间相互作用的紧密度进行聚类。图2可直观看出,黄芪-丹参药对通过中药材的多成分,从而达到多途径、多层次、多靶点、多环节的抗心肌梗死作用,能有效预测到中药、证素、疾病、靶点之间可能存在的联系,此外复杂的网络图也间接反映出药物之间相互作用的复杂程度。黄芪-丹参药对组合共包含123个化学成分,潜在靶标369个,这些成分通过联合调控白介素、肿瘤域突变体、卵巢肿瘤结构域蛋白酶、eNOS、TGF-β、激酶非活性BRAF等靶标,直接或间接参与炎症信号通路、雌激素信号通路、SMAD通路、RAF信号的异常激活、调控基因的转录等作用。

图2 黄芪-丹参抗心肌梗死的“中药-成分-靶点-通路”多维网络分析
3 讨论
阐明中医证候的本质,一直是中医学者们力求解决的科学问题之一。中医证候往往被拆解为多个证素进行深入挖掘,即按照证候表现将证素划分到某一西医疾病范畴内,然后再进行分子量级的基础实验研究,研究本身具有科学意义,但研究成果与中医的联系往往较牵强附会。此外,天然药物的成分较为复杂,成分之间的协同/拮抗作用尚未完全阐明,因而以单体活性成分代替生药进行生物学研究欠为妥当。整合药理学结合中药成分、证候要素、疾病靶点的多层次研究,从药物自身出发,能够较为完善地完成中药-证素-疾病-靶标-通路的衔接性研究,形成中医药现代研发体系,从分子角度解释中医疗效内涵。
本研究旨在探讨中药抗心肌梗死气虚血瘀证证候本质,完善现有证据,并提出新的中医证候本质研究策略。目前国内诸多团队都在进行这一工作,其中韩晶岩教授团队对此进行了深入研究[23],对芪参益气滴丸通过心肌能量代谢途径、心肌线粒体复合物及其亚单位、调控线粒体复合物去乙酰化酶-1、小G蛋白家族的Ras同系物家族成员A(ras homolog family member A,RhoA)/Rho相关卷曲螺旋蛋白激酶-1(rho-associated coiled-coil kinases1,ROCK1)、细胞骨架、心肌结构、心功能、心脏微循环动态等综合研究,部分阐明了心气虚血瘀的科学内涵,揭示了补气活血的作用机理,及其主要成分协同作用的机理,支撑了益气活血药物在治疗心肌缺血再灌注损伤和心肌肥厚方面的应用。
本研究借助智能化数据挖掘平台TCMIP v2.0和国际通用靶标、基因数据库,对益气活血药对黄芪-丹参的药物候选靶标与疾病进行关联,并以网络可视化形式展现出来,预测其可能靶标和分子信号通路。分析结果表明,黄芪-丹参能够联合调控炎性因子、信号通路、调节能量代谢、调控基因转录。此外,多维网络分析显示,黄芪-丹参潜在靶标与炎症靶标的共同生物进程调控细胞周期蛋白依赖性激酶抑制剂(cyclin-dependent kinase inhibitor,CDKN)转录与其心梗机制密切相关,在乏力、短气证素表现中也较为明显。该通路的支持文献表明,细胞周期蛋白依赖性激酶抑制剂对冠心病的易感性也有一定影响[24],用模仿CDKN2A /2B基因作用的药物进行治疗可能是一种延缓动脉粥样硬化的有前途疗法[25]。此课题将继续深入开展对该通路的动物、细胞实验,以期对心肌梗死气虚血瘀证的进一步揭示。
