lncRNA PVT1沉默对高糖诱导的血管内皮细胞增殖、凋亡及氧化应激的影响*
2021-12-10罗建华范元硕冯志宇
刘 波, 顾 燕, 罗建华, 范元硕, 冯志宇
(1. 贵州省人民医院 内分泌科, 贵阳 550002; 2. 贵州省人民医院 肿瘤科, 贵阳 550002)
糖尿病是全球广泛存在的一种代谢性疾病,主要特征是由于胰岛功能异常导致血糖浓度升高,加速机体消耗性损伤[1]。糖尿病血管病变是糖尿病的主要并发症之一,主要包括糖尿病微血管病[2],糖尿病视网膜病变[3]、糖尿病性肾病、糖尿病性坏疽[4],糖尿病性脑血管病[5]和心血管疾病[6]。其中内皮细胞(endothelial cells,ECs)是血管系统的重要组成部分,内皮细胞功能异常是糖尿病性并发症的关键因素[7]。
内皮细胞是血管的重要组成部分,异常的增殖和迁移都会导致血管病变的发生,进一步影响机体功能,比如视网膜病变,动脉粥样硬化等[8]。有研究证实,持续性高糖会诱发产生机体代谢紊乱,进而影响内皮细胞损伤,加速血管病变发生。有研究报道紫草素可以激活Nrf2/HO-1信号通路下调细胞中氧化应激,减缓高糖诱导的血管内皮细胞凋亡,发挥保护作用[9]。此外郭巍巍[10]等研究发现,IL-35可通过调节血管内皮细胞氧自由基的水平而对抗高糖诱导的细胞凋亡[10]。但是高糖诱导内皮细胞功能异常的确切机制尚没有明确。
长链非编码RNA(long non-coding RNAs, lncRNAs)是长度大于200个核苷酸的非编码RNA[11]。lncRNA在细胞增殖,分化,凋亡等方面发挥关键作用。在心血管疾病领域,有研究发现lncRNA影响内皮细胞功能直接影响心血管疾病的进展。在糖尿病大鼠中,lncRNAMALAT1的下调可抑制心肌细胞凋亡,抑制视网膜内皮细胞的增殖和迁移,减缓视网膜血管损伤炎症反应[12]。有研究表明,lncRNAH19调控人脐静脉内皮细胞的增殖和凋亡[13]。在卵巢癌发展过程中lncRNA PVT1(plasmacytoma variant translocation 1)过表达可以抑制细胞凋亡[14]。虽然已有研究证实lncRNA可以调控血管内皮细胞功能发挥作用,但是lncRNA PVT1是否也可以调控内皮细胞,影响高糖诱导的细胞增殖,凋亡和氧化应激仍需要阐明。本研究主要探讨了抑制lncRNAPVT1的表达对高糖诱导内皮细胞的增殖,凋亡和氧化应激的影响,旨在为糖尿病性血管疾病的治疗提供确切的理论依据。
1 材料与方法
1.1 人脐静脉内皮细胞(HUVECs)的培养及分组
HUVECs购自美国ATCC公司。复苏冻存的HUVECs细胞,加入含有10%胎牛血清的DMEM培养基,在37℃,5% CO2培养箱中静置培养。选取生长状态较好的细胞用0.25%胰蛋白酶消化1 min后,加培养基终止。用PBS轻轻吹打,制成细胞悬液。待细胞长满瓶底75%,按照1∶2传代,指标检测实验采用第4~6代细胞。实验中主要分为四组:对照组(5.5 mmol/L D-葡萄糖培养基),高糖组(30 mmol/L D-葡萄糖培养基),高糖+siNC组(高糖组中细胞转染阴性对照组),高糖+siPVT1组(高糖组中细胞转染siPVT1)。
1.2 细胞转染及实时定量PCR(RT-PCR)检测
选取生长状态良好的细胞,待细胞生长至80%左右时,运用LipofectamineTM2000转染试剂盒转染siPVT1及siNC(阴性对照组),分别用无血清培养基稀释适量lipofectamine2000合成的RNA/质粒,轻轻混匀,静置5 min。弃掉培养基,添加有血清的培养基,分别于转染24 h,48 h后收集细胞,根据试剂盒说明书提取总RNA,测浓度后-80℃保存备用。采用SYBR Green 法检测PVT1的相对表达水平。引物序列由上海通用生物公司合成提供。siPVT1上游:5’-GCUUCUCCUGUUGCUGATT-3’,下游:5’-UAGCAGCAACAGGAGAAGCTT-3’;siNC上游:5’-GCUACGAUCUGCCCAAGAUTT-3’,下游:5’-AUCUUAGGCAGAUCGUCGCTT-3’。
1.3 MTT检测细胞增殖活力
分别选择对数生长期的细胞,胰蛋白酶消化制成细胞悬液,调整细胞浓度为1×105cells/ml接种于96孔板中,每孔180 μl,设置3个复孔。37℃培养24 h,48 h后,吸取弃掉培养基。每孔加入20 μl MTT(终浓度为5 mg/ml),继续培养6 h后加入150 μl DMSO溶解,轻轻震荡,直到结晶全部溶解,用酶标仪在570 nm波长处检测各孔吸光度,吸光度越大,细胞数越多,表明细胞增殖能力越强。
1.4 流式细胞术检测细胞ROS水平
培养HUVECs 24 h后,加入终浓度为10 μmol/L的H2DCFDA,置于CO2恒温培养箱中,37℃培养20 min后弃掉培养液。PBS洗轻轻吹洗3 次,加入0.01%EDTA的胰蛋白酶消化细胞,制成细胞悬液备用。利用FACScan流式细胞仪检测细胞的ROS水平。
1.5 流式细胞术检测细胞凋亡水平
收集处理好的细胞,1×PBS洗3次后加入800 μl PBS制成悬液,置于1.5 ml EP管中,避光条件下分别加入5 μl Annexin V及5 μl PI,轻轻混匀,室温条件避光反应20 min,上流式细胞仪检测凋亡率,凋亡率=坏死细胞数/总细胞数×100%
1.6 蛋白免疫印迹法(Western blot)检测细胞凋亡相关蛋白的表达水平
收集细胞,1×PBS洗3次,加入RIPA裂解液提取蛋白,冰上裂解细胞30 min后,4℃低温高速离心,12 000 r/min,离心10 min,取上清备用。采用BCA试剂盒测定蛋白浓度,添加上样缓冲液,稀释为均一浓度,99℃金属浴加热5 min变性。10%SDS-PAGE胶电泳分离蛋白,转模,5%脱脂牛奶室温封闭3 h,加入稀释后的一抗(Bax,1∶1 000;Bcl-2,1∶1 000;cleaved-caspase-3, 1∶1 000; GAPDH,1∶900),4℃过夜孵育。1×TBST洗脱3 次,每次8 min,室温孵育HRP标记的二抗(抗兔,1∶10 000稀释)1 h,1×TBST洗脱3 次,每次8 min,ECL法暗室显影,应用凝胶成像分析仪测定蛋白条带灰度值,其中GAPDH为内参。
1.7 统计学处理
2 结果
2.1 转染后siPVT1后HUVECs细胞中PVT1的表达水平
实时定量PCR结果显示,和control+siNC组(0.78±0.19)比较,转染组中PVT1(0.37±0.07)的表达水平明显下调(P<0.01),结果表明siPVT1转染成功。
2.2 siPVT1对高糖诱导的HUVECs细胞增殖能力的影响
MTT结果显示(表1),和对照组比较培养24 h和48 h后高糖组中HUVECs细胞增殖活力显著降低(P<0.05)。转染siPVT1后,与HG+siNC组比较,培养24 h和48 h后,HG+siPVT1组中HUVECs细胞增殖活力显著增加(P<0.05)。结果表明,siPVT1可以增加高糖诱导HUVECs细胞增殖活力。

Tab. 1 The effects of siPVT1 on hyperglycemia-induced proliferation activity of HUVECs cells n=3)
2.3 siPVT1对高糖诱导的HUVECs细胞氧化应激和凋亡的影响
流式细胞术结果显示(表2, 图1),与对照组比较,高糖诱导的HUVECs细胞氧化应激和凋亡率均显著增加(P<0.05,P<0.01)。与转染组比较,HG+siPVT1组中细胞氧化应激水平显著减少,凋亡率也显著降低(P<0.05)。结果表明,siPVT1可以减少高糖诱导的HUVECs细胞的氧化应激,抑制细胞凋亡。
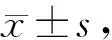
Tab. 2 The effects of siPVT1 on oxidative stress and apoptosis induced by hyperglycemia in HUVECs cells (%, n=3)

Fig. 1 Comparison of apoptosis in HUVECs in each group
2.4 siPVT1对高糖诱导的HUVECs凋亡相关蛋白的影响
采用Western blot检测,结果显示,与对照组比较,高糖组中Bax和cleaved-caspase-3表达水平均显著上调,Bcl-2表达显著下调(表3,图2,P< 0.05)。与HG+siNC组比较,HG+siPVT1组中HUVECs细胞中Bax和cleaved-caspase-3表达显著下调,Bcl-2表达显著增加(P<0.05)。

Tab. 3 Protein expressions of Bax, Bcl-2 and cleaved-caspase-3 in HUVECs induced by hyperglycemia n=3)

Fig. 2 Comparison of the expressions of apoptosis-related proteins in HUVECs in each group
3 讨论
随着生活水平的提高,糖尿病是现代社会发病率极高的一种代谢性疾病,伴随着并发症发病率增加,死亡率也逐年增加,因此研究糖尿病并发症的发病机制具有重要意义[15]。其中糖尿病血管病变是发病率最高的一类疾病,内皮细胞在高糖环境下的功能障碍被认为是糖尿病性血管病变的关键影响机制[16]。有研究表明,高糖环境下内皮细胞增殖能力下降,凋亡增加直接导致内皮功能异常,间接加重血管炎症发生[9]。此外有研究表明,内皮细胞凋亡是早期血管病变的关键启动步骤[17]。
lncRNA对于细胞功能的调控更加精细,已有的研究显示,lncRNA参与了染色质沉默、基因组印记等关键的生理过程[18,19]。此外lncRNA 与各种肿瘤的发生发展有着密切的关系,参与调控血管生成,肿瘤细胞侵袭,凋亡等的发展。 lncRNA PVT1位于原癌基因 MYC下游,已被证明与多种肿瘤的发生、发展密切相关,具有癌基因的作用[20]。有研究发现, lncRNA-PVT1可以促进肿瘤细胞的增殖和侵袭,那么PVT1是否可以影响内皮细胞的增殖和凋亡,参与血管病变的发展尚不十分清楚。因此本文主要采用转染siPVT1至HUVECs细胞中探讨抑制lncRNA PVT1对高糖诱导的HUVECs细胞增殖,氧化应激和凋亡的影响。
本实验中首先采用细胞转染siPVT1和siNC,RT-PCR结果证实PVT1表达显著降低,转染成功。MTT法检测siPVT1对高糖诱导的HUVECs细胞增殖能力的结果提示,siPVT1明显促进高糖诱导的细胞增殖。流式细胞术检测细胞凋亡和氧化应激的结果表明,lncRNA PVT1沉默可以显著抑制细胞凋亡和氧化应激。Bax是一种促凋亡蛋白,Bcl-2是抑制凋亡蛋白[21]。Western blot蛋白表达水平的结果显示,siPVT1可以显著下调高糖诱导条件HUVECs细胞中Bax和cleaved-caspase-3的表达,上调Bcl-2的表达水平。据此推测高糖诱导的血管内皮细胞中会产生大量氧自由基,细胞启动自我保护机制,加速抗氧化酶的合成和分泌。在氧化应激大范围发生时,Bax等促凋亡蛋白也会同时被激活,加速细胞凋亡,高糖持续刺激可以进一步加剧血管内皮细胞内氧化应激及凋亡。本实验提示,沉默PVT1的表达可以抑制高糖环境下内皮细胞的凋亡和氧化应激,促进增殖,减轻内皮细胞损伤。有关siPVT1在高糖诱导的内皮细胞中抗氧化应激和抗凋亡的分子机制尚有待进一步研究。
总之,由于内皮细胞在持续高糖环境下发生的功能异常导致血管病变的发生,这提示我们将保护内皮细胞作为治疗策略,降低糖尿病并发症,提高患者生活质量。我们的研究提供了一种治疗糖尿病血管病变的新策略,可以将PVT1作为潜在的靶基因,抑制内皮细胞凋亡,保护内皮细胞功能,这对未来寻找防治糖尿病并发血管病的措施具有重要指导意义。
