二氢苯并呋喃醇化合物体外抗衣原体活性研究*
2021-11-30石禹包小峰陆群乔进刘凌燕
石禹,包小峰,陆群,乔进,刘凌燕
(1.南通大学附属第三人民医院临床药学室,南通 226006;2.南通大学药学院,南通 226001;3.南开大学元素有机化学国家重点实验室,天津 300071)
衣原体是一类严格在真核细胞内专性寄生生活的革兰阴性病原体,它在宿主细胞内的增殖呈现两种不同的形态结构,称为原体(elementary body,EB)和网状体(reticular body,RB),衣原体具有从EB到RB再到EB独特的发育周期[1]。目前临床上衣原体感染的治疗主要依靠包括四环素类(如多西环素)、大环内酯类(如阿奇霉素)等抗菌药物[1],虽然在大多情况下抗感染治疗有效,但是耐药现象同样屡见不鲜,并且临床上衣原体持续隐蔽感染和复发的病例日益增多[2-3]。目前,仍没有可以投入临床使用的新型抗衣原体药物[4],本文主要研究合成的二氢苯并呋喃醇衍生物的抗衣原体活性,分析其抗衣原体作用的机制,为寻找更好的抗衣原体化合物提供基础。
1 材料与方法
1.1细胞、衣原体及化合物 细胞:人宫颈癌细胞HeLa S3、人喉癌上皮细胞Hep-2。衣原体:沙眼衣原体L2(CtL2),接种于HeLa S3细胞37 ℃培养,肺炎衣原体AR39(CpnAR39),接种于Hep-2细胞35 ℃培养。化合物:5个前期合成的二氢苯并呋喃醇类化合物由南开大学柳凌艳老师提供[5],简称为1-5,其结构如图1所示,固体粉末溶于二甲亚砜(DMSO)配制成100 mmol·L-1储存液,-20 ℃避光保存;实验时用完全培养基稀释至需要的浓度。

图1 化合物1-5的化学结构
1.2药品与主要试剂 DMEM/HIGH GLUCOSE 培养基购自美国Hyclone公司(AC11018291);胎牛血清购自美国Sigma公司(17D178);PBS购自美国Hyclone公司(AF29485473);细胞染料4',6-二脒基-2-苯基吲哚(4',6-diamidino-2-phenylindole,DAPI)购自武汉博士德生物工程有限公司(130307);叠氮钠购自青岛雪洁助剂有限公司(404C051);Na2HPO4、KH2PO4购自中国医药集团上海化学试剂公司(20130205)。四环素购自生工生物上海有限公司(200-593-8)洁助剂有限公司(404C051)本实验室自制的小鼠来源的抗鼠衣原体MoPn(C.muridarum strain Nigg II)抗血清用于检测CtL2[6],自制的小鼠来源的抗CpnAR39抗血清用于检测CpnAR39[7](KHP2016073),FITC亲和标记的山羊抗小鼠二抗够自美国Sigma公司(SLBX2002)。
1.3免疫荧光染色实验 将HeLa S3细胞接种于放置了盖玻片的24孔板中,培养过夜。按每孔感染复数(multiple of infection,MOI)0.2分别加入CtL2,并在感染的同时分别加入0.5,1,2,4,8,16 μmol·L-1的化合物,0.1% DMSO为阴性对照,11.25 μmol·L-1四环素为阳性对照[8]。在37 ℃继续培养36 h后,甲醇固定细胞,依次使用对应的检测抗体和FITC标记的二抗进行免疫荧光染色,同时使用伊文思蓝(Evans Blue)染色细胞质,通过Olympus IX51荧光显微镜采用20×物镜拍摄图片。
1.4感染性子代滴度测定实验 将细胞接种到48孔板中,培养过夜后按上述方法感染衣原体并加入化合物。对于CpnAR39,需室温900×g离心1 h以促进其感染。在37 ℃(CtL2)或35 ℃(CpnAR39)培养36 h后,刮取细胞,并超声裂解释放子代衣原体。将裂解液按1:10连续稀释后,再次感染96孔板中的细胞,36 h后同上方法进行免疫荧光染色,显微镜下计数包涵体的数量,并由此计算出每个样品中的感染性子代的滴度值。最后,将各实验组的滴度值按(阴性对照组-实验组)/ 阴性对照组×100% 得到各实验组的抑制率,采用非线性回归计算出半数抑制浓度(IC50)值,并以平均值(95%置信区间)表示。
1.5细胞毒性测定实验 取生长状态良好且处于对数生长期的细胞种于48孔板中,分别给予16 μmol·L-1化合物处理,对照组为0.1% DMSO。48 h后甲醇固定,Evans Blue染细胞形态(红色),DAPI染细胞核(蓝色)。或者将上述化合物处理的细胞在48 h后用胰酶消化,计数细胞数量。
1.6宿主细胞预处理实验 将16 μmol·L-1化合物与48孔板中的宿主细胞在37 ℃预孵育2 h,洗去化合物后按MOI 0.2加入CtL2感染细胞,继续培养36 h后进行免疫荧光染色,计数包涵体数量,包涵体的数量即反映感染进入细胞的衣原体数量。
1.7衣原体预处理实验 将16 μmol·L-1化合物与CtL2 在4 ℃预孵育1 h,洗去化合物后按MOI 0.2加入CtL2感染细胞,继续培养36 h后进行免疫荧光染色,计数包涵体数量,包涵体的数量即反映感染进入细胞的衣原体数量。
1.8后加药实验 以MOI 0.2的CtL2感染过夜培养的HeLa细胞,而后分别在感染后0(即感染同时加入化合物,阳性组)2,12和24 h加入16 μmol·L-1化合物,继续培养至36 h收获细胞,测定感染性子代的滴度值。以感染但不给予化合物处理作对照组,将各组滴度值按(对照组-实验组)/对照组×100% 计算各实验组的抑制率。
1.9撤药实验 以MOI 0.2的CtL2感染过夜培养的HeLa细胞,感染的同时即加入16 μmol·L-1化合物,而后分别在感染后2,12,24和36 h(即感染全程化合物处理,阳性组)洗去化合物,继续培养至36 h收获细胞,测定感染性子代的滴度值。以感染但不给予化合物处理作对照组,将各组滴度值按(对照组-实验组)/对照组×100% 计算各实验组的抑制率。
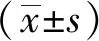
2 结果
2.1化合物对CtL2生长有抑制作用 免疫荧光染色结果显示(图2),随着化合物处理浓度的增加,包涵体数量逐渐减少、大小也逐渐减小,呈现明显的浓度依赖性关系。感染性子代滴度测定结果显示(图3),化合物1—5对CtL2感染性子代也呈现出明显的浓度依赖性抑制效果,该作用与免疫荧光染色实验的直接抑制效果一致,由此得出二氢苯并呋喃醇类化合物1—5可以抑制CtL2的生长。化合物对CtL2感染性子代滴度的IC50值见表1,为4~6 μmol·L-1。
2.2化合物对CpnAR39生长也有抑制作用 感染性子代滴度测定结果显示见图4,化合物对CpnAR39感染性子代也都呈现出明显的浓度依赖性抑制效果,其IC50值为4~8 μmol·L-1。结合CtL2结果可以得出二氢苯并呋喃醇类化合物1—5对衣原体的生长抑制作用具有广谱性。对比表1中5个化合物的IC50值发现,它们对CtL2 的抑制作用略强于CpnAR39。基于此,后面的机制探索将以CtL2为研究对象。
2.3化合物的抗衣原体活性与细胞毒性无关 Evans Blue和DAPI染色结果显示(图5A),与对照组相比,化合物处理48 h后的宿主细胞形态和细胞核均没有发生改变,表明在16 μmol·L-1(抗衣原体活性检测中的最高浓度)时化合物处理不存在明显的细胞毒性作用。活细胞计数实验也得到了相似的结果(图5B),与DMSO组相比化合物处理没有改变细胞数量,进一步证明5个二氢苯并呋喃醇类化合物对宿主细胞没有毒性作用。
2.4化合物对衣原体感染过程的影响 宿主细胞预处理实验显示(图6A),化合物处理组的包涵体数量与对照组(0.1% DMSO)相比没有统计学差别,说明宿主细胞的化合物预处理不会影响衣原体感染进入细胞。衣原体预处理实验显示(图6B),化合物处理组的包涵体数量与对照组相比也没有统计学差别,说明衣原体的化合物预处理也不会影响衣原体感染进入细胞。综上所述,本研究中的5个二氢苯并呋喃醇类化合物不影响衣原体的感染过程。
2.5化合物对衣原体增殖过程的影响 后加药实验结果显示(图7A),对化合物1,3,5来说,与阳性组相比,在感染2或12 h后加入对它们的抑制效果影响不大,只有在感染24 h后加入才会显著降低它们的抑制作用,说明化合物1,3,5对衣原体的生长抑制主要作用于12 h以后的阶段,即RB增殖和RB向EB转化阶段;对化合物2,4来说,与阳性组相比,在感染2 h后加入化合物就开始对它们的抑制效果产生影响,晚于12 h再加入化合物会极大影响它们的抑制能力,说明加入化合物时间越早则抑制效果越强,化合物2,4对衣原体的生长抑制需要全程的持续作用。
撤药实验结果显示(图7B),对所有化合物来说,与阳性组相比,在感染后2 h撤去化合物它们的抑制作用几乎消失,说明它们的抑制作用不在感染后的0~2 h即EB进入宿主细胞的阶段,而在EB进入宿主细胞之后的阶段;对化合物1,3,5来说,与阳性组相比,在感染后12 h撤去化合物对它们的抑制作用影响不大,说明化合物1,3,5对衣原体生长的2~12 h即EB向RB转化过程有很强的抑制作用;对化合物2,4来说,与阳性组相比,在感染后12 h撤去化合物对它们的抑制仍然影响很大,只有在感染24 h后撤去化合物才不会对它们的抑制作用产生影响,说明化合物撤去的越晚对它们的抑制作用影响越小,也进一步表明化合物2,4对衣原体的生长抑制需要全程的持续作用。
3 讨论
抗菌药物一直是临床上治疗衣原体感染的首选药物[9],然而抗菌药物耐药、持续感染和复发等现象对抗菌药物治疗衣原体感染带来了挑战。在缺少有效抗衣原体疫苗的情况下,寻找新的抗衣原体化合物可能是一个解决问题的有效途径[9]。
本研究以前期合成的5个二氢苯并呋喃醇类化合物为对象,报道了该类化合物的体外抗衣原体活性。5个化合物的抗衣原体活性具有广谱性,对可导致性病淋巴肉芽肿的CtL2(图1)和可引起肺炎等呼吸系统疾病的CpnAR39(图4)这两个人源病原株都具有较好的抑制作用。另外它们对鼠衣原体MoPn也具有抑制作用,只是活性相对要弱一些,IC50值都在10 mmol·L-1以上。

图2 免疫荧光染色代表图

图3 化合物对CtL2感染性子代滴度抑制率
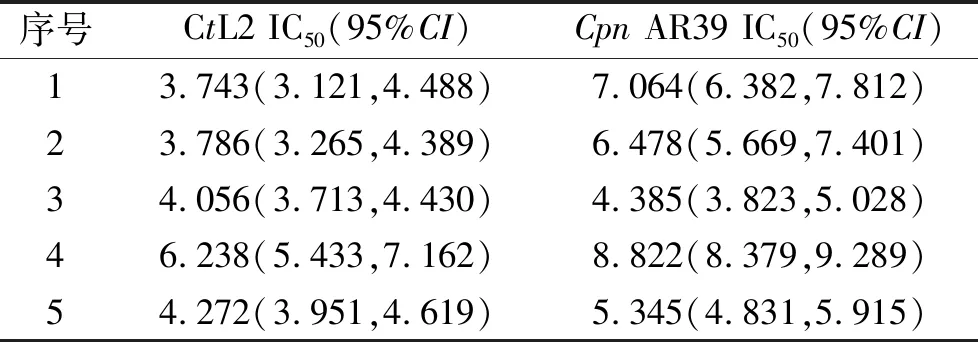
表1 化合物1—5抑制CtL2和Cpn AR39的IC50值

图4 化合物对Cpn AR39感染性子代滴度抑制率
衣原体是严格的宿主细胞内寄生病原菌,宿主细胞的生长状态也会影响衣原体的生长,为此本研究评估了化合物对宿主细胞的毒性作用。Evans Blue细胞形态染色、DAPI细胞核染色和活细胞计数实验表明(图5),本研究中的5个二氢苯并呋喃醇类化合物对宿主细胞没有毒性作用,这些结果证明了其抗衣原体活性与其宿主细胞毒性作用无关。

A.荧光染色代表图,Evans Blue(红色),DAPI(蓝色);B.活细胞数量。

A.宿主细胞预处理实验;B.衣原体EBs预处理实验。
衣原体的生长发育具有独特的EB和RB两相发育周期,因此其生长发育过程可分为感染和增殖两个阶段。在感染阶段,EB与宿主细胞接触粘附后通过胞吞作用进入细胞[1],本研究发现,将宿主细胞或EB分别与化合物预孵育均不能影响EB感染进入细胞(图6),这些结果说明5个二氢苯并呋喃醇类化合物的抗衣原体作用不涉及衣原体的感染过程。对于CtL2来说,一般情况下感染宿主细胞后的0~2 h主要是EB粘附、进入细胞的过程,2~12 h主要是EB→RB的转化过程,12~24 h主要是RB→RB的复制(即RB增殖)过程,24~36 h主要是RB→EB的转化过程[1],为此,笔者设计了后加药和撤药实验,进一步分析了化合物对衣原体不同发育阶段的影响。研究发现,在衣原体感染宿主细胞2 h后就去除化合物,这5个化合物的抗衣原体作用几乎消失(图7B),说明仅有0~2 h的化合物作用不能抑制衣原体生长,表明5个二氢苯并呋喃醇类化合物对衣原体感染进入宿主细胞的过程没有影响,这一结果也进一步验证了宿主细胞或EB预处理的结果(图6)。对于化合物1,3,5在感染后12 h再加入对它们的抑制效果影响不大(图7A),如果改成感染时即加入而后在12 h撤去同样对它们的抑制效果影响不大(图5B),这些结果表明化合物1,3,5对衣原体的增殖全过程都具有很强的抑制作用,可以抑制EB→RB的转化过程、RB→RB的增殖过程和RB→EB的转化过程。对于化合物2,4来说,在感染后2 h加入就会削弱它们的抗衣原体效果,晚于12 h则影响极大(图7A),如果改成感染时即加入化合物则早于24 h撤去同样对其抑制效果影响很大(图7B),这些结果表明化合物2,4对衣原体增殖的过程抑制作用较弱,并且需要全程的持续作用,作用的时间越长效果越强。

A.后加药实验;B.撤药实验。
四环素类(主要是多西环素)作为衣原体感染的临床首选药物,四环素抑制CtL2的IC50值约为20 nmol·L-1[7],而二氢苯并呋喃醇类化合物的IC50值约为5 mmol·L-1,活性差距较大。尽管如此,本研究报道了二氢苯并呋喃醇类化合物的抗衣原体活性,可作为先导化合物为今后研究其衍生物的抗衣原体活性奠定基础,将有助于推动新型抗衣原体药物开发的进程[10]。
