Ga助剂对Cu@ZnO催化CO2加氢制甲醇性能的影响
2021-11-27胥月兵刘小浩
王 莉 姜 枫 胥月兵 刘 冰 刘小浩
(江南大学 化学与材料工程学院,江苏 无锡214122)
在过去的几个世纪中,对化石燃料的过度依赖导致二氧化碳(CO2)的大量排放,造成了一系列严峻的环境问题,例如气候变化、全球变暖,海洋酸化等。因此,将CO2转化为具有高附加值的化学品和燃料,不仅有利于控制大气中CO2的浓度,还可以缓解对化石资源的依赖。在众多CO2加氢的产物中,甲醇(CH3OH)是重要的化工原料,可用作燃料替代品和添加剂,也是合成高附价值化学品的关键原料,因此成为备受关注的目标产物。从环境保护和能源利用的角度,CO2加氢合成甲醇无疑成为兼具环保和经济的一条转化路线[1]。20 世纪初化学家已经研究了均相和非均相催化剂用于CO2加氢,然而后者在成本、稳定性、分离、催化剂的处理和再利用以及反应器的设计上更具优势,同时非均相催化也是目前工业上合成气制甲醇的主要方法[2]。
Cu 基催化剂具有价格低廉,有显著的催化活性等特点。目前,Cu/ZnO 催化剂在富含CO2的原料气中生成甲醇的活性较低,因此需要加入Ga 来提高催化活性[3]。Ga 的加入有助于提高催化剂的分散度和还原能力[4]。目前针对Ga 助剂对Cu 基催化剂的促进作用的报道主要集中于还原能力和分散度对催化性能的影响,并且Ga 对催化剂还原能力的影响仍然存在争议[4-5],而对Ga 助剂对CuZn 催化剂碱性位数量影响的研究仍然鲜有报道。本文研究了Ga 助剂的加入对催化剂还原能力和碱性位数量的影响。
1 试验材料和方法
1.1 催化剂制备
通过沉淀法合成CuO 纳米颗粒,合成方法如下:称取所需量的Cu(NO3)2·3H2O 溶解在去离子水中,记作溶液A,将1 M Na2CO3溶液记作溶液B。将溶液A 在70 ℃的温度下进行水溶加热,并在磁力搅拌下将溶液B 滴加到溶液A 中,直到pH =7。将沉淀液在70 ℃下搅拌30 min,80 ℃下老化3 h,随后将沉淀液用去离子水抽滤洗涤数次,去除多余的Na+。所得到的滤饼在烘箱中120 ℃下干燥过夜,将干燥后的样品在400 ℃的空气中焙烧3 h。然后,采用沉积-沉淀法制备x% Ga -Cu@ZnO 催化剂。具体制备过程如下:将上一步制备的CuO 分散在去离子水中,加入所需量的Zn(NO3)2·6H2O 和Ga(NO3)2·xH2O,记作悬浮液C。将溶液B 滴加到悬浮液C 中,直至pH=7。得到的沉淀和上一步制备CuO 的处理方式相同,最终样品标记为x% Ga -Cu@ZnO,其中x 表示Ga 所占的摩尔百分数,且Zn/Cu 摩尔比为1。Cu@Ga2O3中Cu 和Ga 的含量与5% Ga -Cu@ZnO一致。将所有焙烧后样品研磨并压片,筛分为280 ~450 μm 的颗粒,备用。
1.2 催化剂评价
催化剂活性评价在内径为8 mm 的固定床反应器中进行。将0.3 g 的催化剂(280 ~450 μm)和2 g石英砂充分混合并装填在反应管的恒温区。先在H2(30 mL·min-1,0.1 MPa)中300 ℃预还原2 h,随后降温到230 ℃切入72.7%H2/24.3%CO2/3%N2原料气,并将压力升高到3 MPa,温度升高到240 ℃进行反应。采用配有TCD - FID 检测器的气相色谱(Agilent GC-7820A)在线分析产物。
1.3 分析与计算方法
CO2(XCO2)的转化率计算如公式(1)所示。
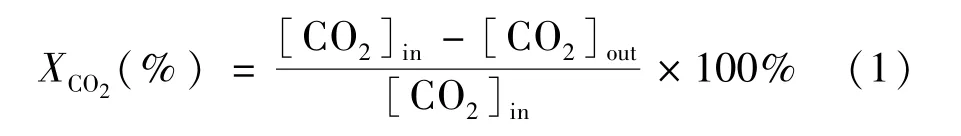
其中[CO2]in和[CO2]out分别代表入口气体和出口气体中CO2的摩尔浓度。
CO 选择性(SCO)和CH4选择性(SCH4)计算:
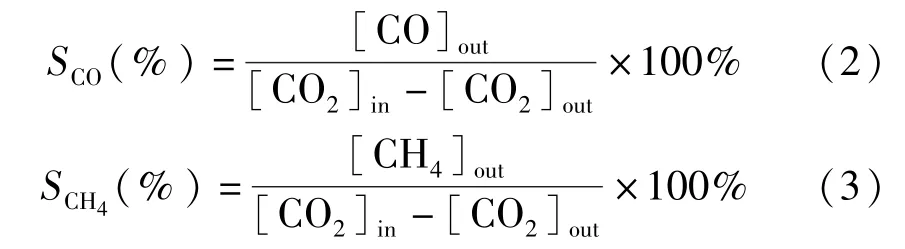
其中[CO]out和[CH4]out分别表示出口气体中CO 和CH4的摩尔浓度。
CH3OH 选择性(SCH3OH)计算:

其中[CH3OH]out表示出口气体中CH3OH 的摩尔浓度。
1.4 催化剂表征
N2吸脱附等温线由AutosorbiQ 型全自动比表面积和孔径分析仪测得。N2O 化学吸附、H2程序升温还原(H2-TPR)和CO2程序升温脱附(CO2-TPD)由天津先权工贸发展有限公司的TP-5076 测得。
2 结果与讨论
2.1 催化剂的表征
焙烧后催化剂的结构性质由N2吸脱附曲线(图1)得到。从图1 可以发现所有催化剂表现为Ⅱ型等温线,其中Cu@Ga2O3催化剂没有回滞环,表明Cu@Ga2O3中不存在介孔结构[6]。这可能是由于Ga 的相对含量过低导致的。催化剂的BET 表面积、孔体积和平均孔径的测定结果如表1 所示,催化剂比表面积从小到大依次为:Cu@Ga2O3<Cu@ ZnO <0.5%Ga-Cu@ ZnO <5%Ga -Cu@ Ga2O3<10%Ga - Cu@Ga2O3。结果表明,随着Ga 的加入,催化剂的比表面积明显增大,即Ga 的引入有助于提高催化剂的比表面积。
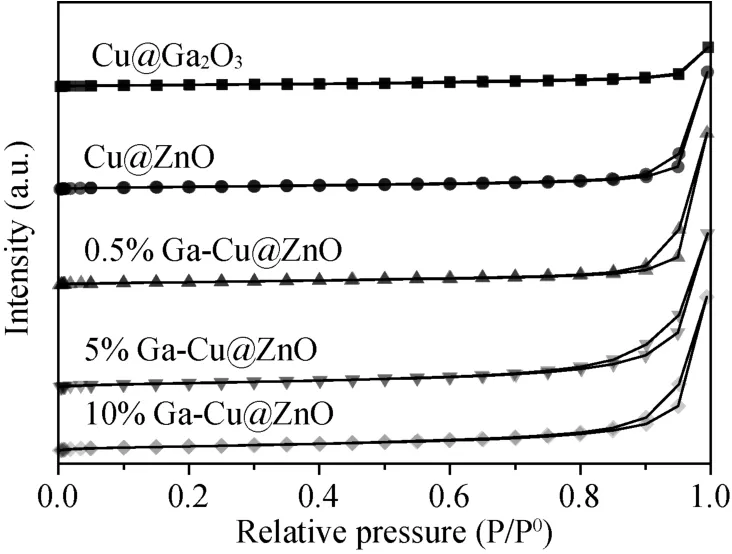
图1 x%Ga-Cu@ZnO 催化剂的N2吸脱附曲线Fig.1 The N2adsorption-desorption isotherms of x%Ga-Cu@ZnO catalysts
通过N2O 化学吸附对Cu 分散度和Cu 颗粒尺寸大小进行了测定,结果如表1 所示。结果表明,Ga 的加入改变了Cu@ ZnO 催化剂中Cu 物种的分散度。其中,Cu@Ga2O3的Cu 分散度最低,为1.9%,其次是Cu@ZnO 为5.6%。随着Ga 含量的增加,x%Ga-Cu@ZnO 催化剂的分散度逐渐提高,当Ga 含量为10%时,催化剂对应的Cu 分散度达到最大值为7.5%。同样的,N2O 化学吸附测试结果表明,随着Ga 的加入,Cu 颗粒尺寸呈现出减小的趋势,10%Ga -Cu@ZnO 催化剂上Cu 颗粒尺寸最小,为13.9 nm。
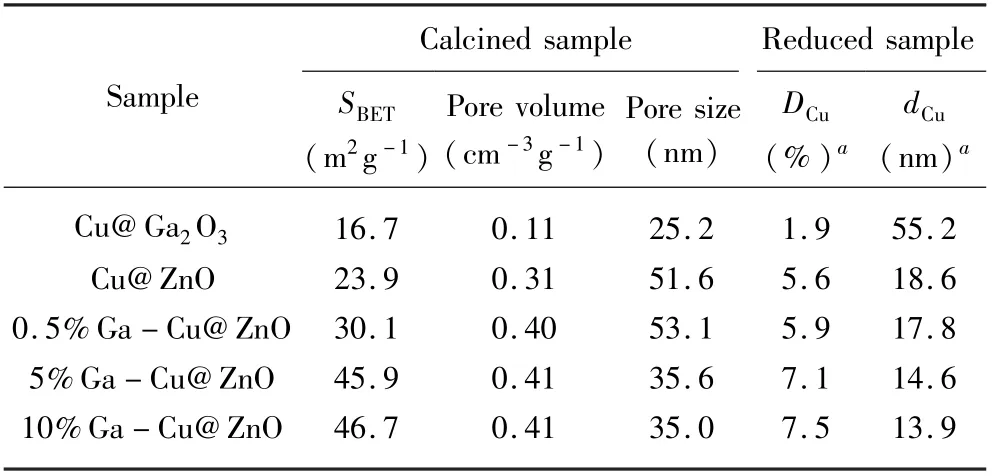
表1 催化剂的结构性质Tab.1 Textural properties of prepared catalysts_
用H2-TPR 对催化剂的还原性进行了表征,对应的还原曲线如图2 所示。随着Ga 的加入,x%GaCu@ZnO 催化剂的还原峰向低温偏移,在没有Ga的情况下,完全还原Cu2+需要更高的温度,这使得x%GaCu@ZnO 催化剂在动态反应条件下对Cu 活性位点的利用效率低下。因此Ga 的加入提高了催化剂的还原能力和Cu 活性位点的利用效率。
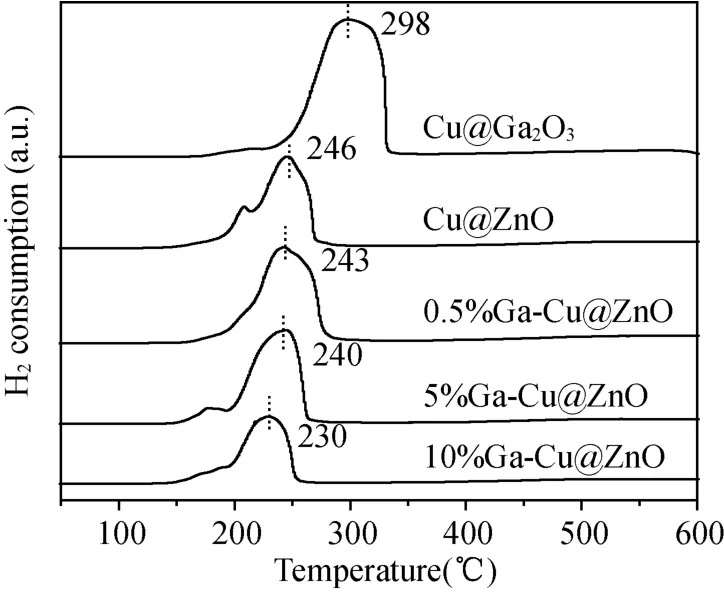
图2 x%GaCu@ZnO 催化剂的H2 -TPR 曲线Fig.2 H2 -TPR profiles of x%GaCu@ZnOcatalysts
采用CO2-TPD 对样品表面的碱性位强度进行了检测,结果如图3 所示。

图3 x%GaCu@ZnO 催化剂的CO2 -TPD 曲线Fig.3 CO2 -TPD profiles of x%GaCu@ZnO catalysts
可以观察到两种CO2脱附峰,分别在50 ℃~200 ℃(α 峰)和200 ℃~550 ℃(β 峰)范围内,分别归因于OH-基团的弱碱性位和金属-O(包括Zn -O、Cu-O 或Ga -O)键的中等强度碱性位[7]。碱性位点的定量数据和峰位置如表2 所示。计算得到的碱性位的数量从小到大的变化规律和催化剂所对应的CO2转化率变化规律一致。一般来说,在CO2加氢反应中,催化剂具有的碱性位点数量越多,越有利于提高其催化活性。一方面,Ga 的加入进一步提高了催化剂活性组分的分散度,增加活性组分和CO2的接触面积。另一方面,Ga 的引入使催化剂表面碱性增强,提高了催化剂对CO2的吸附和活化能力。
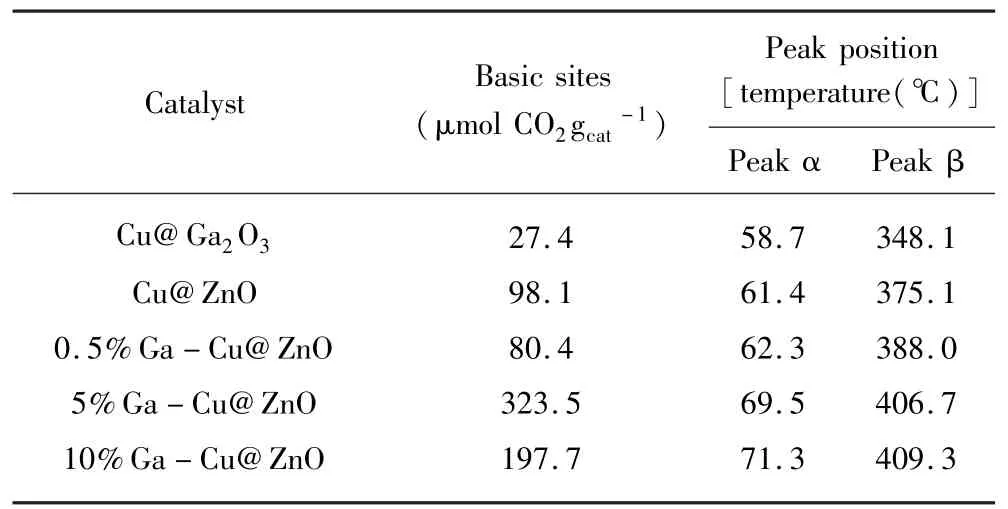
表2 x%Ga-Cu@ZnO 催化剂碱性位点的数量和分布Tab.2 The amount and distribution of basic sites of the x%Ga-Cu@ZnO catalysts
2.2 催化性能
对不同Ga 含量的催化剂的催化性能进行测试,评价结果如表3 所示。测试结果表明,5%Ga -Cu@ZnO 催化剂具有最高的CO2转化率(7.7%)和甲醇产率(5.30%),Cu@Ga2O3催化剂所对应的CO2转化率和甲醇产率最低,分别为3.5%和3.32%。随着Ga的加入,甲醇的产率明显增加,当Ga 含量为5%和10%时,CO2转化率明显高于Cu@ZnO 催化剂。结合CO2-TPD 结果,可以推断Ga 的加入增强了催化剂对CO2的吸附和转化能力。
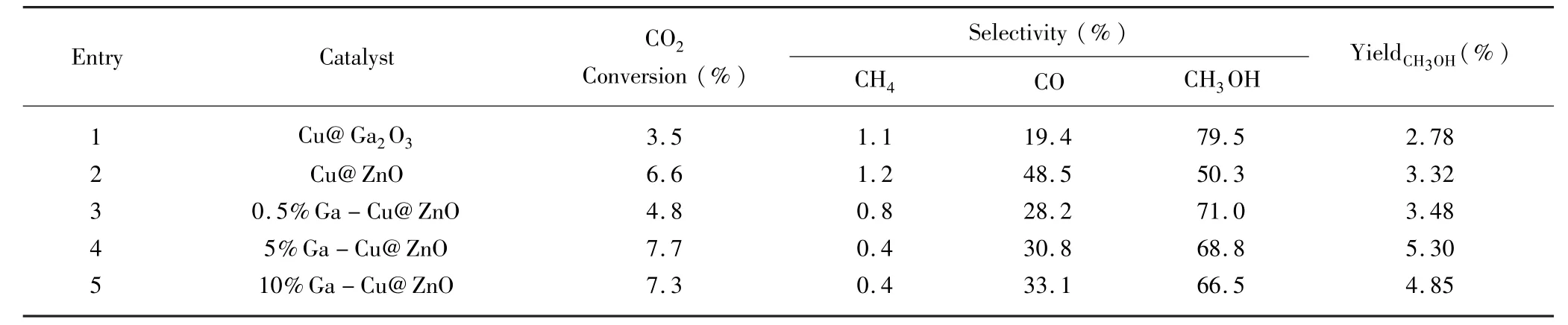
表3 x%Ga-Cu@ZnO 催化剂在CO2加氢中的催化性能Tab.3 Catalytic performance of x%Ga-Cu@ZnO catalysts in CO2 hydrogenation
3 结论
本文通过通过沉积-沉淀法制备了一系列x%Ga-Cu@ZnO 催化剂,研究了Ga 对Cu@ ZnO 催化剂表面积、Cu 分散度、还原能力以及CO2吸附量的影响,主要结论如下:
(1)Ga 的加入提高了Cu@ ZnO 催化剂的表面积,其中5%Ga -Cu@ZnO 和10%Ga -Cu@ZnO 比表面积相似,分别为45.9 和46.7 m2·g-1;
(2)TPR 结果表明Ga 加入后CuO 的还原峰向低温移动,Ga 可促进Cu 物种的还原;
(3)Ga 的加入进一步提高了催化剂活性组分的分散度,增加活性组分和CO2的接触面积的同时,也使催化剂表面碱性增强,提高了催化剂对CO2的吸附和活化能力。
