合金元素对锌空气电池阳极电化学性能的影响
2021-11-25宁庆波何立子王鑫刘宏亮高思睿
宁庆波,何立子,王鑫,刘宏亮,高思睿
(1.东北大学材料电磁过程研究教育部重点实验室,辽宁沈阳,110819;2.东北大学材料科学与工程学院,辽宁沈阳,110819)
近年来,金属空气电池作为一种绿色能源取得了迅速发展[1-2],其中,锌空气电池具有质量能量密度高(4.86 MJ/kg 以上)、安全性好、工作电压稳定、价格较低廉等优点,在助听器、照明指示灯等领域具有广泛应用[3]。然而,锌空气电池阳极存在自腐蚀、钝化、功率密度较小等问题[4],其限制了锌空气电池的应用拓展。近年来,为进一步提高锌阳极的性能,研究人员进行了一系列探索。为解决锌阳极自腐蚀的问题,通常在电极或者电解液中加入缓蚀剂来抑制共轭腐蚀反应,从而降低腐蚀速率。常用的缓蚀剂金属有Hg,Pb,In,Cd,Bi,Sn 和Ga 等[5-14],这些金属具有较高的析氢过电位,能够提高锌合金在碱液中的耐蚀性。针对锌易于钝化的问题,通常采取提高碱性电解液浓度、增加ZnO 的浓度以及添加适量的表面活性剂如十二烷基苯磺酸钠[15]等方式以抑制钝化膜的产生。YANO 等[7]通过研究发现采用干法包覆工艺制备的Zn-0.10% In-0.025% Bi 合金粉末与Zn-0.15% Hg 合金具有相同的抑制析氢效果。HUOT等[8]在纯锌粉中添加Pb,Bi,Ca 和Al,发现锌粉的材料利用率得到提高。石建珍等[13]发现添加Pb,Cd,In和Hg提高了锌电极析氢过电位,抑制了锌电极在碱性溶液中的自放电,而添加Bi 会促进锌电极上氢的析出。胡经纬等[14]发现Bi对Zn在KOH溶液中的电化学行为具有明显的活化作用。LEE等[16]发现于500 ℃烧结的Zn-7.5% In-2.5% Bi 合金抑制了锌电池的析氢反应,充放电次数可达100次以上。但是,锌阳极存在的自腐蚀、钝化等问题并未得到根本的解决。本文通过正交实验,结合交流阻抗谱及循环伏安曲线实验,分析研究In,Bi和Ca 这3 种元素对锌空气电池阳极的电化学性能及放电性能的影响,并筛选出一种综合性能较好的锌合金阳极成分。
1 实验
1.1 实验原料
采用L9(34)正交表设计锌合金成分,以In,Bi和Ca质量分数这3个因素为考察对象,各因素设3个水平(见表1)。将99.99%(质量分数)的高纯锌放入石墨坩埚中,升温到600 ℃后加入99.99%(质量分数)的Ca,待其熔化后降温至550 ℃加入99.99%(质量分数)的In 与Bi,于500 ℃保温5 min 后浇筑成长×宽×高为150 mm×100 mm×10 mm的铸锭。
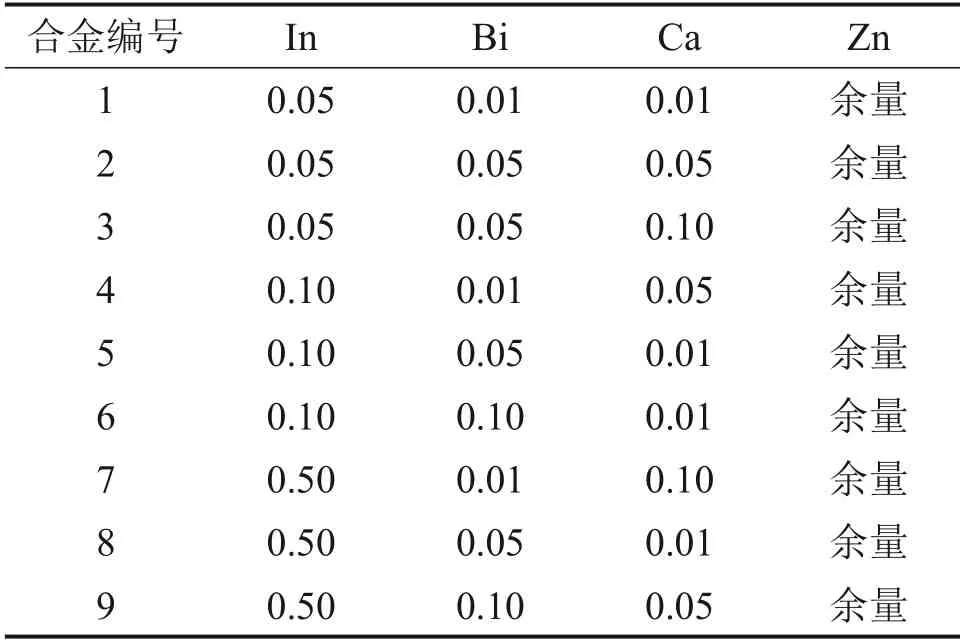
表1 锌合金阳极成分(质量分数)Table 1 Composition of zinc alloy anode materials %
1.2 实验测试
1.2.1 析氢测试
自制析氢测试装置如图1所示。根据每小时量筒中液体上升的高度计算析氢速率。测试前向抽滤瓶中加入400 mL 的6 mol/L KOH 溶液,并将其放入50 ℃的恒温水浴锅中,保温1 h。开始测试时,向抽滤瓶中放入长×宽×高为20 mm×30 mm×5 mm的锌合金阳极块,并用橡胶塞塞紧瓶口,接着向量筒中加入1 mL 液体石蜡,防止碱液挥发。静置30 min后,每1 h记录液柱的刻度值,共记录24 h。
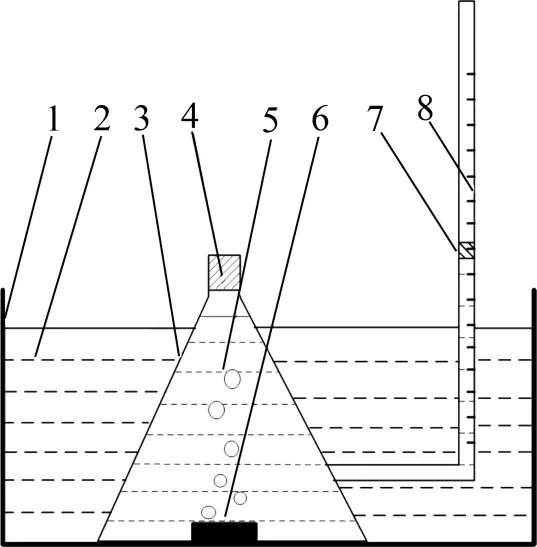
图1 析氢实验量气装置Fig.1 Gas measuring device for hydrogen evolution experiment
1.2.2 电化学实验
在CHI660E 型电化学工作站上进行电化学实验。电化学实验采用三电极体系,锌合金阳极为工作电极,工作面长×宽为10 mm×10 mm;Hg/HgO电极为参比电极;铂片电极为辅助电极,其长×宽为15 mm×15 mm。电解液为50 mL的6 mol/L KOH溶液,锌合金阳极与Hg/HgO电极间距保持8 mm,测试温度为25 ℃。动电位极化曲线的扫描电压范围为-1.7~-1.2 V,扫描速度为1 mV/s。交流阻抗曲线测试电位为各锌合金阳极的腐蚀电位,扫描频率范围为1~105Hz,交流电幅值为5 mV。循环伏安曲线测试扫描电压范围为-1.7~-0.9 V,扫描速度为5 mV/s。
1.2.3 电池测试
电池测试在武汉蓝电CT3001A 型测试系统上进行,自制电解槽装置如图2所示。测试前,将长×宽为40 mm×40 mm 的阴极放入电解槽侧面,盖上镍网及盖板并拧紧螺母,盖板中部区域长×宽为20 mm×20 mm。测试时,加入100 mL 的6 mol/L KOH溶液,安装长×宽为20 mm×20 mm的锌合金阳极,保持阴阳极间距为7 mm,测试温度为25 ℃。采用短时间恒定电流测定电压的方法进行I-V测试,设定电流从0 A 增加到2 A,上升梯度为5 mA/s。恒流放电测试设定电流为0.4 A,电流密度为100 mA·cm-2,放电时长为200 min。
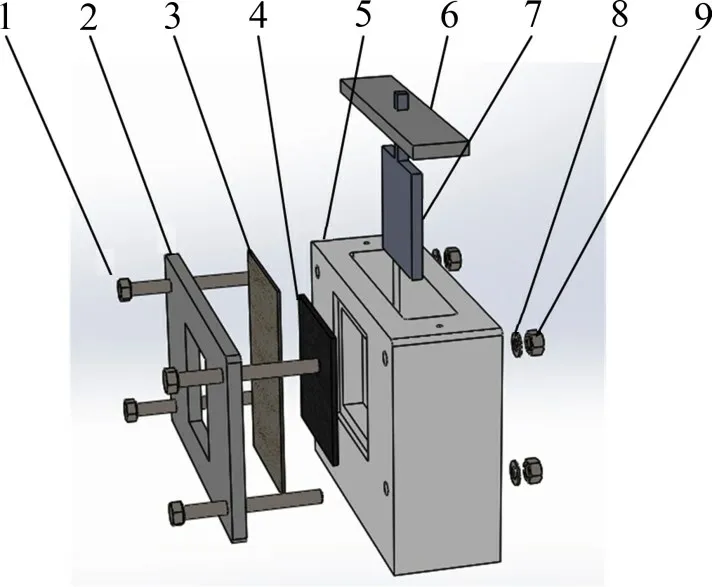
图2 电解槽装置Fig.2 Electrolytic cell device
2 结果与讨论
图3所示为锌合金阳极的动电位极化曲线(其中,j为腐蚀电流密度)。从图3可见:在阳极极化区,随着极化电位的正向移动,锌合金的腐蚀电流连续增加,未出现钝化曲线,这一现象说明了各锌合金阳极的电化学活性较高。锌合金阳极的腐蚀电位、腐蚀电流密度、极化电阻和析氢速率如表2所示。从表2可见:锌合金1,2和5的腐蚀电位绝对值最大,为1.477 V,锌合金8 腐蚀电位绝对值最小,为1.452 V。腐蚀电流密度与极化电阻呈负相关;与析氢速率大致呈正相关。锌合金7具有最小的腐蚀电流密度(0.130 mA·cm-2)、最大的极化电阻(164.5 Ω·cm2)和最小的析氢速率(0.637 mL·cm-2·d-1),其耐蚀性最好。
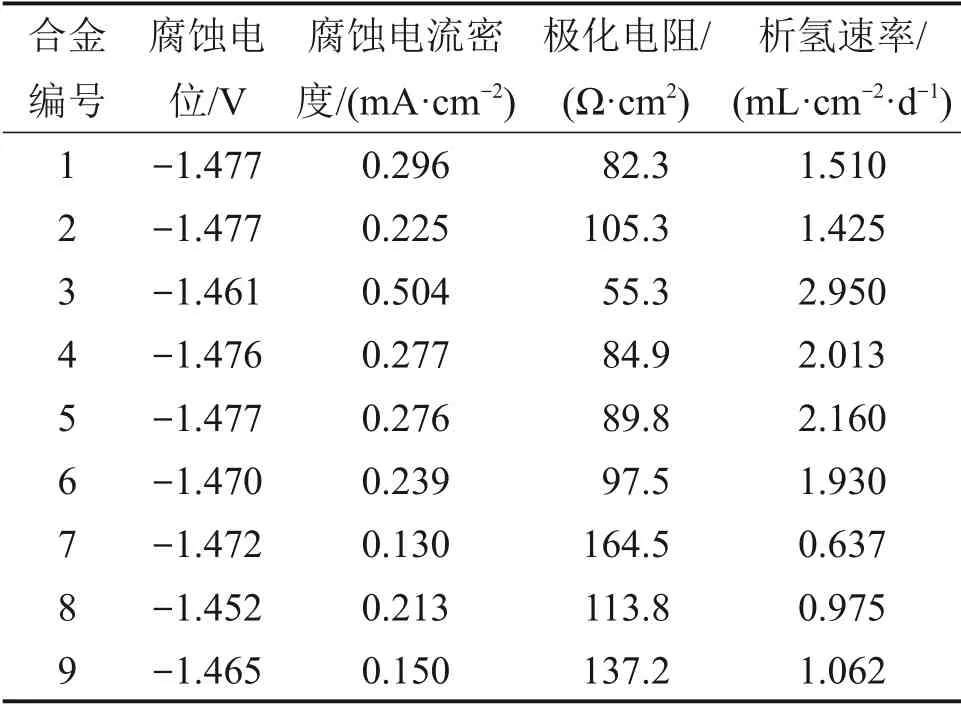
表2 锌合金阳极的腐蚀电位、腐蚀电流密度、极化电阻和析氢速率Table 2 Corrosion potential,corrosion current density,polarization resistance and hydrogen evolution rate of zinc alloy anode materials
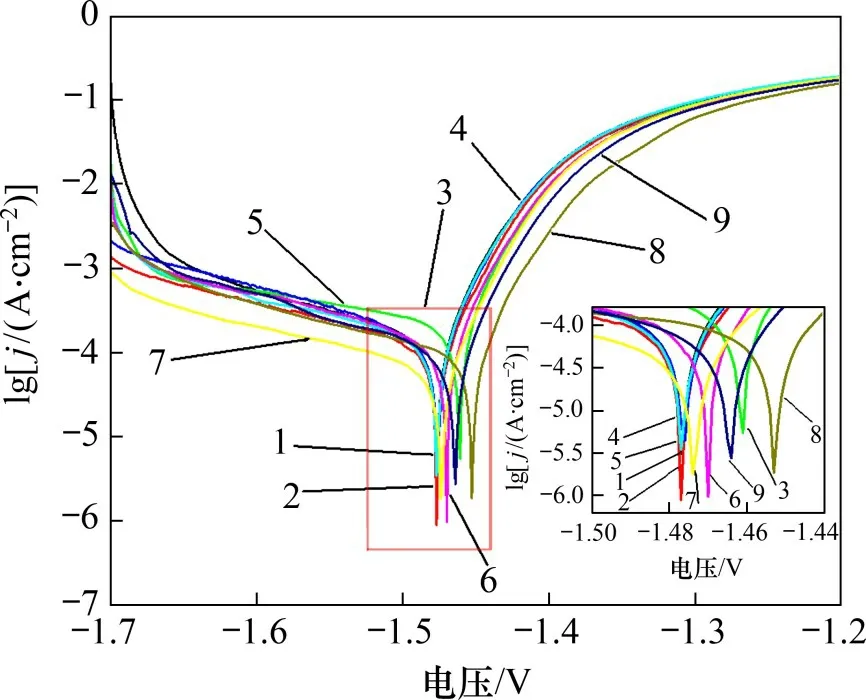
图3 锌合金阳极在6 mol/L KOH溶液(25 ℃)中的动电位极化曲线Fig.3 Polarization curves of zinc alloy anode in 6 mol/L KOH solution at 25 ℃
锌合金阳极的腐蚀电位、腐蚀电流密度、极化电阻、析氢速率的正交试验结果如表3所示。由表3可知:影响锌合金的腐蚀电位和极化电阻的因素按主次顺序排列依次为In,Bi,Ca;影响腐蚀电流密度的因素按主次顺序排列依次为In,Ca,Bi;影响锌合金析氢速率的因素按主次顺序排列依次为In,Bi,Ca。In 元素对于腐蚀电位、腐蚀电流密度、极化电阻、析氢速率的影响占主导地位,能够提高锌合金阳极的耐蚀性,降低析氢速率;Ca,Bi 元素对以上参数影响较小,会引起腐蚀电压波动,降低锌合金阳极的耐蚀性,提高析氢速率;In元素能提高锌表面的析氢过电位,抑制锌的析氢反应和阳极氧化,从而抑制锌在碱液中的自腐蚀[17];Bi元素具有提高阳极活性的作用,能促进锌合金阳极溶解[15]。综合考虑以上因素,耐蚀性最优的锌合金阳极成分质量分数比w(In)∶w(Bi)∶w(Ca)=0.50∶0.01∶0.05。
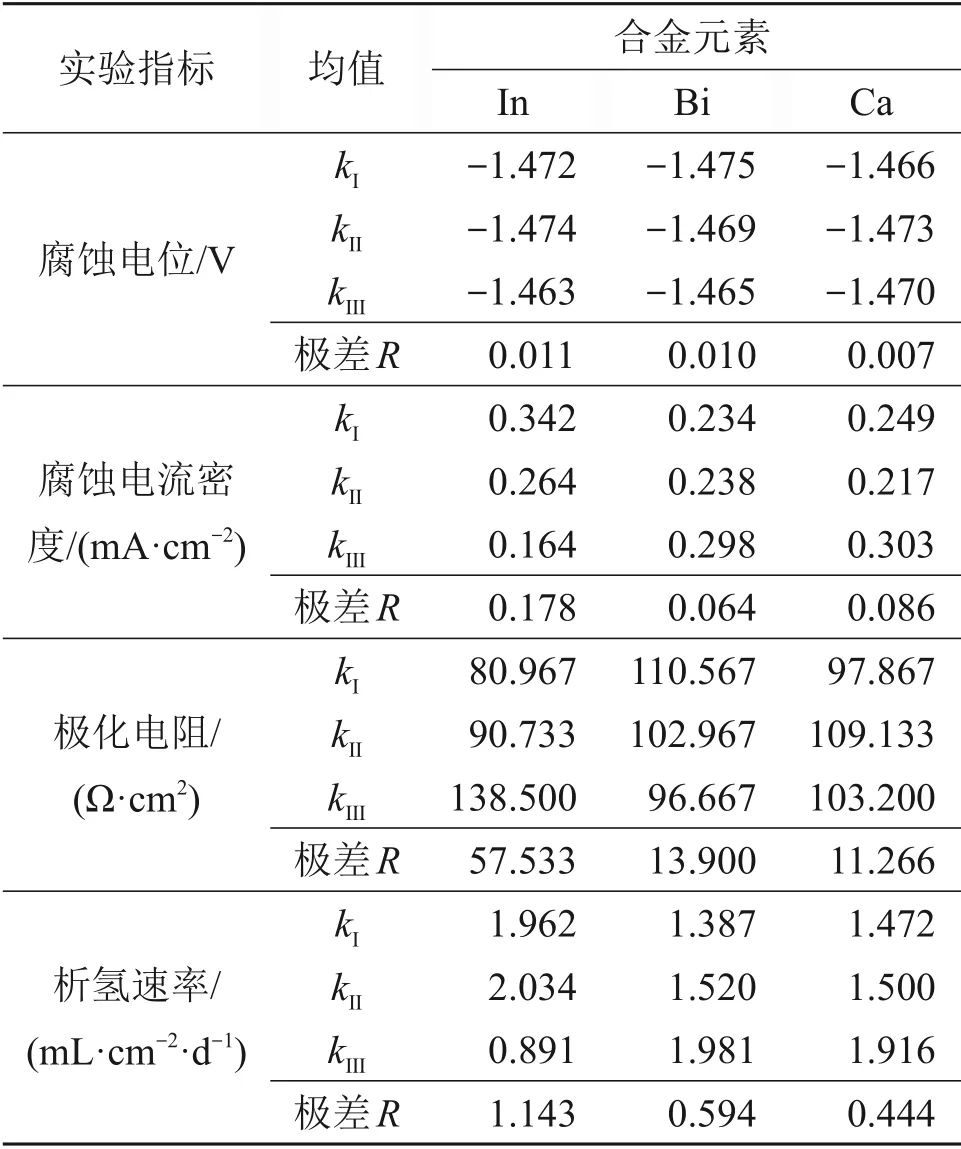
表3 锌合金阳极的腐蚀电位、腐蚀电流密度、极化电阻、析氢速率的正交试验结果Table 3 Results of orthogonal tests of corrosion potential,corrosion current density,polarization resistance and hydrogen evolution rate of zinc alloy anode materials
图4(a)所示为锌合金阳极的I-V曲线。从图4(a)可见:随着电流密度的增加,电压逐渐下降,锌合金阳极的功率密度呈先上升后下降的趋势。图4(b)所示为锌合金阳极的恒流放电曲线。从图4(b)可见:各合金阳极(除合金1 外)在放电过程中比较稳定,说明锌合金在电流密度100 mA·cm-2的条件下放电性能良好;合金7,8 和9 在放电后期出现电压下降的现象,放电性能出现衰减。锌合金阳极的最大功率密度、恒流放电平均电压如表4所示。从表4可见:各个锌合金阳极放电最大功率密度差距较大,合金1~6 的放电最大功率密度分别 为176.99,160.42,169.03,172.84,167.89,169.71 mW·cm-2,高于合金7~9的142.84,151.37,141.49 mW·cm-2。各个锌合金阳极恒流放电平均电压差距较大,在25℃6 mol/L KOH 溶液中,电流密度为100 mA·cm-2的条件下,合金6 的放电平均电压最高,为0.93 V,合金4的平均电压最低,为0.81 V。

图4 锌合金阳极在6 mol/L KOH溶液(25 ℃)中的放电测试曲线Fig.4 Discharge test curve of zinc alloy anode in 6 mol/L KOH solution at 25 ℃
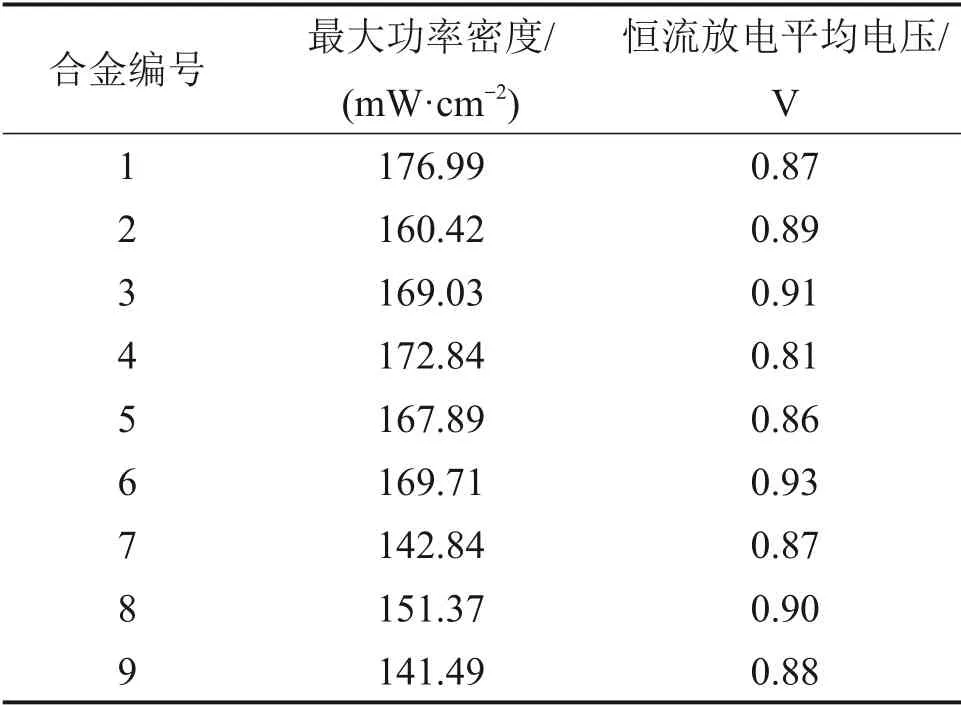
表4 锌合金阳极的最大功率密度、恒流放电平均电压Table 4 Maximum power density and average constant current discharge voltage of zinc alloy anode materials
锌合金阳极的最大功率密度、恒流放电平均电压的正交试验结果如表5所示。由表5可知:In元素对锌空气电池最大功率密度的影响较大,Ca 和Bi 的影响较小;在锌合金阳极中添加In 元素较多会导致锌合金阳极的活性下降,放电性能降低;在温度为25℃、浓度为6 mol/L KOH溶液中,在电流密度为100 mA·cm-2的条件下,In,Bi 和Ca 元素对锌空气电池恒流放电平均电压的影响较弱(极差R分别为0.02,0.06 和0.04)。比较来看,影响因素按主次顺序排列为Bi,Ca,In。Zn添加Al,Ca和In 元素,可以提高锌阳极的反应活性,联合添加金属元素具有协同效应,提高锌阳极的放电性能[18]。Zn 合金中添加适量的In,Bi 和Ca 元素可以提高锌合金阳极的放电性能,放电性能较好的锌阳极合金元素质量分数比w(In)∶w(Bi)∶w(Ca)=0.10∶0.01∶0.01。
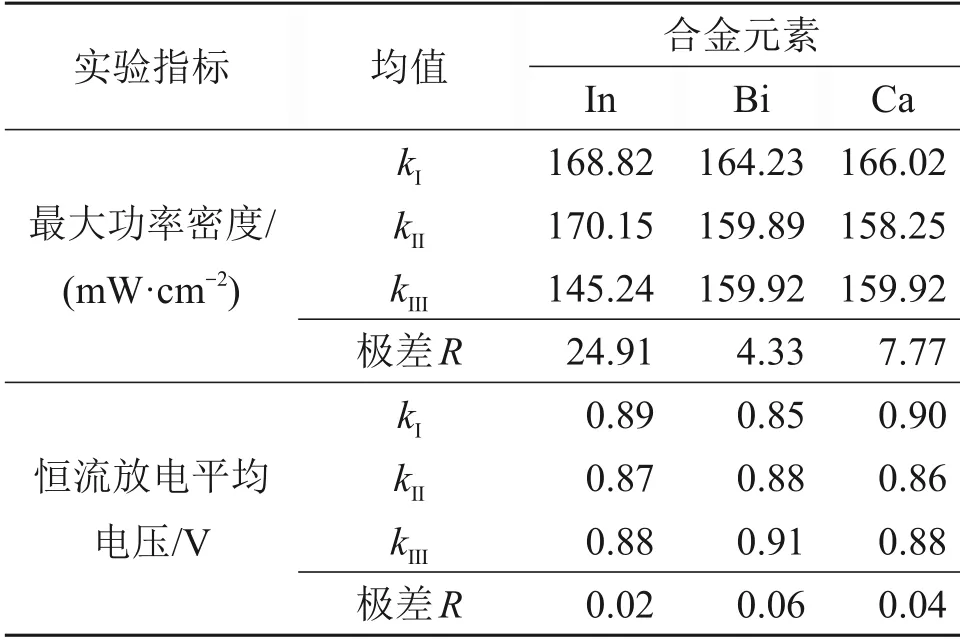
表5 锌合金阳极的最大功率密度、恒流放电平均电压的正交试验结果Table 5 Results of orthogonal tests of maximum power density and constant current discharge average voltage of zinc alloy anode materials
优良锌合金阳极需要具备较低析氢速率、较低的腐蚀电流、较大的功率密度以及稳定的放电性能。在不同的实验指标下得到的锌合金阳极最优水平并不完全一致,故采用综合平衡的原则对成分进行筛选。In 元素对析氢速率、腐蚀电位、腐蚀电流密度、极化电阻、最大功率密度这6个实验指标的影响都最大。锌空气电池的最大功率密度反映了锌阳极的放电性能及电池的整体性能,应优先考虑,故In 质量分数取0.1%。Bi 元素对恒流放电平均电压的影响最大,因此,取Bi 的质量分数为0.1%。对于Ca 元素,其对以上6 个实验指标都不是最主要影响因素,且Ca 元素质量分数为0.01%的最优水平出现次数最多,故选择Ca 元素质量分数为0.01%。综上所述,正交实验的最佳的锌阳极配比为Zn-0.1%In-0.1%Bi-0.01%Ca(质量分数)。
为进一步研究In,Bi 和Ca 对锌合金阳极的电化学性能的影响,对合金1、合金9 及最佳成分合金6进行交流阻抗谱实验及循环伏安曲线实验。图5所示为锌合金阳极在6 mol/L KOH 溶液中的复数阻抗平面图(其中,ZIm为复数阻抗虚部,ZRe为复数阻抗实部)。如图5所示,锌合金阳极的交流阻抗图谱由1个高频容抗弧和1条低频直线(斜率为n)组成。锌合金阳极在碱液中的腐蚀分为2个过程:第一个过程为锌失去电子产生ZnO22-或Zn(OH)42-,对应交流阻抗谱中的高频容抗弧,由电子传递步骤控制;第二个过程为ZnO22-或Zn(OH)42-由电极表面扩散至电解质溶液中,对应交流阻抗谱中的低频直线,由扩散传质步骤控制[19]。锌阳极在KOH 溶液中腐蚀的等效电路见图6,模拟结果如表6所示。(图6中:Raq为电解液的欧姆电阻;Cdl为电化学反应界面双电层电容;Rt为腐蚀反应的电荷转移电阻;R1和Q1分别为电化学反应电阻和等效电路元件电容,与电极反应中间产物等从锌合金阳极表面脱出的情况有关)。由表6可知,锌合金1的腐蚀反应的电荷转移电阻Rt最小,为2.704 Ω·cm2,其容抗弧半径最小;锌合金9的腐蚀反应的电荷转移电阻Rt最大,为3.152 Ω·cm2,其容抗弧半径最大,说明In,Bi 和Ca 的联合作用会使锌合金阳极腐蚀反应的电荷转移电阻增大,其抑制了锌的腐蚀反应。此外,随着In,Bi 和Ca 质量分数增加,电化学反应电阻R1也呈增大的趋势,说明锌的中间产物从锌合金阳极表面脱出逐渐困难,从而抑制了锌在碱液中的腐蚀。以上分析结果与Tafel 曲线所示结果及析氢实验结果一致。
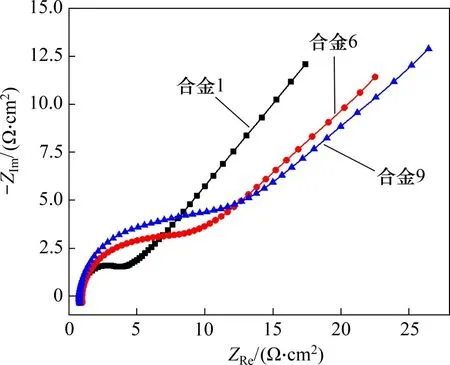
图5 锌合金阳极在6 mol/L KOH溶液(25 ℃)中的复数阻抗平面图Fig.5 Complex impedance plane of zinc alloy anode materials in 6 mol/L KOH solution at 25 ℃
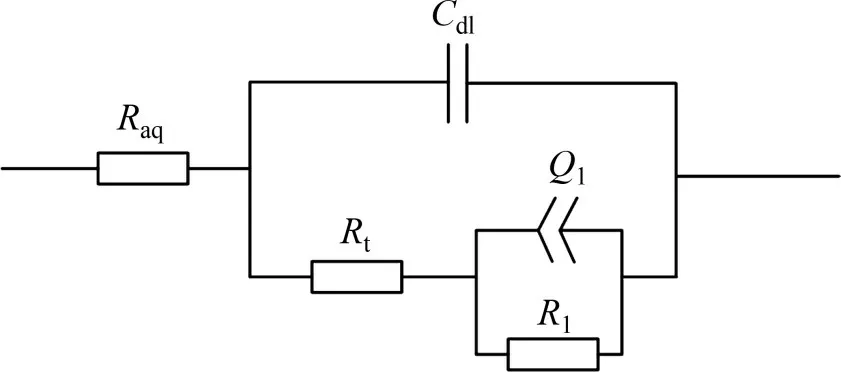
图6 锌合金阳极在6 mol/L KOH溶液中的复数阻抗平面等效电路Fig.6 Complex impedance plane equivalent circuit of zinc alloy anode in 6 mol/L KOH solution
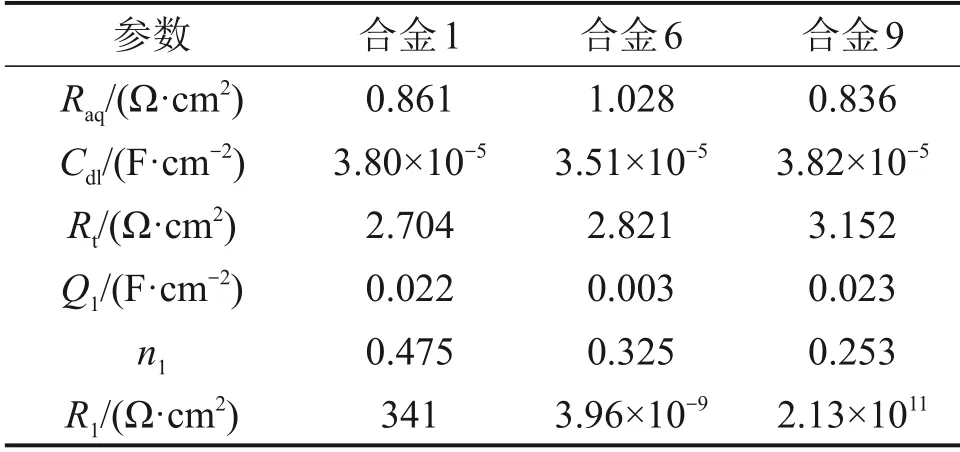
表6 等效电路模拟结果Table 6 Equivalent circuit simulation results
图7所示为锌合金阳极在6 mol/L KOH 溶液(25 ℃)中的循环伏安曲线。由图7可知,在-1.1~-1.0 V 出现了氧化峰A 和氧化峰B,在-1.5~-1.4 V 之间出现了还原峰C,这分别对应于锌在碱性溶液中的氧化(溶解)和还原(沉积)反应:Zn+4OH--2e-⇌Zn(OH)42-。在阳极扫描中,氧化峰A的出现是由于锌被氧化并形成Zn(OH)42-,然后转化为结构致密的ZnO 钝化膜。在阴极扫描中,氧化峰B 的出现是源于致密的ZnO 钝化膜进一步溶解为Zn(OH)42-[3,20]。表7所示为锌合金阳极循环伏安曲线的电化学参数。由表7可知,锌合金阳极的循环伏安曲线的氧化还原峰电位差(ΔEp)范围为340~400 mV,这说明锌合金阳极在6 mol/L 的KOH 溶液中的氧化还原反应为准可逆过程。合金9 的ΔEp比合金6 的小0.040 V,比合金1 的小0.059 V,表明锌合金阳极可逆性按从大到小的顺序排列依次为合金9、合金6、合金1。锌合金阳极中适量添加In,Bi 和Ca 可以提高合金的可逆性。在锌合金氧化过程中,合金9 的氧化峰A 较合金1的氧化峰A提前出现,且峰值电流密度比合金1的大,说明锌合金9较锌合金1易于被氧化;在锌合金阳极还原过程中,合金9的氧化峰B较合金1的氧化峰B延迟出现,合金9的还原峰C的峰值电流密度比合金1 的大,说明合金9 的钝化膜较合金1的钝化膜难溶解。在锌合金中适量添加In,Bi 和Ca 促进了锌溶解的过程,抑制了ZnO 钝化膜的溶解,提高了锌合金阳极的可逆性。
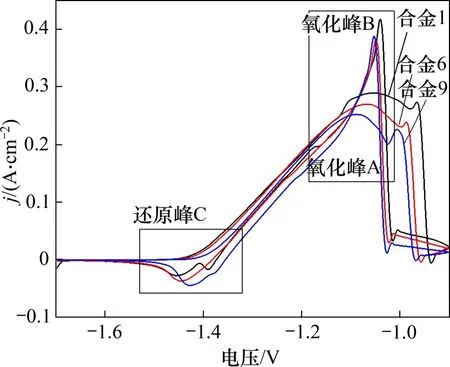
图7 锌合金阳极在6 mol/L KOH溶液(25 ℃)中的循环伏安曲线Fig.7 Cyclic voltammetry of zinc alloy anode in 6 mol/L KOH solution at 25 ℃
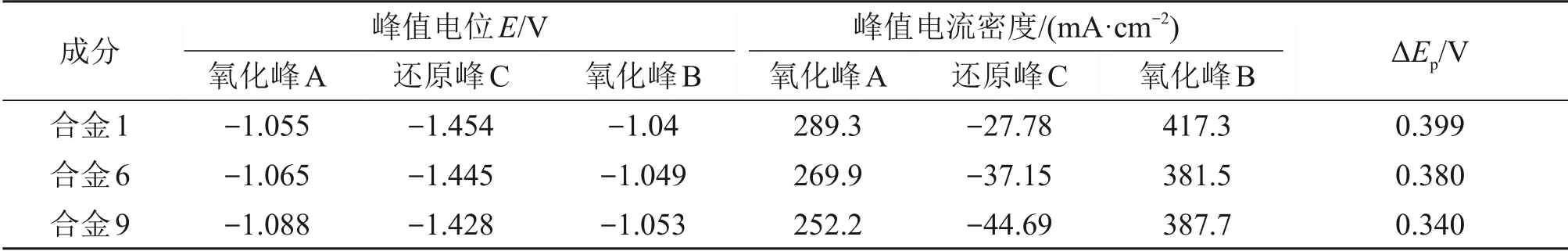
表7 锌合金阳极循环伏安曲线的电化学参数Table 7 Electrochemical parameters of cyclic voltammetry curve of zinc alloy anode
3 结论
1)通过正交实验,优选出了一种在温度为25 ℃、浓度为6 mol/L KOH 溶液中具有最优综合性能的锌合金阳极,其成分为Zn-0.1% In-0.1%Bi-0.01% Ca(质量分数),最大功率密度为169.7 mW·cm-2,能在100 mA·cm-2的条件下以0.93 V稳定恒流放电200 min以上。
2)In,Bi 和Ca 的联合作用增大了锌合金阳极腐蚀的反应电阻,并抑制了锌中间产物的脱出,减弱了锌在碱液中的腐蚀;同时,适量添加In,Bi和Ca 可促进锌的溶解,抑制ZnO 钝化膜的溶解,在一定程度上可提高锌合金阳极的放电性能。
