Mo-Sn 催化剂上甲醇低温氧化制甲缩醛
2021-11-20王文秀高秀娟张俊峰宋法恩张清德韩怡卓谭猗生
王文秀 ,高秀娟 ,熊 盼 ,张俊峰 ,宋法恩 ,张清德,3,* ,韩怡卓 ,谭猗生
(1. 中国科学院山西煤炭化学研究所 煤转化国家重点实验室,山西 太原 030001;2. 中国科学院大学,北京 100049;3. 中国科学院洁净能源创新研究院,辽宁 大连 116023)
甲醇是一种重要的化工原料,可以由煤、天然气、生物质等[1− 3]通过合成气的途径制得,但由于近年来合成气制甲醇技术的成熟,甲醇产量显著增加造成了产能过剩,开发甲醇下游产品受到广泛关注。甲醇可以制取乙烯、丙烯、芳烃、环烷烃等有机化工产品[4],且也可通过氧化的方法制取甲醛、甲缩醛、甲酸甲酯(MF)等含氧化合物[5],而甲醇氧化的路径原子经济性好,能耗低,具有广阔的应用前景。
甲缩醛(DMM),是一种理想的新型绿色环保型溶剂[6,7],因其拥有优良的理化性质在医疗、化妆品、涂料等多个行业得到广泛应用[8−10]。另外,甲缩醛作为一种新的平台含氧化合物,受到越来越多的关注和重视,以其为原料可以合成高附加值的甲氧基乙酸甲酯、乙二醇及清洁柴油添加剂聚甲氧基二甲醚等[11,12]。目前,工业上制取甲缩醛的方法主要是甲醇、甲醛缩合法,但由于该法采用催化剂酸性较强,对设备腐蚀性强,不适宜装置的长期使用。因此,采用甲醇氧化一步法制取甲缩醛得到了广泛的关注。
近年来,研究人员对甲醇氧化直接制取甲缩醛进行了较多的研究,开发出了以贵金属Ru 基、Re基催化剂[13],杂多酸催化剂[14]以及非贵金属V 基催化剂为代表的多种催化剂。但由于贵金属价格昂贵,杂多酸催化剂操作温度较高、易分解等原因限制了其推广使用。其中,V 基催化剂是该反应中研究较多的催化剂,在研究人员的努力下,V 基催化剂上已经实现了高选择性制取甲缩醛[15−17],然而V 基催化剂存在着钒源毒性较大,TiO2热稳定性差、机械强度不高等问题,这在很大程度上限制了其进一步在工业上规模化应用。因此,采用环境友好、价格低廉的非贵金属催化剂实现甲醇低温氧化高效制备甲缩醛,且过程无COx生成,是非常有必要的。
先前的研究发现,Mo-Sn 催化剂在醇醚氧化中具有良好的性能。Ai[18]在Mo-Sn 催化剂上实现了甲醇氧化高选择性制取甲酸甲酯,并发现甲醇氧化为甲醛是该反应中的决速步。近年来,本课题组在Mo-Sn 催化剂催化二甲醚低温氧化上开展了系统的研究工作。发现,采用浸渍法制备的Mo-Sn 催化剂上适当的Mo−O 键配位数(1.94 Å)的存在,是催化剂性能提升的主要原因[19]。而对于共沉淀法制备的Mo-Sn 催化剂来说,Mo-Sn 界面处存在的少量Mo5+是促进催化剂活性提高的重要因素[20]。杨奇等[21]采用了水热合成法制备的Mo-Sn 催化剂具有较多的Mo5+物种,这些Mo5+物种的存在有利于二甲醚分子C−O 键断裂产生的甲氧基进一步氧化转化为甲醛。同时,甲氧基氧化脱氢为甲醛也是甲醇转化的关键步骤,且相比二甲醚分子,甲醇分子比较简单,含有一个甲氧基,为了进一步认识Mo5+的形成机理及低温氧化C-H 的作用机制,本实验开展了在钼锡催化剂上甲醇氧化转化的研究。
本工作采用水热合成的方法,制备了一系列具有不同Mo 含量的Mo-Sn 催化剂,并将其用于甲醇氧化制取甲缩醛反应。到目前为止,在Mo-Sn 催化剂上甲醇氧化高选择性制取甲缩醛的文献报道还极少。实验结果表明,低Mo 含量的催化剂具有良好的甲醇氧化制取甲缩醛的性能。采用一系列表征手段,并结合催化剂性能评价,研究了Mo的量对催化剂活性位结构的影响以及促进Mo5+形成的关键因素。
1 实验部分
1.1 催化剂的制备
采用水热合成的方法制备不同Mo 含量的Mo-Sn 催化剂,Mo/Sn 物质的量之比为1∶1、1∶2、1∶3、1∶4、1∶5、1∶8、1∶10、1∶20。以SnCl4·5H2O与(NH4)6Mo7O24·4H2O 为前驱体,按照所需物质计量比称取SnCl4·5H2O 与(NH4)6Mo7O24· 4H2O,加入到盛有去离子水的聚四氟乙烯内衬中,60 ℃水浴加热,待药品完全溶解后转移至均相反应器中,120 ℃反应24 h。对冷却得到的沉淀物进行离心、洗涤、干燥,最后置于管式炉中,氧气气氛下500 ℃焙烧8 h 得到不同Mo 含量的Mo-Sn 催化剂,分别标记为Mo2Sn1、Mo1Sn1、Mo1Sn2、Mo1Sn3、Mo1Sn4、Mo1Sn5、Mo1Sn8、Mo1Sn10、Mo1Sn20。
1.2 活性评价装置
甲醇氧化反应在常压连续流动固定床反应装置上进行。催化剂(20−40 目)的装填量为0.5 mL。为防止反应过程中由于剧烈放热导致催化剂快速失活,在装填的催化剂中使用三倍于其体积的细瓷环(20−40 目)进行稀释。反应前催化剂在氧气气氛下活化2 h,甲醇进料流量为0.817 mL/h,体积空速为7200 h−1。
1.3 产物分析及定量
反应出口产物采用三台色谱进行取样分析:有机含氧化合物采用GC-2014CPF/SP L(日本岛津公司,FID 检测器,DB-1 毛细管柱)、GC-2014(日本岛津公司,色谱柱为3 m Porapak T 填料),TCD检测器分析;同时在GC-4000A 色谱(北京东西分析仪器有限公司)上分析永久性气体H2、CH4和COx。
将以上三台色谱所得到的结果进行校正处理后根据下列公式计算甲醇(CH3OH)的转化率及相关产物的选择性:


式中,i,分别为产物中的CH3OCH3、HCHO、HCOOCH3、CH3OCH2OCH3、CO、CO2;si:产物i的碳摩尔选择性;ai:产物i分子内的碳原子数目;ni:尾气中产物i的摩尔数。
1.4 催化剂的表征
程序升温脱附(NH3-TPD)测试是在TP 5080化学吸附仪上进行的。将100 mg 催化剂样品(20−40 目)置于样品管中,N2气氛下程序升温至400 ℃,恒温1 h 后降温至50 ℃,通入NH310 min 并静置10 min,然后用N2吹扫30 min 后程序升温至600 ℃进行脱附并记录信号。
程序升温还原(H2-TPR)测试是在TP 5080 化学吸附仪上进行的。取100 mg 催化剂样品(20−40 目)置于样品管中,N2气氛下程序升温至200 ℃,恒温1 h 后降温至50 ℃。然后,通入N2与H2混合气,待基线平稳后,以10 ℃/min 的速率程序升温至900 ℃进行升温还原,并记录信号。
X 射线衍射(XRD)测试在Bruker Advanced XRay Solution/D8 型X 射线衍射仪上实现。扫描角度为5°−90°,使用CuKα 射线,电流15 mA,电压40 kV。
拉曼(Raman)表征在LABRAM-HR800 型拉曼光谱仪进行测试,测试激光波长532 nm,扫描100−1100 cm−1。
X 射线光电子能谱(XPS)表征是在AXIS ULTRA DLD 型X 射线光电子能谱仪上检测的,粒子源为AlKα(hν= 1486.6 eV),加速电压12.5 kV,能谱功率250 W,用C 1s的结合能(284.6 eV)与所测元素进行比对校正。
傅里叶变换红外光谱(FT-IR)是在Bruker Tensor 27 上进行的,背景扫描使用的是KBr,仪器检测器为MCT 检测器,扫描点数为64 个,分辨率为4 cm−1,。将粉末状催化剂样品放入红外池中,以Ar 作为载气,升温至200 ℃,处理1 h,然后降至测试温度进行检测。
2 结果与讨论
2.1 Mo-Sn 催化剂上甲醇氧化性能评价
表1 为甲醇在不同Mo 含量的钼锡催化剂上选择性氧化的评价结果。由表1 可知,不同Mo 含量催化剂的催化性能差异较大。随着Mo 掺杂量的减少,甲醇转化率呈现出降低的趋势,DMM选择性明显升高,同时伴随着二甲醚(DME)及MF 选择性的下降。根据之前的研究显示,甲醇会在氧化性位点生成甲醛并与甲醇反应生成半缩醛中间体,而半缩醛会在氧化性位点上脱氢生成甲酸甲酯或在酸中心上生成甲缩醛[22],而评价结果中产物的选择性变化规律,可能是由于催化剂结构变化导致表面性质改变引起的。如表1 所示,当Mo 量在催化剂中所占物质的量比为1∶9 时,产物DMM 的选择性达到87.8%,进一步降低Mo 的含量,DMM 的选择性基本维持在88%左右,说明Mo1Sn8、Mo1Sn10、Mo1Sn20 具有相似的结构或表面性质。且在所有评价的催化剂上,并没有发现COx的生成。另外,单一的SnO2与MoO3并未表现出催化活性,只有在钼锡氧化物上时才有目标产物的产生,且产物分布随Mo 量变化而改变。说明,Mo 掺入量的变化,影响了钼氧化物与锡氧化物之间的相互作用,进而对催化剂的结构及表面性质产生了影响。

表 1 不同Mo 量Mo-Sn 催化剂上甲醇转化的反应性能Table 1 Effect of Mo content on the performance of Mo-Sn catalysts for methanol conversion
2.2 催化剂的表征
2.2.1 XRD 表征
图1 为不同Mo 含量催化剂的XRD 谱图。位于12.7°、23.3°、25.7°、27.3°、33.8°、39.0°的衍射峰归属于斜方晶系MoO3的特征衍射峰(PDF card No.35-0609),而在26.6°、33.9°、37.9°、51.7°处的宽峰归属于四方晶系SnO2(PDF card No.41-1445)的特征衍射峰。可见,当Mo 掺入量减少时,MoO3的衍射峰逐渐消失,SnO2衍射峰的峰高略有增加。这说明,在Mo 量减少的过程中,钼氧化物在SnO2表面可能是以高度分散或以无定形形式存在。而由于这种结构变化所体现出的表面性质的转变,可能是甲醇实现高选择性制取DMM 的原因。
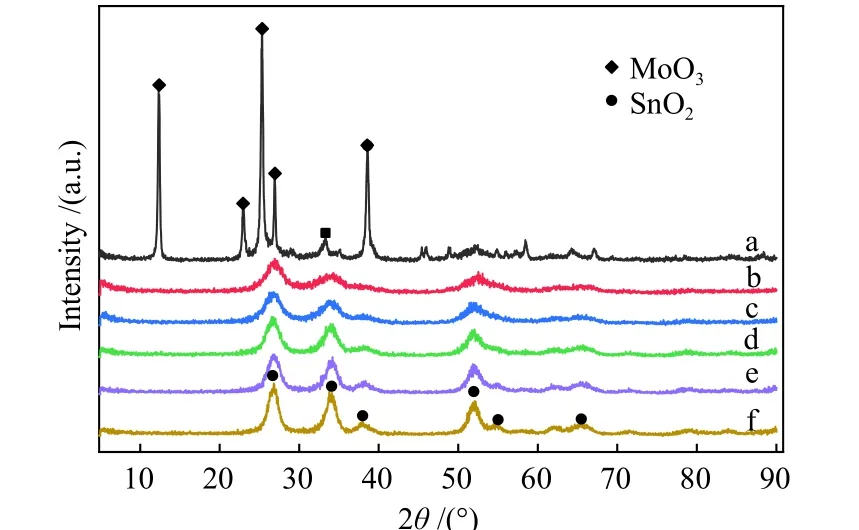
图1 不同Mo 含量Mo-Sn 催化剂的XRD 谱图Figure 1 XRD patterns of Mo-Sn catalysts with different Mo contents a: Mo2Sn1; b: Mo1Sn2; c: Mo1Sn4; d: Mo1Sn8;e: Mo1Sn10; f: Mo1Sn20
2.2.2 Raman 表征
不同Mo 含量催化剂的Raman 表征结果如图2所示。处于627、770 cm−1位置的峰归属于SnO2的特征衍射峰,处于820 cm−1处的峰为MoO3晶体上 Mo−O−Mo 结构中氧的桥式振动峰,处于992 cm−1的峰为MoO3晶体末端Mo=O 双键的伸缩振动峰[19]。可以看出,当Mo 含量较多时,催化剂中钼氧化物主要以MoO3晶形结构为主,随着Mo 含量减少、Sn 含量增多,催化剂的晶型结构逐渐发生了变化;当Mo 含量小于(或等于)1∶9 时,样品主要以MoOx的结构为主,特别是Mo1Sn20 催化剂,位于992 cm−1位置归属于MoO3的衍射峰消失,说明大部分的MoO3转变成了不同形态的MoOx。
图2 中,处于898 cm−1位置的峰为低聚态MoOx中Mo−O−Mo 结构的桥式振动,975 和965 cm−1的峰为低聚态MoOx末端Mo=O 的伸缩振动[21]。随着Mo 含量的减少,归属于低聚态MoOx的峰面积总体在减小,但归属于低聚态MoOx的峰与归属于MoO3的峰面积比却在逐渐增大,表明低含量的Mo 有利于MoOx结构的形成,而该结构的增多也会导致催化剂氧化还原性质的改变[23]。结合评价结果,MoOx结构的相对含量越高,甲醇定向转化成DMM 的能力越强,说明MoOx结构在甲醇氧化生成DMM 过程中起着重要作用。

图2 不同Mo 含量催化剂的Raman 谱图Figure 2 Raman spectra of catalysts with different Mo content a: Mo2Sn1; b: Mo1Sn2; c: Mo1Sn4; d: Mo1Sn8;e: Mo1Sn10; f: Mo1Sn20
2.2.3 FT-IR 表征
进一步对催化剂结构进行FT-IR 表征,具体见图3,不同Mo 含量的Mo-Sn 催化剂表现出不同的结构特征。其中,3524 cm−1处的峰为M−OH 特征峰,Mo2Sn1 中的1015、996 cm−1处的峰为MoO3中Mo=O 的特征峰,且在822 cm−1处存在区别于其他催化剂的代表MoO3中Mo−O−Mo 的特征峰,说明该催化剂中Mo 的主要存在形式为MoO3[24];其他催化剂中977、971、928、908、893 cm−1处的峰归属为低聚态MoOx中Mo=O 的特征峰[25],说明除Mo2Sn1 外催化剂中Mo 主要以MoOx的形式存在,这与Raman结果相一致。并且,随着Mo 含量的减少,MoOx中Mo=O 的特征峰向低波段移动,说明Mo 含量的减少对钼氧化物的相互作用产生了影响,Mo 的存在形式在逐渐发生改变,当Mo 含量极少时,可能影响着MoOx的聚合程度[23]。
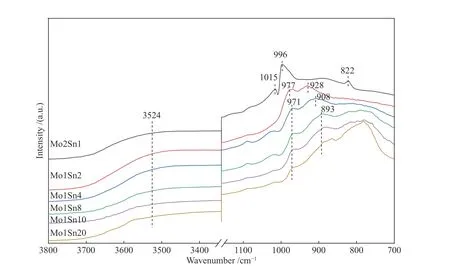
图3 不同Mo 含量Mo-Sn 催化剂的FT-IR 谱图Figure 3 FT-IR spectra of Mo-Sn catalysts with different Mo contents
2.2.4 XPS 表征
催化剂表面的元素价态通常对催化剂的氧化还原性质有着重要的影响,因此,采用XPS 手段对Mo 与Sn 的价态进行了表征分析。如图4 所示,含有不同Mo 量催化剂Sn 3d的结合能峰位于487.19 与495.56 eV,说明Sn 组分以Sn4+的形式存在[26]。在Mo 3d的谱图中,Mo 的位置发生了偏移,说明Mo 的价态或电子结构发生了变化。进一步对Mo 3d的XPS 谱线进行分峰拟合(图5),在236.2、233.1、235.1 与231.8 eV 附 近 可 得 到 四 个拟 合 峰,分 别 归 属 于Mo6+3d3/2、Mo6+3d5/2、Mo5+3d3/2和 Mo5+3d5/2[27]。表2 为XPS-Mo 3d的 分 析结果,定量计算了催化剂表面Mo5+与Mo6+的相对含 量,结 果 显 示,Mo2Sn1、Mo1Sn2、Mo1Sn4 等Mo 含量较多的催化剂所含Mo5+的相对含量较少,而将Mo 的量减少至Mo1Sn8、Mo1Sn20 时Mo5+的相对含量明显提高,说明较少含量Mo 的存在更有利于Mo5+的形成。这一结果与Raman 的结果相对应。根据报道,MoOx域相较于MoO3具有更强的电子离域特性[23],因而可能导致更多Mo5+的产生。另外,在Mo1Sn10、Mo1Sn20 催化剂中,由于Mo 含量较少、分布均匀,可导致加入的钼氧化物几乎都与锡表面作用形成Sn−O−Mo 键[20],钼氧化物在与锡氧化物接触的界面处受到的作用力可能会增强,这种作用力可能会导致钼氧化物的分布状态发生变化,这也可能是Mo5+增多的又一原因。
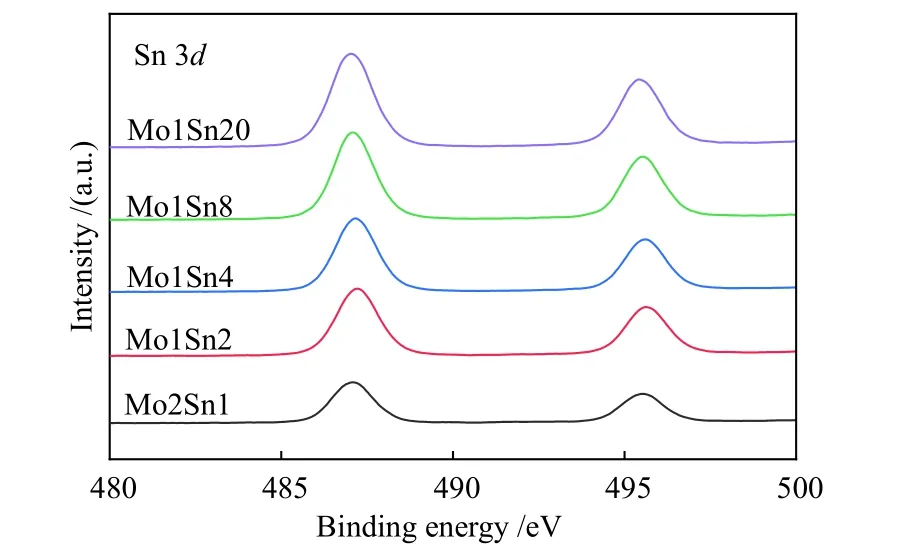
图4 不同Mo 含量Mo-Sn 催化剂的XPS-Sn 3d 谱图Figure 4 XPS-Sn 3d spectra of Mo-Sn catalysts with different Mo contents

图5 不同Mo 含量Mo-Sn 催化剂的XPS-Mo 3d 谱图Figure 5 XPS-Mo 3d spectra of Mo-Sn catalysts with different Mo contents
图6 与表3 分别显示了催化剂中O 1s轨道的结合能变化及拟合结果。在图6 中,随着Mo 含量在催化剂中的变化,O 1s的结合能峰位发生移动;对其进行拟合后发现,随Mo 量减少时归属于羟基的O 物种(OOH)的相对含量有增加的趋势。

图6 不同Mo 含量Mo-Sn 催化剂的XPS-O 1s 谱图Figure 6 XPS-O 1s spectra of Mo-Sn catalysts with different Mo contents

表 2 不同Mo 含量Mo-Sn 催化剂的XPS-Mo 3d 谱图分析Table 2 XPS-Mo 3d analysis of Mo-Sn catalysts with different Mo contents
2.2.5 H2-TPR 表征
通过H2-TPR 表征(图7)发现,谱图中主要存在四种还原峰。其中,位于700 ℃左右的峰为SnO2的还原峰,位于200−400 ℃的还原峰归结于Mo6+→Mo5+的还原,而位于400−500 ℃的还原峰归结于Mo5+→Mo4+的还原,550 ℃左右的还原峰归结于Mo6+→Mo4+的还原,当反应温度较低时主要关注低温段还原峰的变化[21],即Mo6+→Mo5+还原峰的变化。当Mo 含量减少时,Mo6→Mo5+还原峰的位置逐渐向低温方向转移,说明Mo 含量的减少会导致高价态的Mo 更容易被还原,即氧化还原性得到了增强,可能是由于含较低含量Mo 的催化剂中Mo5+含量增多使得Mo6+与Mo5+之间的氧化还原循环更容易及MoOx结构的增多导致了电子离域能力的增强[25],从而使得氧化还原性得到了增强,结合评价结果认为,氧化还原性的增强有利于DMM的生成。

表 3 不同Mo 含量Mo-Sn 催化剂的XPS-O 1s 谱图分析Table 3 XPS-O 1s analysis of Mo-Sn catalysts with different Mo contents
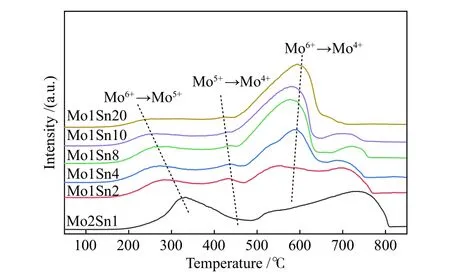
图7 不同Mo 含量Mo-Sn 催化剂的H2-TPR 谱图Figure 7 H2-TPR profile of Mo-Sn catalysts with different Mo contents
2.2.6 NH3-TPD 表征
图8 为含不同Mo 含量催化剂的NH3-TPD 谱图。由图8 可知,在NH3-TPD 谱图中,催化剂显示有两个温度范围的脱附峰;一个脱附峰位于400−500 ℃,归属于中强酸位点,另一脱附峰位于100−250 ℃,归属于弱酸性位点。当Mo 含量减少时,归属于中强酸位的脱附峰向低温方向移动,弱酸位峰面积增加;当Mo 量在催化剂的物质的量比少于(或等于)1∶3 时,中强酸消失,并随着Mo 的量进一步减少,脱附峰逐渐向低温段移动,并且峰面积随之减少。这说明随着Mo 含量的减少,催化剂表面的酸强度逐渐减弱且总酸量也随之减少。根据图6 中不同Mo 含量催化剂的XPS-O 1s拟合结果及表3 中相应的结果可知,随着Mo 含量的不断减少,催化剂中羟基氧的相对数量不断增加。这表明,羟基氧的数量越多其酸性越弱,催化剂表面的酸性与羟基氧有关。结合评价结果及甲醇转化路径分析发现[22],较强的酸性使得甲醇脱水为DME 成为主要的转化方式,而适量弱酸性位的存在促使甲醇向生成DMM 的方向而不是MF 的方向转化。其中,Mo2Sn1 催化剂除存在强酸位点之外同时也存在一定的弱酸性位点,该弱酸位与氧化还原性位的共同作用使得该催化剂与Mo1Sn4催化剂具有相近的DMM 选择性,这进一步说明弱酸性位点是生成DMM 的关键性活性位点之一。

图8 不同Mo 含量Mo-Sn 催化剂的NH3-TPD 谱图Figure 8 NH3-TPD profile of Mo-Sn catalysts with different Mo contents
综合以上表征结果分析认为,催化剂中钼结构的变化导致了催化剂表面性质发生了变化,同时也对甲醇的解离、吸附产生了影响。研究发现,较强的酸性会导致催化剂解离吸附能力的增强,更有利于DME 的产生,抑制了甲醇向DMM 的转化,而氧化还原性位与弱酸性位的共同作用是甲醇高选择性转化为DMM 的主要原因。
3 结 论
本工作研究了Mo 含量的变化对钼锡催化剂中Mo 氧化物结构及甲醇氧化性能的影响。结果显示,水热法制备的Mo-Sn 催化剂具有良好的低温氧化性能,特别是Mo1Sn10 催化剂上,140 ℃、常压条件下,甲醇转化率为14.2%,DMM 的选择性高达88.9%,并且在此过程中未有COx的产生。对催化剂的结构表征后发现,Mo 含量的减少,有利于MoOx结构的形成及Mo5+物种相对含量的增加,特别是Mo1Sn20催化剂中,催化剂中Mo5+相对含量达到最高,并且钼氧化物几乎全转变为MoOx结构。而Mo5+物种和MoOx结构的变化所引起的酸强度的减弱及氧化还原性的增强是催化剂具有良好性能的重要原因。
猜你喜欢
杂志排行
燃料化学学报的其它文章
- 酸活化蒙脱土在二甲醚水蒸气重整制氢中的应用
- Ni 对MoS2 基催化剂活性相及加氢脱氮脱硫性能的影响
- Insight into reaction path and mechanism of catalytic cracking of n-hexane in HZSM-5 zeolites
- CO2/CH4/N2 在MER 型沸石中扩散和分离的分子动力学模拟
- Addition of bismuth to Pt and Pd for electric power generation with selective cogeneration of acetate from ethanol in a fuel cell type reactor
- 淖毛湖褐煤分级萃取可溶有机质的组成结构特征及萃余残渣的热转化性能
