基于动态共价键的纳米纤维素智能凝胶构建
2021-11-19
(闽江学院福建省新型功能性纺织纤维及材料重点实验室,福建 福州 350108)
0 引言
近些年来,智能水凝胶的发展较为迅速,如多响应性水凝胶、高强度水凝胶等性能独特且可控的智能型水凝胶已广泛应用于传感器、组织工程、细胞/药物传送系统和再生医学等众多领域[1]。尽管智能型水凝胶具备优越的性能,但是当水凝胶因为受损而形成了宏观或者微观尺度上的裂痕时,它那优越而独特的性能往往会变差,甚至因此丧失。如果这些裂痕进一步扩大,可能还会影响水凝胶的网络结构完整性和其机械性能,进而缩短水凝胶的使用寿命[2]。与此同时,植入到生物体的水凝胶受损以后很难用人工的方法将其填补、修复。因此,研究并开发出与生物的软组织结构和性能相似,并且在受损后仍然可以恢复材料的原有结构和功能的自愈合型智能水凝胶就具有广泛的科学意义及应用潜力。
根据愈合机理的不同,自愈合水凝胶主要可将其分为两种:物理型自愈合水凝胶和化学型自愈合水凝胶。与传统水凝胶相比,在遭到受力破坏后,自愈合水凝胶依然可以恢复其原本的结构和功能,即具有自愈合性能,因而在近些年来受到了许多关注。而动态建构化学概念的引入则能够充分地促进多响应自愈合水凝胶的发展。作为一种拥有良好生物相容性,且能够被赋予可降解性和刺激响应性等诸多功能的材料,自愈合水凝胶在组织工程、药物传递以及脊髓再生等各个领域都有着广阔的应用前景。然而,就目前而言,该类水凝胶的制备过程都还较为复杂,而且其自愈合速度仍不够快,效率也不够高。
相较于合成高分子水凝胶,天然高分子水凝胶就具备良好的生物相容性和降解性[3],它的使用过程也较为安全,且经济耐用,绿色环保,还拥有优越的力学性能,所以适用于食品包装、生物医药、石油化工以及建筑等众多领域。由于从合成石油基聚合物转向从可再生和可持续来源中获得大分子物质的环境趋势的日益增长,以及天然高分子聚合物在生物医学和制药应用中存在的潜力,由天然高分子聚合物(如纤维素和壳聚糖)制成的水凝胶在过去的几十年里就引起了很大的关注[4-5]。
纤维素纳米晶体(CNC)是一种源自纯天然可再生资源的天然生物聚合物。作为一种十分有前景的生物质材料,它因拥有良好的生物相容性,高比表面积和长宽比以及较高的机械强度和刚度而引起了巨大关注[6-7]。这些突出的特性使得CNC能够作为增强纳米填料而广泛地应用于聚合物水凝胶的基质中。然而,在大多数由CNC增强的水凝胶中,原始的CNCs仅物理地包埋在其基质中以改善其机械性能。但由于CNC分子内含有大量的羟基,相互之间容易形成大量的氢键而发生团聚,不利于反应的进行,使得制备的水凝胶的机械强度和韧性仍然较差。

图1 高碘酸钠氧化原纤维过程示意图Fig.1 Schematic diagram of the process of oxidizing fibril with sodium periodate
双醛基纳米纤维素主要是将原纤维用高碘酸钠氧化而制得,反应机理见图1。该方式主要是将2,3-二羟基转化成2,3-二醛基而实现,通过醛改性可以很容易地将纳米纤维素转化成高活性的交联剂。壳聚糖及其衍生物拥有的最重要的特征之一就是其伯氨基团丰富。来自羧甲基壳聚糖的氨基团可以与聚合物的醛基团反应形成动态且可逆的席夫碱键,它易于破碎和重新成形,使水凝胶实现快速自愈。考虑到羧甲基壳聚糖中存在丰富的氨基团和醛基纳米纤维素拥有较大的比表面积和大量的活性醛基,从而假定由羧甲基壳聚糖和醛基纳米纤维素组成的自愈合水凝胶能够迅速成形,并且其在生理条件下发生断裂后又可快速自愈合。此外,当其被浸入水性体系中时,水凝胶中的醛基纳米纤维素可以起到支持和保护网络结构的作用。
本研究将改性的双醛基纳米纤维素与羧甲基壳聚糖相结合,通过二者之间的席夫碱反应来形成动态亚胺键,从而制备出纳米纤维素自愈合水凝胶的过程。选用氨基或醛基化改性修饰过的生物质大分子来作为交联剂的席夫碱反应来构筑自愈合水凝胶体系,可以避免用戊二醛、乙二醛等小分子交联剂反应时产生的生物毒性。同时,亚胺键的动态化学平衡可以使得材料对外界的环境具有多重响应性,从而将之应用于开发新型的智能水凝胶,满足不同的应用需求,在细胞治疗及通过刺激响应性药物来靶向传送载体等生物医学领域具有广泛的应用前景。该方法使用的原料为天然高分子聚合物,无毒无害,易降解可再生,其制作过程简便,条件温和,能耗低,效率高,成形迅速,环境污染少,且产品性能优良、化学品的用量少,是制备自愈合水凝胶的较好方法之一。
1 实验部分
1.1 原料与试剂
漂白竹纤维(α-纤维素含量≥94%),购自福建省南纸股份有限公司;高碘酸钠(分析纯),浓硫酸(分析纯),乙二醇(分析纯),购自国药集团化学试剂有限公司;羧甲基壳聚糖(取代度>80%),购自阿拉丁试剂(上海)有限公司。
1.2 醛基纳米纤维素的制备
用高速多功能粉碎机打碎竹浆,直至纤维素浆料呈粉末状均匀分散,然后放置在60 ℃的烘箱内烘干以备用。往4个重量基本相等的球磨罐中均各加入2 g绝干竹浆、1 g高碘酸钠以及25 ml提前配好的pH=4.0的硫酸溶液。将这4个球磨罐分别用保鲜膜密封好后以对角线质量对等的放法放入球磨机中,在转速为500 rad·min-1的条件下进行3 h的球磨,然后再分别往4个罐中加入2 g高碘酸钠,继续在同样转速下再球磨3 h。球磨结束后用去离子水将所有混合浆液冲洗到烧杯中,再加入25 ml乙二醇溶液并遮光搅拌12 h,以彻底分解剩余的高碘酸钠。用去离子水配合高速离心机反复洗涤至上清液呈中性后,再次利用超声波细胞粉碎仪对样品进行一段时间的超声处理,最后于5 000 rad·min-1的条件下多次离心收集上层悬浮液,并对悬浮液进行浓缩处理,即得到双醛纳米纤维素。对其进行固含量测定,结果表明,制得的双醛纳米纤维素的固含量为5.86%。

图2 醛基纳米纤维素制备流程图Fig.2 Aldehyde-based nanocellulose preparation flow chart
1.3 纳米纤维素自愈合水凝胶的构建
首先需将粉末状的羧甲基壳聚糖溶解于水并按比例配制成一定浓度的溶液。再将制备好的醛基纳米纤维素加入水进行充分溶解,因制备的醛基纳米纤维素溶液浓度较低,故应尽量提高壳聚糖溶液的浓度以降低凝胶含水率,但浓度过高则会导致壳聚糖溶液流动性差,不利于反应的进行,因而需配制适当浓度的壳聚糖溶液。本实验中选择配制6%、7%、8%的羧甲基壳聚糖溶液。取适量制得的醛基纳米纤维素溶液分别与这3种不同浓度的羧甲基壳聚糖溶液均按照1∶5、1∶6、1∶7、1∶8的比例进行混合,搅匀后迅速倒入模具中,3~4 s即可成形。
2 分析表征
2.1 样品形貌分析
采用场发射扫描电子显微镜(FESEM)来观察及分析制备的水凝胶样品的微观形貌。使用液氮将制备的水凝胶样品冷冻后用锤子敲碎,随后放入冷冻干燥机中将其进行冷冻干燥,待干燥完毕后取出并马上在其颗粒表面喷铂,然后用场发射扫描电镜对样品水凝胶的内部形貌进行检测观察。
采用透射电子显微镜来扫描观察醛基纳米纤维素的微观形貌。用乙醇将制备的双醛基纳米纤维素悬浮液进行稀释,然后超声15 min,再用胶头滴管取一滴超声完的分散液滴在覆有碳膜的扫描电镜样品网格上,在40 ℃条件下干燥后进行观察。
2.2 压缩性能测试
根据GB/T 1041-92标准,对基于动态共价键作用的纳米纤维素自愈合水凝胶样品进行压缩应变及压缩强度的测试。将水凝胶制成高度为8 mm,直径为15 mm圆柱状,在25 ℃的条件下,在万能试验机上以20 mm·min-1的速度进行测试,每个浓度配比的水凝胶样品均测试4次取平均值。
2.3 红外光谱分析
采用KBr压片法对制备的样品进行傅里叶变换红外光谱分析。进行分析前先用冷冻干燥机对样品进行冷冻干燥,待样品干燥到能顺利进行研磨的程度后,用玛瑙研钵将样品与KBr粉末以1∶100的质量比混合研磨至粉末状,然后压片进行测试。波数范围设定为4 000~400 cm-1,仪器的分辨率为4 cm-1,扫描频率为32 次·s-1。
2.4 XRD分析
采用Ultima IV型X射线粉末衍射仪(XRD)来检测样品水凝胶粉末的晶体结构。检测时设置参数为:Cu-Ka射线,镍片滤波,管电压40 kV,扫描范围2θ=5°~60°(θ为衍射角),扫描速度0.02°·s-1。结晶度(XC)的计算公式如下:
结晶度(XC)=AK/(AK+AA)×100%
其中,AK指的是(002)峰的峰面积,即晶区面积;AA为无定形区面积;总面积=AK+AA。
2.5 TG分析
采用TG 209 F3型热重分析仪对样品水凝胶粉末进行热稳定性分析。分析过程选用氮气为保护气,测试时将5 mg样品粉末放在氧化铝坩埚内,设置温升速率为10 K·min-1,温度范围为25 ~700 ℃。
3 结果与讨论
3.1 形貌分析
图3为不同壳聚糖溶液浓度制备的双醛基纳米纤维素与壳聚糖质量比为1∶8的复合水凝胶切面电镜图。由图3可以看出,3种不同壳聚糖浓度的水凝胶都呈现出复杂的孔隙结构,这是由水凝胶内所含水分经冷冻干燥后所呈现。相较于壳聚糖溶液浓度为6%的水凝胶的电镜图,壳聚糖溶液浓度为7%的水凝胶的电镜图中的孔隙较小,而且大部分的孔径也随着水凝胶中壳聚糖浓度的增大而减小,但二者的孔隙分布都较不均匀;而壳聚糖溶液浓度为8%的水凝胶的电镜图中的孔隙则更小,且分布整体均匀(图3)。观察水凝胶断面的不规则孔隙结构,结果表明水凝胶的孔洞结构可能与其内部的动态共价键有着紧密的联系。化学交联的水凝胶中的席夫碱键增大了网络密度,也提供了更多分子间作用力以形成更多交联点,而这些交联点又反过来影响了该水凝胶的孔隙结构、孔径以及分布等[8]。

图3 在原料配比为1∶8下,壳聚糖浓度不同的水凝胶断面的扫描电镜图Fig.3 Scanning electron micrograph of hydrogel section with different chitosan concentrations at a raw material ratio of 1∶8
图4中展示的是双醛纳米纤维素以及未改性的纳米纤维素在透射电子显微镜下的微观形貌。由图4中可以看出:未改性的纳米纤维素呈短棒状,但由于羟基之间强烈的形成氢键作用的趋势,纳米纤维素之间相互结合呈束状聚集,易产生自团聚现象。而相较于未改性的纳米纤维素,双醛基纳米纤维素则较少呈现出聚集状态,这是由于改性后的醛基纳米纤维素分子间的氢键作用力有所减弱从而减少了侧向聚集,有助于其与羧甲基壳聚糖分子中的氨基反应构成席夫碱键。改性后的双醛纳米纤维素的样貌呈现出扁平的棒状结构,它的尺寸与样貌都没有因为通过高碘酸钠改性而发生改变。

图4 纳米纤维素的透射电镜图Fig.4 Transmission electron micrograph of nanocellulose
3.2 压缩性能测试
该纳米纤维素自愈合水凝胶的压缩性能采用应力-应变曲线的形式体现。如图5所示,对比不同羧甲基壳聚糖浓度以及不同配比对水凝胶压缩性能的影响。在图5(a)中,同样是6%的羧甲基壳聚糖溶液原料,配比为1∶7时水凝胶的压缩模量最大,抗压性能最好,1∶8配比的水凝胶次之,最差的是1∶6的配比;而图5(b)、图5(c)中在同等羧甲基壳聚糖原料浓度条件下,在配比为1∶8时其压缩模量均最大。该数据体现了在羧甲基壳聚糖原料浓度相等的情况下增加水凝胶中的羧甲基壳聚糖含量有助于提高水凝胶的抗压强度。在图5(d)中,对比同配比不同羧甲基壳聚糖原料浓度的水凝胶的压缩性能可发现压缩模量的大小为:8%壳聚糖浓度>7%壳聚糖浓度>6%壳聚糖浓度。这说明水凝胶中含水量的降低有利于其抗压强度的提升。压缩强度的提升可归结于分子内部动态亚胺键的增强,氨基和醛基的化学交联使得凝胶内形成紧密的交联点,从而增强水凝胶的抗压能力。

图5 不同壳聚糖和原料配比的水凝胶的压缩曲线Fig.5 Compression curve of hydrogel with different concentration of chitosan solution at different ratio of raw material
3.3 产物结构分析
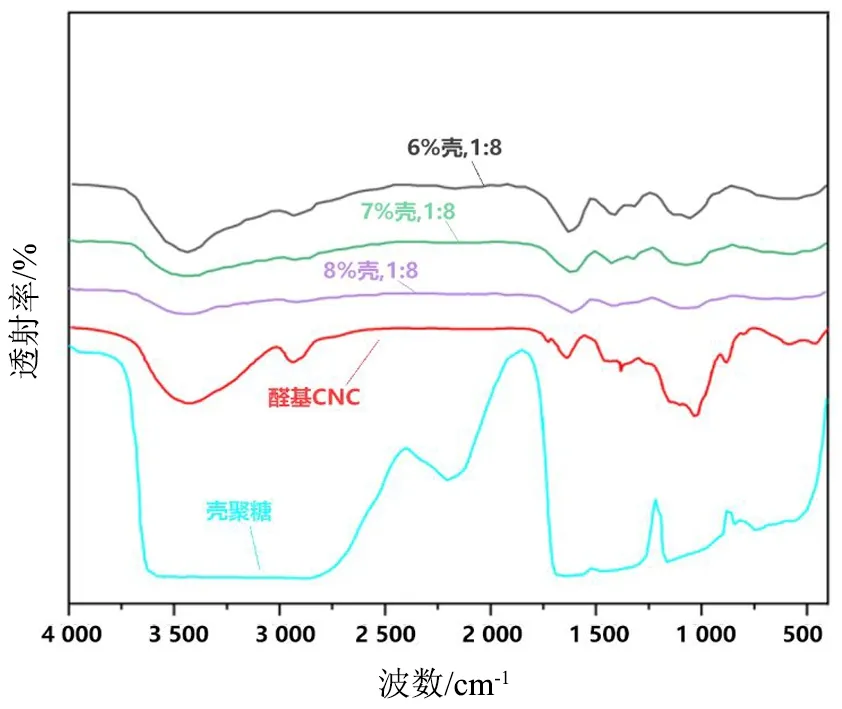
图6 原料配比为1∶8情况下不同壳聚糖溶液浓度的水凝胶以及壳聚糖原料的FTIR谱图Fig.6 FTIR spectra of chitosan and hydrogels with different concentrations of chitosan solution at a raw material ratio of 1∶8
图6为各个不同浓度配比的纳米纤维素自愈合水凝胶、醛基纳米纤维素和羧甲基壳聚糖原料的FTIR谱图。分析羧甲基壳聚糖原料的FTIR谱图可知,在1 024 cm-1和1 068 cm-1处的峰是壳聚糖的-CO伸缩振动峰,在1 600 cm-1和1 419 cm-1处的峰是-COO的不对称和对称的伸缩振动峰,而在3 400 cm-1处的宽峰则是氨基的伸缩振动和羟基的伸缩振动重叠的峰。而在水凝胶的FTIR谱图中:在1 068 cm-1及1 160 cm-1处的峰分别为纤维素中-CO的伸缩振动和-CC骨架的伸缩振动[9],在3 443 cm-1、2 926 cm-1以及1 626 cm-1处的峰则对应-OH的伸缩振动、亚甲基的-CH伸缩振动和-COO的伸缩振动峰,在1 328 cm-1和1 420 cm-1处则对应-CN的弯曲振动和-CH3的对称变形,而在1 670 cm-1处出现的新的吸收峰则是-CN的伸缩振动峰。对比水凝胶的吸收峰与壳聚糖的吸收峰可发现:水凝胶在3 443 cm-1处的峰变得窄且弱,而在1 670 cm-1处出现了新的吸收峰,这是由于双醛纳米纤维素的醛基与羧甲基壳聚糖的氨基之间发生了席夫碱反应生成动态亚胺键,从而导致氨基的伸缩振动峰消失。
3.4 晶体结构分析
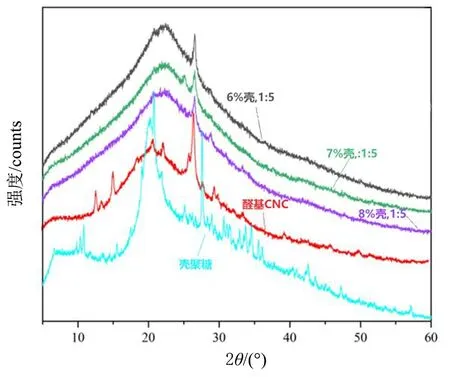
图7 原料配比为1∶5情况下不同壳聚糖溶液浓度的水凝胶以及壳聚糖原料的XRD谱图Fig.7 XRD patterns of chitosan and hydrogels with different concentrations of chitosan solution at a raw material ratio of 1∶5
图7为各个不同浓度配比的纳米纤维素自愈合水凝胶和壳聚糖原料的XRD谱图。由图7可知,壳聚糖在2θ=10.7°及20.8°时出现了较强的衍射峰,而水凝胶则在2θ=22.3°时出现较强的衍射峰,其主要为纳米纤维素的特征峰。壳聚糖在10.7°的特征峰之所以在与双醛纳米纤维素反应形成水凝胶后消失,是因为羧甲基壳聚糖中的氨基与双醛纳米纤维素中的醛基发生了席夫碱反应构成了动态亚胺键,从而导致其晶体结构遭到破坏,使衍射峰消失。按公式计算可得:壳聚糖的结晶度为63.0%,6%壳聚糖浓度、配比为1∶5的水凝胶的结晶度为17.7%,7%壳聚糖浓度、配比为1∶5的水凝胶的结晶度为16.3%,8%壳聚糖浓度、配比为1∶5的水凝胶的结晶度为15.8%。分析结晶度可知水凝胶中壳聚糖及纤维素含量越多其结晶度越小。这是因为有更多的壳聚糖中的氨基与双醛纳米纤维素中的醛基发生交联反应,使得羧甲基壳聚糖的晶体结构被破坏得更加彻底,分子间的氢键也被破坏更多[10]。
3.5 热稳定性分析
图8为各个不同浓度配比的纳米纤维素自愈合水凝胶和羧甲基壳聚糖原料的TG谱图。分析图8(a)可发现,当温度小于100 ℃时,水凝胶和壳聚糖的质量也有一定幅度的下降,这是因为样品受热而导致了水分的挥发,因而样品质量有所下降。而在图8(b)中,羧甲基壳聚糖原料受热而发生分解的起始温度为99.0 ℃,受热分解最大速率在270.7 ℃,分解终止温度为563.0 ℃,受热分解导致的质量损失为46.99%。配比为1∶8,壳聚糖浓度为6%、7%、8%的水凝胶的起始分解温度分别为99.6 ℃、110.3 ℃、103.0 ℃,受热分解最大速率分别处于272.8 ℃、282.5 ℃、282.5 ℃,终止分解温度为550.1 ℃、603.8 ℃、521.2 ℃,受热分解导致的质量损失为47.59%、48.91%、47.70%[11]。分析以上数据可发现:羧甲基壳聚糖的发生热分解的起始温度低于水凝胶发生热分解的初始温度温度,且当二者的热分解速率均最大时,壳聚糖的温度也是低于水凝胶的温度,这主要是由于改性后的双醛纳米纤维素和羧甲基壳聚糖之间的化学交联作用提高了水凝胶的热性能,其热稳定性会随着交联度的增大而提升[12]。

图8 原料配比为1∶8时壳聚糖浓度不同的水凝胶和羧甲基壳聚糖的TG图Fig.8 TG spectra of carboxymethyl chitosan and hydrogels with different concentrations of chitosan solution at a raw material ratio of 1∶8
3.6 水凝胶自愈合性能测试
宏观上,采用自我修复测试来验证该水凝胶的自愈合性能,过程如图9所示。分别制备两段同等浓度及配比的纳米纤维素自愈合水凝胶,其中一段凝胶中加入Rhodamine B(罗丹明 B)作为指示剂。将两段水凝胶各切掉一小段,然后将其切口对应接触,用保鲜膜将其封闭起来以隔绝外界影响,在室温条件下放置1 h,会发现二者之间的缺口重新愈合[13]。如图9所示,二者之间的颜色界限变得模糊,且4段凝胶均各自融合成有单一连接点的一段水凝胶。此外,重新自愈合后的水凝胶还可维持原有形状,并在水中浸泡后不会发生分裂。且弯折自愈合后的水凝胶其缺口并不会裂开,这表明了该水凝胶拥有较强的自愈合能力[14]。

图9 宏观上的水凝胶自愈合性能的测试Fig.9 Macroscopic test of self-healing properties of hydrogels
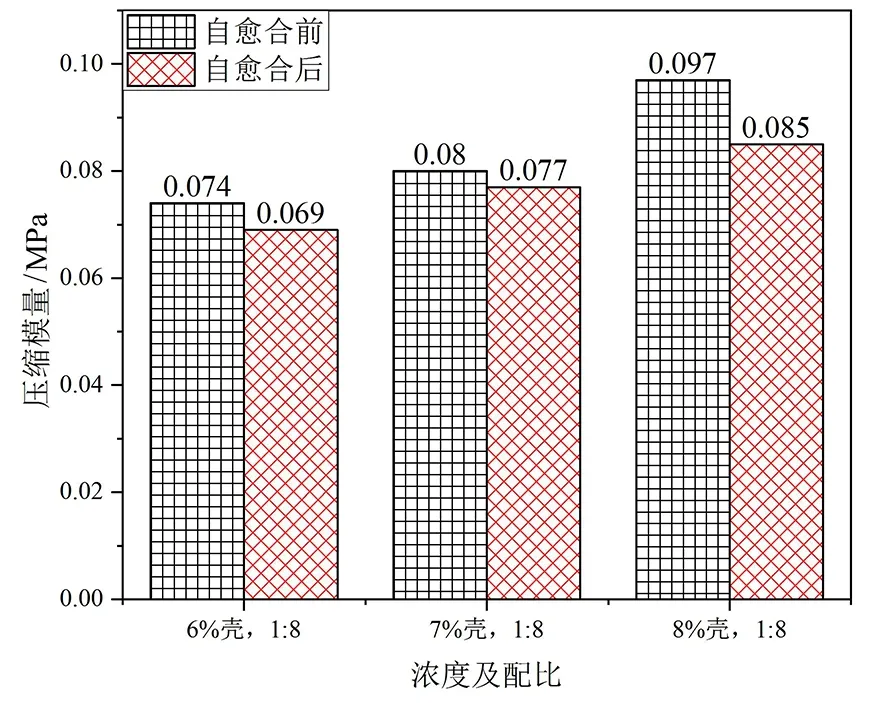
图10 自愈合前后的水凝胶的压缩模量对比图Fig.10 Comparison of compressive modulus of hydrogels before and after healing
图10是对自愈合前后的水凝胶的压缩模量进行测试及比较的结果的柱状图。通过图10中数据可知:6%羧甲基壳聚糖配比为1∶8、7%壳聚糖配比1∶8、8%壳聚糖配比为1∶8的水凝胶自愈合前后的压缩模量的变化率分别为6.8%、3.7%、12.4%,三者的自修复效率分别为93.2%、96.3%、87.6%,其中壳聚糖溶液浓度为7%配比为1∶8的水凝胶的自修复效率最高,其自愈合性能最好[15]。总体来看,自愈合后水凝胶的压缩模量相较自愈合前均有所降低,但变化并不大,均在13%以内,说明该水凝胶的自愈合性能仍较为良好[16]。
4 结论
1)通过双醛基纳米纤维素的醛基和羧甲基壳聚糖的氨基之间进行的席夫碱反应形成动态亚胺键,从而构筑的纳米纤维素自愈合水凝胶,凝胶成形迅速,可在常温条件下断裂后又重新快速自愈合,并且当该水凝胶被浸泡在水中时,水凝胶中的醛基纳米纤维素成分可以起到支持和保护其网络结构的作用,从而保证其不开裂。
2)水凝胶具有良好的抗压性能和热稳定性,两段水凝胶之间的缺口重新愈合,且愈合后其形貌基本维持不变,当其浸入水中时也不会发生开裂,这表明了该水凝胶的自愈合能力较为良好。
3)该方法使用的原料为天然聚合物,无毒无害,易降解可再生,其制作过程简便,条件温和,能耗低,效率高,成形迅速,环境污染少,且产品性能优良,化学试剂的用量少,是制备自愈合水凝胶的较好方法之一。
