磷钼酸铵负载聚丙烯无纺布吸附剂的辐射接枝法制备及其对Cs(I)的吸附性能
2021-11-17王焕潘晓晗薛怡俎建华
王焕 潘晓晗 薛怡 俎建华
(上海交通大学核科学与工程学院 上海 200240)
2011年3月11日,日本发生9级地震并引发了海啸,造成福岛核电站发生重大事故,事故应急处理和后续处理过程中排放了大量的放射性废水,导致福岛周围海域放射性核素含量严重超标[1]。排放的废水中含量最高的放射性元素是137Cs,它的衰变释放能量强,同时半衰期长达30a,极易通过环境和食物链到达人体,危害人类健康[2],因此周围海域中的137Cs亟需处理。到目前为止,针对放射性137Cs移除的方法包括:沉淀法[3]、溶剂萃取法[4-5]、离子交换和吸附法[6-9]等,其中,离子交换和吸附法是目前国内外去除和分离铯的主要方法之一。吸附Cs(I)时利用的主要材料有沸石[10]、多价金属磷酸盐[11]、亚铁氰化物[12]和杂多酸盐磷钼酸铵(AMP)[13-14]等。相比其他吸附材料,AMP因具有选择性强、吸附量大和稳定性良好等特点,被广泛用于核电站Cs(I)的吸附分离[15]。然而,AMP呈粉末微晶状,机械强度差,受到挤压容易结块,堵塞吸附柱出口,影响柱分离装置的稳定运行[16]。
为了解决这一问题,本研究选用了聚丙烯(PP)无纺布作为载体,采用电子束预辐照法,将甲基丙烯酸环氧丙酯(GMA)接枝到PP无纺布上[17-18],生成PP-g-GMA,AMP晶体在接枝过程中包裹载入反应物中,最终生成了一种负载有AMP的吸附剂PP-g-GMA@AMP。通过电子束引发预辐射接枝法合成吸附剂PP-g-GMA@AMP,通过傅里叶变换红外光谱(FTIR)和扫描式电子显微镜(SEM)等手段表征吸附剂的基团和元素构成以及表面形貌,研究各种因素对吸附剂PP-g-GMA@AMP在静态和动态吸附移除Cs(I)性能的影响以及它对Cs(I)的选择性吸附行为。该吸附剂既具有AMP的优秀吸附性能,同时结构稳定,易于填充色谱柱,能够满足柱色谱法吸附放射性Cs(I)的需求,另外该吸附剂对Cs(I)的选择性吸附能力十分出色,可将Cs(I)从模拟放射性海水中的共存离子Ca(II)、Na(I)、Mg(II)中选择性分离。
1 材料与方法
1.1 试剂和仪器
AMP、硝酸铯(CsNO3)、甲基丙烯酸环氧丙酯(GMA)、二甲基亚砜(DMSO)、吐温80、PP无纺布等,试剂均为分析纯。GJ-2型地那米电子加速器,上海先锋电机厂;A-1000S恒温水浴摇床,日本EYELA公司;DC-1500C自动馏分收集器,东京理化器械株式会社;ICPS7510电感耦合等离子体发射光谱仪,日本SHIMADZU公司;傅里叶变换红外光谱仪,日本SHIMADZU公司;SP3880原子吸收分光光度计,上海光谱公司;低真空超高分辨场发射扫描电子显微镜(NOVA Nano SEM230),美国FEI公司。
1.2 样品制备
将PP无纺布放入密封袋,抽真空并密封,置于加速器电子束下的传送装置上进行间歇式辐照,电子束能量为2MeV,束流强度为1mA,总吸收剂量为100kGy。辐照后利用干冰低温运输,密封保存于超低温冰箱备用。将吐温80、AMP、GMA、DMSO以1%、1%、10%、88%的质量配比加入烧杯,充分搅拌形成AMP悬浊液装入球形烧瓶,持续通入氮气20min,以排除悬浊液中的氧气。随后将电子束照射过的PP无纺布浸入悬浊液中,继续通入氮气来防止PP无纺布上的自由基被氧化,在50℃持续搅拌反应4h。反应完后,取出无纺布,依次用去离子水和乙醇洗涤,在50℃下真空干燥24h,最终得到吸附剂PP-g-GMA@AMP。图1展示了PP-g-GMA@AMP的合成路线。
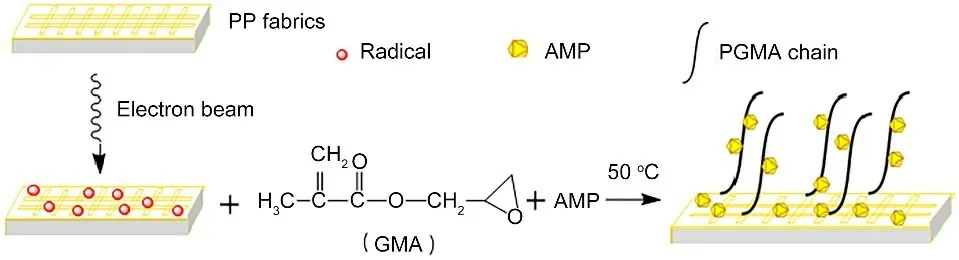
图1 PP-g-GMA@AMP的合成路线Fig.1 Synthesis route of PP-g-GMA@AMP
1.3 材料表征
FTIR用于检测判断PP无纺布上GMA接枝与AMP搭载,以及PP-g-GMA@AMP吸附铯以后功能基团的改变,SEM研究PP和PP-g-GMA@AMP的表面特性以及AMP的颗粒负载形态。
1.4 吸附实验
0.1g PP-g-GMA@AMP分别放入20mL 10mg/L的Cs(I)溶液中,调节pH=1~7,20℃下振荡吸附一定的时间,使用0.2μm的滤膜分离PPg-GMA@AMP和溶液。吸附前后溶液中Cs(I)的浓度使用原子吸收光谱仪测量,吸附剂在不同条件下对Cs(I)的吸附效率(R)计算见公式(1)。
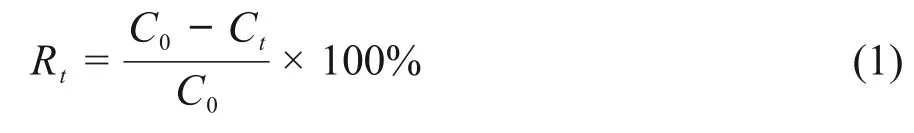
式中:C0、Ct分别指在初始时刻和t时刻Cs(I)的质量浓度,mg/L。
对于选择性吸附性能的考察,0.1g PP-g-GMA@AMP加入到20mL质量浓度10mg/L的Cs(I)、Ca(II)、Na(I)和Mg(II)混合溶液后,持续振荡吸附,分别于5min、15min、30min、45min、60min、120min、180min、240min后取出混合溶液,采用电感耦合等离子体发射光谱仪测定不同吸附时间时的Cs(I)、Na(I),原子吸收光谱仪测量Ca(II)和Mg(II),分配系数Kd(mL/g)和分离因子FS,A/B来研究离子在固定相和流动相的平衡性质,计算见公式(2)、(3)。
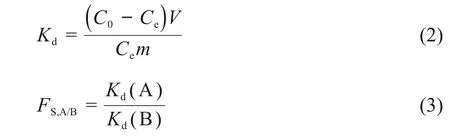
式中:C0、Ce分别指在初始和平衡时刻离子的浓度,mg/L;V为吸附溶液的体积,mL;m为吸附剂的质量,g;Kd(A)和Kd(B)为任意两种离子的分配系数。
2 结果与讨论
2.1 材料表征
2.1.1 成分质量分析
吸附剂的总质量部分由PP材料部分、接枝上的GMA以及负载其中的AMP组成。将吸附剂浸泡在1mol/L的NaOH溶液中反应72h,分离吸附剂和溶液,稀释溶液,使用ICP测试Mo元素浓度,计算AMP的质量。吸附剂充分清洗并干燥,得到去除AMP后材料质量。根据公式(4)、(5)计算出AMP的负载率Dg为5.72%,GMA接枝率Pg为32.41%。
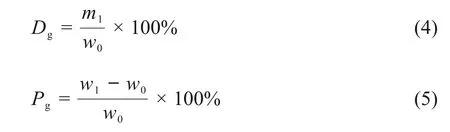
式中:w0为接枝前PP材料质量,g;w1为去除AMP后材料质量,g;m1为AMP的质量,mg。
2.1.2 FTIR分析
图2为PP、PP-g-GMA@AMP、吸附Cs(I)的PP-g-GMA@AMP的FTIR光谱。与PP红外光谱相比,PP-g-GMA@AMP的红外光谱含有羰基(C=O)的振动峰(1720cm-1)和环氧基的振动峰(1240cm-1),表明GMA成功接枝到PP上。在PPg-GMA@AMP的红外光谱中含有AMP的Keggin结构特征峰1064cm-1、958cm-1、860cm-1以及NH的弯曲振动吸收峰1407cm-1,表明AMP([NH4]3[PMo12O40])已成功负载到PP上。观察吸附Cs(I)后的PP-g-GMA@AMP的红外光谱,1407cm-1处N-H的弯曲振动吸收峰消失,证实[NH4]+被Cs(I)取代。综上所述,PP-g-GMA@AMP成功制备并且吸附了Cs(I)。
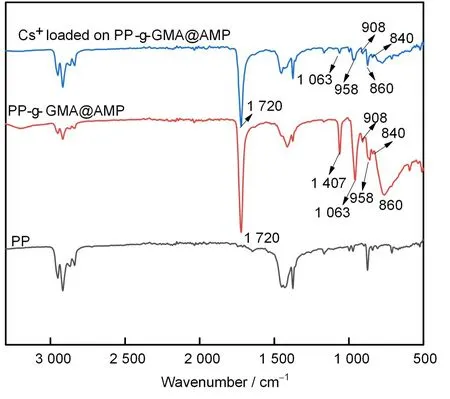
图2 PP、PP-g-GMA@AMP及PP-g-GMA@AMP吸附Cs后的FTIR图Fig.2 FTIR spectra of PP,PP-g-GMA@AMP,and PP-g-GMA@AMP after the adsorption of Cs(I)
2.1.3 SEM分析
图3为PP和PP-g-GMA@AMP的SEM图。从图3(b)可知,PP-g-GMA@AMP多孔纤维表面和纤维交织区域均包覆AMP晶体状颗粒,表明AMP负载到PP上,成功制备PP-g-GMA@AMP。

图3 PP(a)与PP-g-GMA@AMP(b)的SEM图像Fig.3 SEM images of PP(a)and PP-g-GMA@AMP(b)
2.2 溶液pH对吸附效果的影响
0.1g PP-g-GMA@AMP分别放入20mL10mg/L的Cs(I)溶液中,调节pH=1~7,20℃下振荡吸附24h后测量吸附溶液中Cs(I)浓度,并使用公式(1)计算吸附效率R,结果如图4所示。图4中的曲线反映了pH对PP-g-GMA@AMP吸附Cs(I)效率的影响。当pH为1时,最低吸附效率为92.34%;当pH=6时,最高吸附效率为97.23%。PP-g-GMA@AMP吸附Cs(I)的机理是Cs+(Cs(I)离子)与AMP上[NH4]+的阳离子交换,而酸性条件下大量的H+会与产生Cs+竞争性吸附[19],影响PP-g-GMA@AMP对Cs(I)的吸附效果。由于AMP在碱性条件下的稳定性较差,故微量的H(I)使得AMP负载吸附剂保持稳定,对其吸附过程起到促进作用。通过图4发现,在pH=6时,PPg-GMA@AMP吸 附Cs(I)效 率 达 到 最 佳 为97.23%。海水的pH=7,可以通过加入一定比例的酸,调节pH=6,来提高海水中PP-g-GMA@AMP吸附Cs(I)的效果。
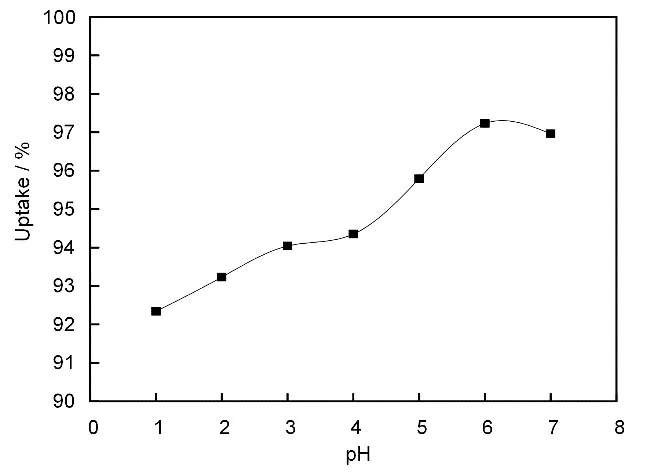
图4 pH对PP-g-GMA@AMP吸附Cs(I)效果的影响Fig.4 Effect of pH on the adsorption of PP-g-GMA@AMP for Cs(I)
2.3 接触时间对吸附的影响
吸附速度是评价吸附剂实际应用的重要参数之一,PP-g-GMA@AMP吸附Cs(I)的效率由接触时间的变化曲线可以反映出各个阶段吸附速度的快慢,还可以确定吸附平衡时间[20]。在20℃,pH=6的条件下,0.1g PP-g-GMA@AMP分别放入20mL10mg/L的Cs(I)溶液中,振荡吸附5min、15min、30min、45min、60min、120min、180min、240min后测量吸附溶液中Cs(I)浓度,并计算吸附效率R,结果如图5所示。从图5中曲线看出,前60min吸附效率提升速度很快,吸附率达到90%,约在120min时可以达到吸附平衡,最高吸附率97.73%。
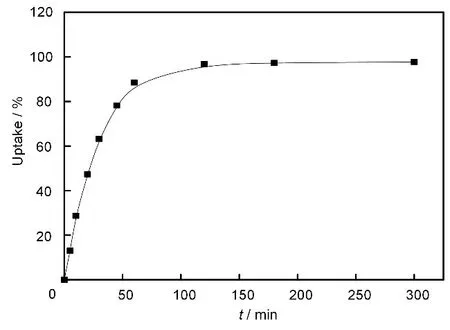
图5 接触时间对Cs(I)吸附率的影响Fig.5 Effect of contact time on the adsorption of Cs(I)
2.4 吸附动力学
PP-g-GMA@AMP吸附Cs(I)的行为可以用准二级动力学方程进行描述,见公式(6)。

式中:Qt和Qe分别是t时刻和平衡时刻的吸附容量,mg/g;k是准二级动力学方程吸附速率常数,g/(mg·min)。
图6为PP-g-GMA@AMP吸附Cs(I)的线性拟合,相关系数R2=0.9992(R2>0.99),因此PP-g-GMA@AMP对Cs(I)的吸附符合准二级动力学方程,根据式(6)计算得到吸附速度常数k=0.01918g/(mg·min)。
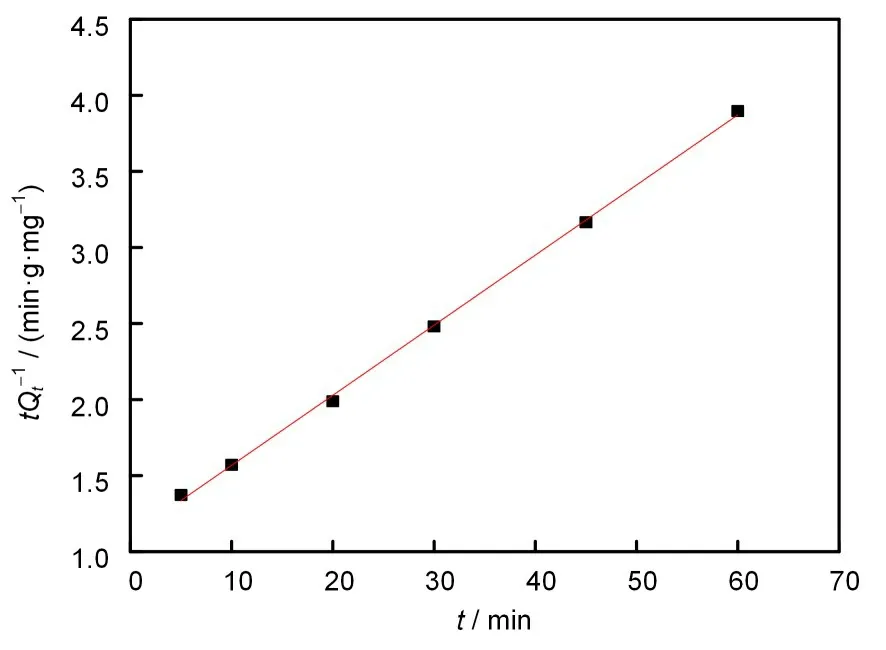
图6 准二级动力学拟合Fig.6 Adsorption kinetics of Cs(I)adsorption on PP-g-GMA@AMP
2.5 吸附等温线
吸附等温线指的是平衡时被吸附物在吸附剂和液相之间的关系曲线,可以通过吸附模型拟合判断吸附过程,并计算理论最大饱和吸附量。常见的吸附等温模型有Langmuir和Freundlich模型,其方程分别为公式(7)和公式(8)。
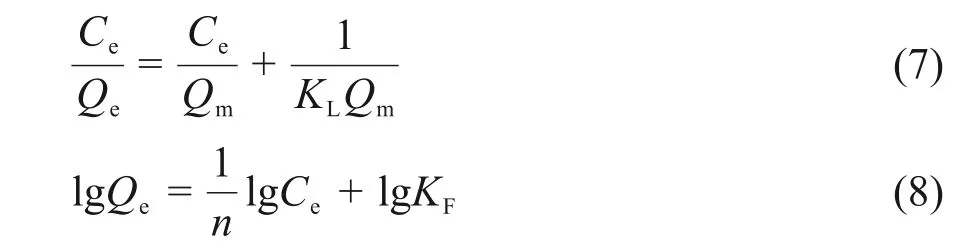
式中:Ce表示达到吸附平衡时液相中的Cs(I)容量,mg/L;Qe表示达到吸附平衡时固相中的Cs(I)容量,mg/g;Qm表示理论最大吸附容量,mg/g;KL和KF分别表示Langmuir和Freundlich常数。
通 过PP-g-GMA@AMP吸 附Cs(I)的Langmuir和Freundlich模型拟合数据(图7)发现,Langmuir模型拟合线性相关系数为0.9998(R2>0.99),而Freundlich模型拟合线性相关系数仅为0.8481,可以得出:PP-g-GMA@AMP吸附剂对Cs(I)的吸附符合Langmuir模型,说明PP-g-GMA@AMP对铯的吸附是单层吸附。另外,根据Langmuir吸附等温线的斜率可知,PP-g-GMA@AMP吸附剂对Cs(I)理论最大吸附容量为2.59mg/g。
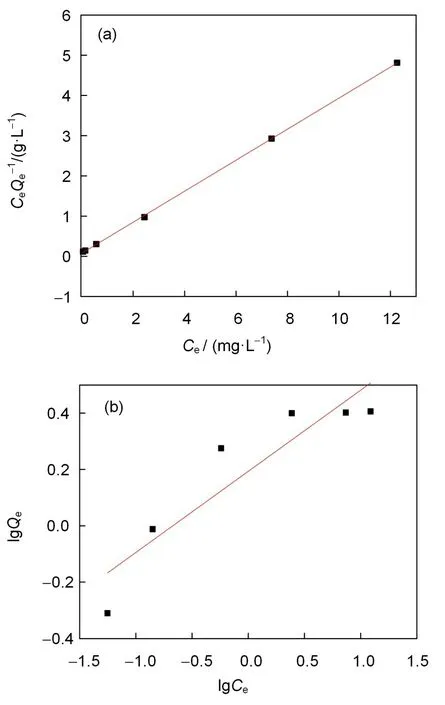
图7 Langmuir(a)和Freundlich(b)吸附等温线Fig.7 Adsorption isotherms of Langmuir(a)and Freundlich(b)
2.6 吸附剂的回收利用
考察PP-g-GMA@AMP吸附剂的循环使用性能。在温度20℃条件下使用吸附剂静态吸附pH=6、Cs(I)质量浓度为10mg/L的硝酸铯溶液6h后,使用1mol/L氯化铵溶液洗脱,然后清洗、干燥后重新进行静态吸附实验,重复3次,分别计算吸附6h的吸附容量,3次吸附容量分别为2.32mg/g、2.20mg/g、2.09mg/g,计算第3次重复使用后吸附容量与第一次吸附容量,仅降低9.91%,表明吸附剂具有良好的稳定性,可循环使用。
2.7 共存离子对PP-g-GMA@AMP吸附Cs(I)的影响
静态分离实验的考察能够为PP-g-GMA@AMP动态柱吸附分离条件的建立有很好的指导作用。图8展示了PP-g-GMA@AMP静态吸附Cs(I)与共存离子时接触时间对吸附率的影响,120min内可以达到吸附平衡,此时Cs(I)的吸附率为97.63%。根据实验结果计算得出,达到吸附平衡时PP-g-GMA@AMP对Cs(I)的分配系数达120.45,对Na(I)、Ca(II)和Mg(II)的分配系数分别是2.70、2.12和1.26。根据公式(2)、(3)计算分离因子SFCs/Ca、SFCs/Mg、SFCs/Na分别为97.45、65.24、61.53,均远大于1,这说明在静态吸附的条件下PP-g-GMA@AMP能够有效分离Cs(I)和共存离子Na(I)、Ca(II)和Mg(II)。
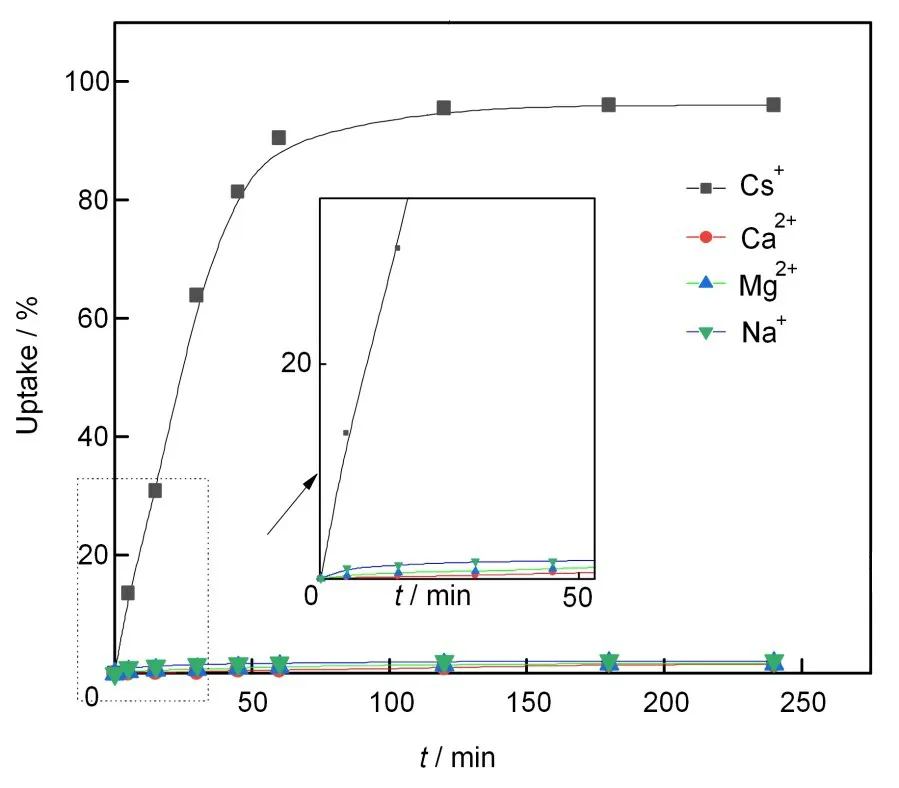
图8 接触时间对Cs(I)、Na(I)、Mg(II)和Ca(II)吸附率的影响Fig.8 Effects of contact time on uptake of Cs(I),Na(I),Mg(II),and Ca(II)
2.8 穿透实验
穿透曲线是变压吸附动态的重要特性曲线,它反映了流动相和固定相之间的吸附平衡关系及吸附动力学行为,是研究吸附过程和吸附柱吸附性 能 的 主 要 依 据[20]。在20℃下,4g PP-g-GMA@AMP填入Φ10mm×200mm吸附柱内部,20mg/L Cs(I)溶液以0.5mL/min的流速流过柱子,饱和吸附后选用0.5mol/L NH4Cl溶液作为洗脱液淋洗色谱柱,流速为0.5mL/min,自动馏分收集器收集流出液,最后测量样品中各金属离子浓度,并绘制穿透曲线与解吸曲线,计算动态饱和吸附容量和洗脱总量。图9显示了柱吸附实验的结果,由图9可知,吸附剂对Cs(I)的5%穿透点位于180mL处,5%穿透时间约90min,100%穿透体积为250mL,100%穿透时间为125min。使用积分法计算得出动态饱和吸附容量为2.13mg/g,与静态最大理论吸附容量2.59mg/g接近。
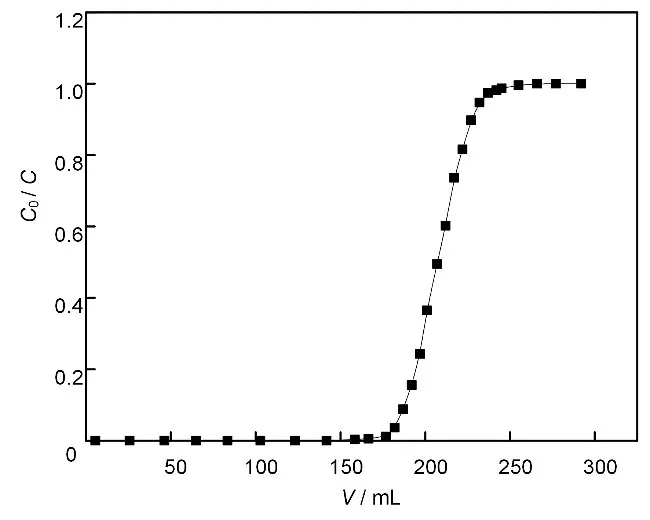
图9 PP-g-GMA@AMP对Cs(I)的穿透曲线Fig.9 Breakthrough curve for Cs(I)on PP-g-GMA@AMP
2.9 洗脱
PP-g-AMP@PP的洗脱曲线呈现出一个陡峭的峰形,流出液体积为20mL左右时达到最大洗脱浓度239.5mg/L,60mL时已淋洗出90%的Cs(I),流出液体积为100mL时,NH4Cl对PP-g-AMP@PP吸附柱的总洗脱量为2.05mg,总洗脱率约为96.2%,说明NH4Cl可以有效地将Cs(I)从PP-g-GMA@AMP上洗脱下来。通过对比图9和图10可以发现,完全穿透所需溶液体积为300mL,而Cs(I)被完全洗脱时,流出液体积仅需60mL。由此得出结论,低浓度的含Cs(I)模拟放射废液流经含PP-g-GMA@AMP的色谱柱时,在流出液中可实现Cs(I)富集,浓缩倍数约为5倍。
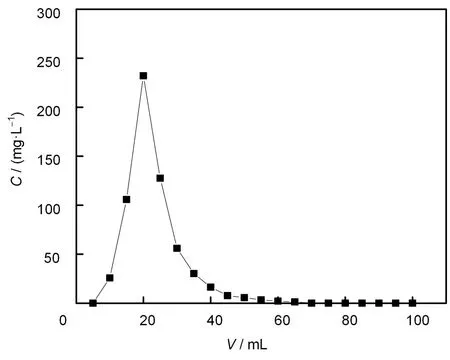
图10 PP-g-GMA@AMP对Cs(I)的洗脱曲线Fig.10 Elution curves for Cs(I)on PP-g-GMA@AMP
2.10 共存离子吸附洗脱实验
取4g PP-g-GMA@AMP填入同样规格吸附柱内,进料液为20mg/L的Cs(I)、Ca(II)、Na(I)和Mg(II)的混合溶液,进料吸附50min后立即通入0.5mol/L NH4Cl溶液进行洗脱,动态吸附和洗脱时被吸附溶液和洗脱剂的流速均为0.5mL/min,实验结束后测定每个流出液收集管中Cs(I)、Ca(II)、Na(I)和Mg(II)的浓度。图11及其放大部分(图12)展示了PP-g-GMA@AMP对Cs(I)、Ca(II)、Na(I)和Mg(II)动态吸附和洗脱行为,吸附柱几乎完全不吸附Ca(II)、Na(I)、Mg(II),动态吸附过程中PP-g-GMA@AMP仅选择性吸附Cs(I)。
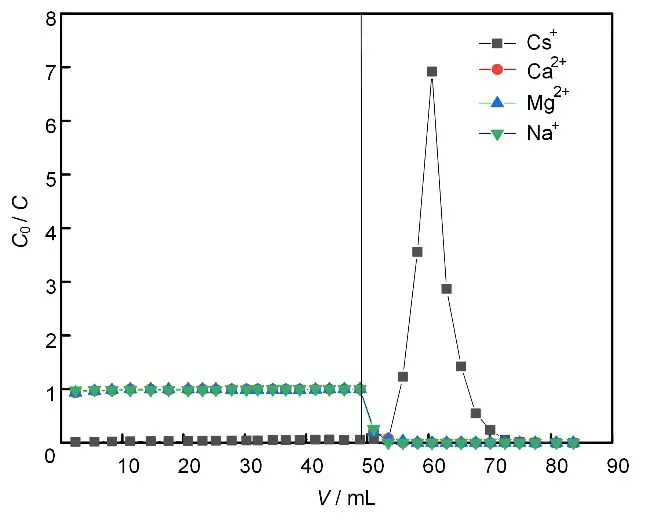
图11 Cs(I)、Na(I)、Mg(II)和Ca(II)在色谱柱上的吸附和洗脱过程Fig.11 Adsorption and elution of Cs(I),Na(I),Mg(II),and Ca(II)on the resin column
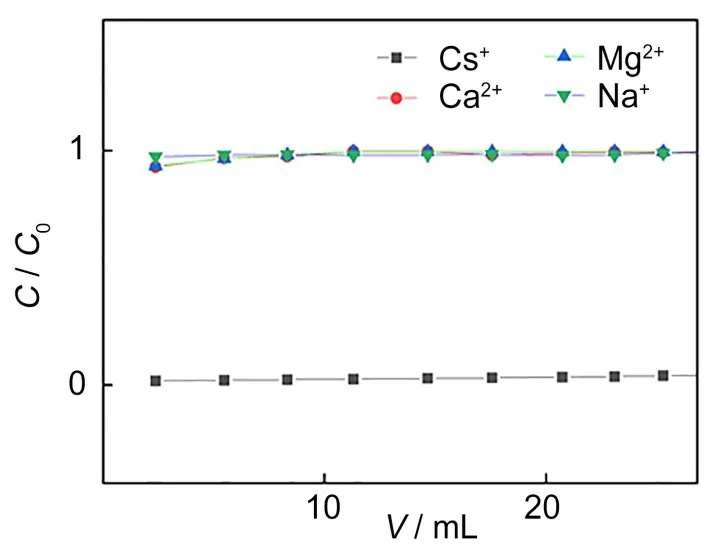
图12 Cs(I)、Na(I)、Mg(II)和Ca(II)在色谱柱上的吸附和洗脱过程(放大部分)Fig.12 Adsorption and elution of Cs(I),Na(I),Mg(II),and Ca(II)on the resin column(enlarged part)
根据注入液、流出液的体积及对应离子浓度,使用积分法计算得到吸附在PP-g-GMA@AMP树脂柱上Cs(I)的总吸附容量为0.532mg,流出液中Cs(I)的总量为0.521mg,回收率达97.93%。说明吸附在PP-g-GMA@AMP上的Cs(I)被NH4Cl洗脱液基本完全洗脱。
3 结论
采用电子束引发预辐射接枝法在PP无纺布基体上接枝GMA,制备接枝共聚物PP-g-GMA,同时在共聚物的纤维孔道中负载AMP,成功合成一种结构稳定、循环使用性良好、适合装柱的新型Cs(I)吸附剂PP-g-GMA@AMP,其中AMP负载率为5.72%,GMA接枝率为32.41%。研究表明:PP-g-GMA@AMP对Cs(I)的吸附受共存离子Na(I)、Ca(II)、Mg(II)的影响较小,对Cs(I)分配系数达120.45。PP-g-GMA@AMP对Cs(I)的吸附过程符合Langmuir吸附等温模型,对Cs(I)的理论最大吸附容量为2.59mg/g。重复使用实验表明PP-g-GMA@AMP在静态实验重复3次后,仍然保持90.09%的吸附容量。PP-g-GMA@AMP色谱柱实验表明,Cs(I)在色谱柱内穿透时间为90min,计算得到动态饱和吸附容量2.13mg/g。NH4Cl溶液具备浓缩Cs(I)的效果,洗脱过程中0.5mol/L NH4Cl溶液为淋洗液,进料液与流出液体积比为5∶1。动态色谱分离实验表明0.5mol/L NH4Cl溶液作为淋洗液可实现Cs(I)与Na(I),Ca(II),Mg(II)的完全分离,而且Cs(I)回收率为97.93%。此外,在动态吸附柱对吸附剂进行重复实验时发现,吸附剂可依据以上结论,PP-g-GMA@AMP有望通过色谱柱的方法应用于受污染的海水中放射性137Cs的选择性去除及浓缩。
