木聚糖酶对全麦发酵面团水相溶液流变及泡沫特性的影响
2021-11-14佟立涛王丽丽王凤忠刘丽娅
岳 颖,佟立涛,王丽丽,王凤忠,刘丽娅
(中国农业科学院农产品加工研究所,农业部农产品加工重点实验室,北京 100193)
近年来,全麦食品由于其营养与健康益处受到越来越多消费者的喜爱。长期摄入全麦主食有助于减少心脑血管疾病、糖尿病、肥胖等多种慢性疾病的发生[1-2]。然而,全麦发酵面制品加工品质和食用品质不佳,限制了全麦主食在国内的推广和应用。为改善全麦发酵面制品的品质,常采用多种方法对其品质进行改良,如添加外源物质[3-4]、改变加工方式等[5-6]。
均匀且细腻的气室结构是衡量发酵面制品品质的重要指标[7]。过去研究普遍认为面团气室结构稳定性主要与面筋蛋白网络结构的强度有关,通过改善面筋蛋白网络结构可以提高面团气室稳定性,改善面制品品质[8]。但有研究发现,在面团内部面筋蛋白-淀粉基质和面团气体分散相之间还存在一层薄层液膜结构[9],当面筋蛋白在发酵后期和早期烘烤阶段出现断裂时,这层液膜结构可以防止面团中的气泡破裂。该液膜结构源自于面团的水相,其中包含一些可溶蛋白[10]、脂类和非淀粉多糖[11],这些物质对面团水相溶液的性质产生影响,进而调控面团气室稳定性。目前,通过研究超高速离心分离制得面团水相溶液的性质,可以间接获得关于薄层液膜的相关信息[12]。
阿拉伯木聚糖(arabinoxylan,AX)是全麦粉中主要的膳食纤维,根据其溶解性可以分为水溶性阿拉伯木聚糖(water-extractable arabinoxylan,WEAX)和水不溶性阿拉伯木聚糖(water-unextractable arabinoxylan,WUAX)[13]。普遍认为,WUAX是导致全麦发酵面制品品质劣化的主要原因,而WEAX可以增加全麦发酵面制品体积,改善面团内部质地结构[14]。木聚糖酶(xylanase,XYL)对面制品品质的改良作用早在上世纪九十年代就已得到公认,但作用机理至今仍不完全清楚。目前的共识是木聚糖酶消除了WUAX的不良影响,增加了WEAX的含量,使面筋网络结构形成更加充分[15]。
本团队前期研究发现,一定剂量的XYL可显著改善全麦馒头气室结构稳定性[15],且证实XYL改善了脱脂面团水相溶液的泡沫稳定性[16]。事实上,全麦中较高的脂质含量可能对水相溶液性质产生重要影响,进而改变薄层液膜的性质和面团气室稳定性,然而这一推论尚未得到证实。基于此,本文研究脂质存在情况下,经XYL改性的全麦发酵面团水相溶液组成、流变特性和泡沫稳定性变化,为从薄层液膜层面揭示XYL改良全麦发酵面制品品质提供理论依据。
1 材料和方法
1.1 材料与仪器
小麦(津强5号) 北京古船食品有限公司提供;低糖高活性干酵母 安琪酵母股份有限公司提供;木聚糖酶(Pentopan Mono BG,酶活力2500 FXU/g) 诺维信中国投资有限公司提供;盐酸等其他试剂 均为国产分析纯。
L100-XP超速冷冻离心机 美国贝克曼库尔特公司;LRMM-8040-3-D型布勒实验磨粉机 布勒粮食检验仪器无锡有限公司;SCIENTZ-10N冷冻干燥机 宁波新芝生物科技股份有限公司;LXJ-11B低速离心机 上海安亭科学仪器厂;UV-9000紫外可见分光光度计 上海元析仪器有限公司;DAWN-EOS十八角度激光光散射仪 Wyatt技术公司;Physica MCR301流变仪 奥地利安东帕有限公司;KJE LTEC2300自动凯氏定氮仪 瑞典FOSS仪器有限公司;WT-12水浴氮吹仪 杭州米欧仪器有限公司;JHMZ 200针式和面机 北京东孚久恒仪器技术有限公司;KENWOOD和面机 邑隆贸易(上海)有限公司;CF-6000家用发酵箱 中山卡式电器有限公司;FW80高速万能粉碎机 天津市泰斯特仪器有限公司;XHF-DY高速分散器 宁波新芝生物科技股份有限公司;TXTD4002标准检验筛(40目) 浙江上虞市肖金标准筛具厂。
1.2 实验方法
1.2.1 全麦粉及全麦发酵面团制备 参考杨炜[17]的方法,小麦清理除杂、洗净烘干后测定水分含量,并根据实际水分含量调节小麦水分至15.5%。在室温下润麦24 h后用布勒磨研磨得到粗麸、细麸和面粉,出粉率控制在65%±2%。将收集的麸皮于130 ℃烘箱中灭酶2 h后粉碎过40目筛,按照实际出粉率将麸皮、面粉混匀制得全麦粉并置于4 ℃环境中保存。
根据前期的研究结果[15-16],选择对全麦面团具有明显改良作用的两个XYL剂量,即添加量分别为60和120 μg/g全麦粉,制作全麦发酵面团,并设未加酶样品作空白对照。
称取250 g全麦粉,2.5 g低糖高活性干酵母,175 mL去离子水和一定量的XYL,将其置于针式搅拌机中搅拌30 s形成絮状面团,再用和面机“1”档和面3 min。将制得的面团置于发酵箱中发酵40 min,发酵温度34 ℃,相对湿度85%。
1.2.2 水相溶液分离及得率测定 面团发酵完成后立即取一定量(约10 g)装入离心管中,于30 ℃、210000 ×g离心1 h。由于发酵产生的气体会破坏脂质层使其包含在下层的液相中,离心后将离心管中最上层的液相收集作为包含脂质的面团水相溶液。在冷冻干燥前后称重,用于测定水相溶液干基和湿基得率[18]:

新鲜制备的水相溶液用于流变学和泡沫特性测定。冷冻干燥后的水相溶液用于组分分析。空白及经60、120 μg/g XYL改性的水相溶液分别命名为Control、XYL 60、XYL 120。
1.2.3 水相溶液组成分析 根据NY/T 2335-2013和国标法GB 5009.5-2016测定冻干全麦发酵面团水相溶液中的WEAX和蛋白含量。脂质含量的测定参考Dyer等[19]的方法。称取250 mg冻干样品于10 mL离心管中,向其中依次加入氯仿(2.0 mL)、甲醇(2.0 mL)和水(1.8 mL),采用涡旋仪混合30 s;混合溶液于500 ×g下离心20 min,离心后液体分成三层,收集最下层包含脂质的氯仿相,并将中间层用氯仿、甲醇和水萃取两次,收集最下层包含剩余脂质的氯仿相与第一次收集的氯仿相合并。将三次收集得到的样品,于40~50 ℃下氮气吹干,称重计算脂质含量,天平精度为0.01 mg。
1.2.4 水相溶液多糖重均分子量测定 采用凝胶渗透色谱-十八角度激光光散射联用技术(HPSECMALLS)测定水相溶液多糖重均分子量。以0.1 mol/L的NaCl溶液溶解水相溶液冻干样品,配制成1 mg/mL的溶液并采用0.45 μm滤膜过滤后备用。测试条件:凝胶渗透色谱柱型号为OHpak SB-806M HQ L911061;流动相为0.1 mol/L的NaCl溶液,进样量200 μL,流动相流速0.5 mL/min,测试温度25 ℃。
1.2.5 水相溶液粘度测定 参考文献方法[20],利用流变仪测定水相溶液(未稀释)表观粘度变化情况(锥板探头,直径2.5 cm,Gap值为1 mm)。测试温度分别为25和60 ℃,剪切速率1~100 s-1,塑料盖密封以减少水分流失。采用仪器自带的软件采集数据,并根据幂律模型(Pawer-law模型)对实验结果进行拟合[21],公式如下:

式中:ι代表剪切应力,Pa;K为稠度系数,Pa.s,可衡量溶液的粘稠程度;γ为剪切速率,s-1;n代表流体类型指数(无量纲),其可以描述流体与牛顿模型的差异。对于牛顿流体,n=1;对于非牛顿流体,n<1。
1.2.6 水相溶液粘弹性测定 参考吴伟都等[22]的方法,利用流变仪测定水相溶液粘弹性(锥板探头,直径2.5 cm,Gap值为1 mm)。采用应变扫描模式确定水相溶液样品的线性粘弹区,确定测试条件为:应变0.04%,频率1 Hz。记录样品在25~90 ℃升温过程中,储能模量(G′)、损耗模量(G″)、损耗因子(tan δ=G″/G′)变化情况,升温速率1 ℃/min。
1.2.7 水相溶液泡沫稳定性分析 参考王立峰等[23]的方法。新鲜的水相溶液稀释10倍后移取8 mL于量筒中,用高速分散器(10000 r/min)剪切1 min,读取体积V1,在25和60 ℃下放置30 min后读取体积V2,根据公式计算水相溶液泡沫稳定性:

1.3 数据处理
所有处理均设三次重复,所得结果用平均值±标准差表示。使用SPSS23.0和Origin8.0分别进行统计学分析和绘图,采用F检验进行单因素方差分析,根据单因素方差分析结果进行Ducan’s多重比较分析差异显著性,P<0.05则认为差异显著。
2 结果与分析
2.1 水相溶液物质组成分析
水相溶液基本组分的测定结果如表1所示。数据表明,XYL处理可显著提高水相溶液得率(P<0.05),这可能归功于水相溶液中WEAX和水的回收率增加。当XYL添加量为60 μg/g时,水相溶液中的WEAX含量较对照增加35.70%,而当XYL添加量提高到120 μg/g时,WEAX含量虽仍有提高,但增加幅度减缓。以往研究表明,在全麦体系中,XYL促进WUAX溶解的同时也可使已释放出的WEAX进一步降解[24];且当XYL用量增加到一定水平后,XYL对WEAX的降解作用占主导,对WUAX的增溶程度减缓[17,25]。因此,可以推测,当XYL添加量为60 μg/g时,XYL的作用主要是促进WUAX的溶解,导致水相溶液WEAX增加幅度较大;当XYL添加量为120 μg/g时,WEAX增加速率降低,而水相溶液中WEAX可能被不断降解。

表1 XYL对全麦发酵面团水相溶液得率及组成的影响Table 1 Yield and basic composition of whole wheat fermented dough liquor as affected by XYL
随着XYL添加量的增加,水相溶液中的水回收率增加,可能是因为XYL降低了WUAX的持水量,使面筋-淀粉网络的持水能力下降,水相溶液中回收更多的水。随着XYL添加量的增加,水相溶液中蛋白含量降低,这与Primo-Martín等[26]的结果一致;脂质含量下降,这可能与XYL作用下脂类物质与面筋-淀粉基质中的蛋白相互作用增强有关[18],但相关机制有待进一步研究。
2.2 XYL对水相溶液中多糖分子量及其分布的影响
采用HPSEC-MALLS测定水相溶液中多糖的重均分子量及其分布,结果见图1和表2。可见,XYL对水相溶液中多糖的重均分子量(Mw)产生一定的影响,随着XYL用量的增加,Mw不断下降(表2)。同时,XYL添加量的增加导致水相溶液中分子量较大的多糖相对含量有所降低,且当XYL添加量为120 μg/g时,大分子量多糖含量降低更为明显(图1)。

图1 XYL对全麦发酵面团水相溶液多糖分子量的影响Fig.1 Effect of XYL on the molecular weight distribution of polysaccharides in whole wheat fermented dough liquor

表2 XYL对全麦发酵面团水相溶液多糖重均分子量及分布的影响Table 2 Effect of XYL on the molecular weight distributions of polysaccharides in whole wheat fermented dough liquor
多分散系数反映了多糖分子质量的分散程度。由表2可知,水相溶液中多糖分散系数处于1.142~1.218范围内,多糖分子质量分布较为均一[27]。XYL 60中多糖多分散系数略微减小,但120 μg/g XYL处理提高了水相溶液中多糖的多分散系数。结合WEAX含量的测定结果,可能是因为XYL添加量为60 μg/g时,XYL对AX主要是促溶作用,水相溶液中WEAX比例增加,多糖分子质量分布更加均一。而当XYL添加量为120 μg/g时,XYL以对WEAX的降解作用为主导,水相溶液中低分子量多糖比例增加,多糖分子质量分布更加分散。
2.3 XYL对水相溶液粘度的影响
由于面制品在熟化过程中经历升温过程,因此本研究对水相溶液在不同温度下的性质进行分析。根据前期研究结果[16],分别研究25和60 ℃下XYL对水相溶液粘度的影响,结果见图2。不同水相溶液样品的粘度随着剪切速率的增加均不断降低,表现出剪切稀化效应。这主要受AX等多糖性质的影响[28],同时可能与脂质存在时,水相溶液所形成的乳浊体系在剪切过程中的结构变化有关[29]。值得注意的是,不同温度下XYL对粘度的作用效果与温度密切相关。在25 ℃时,XYL引起水相溶液粘度降低与其对WEAX的降解有关。但是在加热条件下,经XYL处理的水相溶液粘度增加。推测是因为在加热条件下,蛋白和WEAX结合形成凝胶,将水分保留在凝胶网络中[30],XYL处理后水相溶液中较高含量的WEAX限制了其在水相溶液中的移动,并通过与蛋白交联提高了蛋白-WEAX凝胶的表观粘度[31]。
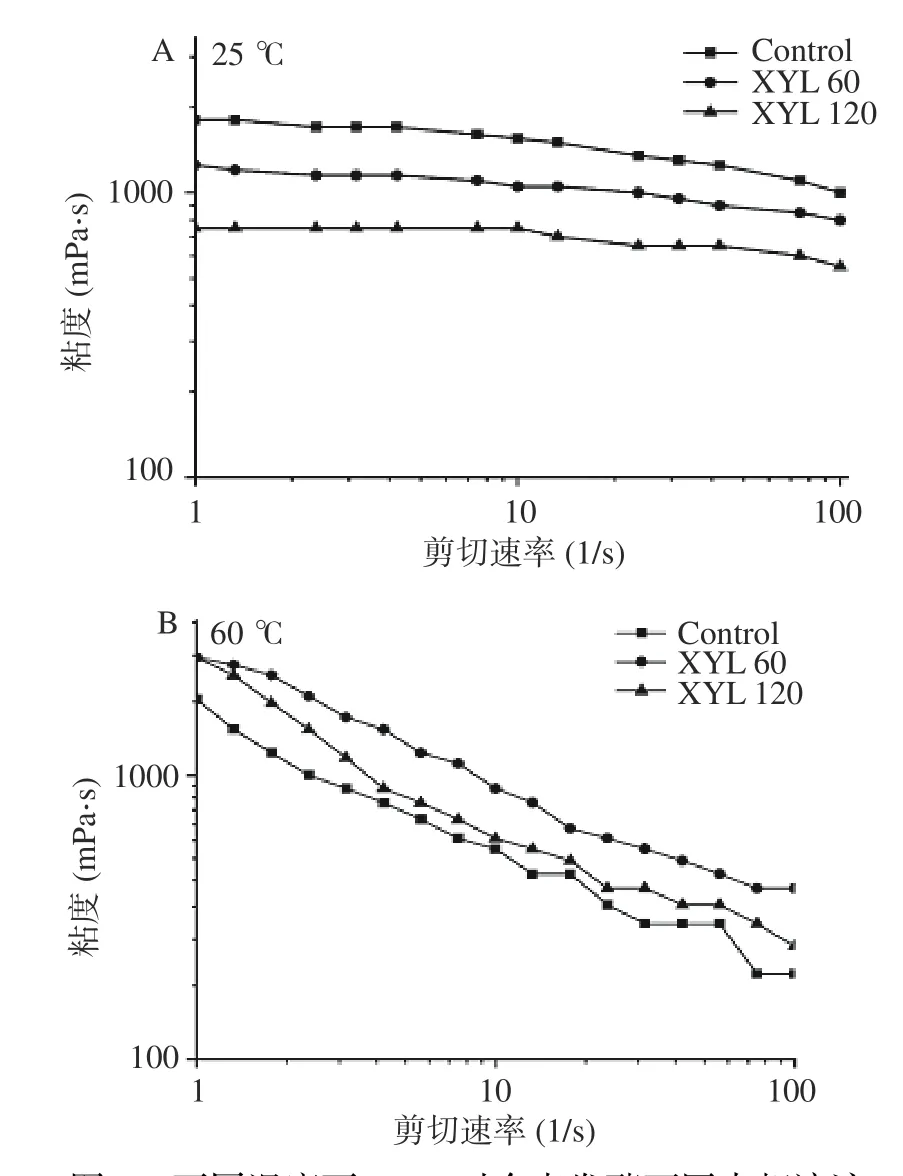
图2 不同温度下XYL对全麦发酵面团水相溶液粘度的影响Fig.2 Effects of XYL on the viscosity of whole wheat fermented dough liquor under different temperatures
采用幂律模型拟合水相溶液的流变数据,结果见表3。所有的幂律模型R2值大于0.99,表明拟合良好。在25 ℃时,经XYL处理的水相溶液稠度系数显著降低,这与图2中的变化趋势相一致。与未包含脂质层的水相溶液相比[16],本研究中未脱除脂质层的水相溶液K值提高7~11倍,推测与水相溶液中较高脂肪含量有关[32]。在25 ℃下,水相溶液n值接近1,接近牛顿流体[33],这与Turbin-Orger等[34]的研究结果一致。在60 ℃下,不同样品的n值降低到0.5左右,表现出较强剪切稀化效应,体现出非牛顿流体的性质。

表3 不同温度下XYL对全麦发酵面团水相溶液K值和n值的影响Table 3 K and n values of whole wheat fermented dough liquor as affected by XYL under different temperatures
2.4 XYL对水相溶液粘弹性的影响
在测定水相溶液粘度随剪切速率的变化时发现,对于60 ℃加热的样品,在实验结束时可形成弱凝胶。因此,进一步考察温度对水相溶液粘弹特性的影响,结果见图3。弹性模量(G′)和粘性模量(G′′)出现交叉的点被认为是凝胶形成的临界点[35]。由图3A可知,水相溶液在60~62 ℃形成凝胶。在低于凝胶温度时,G′始终大于G′,水相溶液表现为粘弹性液体的特征体[36]。当温度高于水相溶液的胶凝温度时,G′大于G′′,水相溶液表现出粘弹性固体的特征。XYL对体系粘弹性的影响在临界凝胶温度以下较为明显。在成胶温度以下,XYL 60的粘弹性高于其他两组样品。
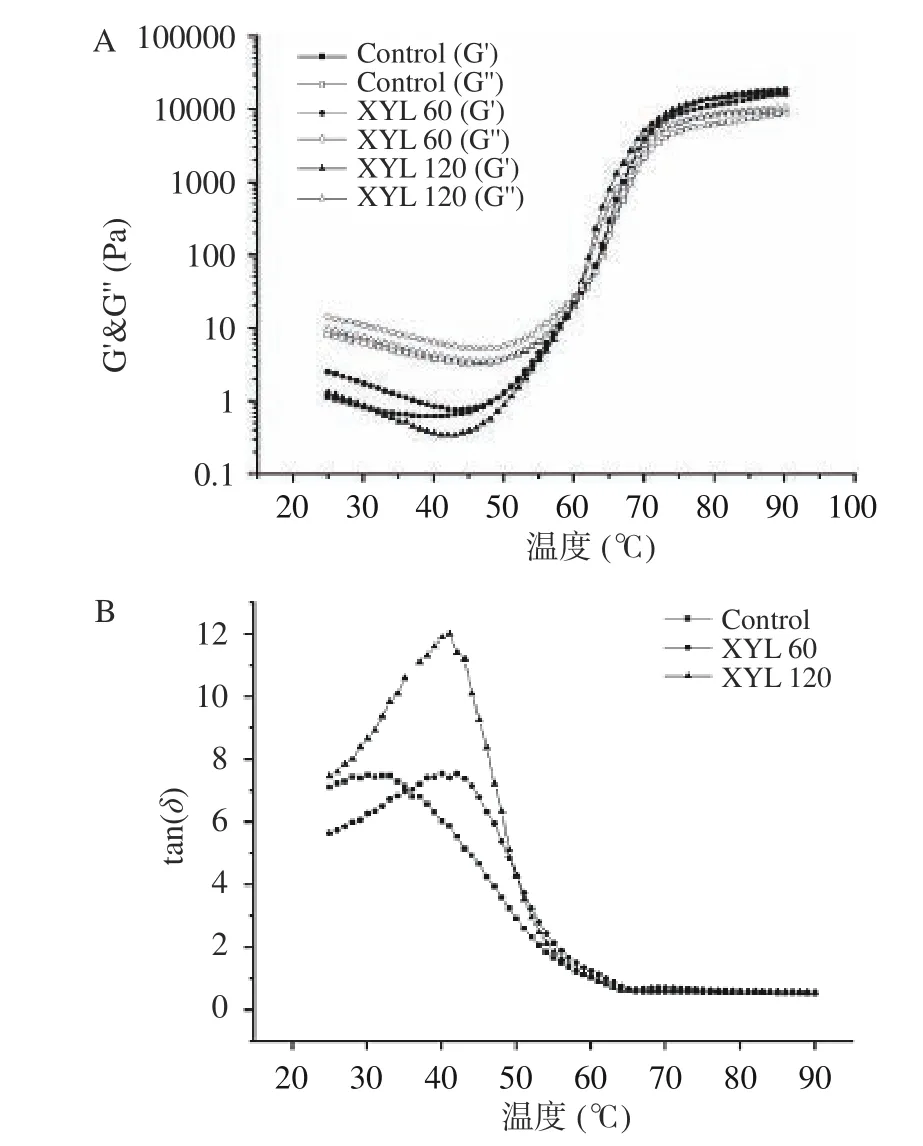
图3 升温过程中XYL处理的全麦发酵面团水相溶液粘弹特性的变化Fig.3 Changes of viscoelastic properties of whole wheat fermented dough liquor treated by XYL during heating process
相角(δ)的变化可以反映样品固态和液态之间的转化,tanδ值的急剧降低标志着样品从溶液态开始向凝胶态转变[37]。由图3B可知,XYL改性水相溶液的tanδ值开始降低时对应的温度较对照组高,这表明XYL提高了水相溶液向凝胶态转变的初始温度,这可能有利于气泡充分膨胀,延缓其发生固化的时间。
2.5 XYL对水相溶液泡沫特性的影响
面团中气泡的稳定性决定了面团混合和发酵过程中产生的气泡随时间聚结的程度,气泡稳定性差会导致面包质地粗糙并减小面包的体积[38]。通过对XYL作用下水相溶液泡沫稳定性进行研究,可在一定程度上间接了解真实面团体系气泡稳定性变化。
图4 为25和60 ℃下,经XYL处理的水相溶液泡沫稳定性的变化情况。结果表明,在25和60 ℃下,XYL处理可显著提高水相溶液的泡沫稳定性(P<0.05)。之前研究表明,在体系脂质含量较低的情况下,AX可以通过与界面处蛋白的相互作用改善水相溶液的泡沫稳定性[39]。本研究进一步证实,在脂质含量较高的水相溶液体系中,虽然部分极性脂质如磷脂可能与蛋白竞争吸附影响水相溶液气-液界面特性[40],XYL仍可显著改善泡沫稳定性。常温条件下,虽然XYL引起水相溶液粘度的降低,但由于其对WUAX的增溶和降解作用,改善了AX与空气-水界面上吸附组分的相互作用,增强了界面膜的强度[41]。而在加热条件下,XYL对泡沫稳定性的改善作用可能与其引起的水相溶液粘度的升高[18]以及泡沫固化时间的延长相关。
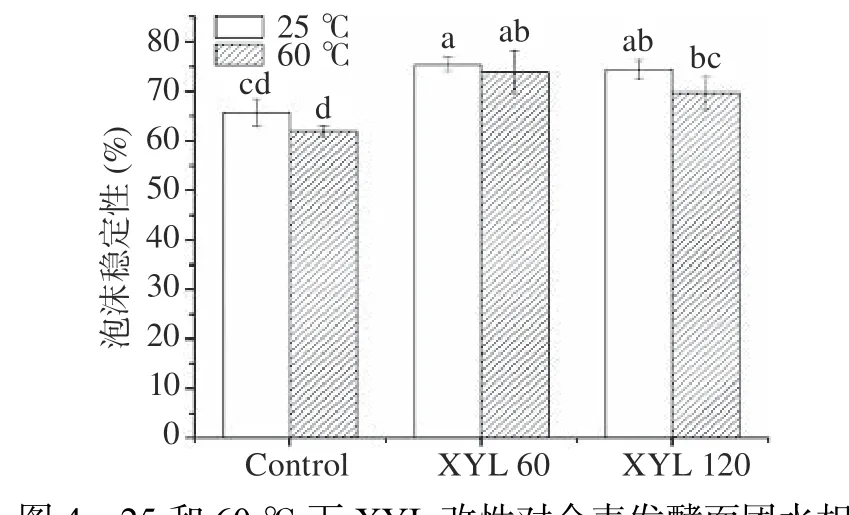
图4 25和60 ℃下XYL改性对全麦发酵面团水相泡沫稳定性的影响Fig.4 Effects of XYL on the foam stability of whole wheat fermented dough liquor at 25 and 60 ℃
3 结论
本文对经XYL改性后未去除脂质层的全麦发酵面团水相溶液主要物质组成、流变及泡沫特性进行了研究。结果表明,XYL处理可显著提高水相溶液得率(P<0.05),这与其促进WEAX的溶出以及降低面筋网络的持水性相关。在60和120 μg/g XYL的作用下,水相溶液中WEAX含量分别提高35.70%和52.15%。多糖分子量随XYL用量的增加表现出下降的趋势,且120 μg/g XYL对AX的降解作用更为明显;XYL处理降低了水相溶液中的蛋白和脂质含量。水相溶液在60~62 ℃形成凝胶,低于成胶温度时XYL 60可提高水相溶液的粘弹性,且XYL处理提高了水相溶液向凝胶态开始转变的温度。在常温(25 ℃)及加热(60 ℃)条件下,XYL引起的水相溶液组成及流变特性的变化显著提高了水相溶液的泡沫稳定性,对面团气室稳定性可能产生有利的影响。
