鳄鱼油微乳制备及性质分析
2021-11-13王海燕
王海燕
(莆田学院 工程实训中心,福建 莆田 351100)
0 引言
鳄鱼是迄今生存着的最原始的动物之一,其全身都是宝,已被开发并广泛应用于食品、医药、化工等领域。研究发现,鳄鱼油中所含的脂肪酸多达24种,不饱和脂肪酸高达71.5%,主要由亚油酸和花生四烯酸组成[1],且其理化特性与人体脂肪相近,具有良好的渗透性,极易为人体接纳与吸收[2]。鳄鱼油已被证实具有防冻防寒、抗菌抗炎、促进皮肤烧伤愈合、抑制疤痕形成等功效[3-4],因此其在化妆品领域具有巨大潜力。目前关于鳄鱼油的研究,大多集中在鳄鱼油提取和精制方面[5-6],而关于鳄鱼油产品方面,国内外已开发出鳄鱼油冻疮膏、鳄鱼油烫伤膏等系列产品,但若能对鳄鱼油进一步开发利用,将其广泛应用于护肤品中,则具有广阔前景。
鳄鱼油富含多不饱和脂肪酸,在生产和储运过程中很多成分容易损失和氧化,影响其深加工和高值化利用。微包埋技术是解决这些问题的有效手段之一,微包埋技术主要包括微胶囊技术[7]和微乳化技术[8]。微胶囊技术是将鳄鱼油固体化进而保护与控释,但固体化形式会制约其在化妆品中的应用。微乳是由水、油、表面活性剂及助表面活性剂依照一定配比自发形成的各向同性且热力学稳定的透明或半透明的溶液体系,粒径在1~100 nm之间[9]。微乳可以在不改变结构的前提下改善鳄鱼油的水溶性,在离心及长时间静置后保持稳定,一系列表面活性剂使其内部结构稳定,且对其他的液体或包嵌分子具备较强的增溶功能[10-11],因而其具有更高的实际应用价值。目前尚未见到关于鳄鱼油微乳包埋的相关研究,本文以鳄鱼油为原料,研究鳄鱼油微乳的制备工艺,以利鳄鱼油的进一步应用与开发。
1 材料与方法
1.1 试验材料
聚氧乙烯山梨糖醇酐单硬脂酸酯(Tween-60,上海麦克林生化科技有限公司);丙三醇(天津市化学试剂供销公司);山梨醇酐油酸酯(Span-80)、异丁醇、苏丹红Ⅲ(上海阿拉丁生化科技股份有限公司);乙二醇、山梨醇酐月桂酸酯(Span-20)、聚氧乙烯山梨糖醇酐单月桂酸酯(Tween-20)、无水乙醇、亚甲基蓝(国药集团化学试剂有限公司);以上试剂均为分析纯。精制鳄鱼油(福建鼍龙集团)。
1.2 试验仪器
FA-25D匀浆机(上海弗鲁克科技发展有限公司);H1850高速离心机(湘仪离心机仪器有限公司);Vortex3旋涡混合仪(广州仪科实验室技术有限公司);HJ-3恒温磁力搅拌器(深圳天南海北实业有限公司);3100C电导率仪(奥豪斯仪器(上海)有限公司)。
1.3 试验方法
1.3.1 鳄鱼油微乳的配方设计
(1)单一表面活性剂的筛选
分别添加0.5 mL Span-20、0.5 mL Tween-20、0.5 mL Span-80、0.5 mL Tween-60到4支试管中。再向试管内分别添加3 mL鳄鱼油,用旋涡混合仪旋涡振摇30 s,使之充分混匀。随后分别加入6.5 mL去离子水,旋涡振摇5 min,使之充分混匀。观察并记录放置一定时长后试管内溶液的分层体积。
(2)复合表面活性剂的筛选
取5支试管,先在5支试管中各添加3 mL鳄鱼油,再分别添加不同亲水亲油平衡值(hydrophilic lipophilic balance,HLB值)的复合表面活性剂0.5 mL,旋涡振摇30 s,使其混合充分。随后各加入6.5 mL去离子水,旋涡振摇5 min,使其完全混合。观察并记录放置一定时长后试管内溶液的分层体积。
(3)拟三相图的绘制
将复合表面活性剂与助表面活性剂按质量比3∶1混匀形成混合表面活性剂,再将混合表面活性剂与鳄鱼油分别按照1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1的质量比进行混合[12],充分搅拌均匀后,边搅拌边缓慢滴加去离子水。观察搅拌过程中乳液从澄清到浑浊再到澄清的现象,记录下临界点水的滴加量,分别计算达到临界状态时各相的质量百分比,以水、鳄鱼油和混合表面活性剂为三个顶点,分别标出各临界点在相图中的点并连成线,即为拟三相图[12]。
(4)助表面活性剂的筛选
将优选的复合表面活性剂分别和助表面活性剂以质量比3∶1的比例混合均匀,置于离心机中以4000r/min的转速离心10 min,观察并记录离心后每支试管中的溶液是否发生分层。绘制拟三相图,比较各微乳区域面积的大小。
1.3.2 样品1的制备
以Span-80和Tween-60为复合表面活性剂,无水乙醇为助表面活性剂,混合表面活性剂与鳄鱼油质量比(S/O)值为9∶1,含水量为80%(以微乳总质量计),制得O/W型鳄鱼油微乳,记为样品1。
1.3.3 鳄鱼油微乳理化性质分析方法
通过观察丁达尔现象初步确定是否形成微乳。通过观察亚甲基蓝和苏丹红Ⅲ在样品1中的扩散速度,判断鳄鱼油微乳是水包油(O/W)型还是油包水(W/O)型。采用电导率仪测定样品1的电导率,观察并记录鳄鱼油微乳电导率随含水量(质量分数)的变化趋势。
1.3.4 鳄鱼油微乳稳定性检测
(1)离心试验
将样品1加入离心管内,放置在离心机中以4000 r/min的转速离心20 min,观察并记录离心之后鳄鱼油微乳外观变化及有无分层、破乳现象发生。
(2)温度试验
取样品1分别在4℃、25℃、40℃放置15 d,观察其外观形态变化,有无分层或浑浊现象发生。
1.4 试验数据处理
表面活性剂复配得到不同HLB值的复合表面活性剂,根据不同的HLB值确定其各自的质量分数,按下式计算:

式中:HLBST,复合表面活性剂的HLB值;HLBS,Span-80的HLB值,HLBS=4.3;HLBT,Tween-60的HLB值,HLBT=14.9;WS,Span-80的质量分数,%;WT,Tween-60的质量分数,%;WST,复合表面活性剂的质量分数,%。
2 结果与分析
2.1 鳄鱼油微乳体系的配方设计
2.1.1 表面活性剂的筛选
单一表面活性剂的筛选结果如表1所示。由表1可得,表面活性剂为Span-20及Tween-20时,乳状液稳定性差,很快就出现分层现象,而表面活性剂为Span-80及Tween-60时,乳状液不易发生分层,则可判断以Span-80及Tween-60为表面活性剂的乳状液更加稳定。
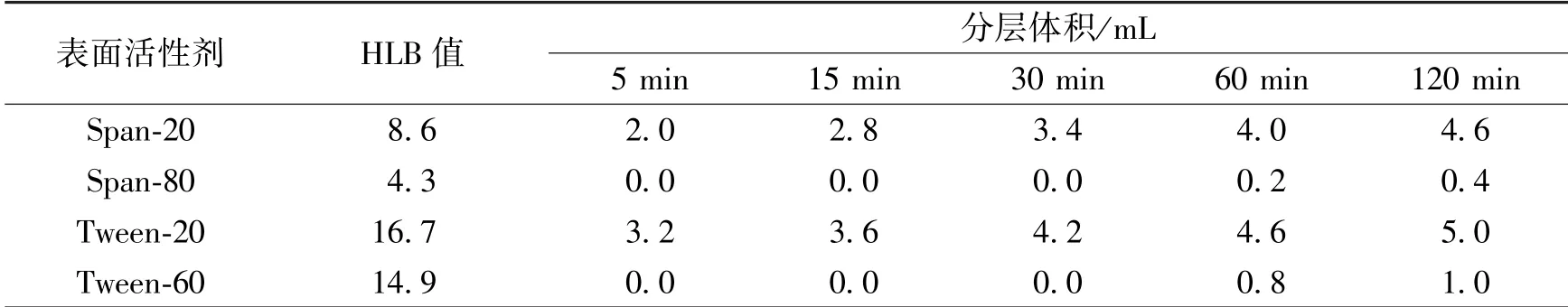
表1 单一表面活性剂筛选结果
复配后的表面活性剂具备协同增溶效果,为了提高乳化效率,将两种不同的表面活性剂复配[13-14]。筛选出乳化效果较好的表面活性剂进行复配,形成复合表面活性剂。本试验以Span-80及Tween-60复配得到不同HLB值的复合表面活性剂,根据HLB值计算公式确定Span-80、Tween-60用量。复合表面活性剂筛选结果如表2所示。由表2可得,当复合表面活性剂HLB值为8时,乳液不易分层,有着良好稳定性,此时复合表面活性剂Span-80和Tween-60的质量分数比为13∶7。
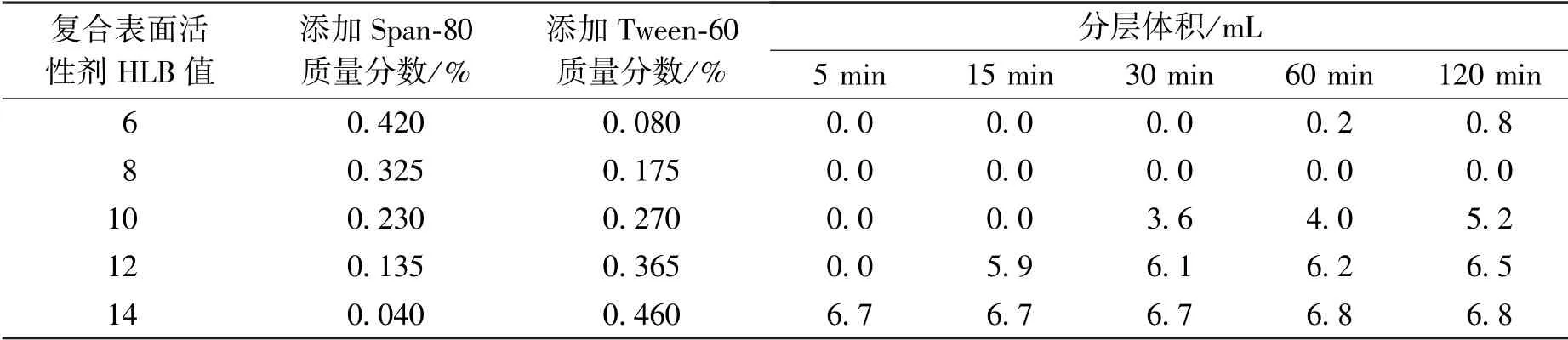
表2 复合表面活性剂筛选结果
2.1.2 助表面活性剂的筛选
通过添加助表面活性剂,调整水或油的极性,改变表面活性剂的表面活性及HLB值,促进微乳的形成。将表面活性剂及助表面活性剂混合,以提高微乳的乳化效率[15]。助表面活性剂从4种常见的短链醇,即无水乙醇、丙三醇、乙二醇和异丁醇中筛选。助表面活性剂筛选结果见图1,可知丙三醇和乙二醇作为助表面活性剂的混合液稳定性差,发生分层,而无水乙醇和异丁醇作为助表面活性剂的混合液稳定性较好,不易分层。

图1 不同助表面活性剂的表现
图2 、图3、图4、图5为采用不同种类助表面活性剂制备鳄鱼油微乳拟三相图,则4种不同助表面活性剂形成的微乳区域面积(阴影部分,下同)从大到小排序如下:无水乙醇>异丁醇>丙三醇>乙二醇。助表面活性剂在微乳形成过程中,能和表面活性剂形成混合界面膜,降低表面活性剂分子间的电荷斥力及互斥力,改善界面膜的流动性和柔顺性,降低形成微乳所需的界面弯曲能,促进微乳的形成[16]。4种助表面活性剂中,无水乙醇的分子量最小,更容易插入表面活性剂的单分子膜,有利于微乳的形成,微乳区域面积相对较大,而异丁醇、丙三醇、乙二醇由于黏度相对较大,易形成液晶或凝胶[17],微乳区域面积相对较小,故本试验选用无水乙醇为助表面活性剂来制备鳄鱼油微乳。
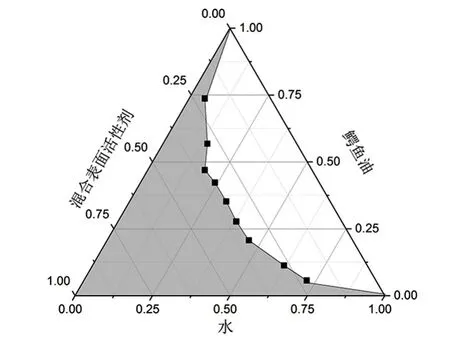
图2 以无水乙醇为助表面活性剂鳄鱼油微乳拟三相图
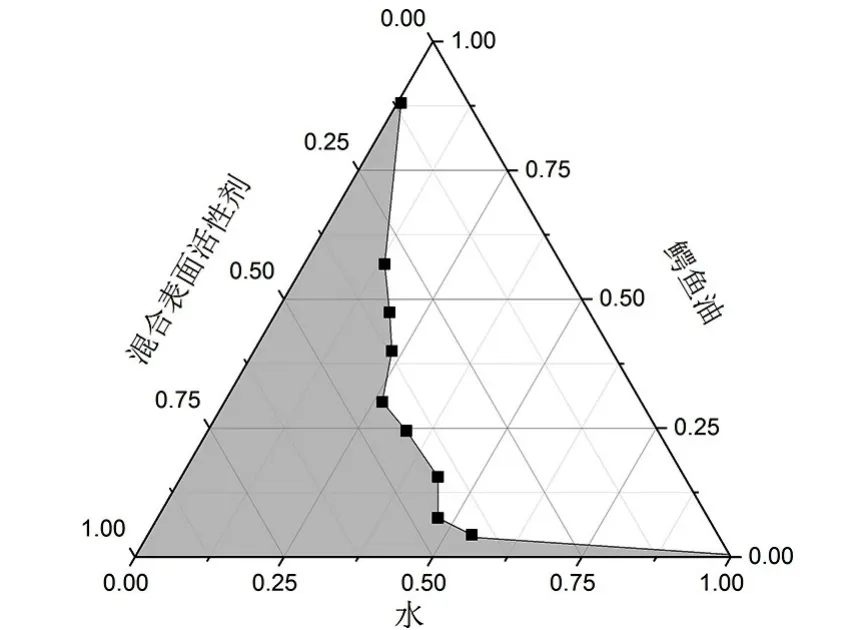
图3 以丙三醇为助表面活性剂鳄鱼油微乳拟三相图
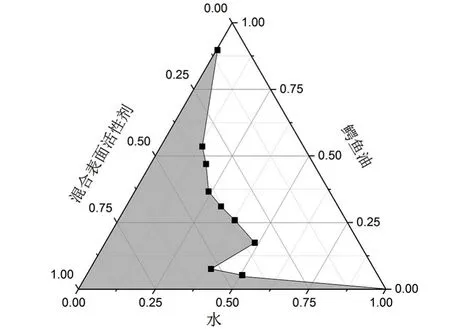
图4 以乙二醇为助表面活性剂鳄鱼油微乳拟三相图
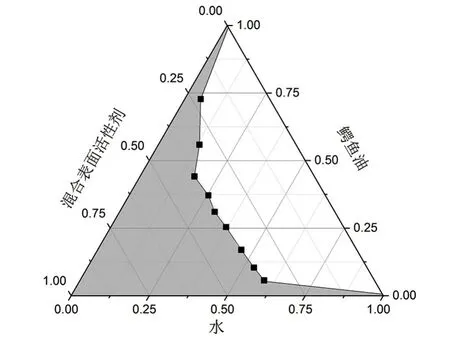
图5 以异丁醇为助表面活性剂鳄鱼油微乳拟三相图
2.1.3 鳄鱼油微乳的制备
微乳的制备方法有Schulman法和Shah法。Schulman法是由水相、油相和表面活性剂三者混匀形成乳状液,再缓慢地将助表面活性剂滴入其中,体系会在某一刻突然变成透明状态从而形成微乳[18];Shah法是先把助表面活性剂、表面活性剂和油相混合均匀形成乳状液,再缓慢地向该乳状液中滴加水,体系会在某一瞬间转为透明状态而形成微乳[19]。采用不同方法制备微乳形成的拟三相图见图6、图7,由图可见,相较Schulman法,Shah法微乳区域面积更大,且在实验过程中,Shah法在相变过程产生的凝胶、液晶和胶团化等状态及现象更加清晰明了、易于观察。

图6 Schulman法鳄鱼油微乳拟三相图

图7 Shah法鳄鱼油微乳拟三相图
2.2 鳄鱼油微乳理化性质分析
样品1外观良好,未出现分层,有丁达尔现象。选用染色法鉴定鳄鱼油微乳构型,亚甲基蓝在鳄鱼油微乳中迅速扩散,而苏丹红Ⅲ在鳄鱼油微乳中基本不扩散,表明制得的样品1为O/W型微乳。
微乳分为油包水(W/O)、水包油(O/W)和双连续(B.C.)三种结构,电导率在一定程度上能反映微乳的相行为及结构特征,常用于鉴别微乳构型[20]。微乳液电导率随着含水量的增加,通常呈现先上升后下降趋势。这是由于当微乳处于W/O状态时,随着水分子的增多,导电粒子碰撞增多,电导率逐渐升高;当微乳处于双连续状态时,微乳中既有W/O微粒,也有O/W微粒,电导率升高速度变慢,直至达到最大值;当微乳处于O/W状态时,随着含水量增加,微乳不断被稀释,电导率有所下降。当S/O=9∶1时能制备出可无限稀释微乳,因此在室温下测量样品1的电导率随着含水量的变化,结果见图8。可见,含水量在10%~70%时,微乳的电导率随含水量的增加而逐渐升高,表明此时微乳以W/O型为主;当含水量为70%时电导率达到最大值,随后随着含水量的增加,微乳的电导率下降,这说明当含水量大于70%时所形成的微乳是O/W型鳄鱼油微乳。
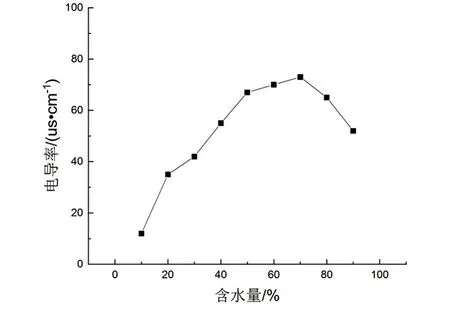
图8 样品1的电导率-含水量曲线图
2.3 稳定性试验
对微乳进行稳定性研究有助于微乳的贮藏、加工和运输。样品1在4000 r/min的转速下离心20 min后仍保持原来的状态,并无分层,且没有发现破乳现象,故所制备鳄鱼油微乳具备良好的离心稳定性。在4℃和25℃条件下保存15 d后,样品1的外观稳定,流动性良好,没有分层现象,表面未出现油滴,说明鳄鱼油微乳短期内在室温下对热较稳定,但在40℃下保存15d后,微乳外观颜色加深,说明该微乳不适宜高温储藏。
3 结论
本研究以鳄鱼油为油相,借助拟三相图优化鳄鱼油微乳配方,同时考察了在S/O值为9∶1,且含水量为80%的条件下制得的微乳(样品1)的理化性质和稳定性。研究发现:以Span-80和Tween-60(质量分数比为13∶7、HLB值为8)为复合表面活性剂,无水乙醇为助表面活性剂,采用Shah法成功制得O/W型鳄鱼油微乳。通过稳定性实验可知,样品1的缓释性能较强,该微乳离心后不发生分层,保持稳定,但高温不稳定,适宜在25℃以下储藏。本研究将鳄鱼油制备成微乳可以增强其渗透性,更易被皮肤吸收,为鳄鱼油在化妆品领域的进一步开发和应用奠定了良好的基础。
