胃癌合并脾包虫病1例报告并文献复习
2021-11-09王永锦郭成旺刘兴吉聂蓬
王永锦,郭成旺,刘兴吉,聂蓬
(甘肃省武威肿瘤医院胃外科,甘肃武威733000)
胃癌是目前常见的消化道恶性肿瘤之一,其发病率居第2 位,而病死率高居第3 位,严重威胁人类健康,手术治疗是可能达到治愈的唯一方式[1]。包虫病在牧区是常见的人畜共患病,其常见发病器官依次为肝脏、肺、脾脏、脑及腹腔等[2]。脾脏虽然是包虫病的第三大常见发病器官,但是脾包虫病在临床上相对较为罕见,其发病率约2.5%~5.8%[3-4]。胃癌合并脾包虫病在临床上极其罕见,目前国内外相关研究尚未报道。孤立的脾脏包虫囊肿与其他原因引起的脾囊肿在影像学上具有相似的表现,且没有敏感特异的实验室检查手段,故手术前的明确诊断仍较为困难,手术切除后病理学诊断是目前最佳的诊断方式[5]。目前胃癌的手术方式是以D2淋巴结清扫的根治性胃切除为主要治疗方案,而脾包虫病的手术干预方式较多,从全脾切除术到保留器官的手术不等,所以该合并症的手术方案可能存在争议[6]。在本文中,笔者希望分享在处理这类特殊合并症中的经验,为非疫区包虫病合并恶性肿瘤的处理提供相关的参考和思路,并提出将“D2淋巴结清扫术、根治性全胃切除、食管-空肠Roux-en-Y 吻合、脾切除术、自体脾片移植术”这一术式作为一种安全有效的胃近端癌合并脾脏包虫病手术方法的想法。
1 病例报告
1.1 一般资料
患者女性,52 岁,农民,主因“间断上腹部胀痛不适1 个月”入院。既往于2019年1月因“卵巢囊肿”行手术治疗;无疫区居住及旅游史,家有牧羊史。查体:下腹部可见5 cm 手术疤痕,上腹部轻压痛,余无其他阳性体征。胃镜检查:胃体近端可见约4 cm 大小溃疡性病灶,周围黏膜堤状隆起,表面污苔附着,质脆、易出血,远端近胃角黏膜粗糙;内镜下诊断:胃体癌(图1A)。病检(178304)示:⑴(胃体小弯近端)胃黏液癌,部分区为印戒细胞癌;⑵(胃体小弯远端)慢性萎缩性胃炎,萎缩(轻度),炎症(轻度),伴肠上皮化生(轻度),伴低级别上皮内瘤变。腹部CT表现:胃体小弯侧局部胃壁增厚并强化,请结合胃镜;脾脏异常密度影,多考虑良性病变,包虫可能性大(图1B)。肿瘤标志物示:CEA 5.87 ng/mL、CA19-9 27.2 U/mL、CA72-4 3.01 U/mL。包虫病不是本地区常见病,故未常规开展包虫抗体检测。诊断:胃癌(cT3NxM0)、脾囊性包虫病。
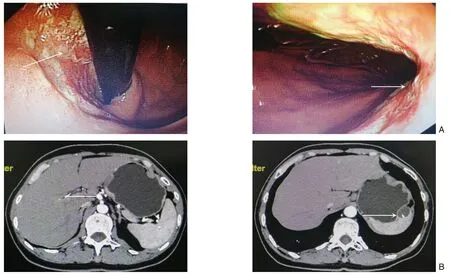
图1 胃镜及腹部CT表现
1.2 治疗方案及经过
经积极术前准备后于2020年1月7日行手术治疗,术中探查见腹腔内无积液,脏、壁层腹膜未见异常结节,肝脏、胆囊、胰腺、大小肠未见异常,盆腔未见异常;胃体小弯侧可见一约4 cm×5 cm大小肿物,呈溃疡型,质硬,胃壁浆膜面完整,胃周及肝总动脉、脾动脉及脾门可见多个肿大淋巴结;脾上极边缘区可见一约3 cm×3 cm 大小囊性肿物,表面凹凸不平。因胃部病灶位于贲门胃体小弯侧,且瘤体较大,常规进行根治性全胃切除术。术中探查时发现脾门淋巴结肿大,应行脾门淋巴结清扫术,而根据日本处理规约脾脏切除才能达到完整的脾门淋巴结清扫;另外考虑到脾脏囊性包虫病位于脾上极边缘区近胃底,离断脾胃韧带时也有可能会损伤脾脏导致包虫囊壁破裂引起腹腔播散,遂决定进行联合脾脏切除的手术,切除脾脏时在其周围常规放置大纱垫保护周边组织器官,以防包虫囊肿破溃造成腹腔播散及过敏性休克等并发症。根据既往经验脾切除后会继发性血小板增高,高者可达1 000×109/L 以上,且肿瘤患者血液处于高凝状态,术后容易发生血栓。为保留部分脾脏功能,术中常规行自体脾片移植术,其过程为:脾脏立体后立即置入1 000 mL 生理盐水中,尽快取远离包虫病灶的脾脏下极组织,剪裁成1.5 cm 大小的脾组织共15 块,置入生理盐水中漂洗备用。因胃癌手术切除了大网膜,最终将脾片移植在横结肠近脾区系膜间,切除标本及脾片移植详见图2。
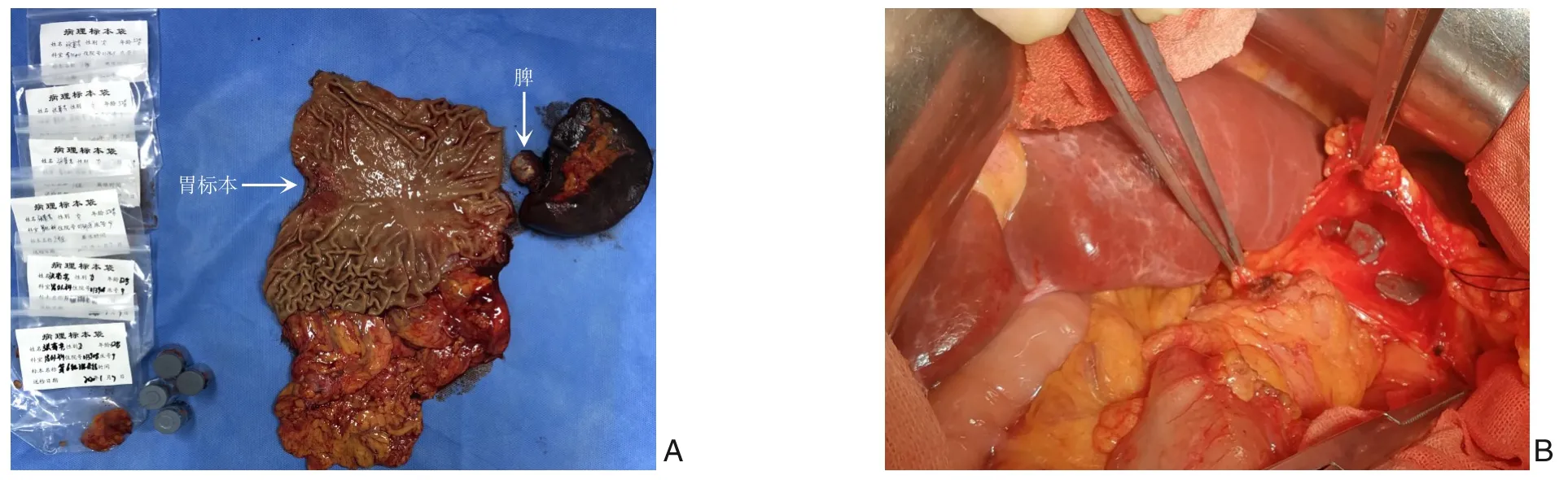
图2 胃根治切除标本及脾片移植情况
1.3 术后病理学资料
术后病检(179048):⑴贲门小弯侧浸润型黏液腺癌,部分区为低分化腺癌(约占30%)及印戒细胞癌(约占10%);Lauren 分型:弥漫型;肿瘤大小4.7 cm×2.3 cm,癌组织浸及浆膜下脂肪组织,神经受浸;淋巴管内见癌栓形成,血管内未见明确癌栓;大网膜及另见肠管(-);标本上、下切缘及另送检切缘未见癌组织;区域淋巴结(2/39)见癌转移,其中1 组淋巴结0/2、2 组淋巴结1/5、3 组淋巴结0/1、4 组淋巴结0/4、5 组淋巴结1/4、6 组淋巴结0/5、7 组淋巴结0/6、8a 组淋巴结0/2、9 组淋巴结0/1、11 组淋巴结0/7、小肠系膜淋巴结0/1、脾门淋巴结0/1;pTNM 分期:pT3N1期。⑵符合脾囊性包虫外囊囊壁组织(图3)。癌细胞免疫组化标记:P53(阳性率>90%)、P-gp(-)、GSTπ(+)、TopoII(++)、Ki-67(阳性率约40%)、TS (-)、C-erbB-2 (-)、MLH1 (+)、MSH2(+)、MSH6(+)、PMS2(+)、CK8/18(+)、EBV(-)。
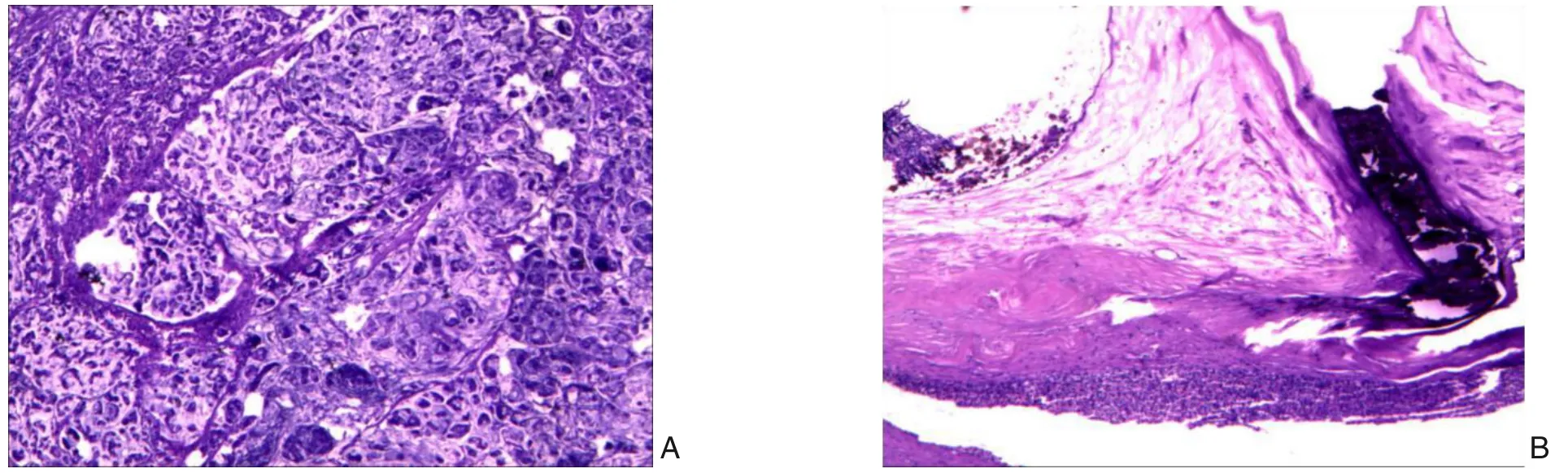
图3 胃癌及脾包虫病组织切片
1.4 术后治疗及随访情况
术后密切监测凝血功能及血小板,于术后4 d血小板开始进行性升高,11 d 升高至602×109/L 达顶峰,之后逐渐下降至正常;D-二聚体术后1 d 明显升高后逐渐下降至正常(图4)。术后第2 天常规予以达肝素钠抗凝治疗,术后10 d 出院后改口服阿司匹林肠溶片,血小板降至正常后停用。术后2 周开始给予口服阿苯达唑(400 mg,1 次/d)抗包虫病治疗,3 个月后患者自行停药。患者系进展期胃癌,分期为pT3N1M0,术后给予6 周期(奥沙利铂联合替吉奥1 周期、紫杉醇联合氟尿嘧啶5 周期)全身静脉辅助化疗。3 个月后监测外周血IgA、IgM、IgG 水平均在正常范围内,说明患者免疫功能恢复正常。术后半年行CT 检查时发现脾窝处有大小不等结节,考虑成活脾片组织。现患者术后15 个月无肿瘤及包虫复发及腹腔播散。
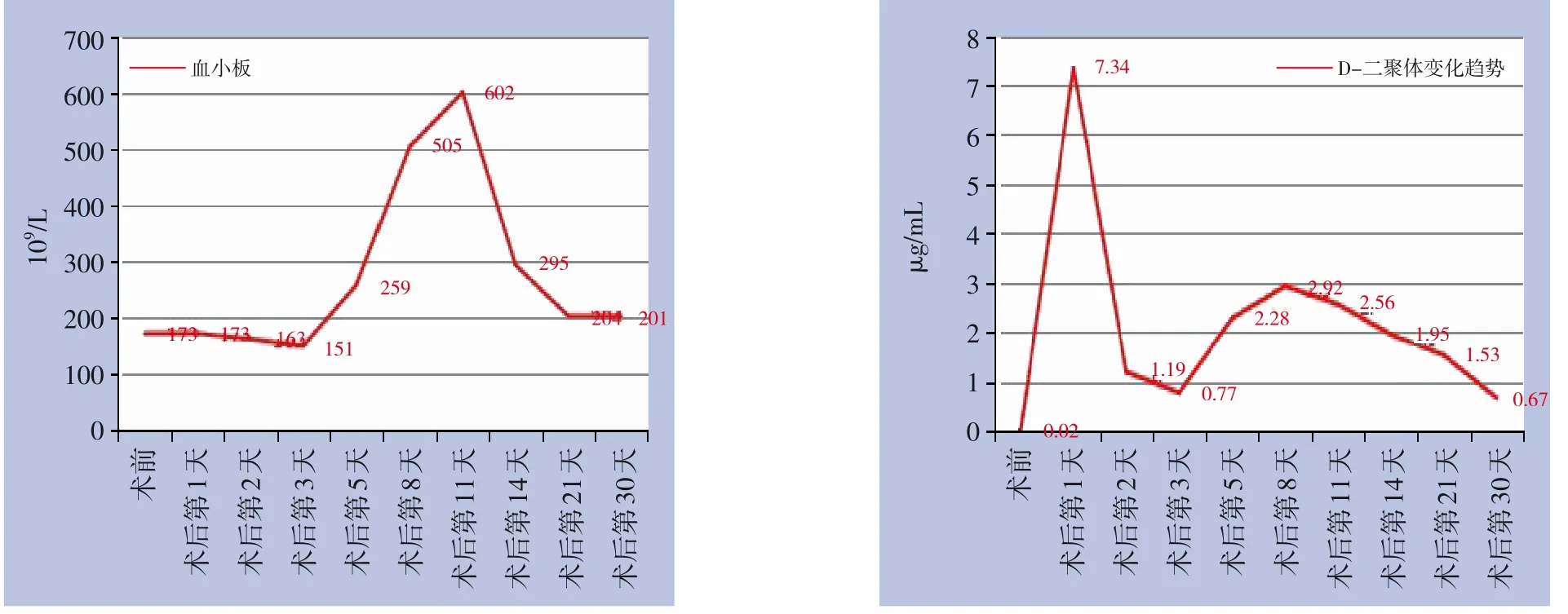
图4 术后血小板及D-二聚体变化趋势
2 文献复习并讨论
在世界范围内胃癌是较为常见的消化道恶性肿瘤之一,具有高发病率和高病死率的特点,在我国则更为明显,截止2019年粗发病率高达43.1/10 万[7]。武威地区是全国胃癌高发区,2015年发病率已经达到107.52/10 万,明显高出全国及全球数倍之多[8]。脾包虫囊肿最先由Berthelot 于1790年在尸体解剖中发现并首次发表[9-10],而在临床上较为少见,其发病率占人体包虫病的0.5%~8%[11],常与肝、肺包虫病并存;原发性孤立脾包虫囊肿更为少见,约占人群发病率的0.07%[12]。虽然甘肃武威是胃癌高发区,但在非疫区出现的胃癌合并脾囊性包虫病在临床上还是极其罕见的,目前国内外相关研究尚未报道。
然而,恶性肿瘤合并脾脏囊肿的诊断是很重要的,直接影响到治疗方案的选择。对于胃癌合并脾脏囊性肿物时,首选应排除远处转移的可能,通过胃癌病期以及增强CT 即可进行鉴别[13]。经验看胃癌患者出现脾脏转移时,首先会发生肝脏及其他远处淋巴结转移,继而才会出现脾脏等其他远隔器官的转移;其次脾脏转移灶多表现低密度病灶伴有不规则强化。本病例通过CT 检查及病史可排除脾脏恶性肿瘤转移。怀疑脾包虫囊肿时,临床诊断应从以下几点考虑:⑴明确是否有疫区居住史或旅游史;⑵患者是否存在左上腹肿痛、隐痛或绞痛的情况;⑶是否可触及肿大的脾脏或左上腹包块;⑷是否有包虫病史,或合并其他部位的病虫病灶;⑸通过Casoni 试验,结果是否为阳性;⑹B 超及CT 是目前诊断脾包虫囊肿较为有效的措施[14]。在本文的研究病例中,患者无疫区居住史,但有牧羊病史;上腹部症状主要是胃癌引起,且未触及包块;通过CT 检查可排除其他部位的包虫病灶,但可初步确定是脾脏原发的孤立包虫病灶。如果条件允许术前应常规进行Casoni 试验进一步明确诊断,但是本院为肿瘤专科医院尚未开展此项检查,故未进一步检查。所以该患者在术前初步诊断为胃癌合并原发性脾囊肿包虫病,最终经病理学明确。
目前,原发性脾囊型包虫手术方式主要是通过开放或腹腔镜方法的脾切除术到器官保留手术,包括部分脾切除术、囊肿摘除术或部分囊壁切除术等[15-17]。根据第十四版日本胃癌处理规约及2019年CSCO 胃癌诊疗指南,局部进展期胃上部癌,胃切除方式首选根治性全胃切除术,淋巴结清扫范围可不包括脾门淋巴结清扫,但是术中探查发现脾门淋巴结有肿大时,可选择保脾的脾门淋巴结清扫术或脾切除术[18]。该患者脾包虫囊肿位于脾上极边缘区,可选择脾切除术或器官保留手术,如部分脾切除术、囊肿摘除术。胃癌合并脾门淋巴结肿大,可考虑进行脾门淋巴结清扫术,但考虑到脾门淋巴结清扫的技术难度、淋巴结清扫的彻底性以及术中损伤脾脏及囊肿导致脾包虫囊肿破裂而引起腹腔播散的危险等,故选择脾脏切除手术是较为合理的。
研究[19]发现,脾脏不仅有储血、造血、滤血和毁血功能,而且对人体的免疫功能起着重要作用。这是因为脾脏具有滤过作用拥有大量功能各异的免疫活性细胞,并分泌许多免疫因子,既可通过吞噬作用完成机体的非特异性免疫,又可通过T 细胞介导的细胞免疫和B 细胞介导的体液免疫完成机体特异性免疫功能。同时,脾脏在抗肿瘤中同样也具有相当的功能[20],脾切除后会导致这些功能的减损甚至丧失。目前,关于脾外伤后保脾手术的相关研究较多,包括脾脏部分切除术、脾片移植术、脾瓣移植术等[21]。不同手术方式有其适应证和优缺点,但共同的目的是尽可能保全脾脏的功能。本例患者本身合并恶性肿瘤,自身免疫力降低,脾切除后不仅会降低免疫力影响术后恢复,且对肿瘤长期生存会有很大影响。所以行全脾切除术后如何保全脾功能是研究的热点。近年来多数学者提出脾切除术后行自体脾片移植具有较好的手术安全性,且尽早能恢复正常的脾脏功能[22-23]。目前,自体脾片移植目前仅由于脾外伤,但在胃癌手术中应用的研究较少。本病例正是基于脾外伤后自体脾片移植的相关研究,实施胃癌手术、全脾脏切除术及自体脾片移植,围手术期无并发症发生,手术安全性可;在术后早期监测血小板情况,发现术后半月移植脾片即发挥了部分毁血功能,持续升高的血小板逐渐恢复正常;3 个月后监测免疫指标发现外周血IgA、IgM、IgG 水平均在正常范围内,说明移植脾恢复了其免疫功能。
根据世界卫生组织指南及相关文献,为了尽可能地减少复发,包虫病患者术后建议服用抗寄生虫治疗[24-25]。该患者术后采用阿苯达唑抗寄生虫治疗,减少复发的风险。
综上所述,胃癌合并原发性脾囊性包虫病在临床上是较为罕见的合并症,尤其在非疫区更为少见。在处理该类合并症时应该兼顾肿瘤和包虫治疗的特殊性,注意术前着重进行病史询问及完善相关检查以明确诊断;制定详细的术前治疗方案、术中相关准备及手术方案;术后应继续加强抗肿瘤及包虫的治疗和随访。
