磷酸铁锂电池粉选择性提锂工艺
2021-11-05姚送送吴国庆朱建楠
姚送送,吴国庆,王 浩,朱建楠
[1.界首市南都华宇电源有限公司,安徽阜阳 236500; 2.南都电源(安徽)新能源科技有限公司,安徽阜阳 236500; 3.安徽南都华铂新材料科技有限公司,安徽阜阳 236500]
随着我国新能源行业的蓬勃发展,作为核心环节的动力电池产量日益攀升[1-2]。磷酸铁锂正极锂离子电池具有循环寿命长、成本低等优点,广泛用于新能源汽车、电动自行车、储能电站等领域[3]。与此同时,电池的报废量也逐年递增,据统计,到2025年,动力电池的退役量将达131万吨[4],动力电池的回收迫在眉睫。动力电池的回收不仅可以回收有价金属,还可以减少电池的不正确处理对环境造成的危害。
目前回收磷酸铁锂动力电池的方法主要有湿法冶金工艺[5-6]、高温再生技术[7-8]以及生物浸出技术[9]等,其中,高温固相再生技术能耗高、难以除杂,不利于大规模生产;生物浸出技术对生物菌的培育时间较长,菌群容易失活,效率低;湿法冶金技术应用较广,工艺较成熟,湿法浸出可以采用硫酸(H2SO4)、盐酸、硝酸和磷酸等。本文作者采用低浓度H2SO4和高浓度硫酸两步法,选择性浸出磷酸铁锂(LiFePO4)正负极混合电池粉中的锂,再通过净化工序除去硫酸锂溶液中的杂质元素。
1 实验
1.1 实验试剂和仪器
实验所用磷酸铁锂正负极混合电池粉为安徽某公司购买的废料,其中,锂、铁、磷、铜、铝和碳的质量分数分别为3.8%、30.1%、17.9%、1.0%、0.9%和12.0%。实验试剂如表1所示,实验仪器如表2所示。
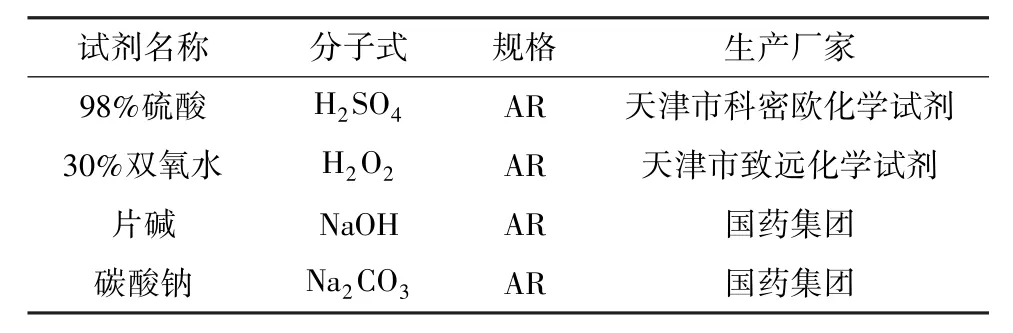
表1 实验试剂Table 1 Experimental reagents

表2 实验仪器Table 2 Experimental instruments
1.2 实验原理
磷酸铁锂在硫酸和双氧水的作用下生成易溶于水的硫酸锂和难溶于水的磷酸铁[见式(1)],在反应过程中需控制好反应条件,减少铁和磷的溶出。
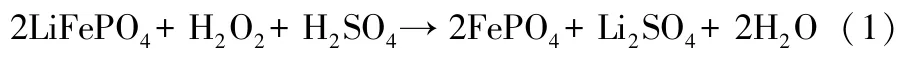
1.3 实验流程
实验的工艺流程如图1所示。
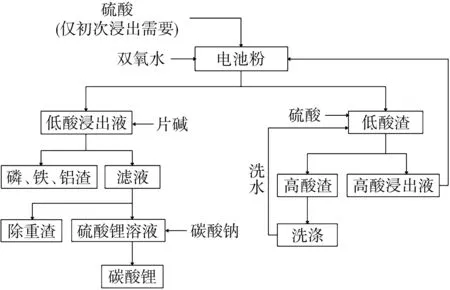
图1 磷酸铁锂电池粉选择性提锂工艺流程图Fig.1 Process flow chart of selective lithium extraction from lithium iron phosphate battery powder
首先采用低酸浸出和高酸浸出两步酸溶浸出法,分别考察浸出硫酸用量、浸出温度和时间等因素的影响。得到的低酸浸出液,通过加入片碱调节pH值,除去滤液中的磷、铁、铝等杂质;向得到的硫酸锂溶液中加入碳酸钠,通过蒸发结晶得到碳酸锂。实验中各元素的含量按GB/T 30835-2014《锂离子电池用炭复合磷酸铁锂正极材料》进行检测[10]。
2 结果与讨论
2.1 低酸浸出
2.1.1 硫酸用量对浸出液pH值的影响
根据式(1)和反应所加的磷酸铁锂电池粉的量,计算硫酸和双氧水的理论用量。硫酸用量分别为理论量的0.10倍、0.15倍、0.20倍和0.30倍,反应温度60℃,反应时间4 h,双氧水用量为理论量的1.10倍,探究硫酸用量对低酸浸出的影响。
从图2可知,当硫酸用量由理论量的0.10倍增加至0.30倍时,低酸浸出液的pH值由4.50降至0.80;当硫酸用量为理论量的0.20倍时,低酸液的pH值为2.51,该pH值有利于低酸浸出磷酸铁的沉淀。
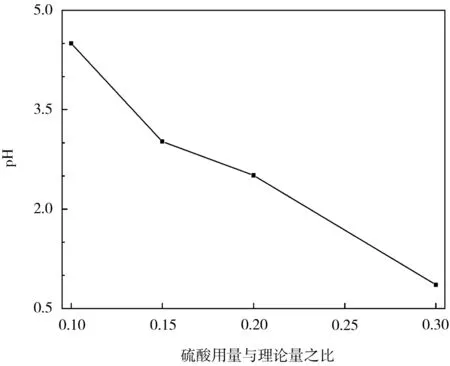
图2 硫酸用量对低酸浸出液pH的影响Fig.2 Effect of sulfuric acid dosage on pH of low-acid leaching solution
2.1.2 温度对锂浸出率的影响
硫酸用量为理论量的0.20倍,反应温度分别为25℃、40℃、60℃和80℃,反应时间4 h,双氧水用量为理论量的1.10倍,探究反应温度对低酸锂浸出率的影响。
从图3可知,温度从25℃升高至80℃时,锂浸出率由11%增加至25%。考虑到温度越高,生产成本会越高,选择在60℃下进行低酸浸出。

图3 低酸浸出反应温度对锂浸出率的影响Fig.3 Effect of reaction temperature on leaching rate of lithium in low-acid leaching
2.1.3 时间对锂浸出率的影响
硫酸用量为理论量的0.20倍,反应温度为60℃,反应时间分别为1 h、2 h、4 h和6 h,探究反应时间对低酸锂浸出率的影响。
从图4可知,随着反应时间由1 h增加至6 h,锂浸出率由10%增加至23%。从生产时间成本角度考虑,确定低酸浸出反应时间为4 h。

图4 低酸浸出反应时间对锂浸出率的影响Fig.4 Effect of reaction time on leaching rate of lithium in lowacid leaching
2.1.4 双氧水用量对磷和铁浸出率的影响
硫酸用量为理论量的0.20倍,反应温度为60℃,反应时间为4 h,探究低酸浸出双氧水用量对磷和铁浸出率的影响。
从图5可知,随着双氧水用量的增加,铁和磷浸出率逐渐减小;双氧水用量为理论量的1.10倍时,反应基本达到平衡。从生产成本角度考虑,确定低酸浸出双氧水用量为理论量的1.10倍。
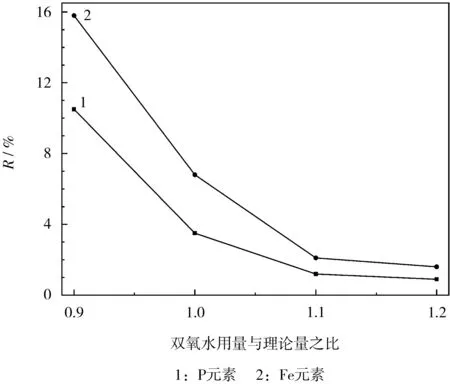
图5 低酸浸出双氧水用量对磷和铁浸出率的影响Fig.5 Effect of hydrogen peroxide dosage on leaching rate of phosphorus and iron in low-acid leaching
2.2 高酸浸出
2.2.1 硫酸用量对锂浸出率的影响
硫酸用量分别为理论量的0.80倍、0.90倍、1.00倍、1.10倍和1.20倍,反应温度90℃,反应时间4 h,探究高酸浸出硫酸用量对锂浸出的影响。
从图6可知,当硫酸用量由理论量的0.80倍增加至1.20倍时,高酸锂的浸出率由75.0%提高至98.5%;硫酸用量大于1.10倍时,锂的浸出率趋于平稳。故选择高酸浸出硫酸用量为理论量的1.10倍。
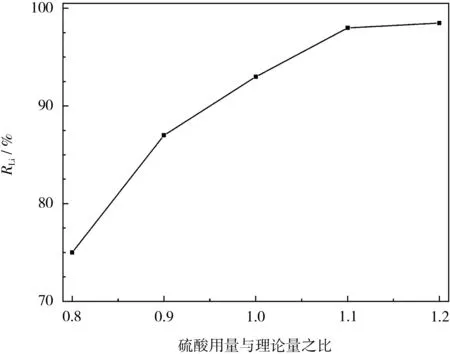
图6 高酸浸出硫酸用量对锂浸出率的影响Fig.6 Effect of sulfuric acid dosage on leaching rate of lithium in high-acid leaching
2.2.2 温度对锂浸出率的影响
硫酸用量为理论量的1.10倍,反应时间4 h,反应温度分别为60℃、70℃、80℃和90℃,探究反应温度对高酸锂浸出率的影响。
从图7可知,温度由60℃升高至90℃时,锂浸出率由85.0%增加至98.5%,因此选择在90℃下进行高酸浸出。
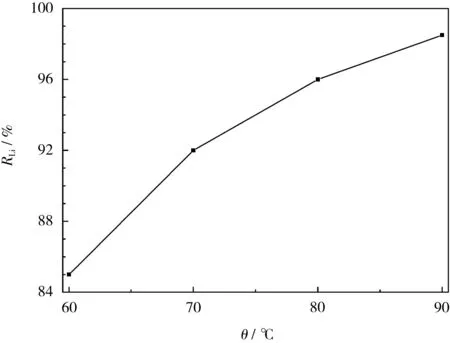
图7 高酸浸出反应温度对锂浸出率的影响Fig.7 Effect of reaction temperature on leaching rate of lithium in high-acid leaching
2.2.3 时间对锂浸出率的影响
硫酸用量为理论量的1.10倍,反应温度为90℃,反应时间分别为1 h、2 h、3 h、4 h和6 h,探究反应时间对锂浸出率的影响。
从图8可知,随着反应时间由1 h增加至6 h,锂浸出率由60.0%增加至98.6%;反应时间长于4 h后,锂的浸出率趋于平衡。从生产时间成本角度考虑,确定高酸浸出反应时间为4 h。
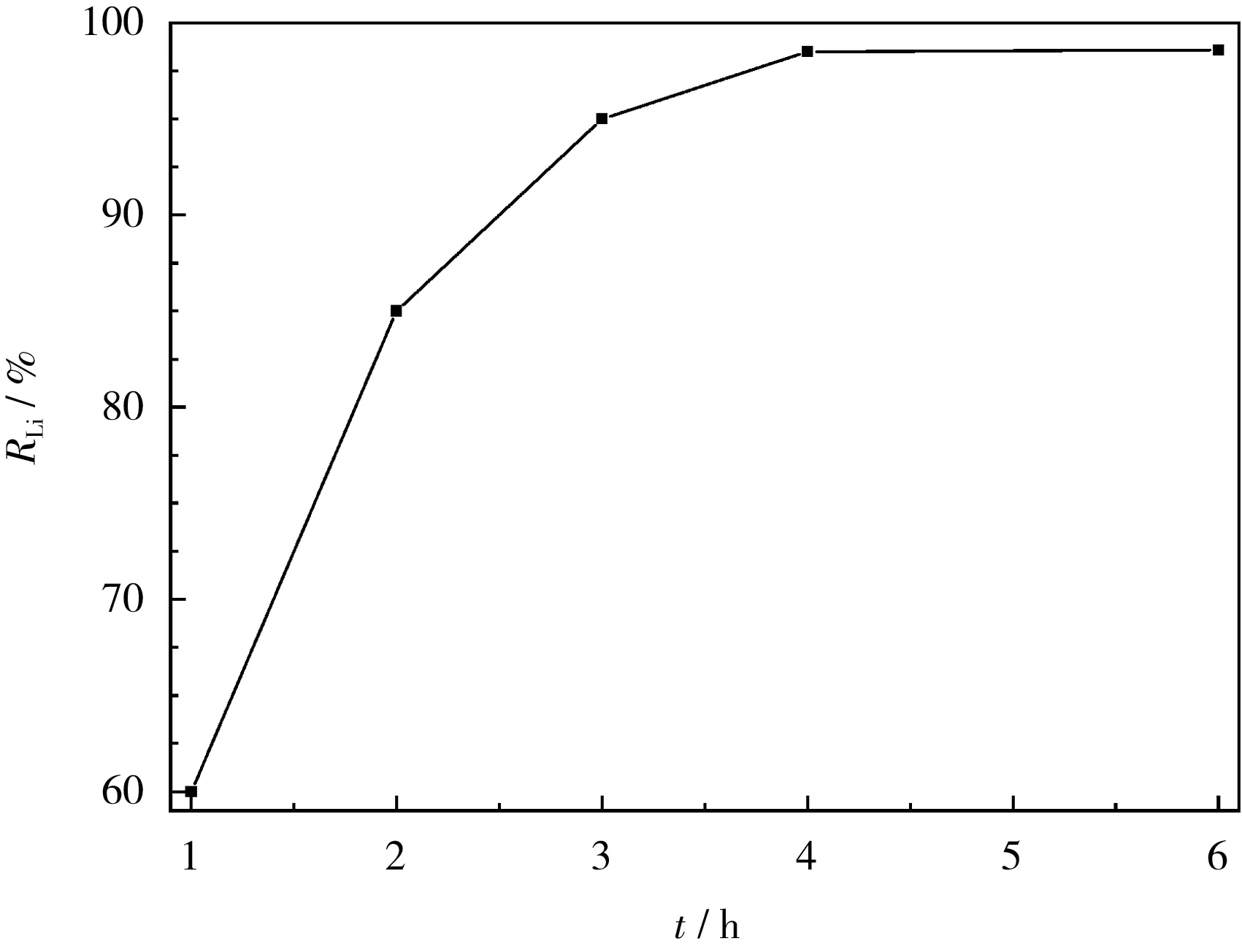
图8 高酸浸出反应时间对锂浸出率的影响Fig.8 Effect of reaction time on leaching rate of lithium in high-acid leaching
2.3 连续式循环浸出实验
根据以上低酸浸出和高酸浸出的实验结果,由图1工艺流程图可知,循环酸浸时,高酸浸出液返回至低酸浸出,此时低酸浸出不需要再补充硫酸。低酸浸出反应温度为60℃,反应时间4 h,双氧水用量为理论量的1.10倍,高酸浸出的酸量为理论量的1.30倍,反应温度为90℃,反应时间4 h,高酸液返回下一次低酸浸出,可实现连续式生产。
2.4 浸出硫酸锂溶液的净化除杂
滤液加液碱,调至中性,过滤除去铝等杂质,得到的滤液再加液碱,将pH值调至10.0~12.0,过滤除去铜等杂质,得到纯净的硫酸锂溶液。
从表3可知,净化除杂后杂质元素都降至1 mg/L以下,再加入碳酸钠,通过蒸发结晶制备碳酸锂产品。

表3 浸出硫酸锂溶液净化前后的元素含量Table 3 Elements content of leaching lithium sulphate solution before and after purification mg/L
2.5 对比实验
对比实验步骤如下:一步酸溶浸出磷酸铁锂电池粉,硫酸用量为理论量的1.30倍,双氧水用量为理论量的1.10倍,反应温度90℃,反应时间4 h,锂的浸出率96.00%,铁的浸出率4.50%,磷浸出率2.10%,浸出液pH值约为1.50。
通过对比实验可知,在连续生产时,同等条件下,两步酸溶法浸出液的pH值为3.00,而一步酸溶法浸出液的pH值为1.50。较低的浸出液pH值一方面不利于磷酸铁的沉淀,导致浸出液中铁和磷含量偏高;另一方面后续碱液调节pH值除重金属时,消耗的碱液较多,产生的渣量相应较多,会增加生产成本。
3 结论
本文作者提出低酸-高酸两步硫酸浸出的方法,低酸浸出反应温度为60℃,反应时间4 h,双氧水用量为理论量的1.10倍;高酸浸出的酸量为理论量的1.30倍,反应温度为90℃,反应时间4 h,高酸液返回下一次低酸浸出。初次浸出时,低酸浸出需要加理论量0.20倍的硫酸,后续循环浸出仅在高酸浸出,加理论量1.30倍的硫酸。
浸出的硫酸锂溶液通过净化除杂后,杂质元素含量都在1 mg/L以下,得到较为纯净的锂液,并通过加碳酸钠后蒸发结晶得到碳酸锂产品。
该工艺可以将低酸浸出硫酸锂溶液的pH值控制在2.5左右,有利于磷酸铁的沉淀,减少净化工序的液碱用量和渣量,并且能够实现连续式生产。与一步酸溶法相比,该方法的成本更低。
致谢:感谢叶明刚、孙朝军、卢广、徐诗艳和陈华勇等在实验方面的指导和帮助!
