人参皂苷Rb1对兔离体肠平滑肌收缩活动的影响*
2021-11-05杨麒民李春臣张建武
杨麒民,罗 涛,李春臣,刘 鑫,陈 卫,陈 缘,郭 芮,张建武
川北医学院,四川 南充637100
人参皂苷Rb1是人参二醇系皂苷,主要分布于五加科植物人参、三七、西洋参等植物中,具有多种药理活性,是一种具有较高药用价值的化学物质。人参、三七、西洋参都是传统中药,应用历史悠久,人参主补五脏,能增强机体免疫力,抗休克、抗肿瘤,对肝脏疾病也有一定的治疗作用[1-3]。随着对人参主要活性成分Rb1的深入研究,医学界对其在中枢神经系统、心血管系统、免疫系统及抗肿瘤、抗肝脏热缺血再灌注等方面的研究非常广泛[4]。裴娟慧等[5]发现,人参皂苷Rb1对大鼠心室肌细胞L-型钙电流有明显的抑制作用,而抑制L-型Ca2+通道是抗心律失常的重要机制,即对心肌收缩舒张具有影响。由于心肌与肠道平滑肌结构和功能上存在部分区别,且其对肠道平滑肌收缩活动的影响尚无报道,故此笔者进行了人参皂苷Rb1对正常状态下家兔离体肠平滑肌自发性收缩活动影响的研究,为进一步开发利用人参皂苷Rb1药用价值提供理论基础。
1 材料与方法
1.1 实验动物中国白兔,体质健康,雌雄兼半,体质量(2.3±0.5)kg,由川北医学院动物实验中心提供,实验动物许可证号:SYXK(川)2018-076。饲养条件:家兔饲养于23~26℃、湿度适宜的实验室环境,12 h光照黑暗循环,实验前动物自由饮水,但需禁食24 h。
1.2 试药及试剂人参皂苷Rb1(成都曼斯特生物科技有限公司,批号:MUST-17060106);钌红(ruthenium red,RR,源叶生物科技有限公司,批号:11103-72-3);肝素(heparin,HP,成都市科华化工试剂厂,批号:9041-08-1);盐酸维拉帕米注射液(Verapamil,V,上海禾丰制药有限公司,批号:43161001,规格:2 mL∶5 mL/支);新鲜的台氏液(g/L):川北医学院机能实验中心制剂(NaCl 40 g,10% KCl 1 g,CaCl21 g,NaHCO35 g,10%MgSO4·7H2O1.3 g,5%NaH2PO4·2H2O 0.325 g,C6H12O65.5 g RO水5000 mL)。
1.3 实验仪器兔类通用实验器械;BL-420型生物机能实验系统(四川成都泰盟公司);FT-100型生物张力传感器(四川成都泰盟软件有限公司);HW-400E型恒温平滑肌槽(四川成都泰盟科技有限公司);优普纯水/超纯水制造系统(四川优普超纯科技有限公司)。
1.4 实验方法
1.4.1 人参皂苷Rb1溶液制备 预热电子天平30 min后,准确称量人参皂苷Rb1,加入台氏液,定容至10~2 mol/L即成。
1.4.2 兔离体肠平滑肌标本的制备[6]取健康家兔,禁食24 h后,用木槌猛击兔头枕部致死。迅速沿腹中线打开腹腔,以胃幽门与十二指肠交界处为起点剪取肠管,每只兔取十二指肠同一肠段置于盛有室温饱和台氏液的烧杯中,洗净肠内容物,剪成1.5~2.0 cm的肠段作为实验标本。
1.4.3 肠管舒缩活动的记录 打开BL-420F生物机能实验系统,调零,定标,在一通道输入接口处安装张力换能器。调节恒温平滑肌槽,使水温保持在(37±0.5)℃,将台式液加入预管内,药物管加入16 mL台式液。将标本一端固定于L-型通气钩上,另一端连接张力换能器,持续通入混合气体(96%O2,4%CO2),每秒1~2个气泡,温度在37℃,标准负荷1 g,平衡1 h,待肠管稳定后,开始进行实验。
1.4.4 人参皂苷Rb1对兔离体肠平滑肌收缩的影响 待肠管收缩稳定后,用BL-420生物机能实验系统描记一段肠管正常收缩曲线,累积加入已配好的人参皂苷Rb1,使终浓度分别达到50、70、90 μmol/L,加药间隔时间为5 min,同时设置一组空白组,于空白组中加入等量台氏液进行实验。观察肠道运动曲线,用区间测量法记录加药前1 min和加药后第5 min的肠道收缩数据(峰峰值、平均值、频率)。
1.4.5 HP、RR和维拉帕米预处理肠管后对人参皂苷Rb1作用于肠管收缩活动的影响 待肠管收缩曲线稳定后,随机分成对照组、钌红组、肝素组、维拉帕米组。分别加入肌浆网ryanodine受体阻断剂钌红(ruthenium red,RR)10 μmol/L,IP3受体阻断剂肝素(heparin,HP)50 mg/L,L-型Ca2+通道拮抗剂维拉帕米(verapamil)0.1 μmol/L孵育15 min,同时设置一组对照组,用等量台式液孵育15 min,当各组孵育后的平滑肌收缩达到平台期后再累计加入人参皂苷Rb1,使终浓度分别达到50、70、90 μmol/L,加药间隔为5 min,记录加入人参皂苷Rb1后第5 min肠管收缩的平均收缩力的变化。
1.5 统计学方法采用SPSS 19.0统计学软件处理实验数据,计量资料采用±s表示,采用t检验,计数资料以率表示,采用χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 兔离体小肠平滑肌的收缩活动在空白组中加入溶剂台式液,对兔离体肠平滑肌的自发性收缩活动并无明显的影响(P>0.05)。人参皂苷Rb1在50~90 μmol/L浓度梯度内能剂量依赖性的抑制兔离体小肠平滑肌的收缩(P<0.05)。见图1。

图1 人参皂苷Rb1对兔小肠平滑肌收缩的影响
2.2 兔离体小肠平滑肌运动的收缩频率、收缩张力、收缩振幅与给药前比较,人参皂苷Rb1对肠管收缩的频率无影响(P>0.05);较低浓度的人参皂苷Rb1(50 μmol/L)对肠管的收缩张力具有抑制作用,随浓度增加,肠管的收缩张力明显受到抑制(P<0.01);较低浓度的人参皂苷Rb1(50 μmol/L)对肠管的收缩幅度具有抑制作用,随浓度的增加,肠管的收缩幅度明显受到抑制(P<0.01)。见表1。
表1 不同剂量人参皂苷Rb1对兔离体小肠平滑肌的收缩频率、收缩张力、收缩振幅的影响(±s)

表1 不同剂量人参皂苷Rb1对兔离体小肠平滑肌的收缩频率、收缩张力、收缩振幅的影响(±s)
注:与给药前(人参皂苷Rb10 μmol/L)比较,*表示P<0.05,**表示P<0.01
?
2.3 HP、RR和维拉帕米预处理肠管后对人参皂苷Rb1作用于离体肠管活动的影响与对照组比较,在钌红组中,用ryanodine受体阻断剂RR预孵后,离体小肠平滑肌的收缩未有明显的变化(P>0.05),再累积加入人参皂苷Rb1,在低浓度时离体肠平滑肌的收缩受到抑制的程度增强(P<0.05),随着人参皂苷Rb1的浓度增加,离体肠平滑肌的收缩受到抑制的程度增强更为明显(P<0.01),表明人参皂苷Rb1对离体肠平滑肌收缩的抑制作用可能与抑制ryanodine受体有关。2)与对照组比较,在肝素组中,用IP3受体阻断剂HP预孵后,离体肠平滑肌的收缩未有明显的变化(P>0.05),再累积加入人参皂苷Rb1,浓度达到70 μmol/L时,离体小肠平滑肌的收缩受到抑制的程度增强(P<0.05),表明人参皂苷Rb1对离体肠平滑肌收缩的抑制作用可能与抑制IP3受体有关。3)与对照组比较,在维拉帕米组中,用L-型Ca2+通道拮抗剂维拉帕米预孵后,离体肠平滑肌的收缩未有明显的变化(P>0.05),再累积加入人参皂苷Rb1,离体肠平滑肌的收缩受到抑制的程度明显增强(P<0.01),表明人参皂苷Rb1对离体肠平滑肌收缩的抑制作用可能与阻断L-型Ca2+通道有关。见表2。
表2 钌红、肝素、维拉帕米预处理后人参皂苷Rb1对兔离体小肠平滑肌活动的影响(±s)
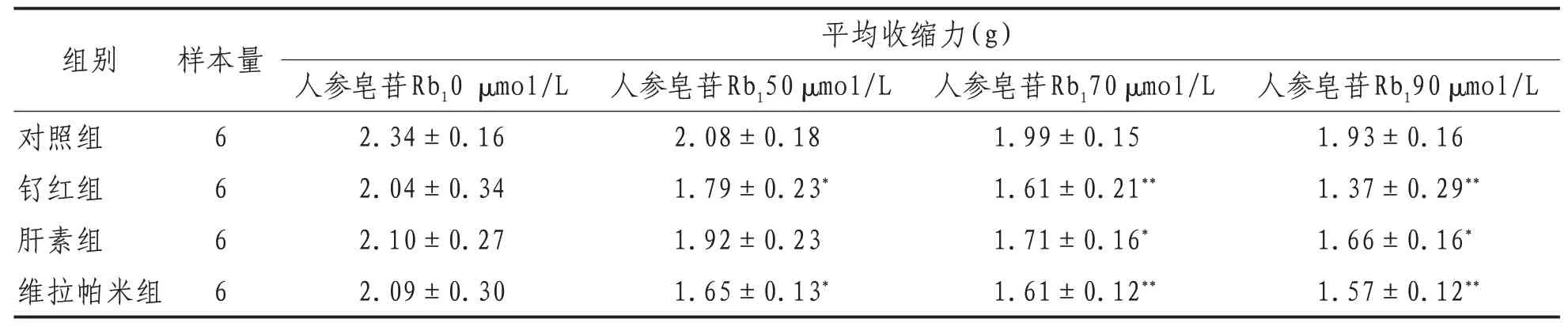
表2 钌红、肝素、维拉帕米预处理后人参皂苷Rb1对兔离体小肠平滑肌活动的影响(±s)
注:与给药前(人参皂苷Rb10 μmol/L)比较,*表示P<0.05,**表示P<0.01
?
3 讨论
腹痛、腹泻等胃肠道疾病通常是由胃肠平滑肌痉挛引起的。肠平滑肌细胞内Ca2+是肠平滑肌收缩的偶联因子,与肠平滑肌兴奋-收缩偶联存在着紧密的关系,细胞外Ca2+进入细胞平滑肌细胞内和细胞内Ca2+肌质网内Ca2+释放是细胞内Ca2+升高的主要途径[7],当胞内Ca2+浓度达到一定水平时,与肌钙蛋白或肌调蛋白结合,触发平滑肌收缩[8]。通过实验结果发现,人参皂苷Rb1能够浓度依赖性的抑制肠平滑肌的自发性收缩,针对人参皂苷Rb1所具有的肠平滑肌的舒张作用,对其与外Ca2+进入的通道和内Ca2+释放的相关受体的影响进行了初步的探究。
细胞内Ca2+的释放主要来自于肌浆网,而肌浆网内释放的Ca2+主要通过IP3和ryanodine受体来完成。当这些受体被激活后,可引起肌浆网内钙离子的释放,从而导致细胞内钙离子浓度增加,诱导平滑肌收缩[9-11]。本实验通过用ryanodine受体阻断剂RR和IP3受体阻断剂HP对肠管进行预处理,来探究人参皂苷Rb1对细胞内Ca2+的释放的相关受体的影响。ryanodine受体是存在于肌细胞肌质网和其他细胞内质网的胞内钙释放通道之一,Ca2+集合后激活RyR1使通道在开放和关闭状态随机转换;进一步集合咖啡因则可将通道保持在开放状态。ryanodine结合于孔道侧壁,低浓度时可将通道锁定在亚电导状态(有部分离子流通过),高浓度则阻断离子的通过[12]。实验结果表明,使用RR预处理肠管后,再加入人参皂苷Rb1后,小肠平滑肌的收缩抑制程度明显加强,由此推断人参皂苷Rb1通过抑制ryanodine受体途径,使得细胞内Ca2+释放减少,从而抑制肠平滑肌的收缩。HP可作用于三磷酸肌醇受体(inositol triphosphate receptor,IP3R),IP3R是广泛存在于各种细胞内质网的一种钙释放通道家族,当IP3R与1,4,5三磷酸肌醇和钙离子两种底物分子结合后,IP3R开放,Ca2+便从内质网钙库释放到细胞质中[13]。实验结果表明,使用HP预处理肠管,再加入人参皂苷Rb1后,小肠平滑肌的收缩抑制程度明显加强,由此推断人参皂苷Rb1通过抑制IP3受体途径,引起细胞内Ca2+释放减少,从而抑制肠平滑肌的收缩。
细胞外的Ca2+主要是通过细胞膜上的Ca2+通道进入细胞内,肠平滑肌中主要的钙通道是L型电压依赖性Ca2+通道[14]。维拉帕米是L-型Ca2+通道拮抗剂,作用机制是阻滞外源性Ca2+经L-型钙离子通道进入细胞内,降低胞内的Ca2+浓度,而Ca2+是细胞内重要的第二信使,高浓度的Ca2+可引起平滑肌收缩,低浓度Ca2+可引起平滑肌舒张[15]。本实验通过用维拉帕米对肠管进行预处理,来探究人参皂苷Rb1对细胞外Ca2+的进入的相关通道的影响。实验结果表明,使用维拉帕米处理肠管后,再加入人参皂苷Rb1后,小肠平滑肌的收缩抑制程度明显加强,由此推断人参皂苷Rb1阻断L-型Ca2+通道,使进入细胞内Ca2+减少,从而抑制肠平滑肌的收缩。
综上所述,人参皂苷Rb1可显著抑制兔离体肠平滑肌自发性收缩,其机制可能是阻断L-型Ca2+通道抑制外钙内流,或阻断ryanodine受体和IP3受体抑制内钙释放,最终使细胞内钙离子浓度降低,从而抑制肠平滑肌的收缩。本实验为人参皂苷Rb1应用于胃肠功能紊乱性疾病的治疗提供了实验依据。
