直接Z型LaNiO3/M n0.2Cd0.8S异质结催化剂光解水产氢性能及机理探究
2021-11-04王兆宇许俊丽张明文陈文韬
王兆宇 许俊丽 张明文 陈文韬
(1福建技术师范学院近海流域环境测控治理福建省高校重点实验室,福清 350000)
(2福州大学能源与环境光催化国家重点实验室,福州 350002)
自1972年日本科学家发现TiO2光解水产氢反应以来,半导体催化光解水产氢反应日益得到研究者的关注[1-4]。然而TiO2由于其带隙较宽(3.2 eV),只能利用太阳光中的紫外线部分,而对于占太阳能50% 左右的可见光则无法利用,因此开发新型可见光响应光催化剂具有重要意义[5-6]。
金属氧化物、硫化物、有机金属配合物、氮化物及其复合物也已经在光解水产氢领域得到大量研究[7-10]。其中CdS是一种可见光响应光催化剂,具有适宜的能带位置和禁带宽度,然而体相CdS中光生电子-空穴复合几率高,同时其晶格中S2-易受空穴氧化,从而导致其光催化活性和稳定性低下,提高CdS基光催化剂的光催化性能是一个亟待解决的问题[11-12]。其中,过渡金属元素掺杂是提高CdS光催化反应性能的一条有效途径。相关报道已经证实,过渡金属元素(Mn、Ni、Co和Zn)的引入能够有效地抑制CdS基光催化剂中光生电子-空穴对的复合,延长光生电子的寿命,从而使得其光催化活性得到有效地提高[13-15]。但是元素掺杂只能提高CdS的光催化活性,CdS基光催化剂易被光腐蚀的缺点依然没能得到有效地解决。
直接Z型异质结的构筑能够有效地促进光生电子和空穴在复合催化剂中不同组分中的分离,同时光生电子和空穴将会积累在复合催化剂的不同组分中[16-18]。LaNiO3是一种常见的钙钛矿材料,被广泛应用于超级电容、锂电池、光催化等领域。其中LaNiO3禁带宽度是1.91 eV,导带和价带位置分别位于0.21和2.12 V。Ding通过合成LaNiO3/ZnIn2S4异质结光催化剂并将其应用于光解水产氢反应,能够有效提高其光解水产氢效率[19]。Jia通过自组装的途径合成出LaNiO3-RGO催化剂,相较于LaNiO3,其光解水产氢活性提高了12倍[20]。众多研究表明结构稳定、能带位置适宜的LaNiO3是一种极具潜力的新型光催化材料。
因此,我们将LaNiO3引入到Mn2+掺杂的CdS合成过程中,通过原位生长的方式合成出直接Z型异质结LaNiO3/MnxCd1-xS光催化剂。LaNiO3的导带位置低于H+/H2氧化还原电位,在光激发下,LaNiO3导带上的光生电子不能用于H2的生成,从而与MnxCd1-xS价带上的空穴结合,光生电子和空穴则分别积累在MnxCd1-xS的导带和LaNiO3的价带,有效地实现光生电子-空穴的分离,提高其光解水产氢的效率。同时光生空穴在LaNiO3价带上的积累能够有效地抑制CdS的光腐蚀现象,提高其稳定性。
1 实验部分
1.1 试剂与仪器
乙酸镉、乙酸锰、乙二胺、硫代乙酰胺、乙醇购自国药集团化学试剂有限公司,所用试剂均为分析纯。去离子水为自制。
所用仪器:样品的晶相结构由Bruker D8 Advance型 X 射线衍射仪(XRD)测试(CuKα,λ=0.154 06 nm,U=40 kV,I=40mA,2θ=20°~70°);样品形貌由日立SU 8010场发射扫描电镜(SEM)拍摄(5 kV);比表面积和孔径分布在物理吸附仪(Micrometric 2020M)上采用液氮(77 K)静态吸附法测定;样品的紫外可见吸收光谱由Varian Cary 500型分光光度计来测定;荧光光谱由日本的F-7000型荧光光谱仪测试;在Epsilon 100电化学工作站上测试样品的电化学性质,以Ag/AgCl(3mol·L-1KCl)作为参比电极,以Pt片电极作为对电极,涂抹有样品的导电玻璃片(FTO)作为工作电极,并采用三电极体系测试催化剂的奈奎斯特曲线。
1.2 催化剂制备
LaNiO3的制备:将硝酸镧(0.433 g,1mmol)和硝酸镍(0.290 g,1 mmol)溶于去离子水(80 mL)中,超声、搅拌,然后加入20 mL NaOH溶液(0.375 mol·L-1)。将上述混合溶液在60℃下回流4 h。反应结束后,将得到的产物用去离子水和乙醇洗涤,70℃烘干。将样品放入马弗炉中,650℃煅烧2 h,得到黑色LaNiO3。
LaNiO3/Mn0.2Cd0.8S的制备:取适量LaNiO3、4.264 g(18mmol)乙酸镉、0.778 5 g(4.5mmol)乙酸锰溶于30mL乙二胺和30mL水的混合液中,加入硫代乙酰胺(1.737 g,23mmol),超声、搅拌30min后将其转移至100mL反应釜中,在160℃下反应24 h,得到的产物用水和乙醇洗涤,在60℃中干燥8 h,即可得到LaNiO3/Mn0.2Cd0.8S催化剂。通过调节LaNiO3的引入量(LaNiO3/Mn0.2Cd0.8S复合催化剂中LaNiO3所占质量分数),其它合成步骤不变,即可得到不同LaNiO3含量的LaNiO3/Mn0.2Cd0.8S异质结光催化剂。在MnxCd1-xS催化剂的合成过程中引入不同量的乙酸锰,其它合成步骤不变。除非特别说明,本实验中所提到的催化剂均为LaNiO3的质量分数为30% 的LaNiO3/Mn0.2Cd0.8S异质结催化剂。
1.3 光解水产氢性能测试
光解水产氢实验在泊菲莱光解水装置上进行。具体实验步骤如下:称取20mg催化剂加入到100 mL含10mL三乙醇胺(TEOA)的去离子水溶液中,搅拌20 min,使催化剂分散均匀,反应温度控制在10℃,将体系抽真空。用λ≥420 nm的截止滤光片控制光源后开启光源进行光解水产氢反应,以岛津8 A气相色谱检测体系中所产生的H2。
2 结果与讨论
2.1 催化剂表征
2.1.1 XRD分析
图1 为 LaNiO3、CdS、Mn0.2Cd0.8S、LaNiO3/CdS 和LaNiO3/Mn0.2Cd0.8S异质结光催化剂的XRD图。在LaNiO3/Mn0.2Cd0.8S的XRD图中分别显示出LaNiO3和CdS的衍射峰。其中2θ=24.9°、26.7°、28.4°、36.9°、44.1°、48.3°、51.2°、52.3°、53.3°、58.8°和67.4°处的衍射峰分别对应六方晶系CdS(PDF No.77-2306)的(100)、(002)、(101)、(102)、(110)、(103)、(200)、(112)、(201)、(202)和(203)晶面,2θ=32.7°、47.1°和58.4°处的衍射峰分别对应斜方六面体LaNiO3(PDF No.33-0711)的(110)、(202)和(122)晶面。LaNiO3/Mn0.2Cd0.8S的XRD图中并未显示出Mn物种所对应的衍射峰,这是因为Mn2+离子的半径(0.066 nm)小于Cd2+的离子半径(0.097 nm),同时2种元素的电负性也相差不大(Mn:1.55,Cd:1.69),Mn2+离子能够进入 CdS 的晶格结构中取代部分Cd2+离子。相较于CdS,Mn0.2Cd0.8S的衍射峰向高衍射角度方向发生了偏移,这是Mn2+离子进入CdS的晶格结构中生成缺陷导致[21-23]。XRD表征结果证明了LaNiO3/Mn0.2Cd0.8S异质结光催化剂的成功制备。

图1 LaNiO3、CdS、Mn0.2Cd0.8S、LaNiO3/CdS和LaNiO3/Mn0.2Cd0.8S异质结光催化剂的XRD图Fig.1 XRD patterns of LaNiO3,CdS,Mn0.2Cd0.8S,LaNiO3/CdS,and LaNiO3/Mn0.2Cd0.8S heterojunction photocatalysts
2.1.2 样品形貌分析
对所制备的样品进行SEM表征(图2)。Mn0.2Cd0.8S的SEM图表明其表面呈现规则的纳米棒形貌(图2a)。LaNiO3由一系列堆积在一起的纳米颗粒所组成(图2b)。原位合成的LaNiO3/Mn0.2Cd0.8S异质结光催化剂的SEM中,LaNiO3纳米颗粒与Mn0.2Cd0.8S纳米棒混合在一起(图2c),这将有利于二者之间异质结构的形成和光生载流子的转移。在LaNiO3/Mn0.2Cd0.8S的能量散射X射线谱图(EDS)中分别显示出La、Ni、O、Mn、Cd和S的信号峰(图2d),这表明LaNiO3/Mn0.2Cd0.8S异质结光催化剂的成功合成,这与XRD表征结果是一致的。同时,Mn和Cd的原子比为0.97/4.1,这与原料中2种元素的比例基本一致。

图2 Mn0.2Cd0.8S(a)、LaNiO3(b)和LaNiO3/Mn0.2Cd0.8S(c)异质结光催化剂的SEM图;LaNiO3/Mn0.2Cd0.8S异质结光催化剂的EDS谱图(d)Fig.2 SEM images of Mn0.2Cd0.8S(a),LaNiO3(b),and Mn0.2Cd0.8S heterojunction photocatalysts(c);EDS spectrum of LaNiO3/Mn0.2Cd0.8S heterojunction photocatalysts(d)
2.1.3 比表面积分析
LaNiO3/Mn0.2Cd0.8S异质结光催化剂的N2吸附-脱附等温线显示出典型的Ⅳ型等温线,在p/p0=0.9~1.0范围内有高吸附容量,这表示样品中存在大量的中孔和大孔(图3)。LaNiO3/Mn0.2Cd0.8S异质结光催化剂的比表面积为24m2·g-1,Mn0.2Cd0.8S和LaNiO3的比表面积分别为 24 和 13m2·g-1,可见通过 Mn0.2Cd0.8S 和LaNiO3的复合,LaNiO3/Mn0.2Cd0.8S的比表面积基本没有发生改变,说明其表面催化反应活性位点数量并没有发生明显的变化。
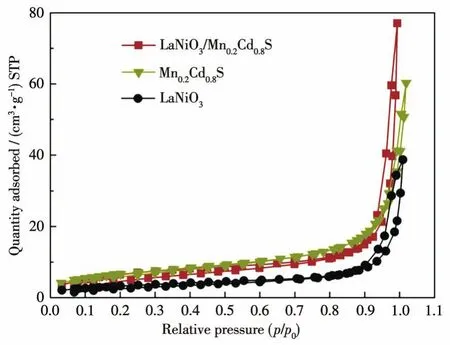
图3 LaNiO3、Mn0.2Cd0.8S和LaNiO3/Mn0.2Cd0.8S异质结光催化剂的N2吸附-脱附等温线Fig.3 N2adsorption-desorption isotherms of LaNiO3,Mn0.2Cd0.8S,and LaNiO3/Mn0.2Cd0.8S heterojunction photocatalysts
2.1.4 XPS分析
通过XPS对所得催化剂进行表征。在LaNiO3/Mn0.2Cd0.8S异质结光催化剂的La3dXPS谱图中,结合能在834.4和851.1 eV处的峰分别对应La3d5/2和La3d3/2的峰,837.9和854.8 eV处的峰对应La3d5/2和La3d3/2的卫星峰(图4a)。与LaNiO3的结合能(833.7和850.4 eV,837.1和854.4 eV,图4c)相比,其结合能正移了0.6 eV,这表明LaNiO3/Mn0.2Cd0.8S异质结光催化剂中LaNiO3和Mn0.2Cd0.8S之间存在紧密的接触。同时LaNiO3/Mn0.2Cd0.8S异质结光催化剂中S2p3/2和S2p1/2对应的结合能位置(161.4和162.4 eV,图4b)相对于Mn0.2Cd0.8S中S2p3/2和S2p1/2的结合能位置(161.7和162.8 eV,图4d)负移了0.3 eV,这证明了LaNiO3/Mn0.2Cd0.8S异质结光催化剂中LaNiO3和Mn0.2Cd0.8S之间的紧密接触,同时电子从LaNiO3向Mn0.2Cd0.8S传输。
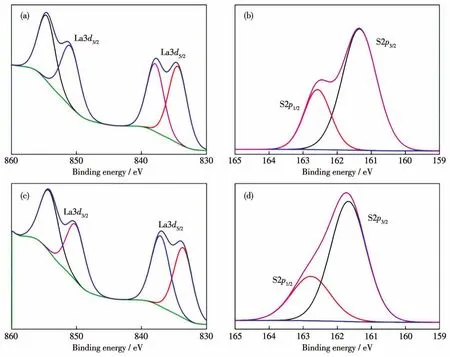
图4 LaNiO3/Mn0.2Cd0.8S异质结光催化剂中La3d(a)和S2p(b)的XPS谱图;LaNiO3和Mn0.2Cd0.8S中La3d(c)和S2p(d)的XPS谱图Fig.4 La3d(a)and S2p(b)XPS spectra for LaNiO3/Mn0.2Cd0.8S heterojunction photocatalysts;La3d(c)and S2p(d)XPS spectra for LaNiO3and Mn0.2Cd0.8S
2.1.5 UV-Vis DRS分析
催化剂的光吸收性能对其光催化反应效率具有较大影响。图5为一系光催化剂在可见光范围内的UV-Vis DRS谱图。从图中可以看出,随着Mn2+的引入,Mn0.2Cd0.8S在可见光区的光吸收强度增强。同时其吸收带边由553 nm蓝移至547 nm,带隙宽度由2.24 eV升高至2.27 eV,这是由于Mn2+离子的引入使得其成核作用增强,由此产生了离子限域效应[23-24]。通过与LaNiO3复合形成异质结构,光催化剂显示出LaNiO3和Mn0.2Cd0.8S的吸光特性,这表明LaNiO3/Mn0.2Cd0.8S异质结光催化剂的成功制备。同时LaNiO3的引入使得催化剂在可见光范围内的吸光度进一步增强,这将会有利于其光催化反应效率的提高。
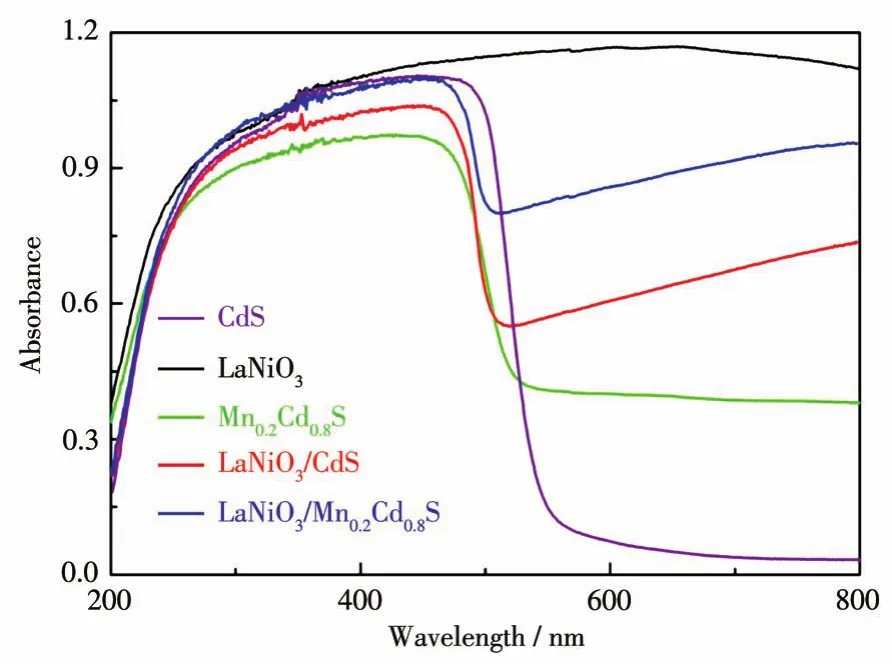
图5 CdS、Mn0.2Cd0.8S、LaNiO3和LaNiO3/Mn0.2Cd0.8S异质结催化剂的UV-Vis DRS谱图Fig.5 UV-Vis DRS spectra of CdS,Mn0.2Cd0.8S,LaNiO3,and LaNiO3/Mn0.2Cd0.8S heterojunction photocatalysts
2.2 光解水产氢性能研究
在可见光(λ≥420 nm)照射下,以三乙醇胺(TEOA)作为牺牲剂,测试催化剂的光解水产氢活性。当以CdS作为光催化剂,其光解水产氢速率为9 μmol·h-1,随着Mn2+离子的引入,其产氢效率提升(图6a)。随着Mn2+离子的引入量达到20%,其产氢活性达到最高(24μmol·h-1)。随着Mn2+离子的引入量进一步提高,其产氢活性降低,这可能是Mn2+离子的过量引入使得其能够作为光生载流子的捕获陷阱,导致光生载流子复合几率升高,从而使得其光催化活性降低。将催化活性最佳的Mn0.2Cd0.8S与LaNiO3复合,合成出不同LaNiO3含量的LaNiO3/Mn0.2Cd0.8S异质结光催化剂,并测试其光解水产氢活性(图6b)。从图中可以看出,随着在Mn0.2Cd0.8S中引入LaNiO3,其产氢活性得到有效提高。当LaNiO3的引入量达到30% 时,LaNiO3/Mn0.2Cd0.8S异质结光催化剂的产氢速率达到了最大值(238μmol·h-1)。然而,随着LaNiO3引入量进一步提高,LaNiO3/Mn0.2Cd0.8S异质结光催化剂的产氢速率降低。这可能有以下2种原因:一是过多的LaNiO3覆盖了Mn0.2Cd0.8S表面的光催化反应活性位点,二是过多的LaNiO3所导致的掩蔽效应阻碍了Mn0.2Cd0.8S的光吸收,从而使得其光解水产氢效率降低。
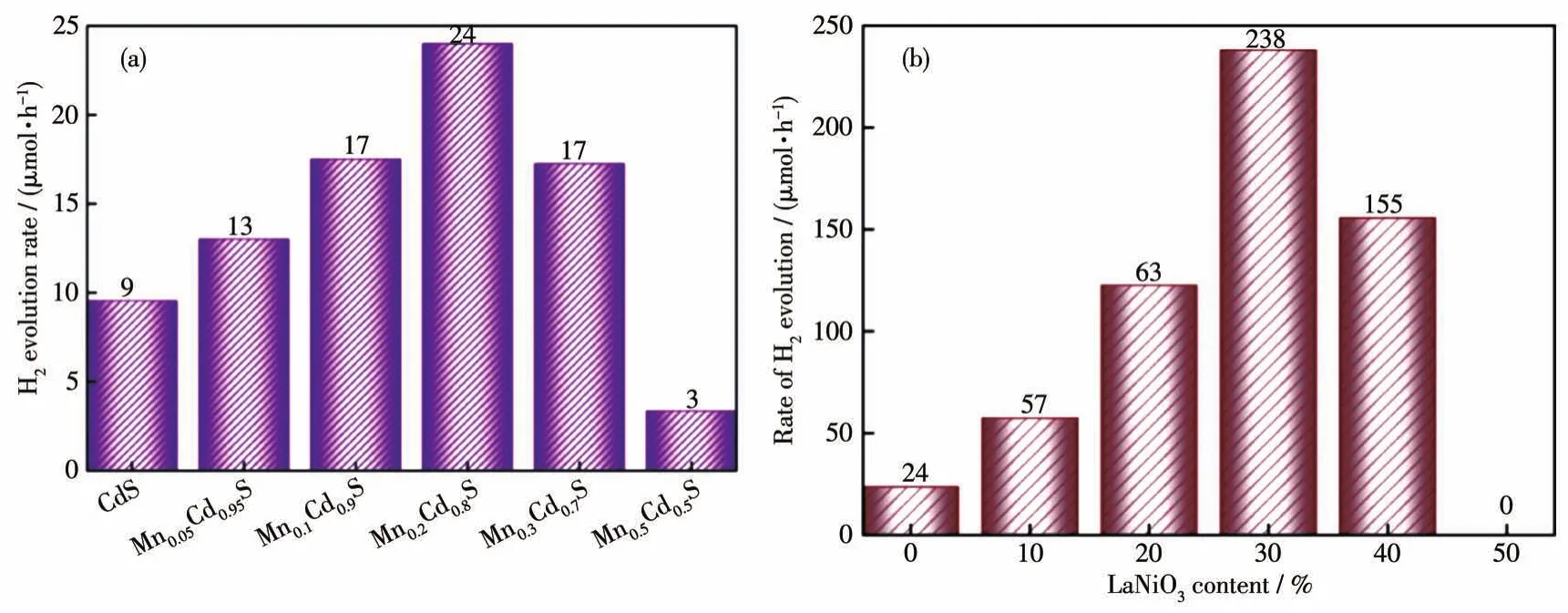
图6 CdS和Mn1-x Cdx S催化剂的产氢活性(a);不同LaNiO3含量的LaNiO3/Mn0.2Cd0.8S异质结光催化剂的产氢活性(b)Fig.6 H2evolution rate over CdS and Mn1-x Cdx Scatalysts(a);H2evolution rate over LaNiO3/Mn0.2Cd0.8S heterojunction photocatalysts with different LaNiO3contents
当以LaNiO3作为光催化剂,并没有H2生成,这表明LaNiO3的光解水产氢惰性(图7)。以CdS作为催化剂时,5 h反应时间内生成47.5μmol H2。而随着Mn元素的引入,H2产量达到118.3μmol,提高了2.5倍,这表明Mn2+离子的引入能够有效地促进其光解水产氢活性的提高。随着LaNiO3的引入,LaNiO3/Mn0.2Cd0.8S异质结光催化剂的光解水产氢性能进一步提高,H2产量高达1 190.3μmol,其产量相较于Mn0.2Cd0.8S和CdS分别提高了10倍和25倍。这一结果表明,LaNiO3的引入能有效地提高其光解水产氢活性。将LaNiO3和Mn0.2Cd0.8S(质量比:3:7)进行机械混合并测试其光解水产氢性能,在相同反应时间内只生成了125.4μmol H2,明显低于LaNiO3/Mn0.2Cd0.8S异质结光催化剂的光解水产氢活性,这证明LaNiO3/Mn0.2Cd0.8S异质结光催化剂中LaNiO3和Mn0.2Cd0.8S之间异质结的构筑在光解水产氢反应中的重要作用。
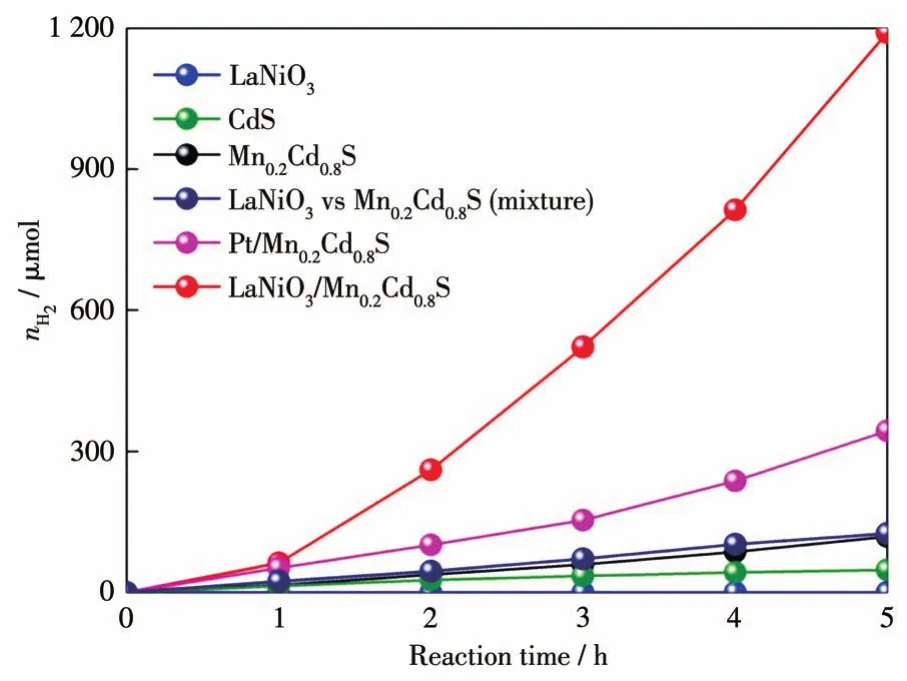
图7 一系列催化剂随时间变化的产氢量图Fig.7 Time-dependent H2evolved over a series of catalysts
以H2PtCl6作为前驱体通过光沉积法制备Pt质量分数1% 的Pt/Mn0.2Cd0.8S,并测试其光解水产氢活性[25-26]。在Pt/Mn0.2Cd0.8S的催化下,相同反应时间内生成了343.3μmol H2,明显低于LaNiO3/Mn0.2Cd0.8S的光解水产氢活性。这一结果表明,LaNiO3的引入能够极大地提高光解水反应效率,甚至高于贵金属Pt的助催化效果,这将有利于LaNiO3在实际生产中的应用。N2吸附-脱附实验已经证实,LaNiO3的引入基本没有影响催化剂的比表面积,因此其催化活性的提高并不是其表面催化反应活性位点数量的变化导致的。
2.3 光电性能测试分析
光生电子-空穴的分离、复合是影响光催化剂光催化反应效率的重要因素,光生电子-空穴的高效分离有利于光催化反应的进行。荧光光谱测试是探测光生电子-空穴分离、复合的有效途径。图8a是催化剂在400 nm激发光下的稳态荧光发射光谱,CdS在500~570 nm范围内有较强的荧光发射峰,这表明CdS中光生电子-空穴的快速复合。Mn2+的引入使Mn0.2Cd0.8S的荧光强度有所降低,说明Mn2+离子能够有效地促进光生电子-空穴的分离,延长光生电子的寿命。同时,随着LaNiO3/Mn0.2Cd0.8S异质结光催化剂中异质结构的构筑,其荧光强度进一步降低,这是由于异质结构的构筑能够有效地提高光生电子-空穴在界面处的迁移、分离,光生电子的寿命进一步得到延长,荧光强度也进一步降低,荧光峰的位移可能是其能带结构的改变导致[27]。因此,Mn2+离子和LaNiO3/Mn0.2Cd0.8S中异质结构的构筑能够有效地延长光生电子的寿命,从而提高其光解水产氢效率。电化学阻抗能直观地显示光生载流子在材料中的传输性能。通过瞬态荧光测试得到CdS的载流子寿命为0.45 ns,Mn2+离子的引入使得其载流子寿命提高至1.00 ns,进一步通过与LaNiO3结合构筑LaNiO3/Mn0.2Cd0.8S异质结光催化剂后,其载流子寿命提高至4.24 ns。这表明Mn2+离子和LaNiO3的引入能有效地提高其光生载流子寿命,有利于其光解水产氢效率的提高。如图8c所示,随着Mn2+的引入,Mn0.2Cd0.8S圆弧半径明显减小,这表明Mn2+的引入确实能降低电荷传输阻力,提高电荷传输效率,降低光生电子-空穴的复合几率。随着LaNiO3的引入,LaNiO3/Mn0.2Cd0.8S异质结光催化剂的圆弧半径进一步减小,这表明LaNiO3/Mn0.2Cd0.8S异质结光催化剂中异质结的构筑能进一步降低电荷传输阻力,促进光生电荷的转移。光电流测试可以研究光生电子-空穴的分离效率。如图8d所示,经过Mn2+的掺杂,Mn0.2Cd0.8S的光电流密度得到提高,这表明Mn2+的引入有利于光生电子-空穴的分离,使得光生载流子寿命延长。进一步通过形成异质结构,LaNiO3/Mn0.2Cd0.8S异质结光催化剂的电流密度进一步得到提高,LaNiO3和Mn0.2Cd0.8S之间异质结构的构筑能够促进光生载流子在界面处的迁移、分离,从而提高光生电子的寿命。以上光电化学测试表征结果证实,LaNiO3/Mn0.2Cd0.8S中Mn2+的引入和异质结的构筑能够有效地促进光生载流子的转移,抑制光生电子-空穴的复合,从而有利于其光解水产氢反应的进行。
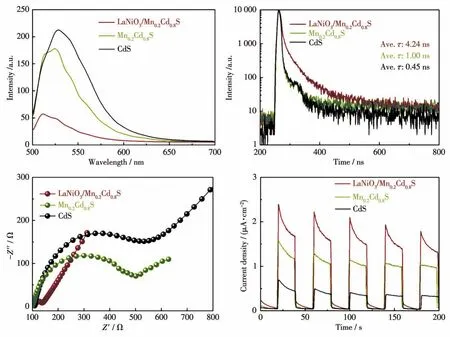
图8 CdS、Mn0.2Cd0.8S和LaNiO3/Mn0.2Cd0.8S的荧光光谱(a)、瞬态荧光光谱(b)、阻抗图谱(c)和瞬态光电流响应曲线(d)Fig.8 Photoluminescence spectra(a),time-resolved photoluminescence spectra(b),electrochemical impedance spectra(c)and transient photocurrent response(d)of CdS,Mn0.2Cd0.8S,and LaNiO3/Mn0.2Cd0.8S
2.4 光催化机理分析
通过测试Mn0.2Cd0.8S和LaNiO3的Mott-Schottky曲线图(图9a和9b),并结合文献报道可知,Mn0.2Cd0.8S的导带、价带位置位于-0.56和1.71 V,LaNiO3的导带、价带位置分别位于0.21和2.12 V[19,28]。因此,我们提出2种可能的反应机理:第一种是传统Ⅱ型异质结构。如图10a所示,在可见光照射下,Mn0.2Cd0.8S价带上的电子激发至其导带上,同时其价带上产生光生空穴。Mn0.2Cd0.8S导带上的电子能够转移至LaNiO3的导带用于H2的生成,而Mn0.2Cd0.8S价带上的空穴转移至LaNiO3的价带。然而LaNiO3的导带位置低于H+/H2的氧化还原电位,其导带上的电子不能还原H+离子生成H2。这一结果排除了LaNiO3/Mn0.2Cd0.8S异质结光催化剂中形成传统Ⅱ型异质结构。因此,我们推测LaNiO3/Mn0.2Cd0.8S异质结光催化剂中形成了直接Z型异质结构(图10b)。在可见光照射下,LaNiO3导带上的电子能够与Mn0.2Cd0.8S价带上的空穴进行复合,从而使光生电子积累在Mn0.2Cd0.8S的导带上用于H2的生成,光生空穴积累在LaNiO3的价带上并由空穴牺牲剂消耗。直接Z型异质结构的构筑能够有效地促进光生-电子空穴的分离,抑制光生电子-空穴的复合,有利于光解水产氢效率的提高。
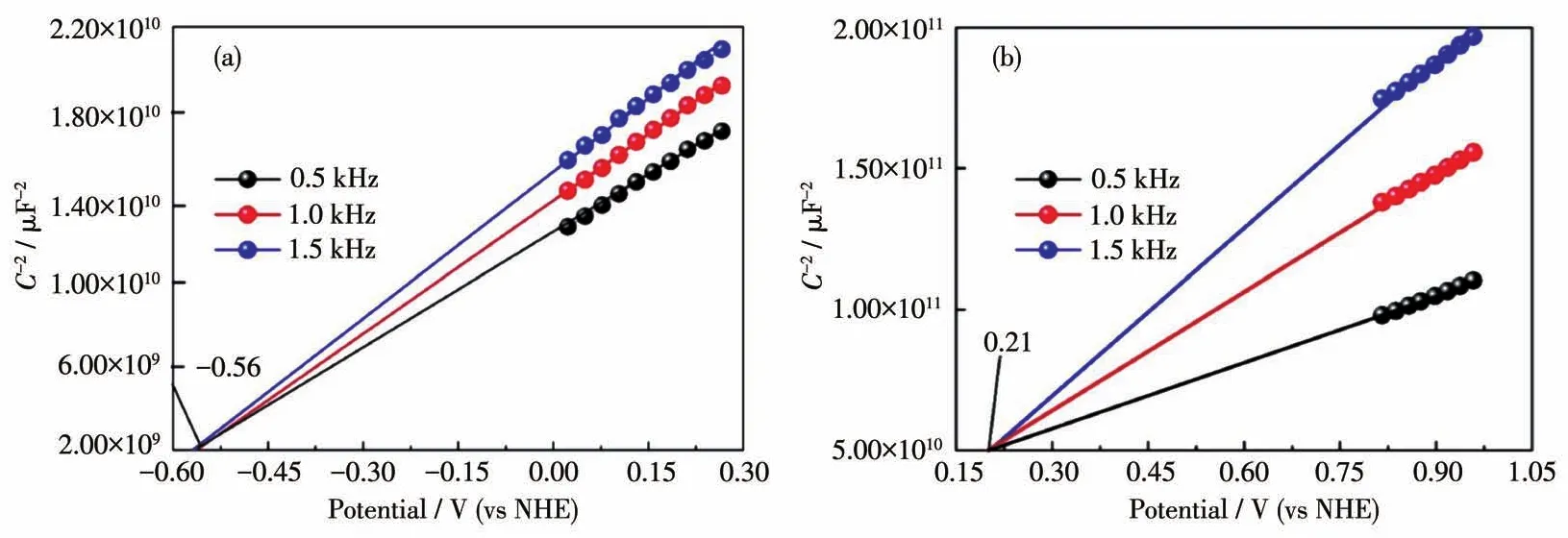
图9 Mn0.2Cd0.8S(a)和 LaNiO3(b)的Mott-Schottky曲线Fig.9 Mott-Schottky plots of Mn0.2Cd0.8S(a)and LaNiO3(b)

图10 直接Z型LaNiO3/Mn0.2Cd0.8S异质结光催化剂在可见光照射下的光解水产氢机理图Fig.10 Proposed mechanism for H2evolution over direct Z-scheme LaNiO3/Mn0.2Cd0.8S heterojunction photocatalysts under visible light irradiation
2.5 循环测试
根据直接Z型异质结的光生电子-空穴转移途径,光生空穴将积累在LaNiO3的价带上,这将抑制光生空穴对Mn0.2Cd0.8S的光腐蚀效应。因此,通过光催化反应循环实验,检测LaNiO3/Mn0.2Cd0.8S异质结光催化剂的结构和活性稳定性,从而进一步证实LaNiO3/Mn0.2Cd0.8S异质结光催化剂中直接Z型异质结的构筑。在光解水产氢循环测试中,4次循环实验后,Mn0.2Cd0.8S光解水产氢的效率降低了33.9% (图11a),这主要是光生空穴对Mn0.2Cd0.8S的光腐蚀导致的。而LaNiO3/Mn0.2Cd0.8S异质结光催化剂在4次光解水产氢反应后,其产氢活性仅仅降低了7.7% (图11b),这表明LaNiO3的引入能够有效地提高LaNiO3/Mn0.2Cd0.8S光解水产氢的稳定性。对循环反应后的催化剂进行XRD表征,从图中可以看出,经过4次光解水产氢反应后,Mn0.2Cd0.8S的XRD图中35.3°处出现一个新的衍射峰,归属于单质硫(PDF No.024-0733,图11c)。而LaNiO3/Mn0.2Cd0.8S在循环反应前后的XRD图并没有显示出明显的差别(图11d)。这一结果证实,LaNiO3/Mn0.2Cd0.8S中直接Z型异质结构的构筑,使得光生电子和空穴分别积累在Mn0.2Cd0.8S的导带位置和LaNiO3的价带位置上,从而抑制光生空穴对Mn0.2Cd0.8S中S2-的氧化,提高Mn0.2Cd0.8S的结构和活性稳定性。
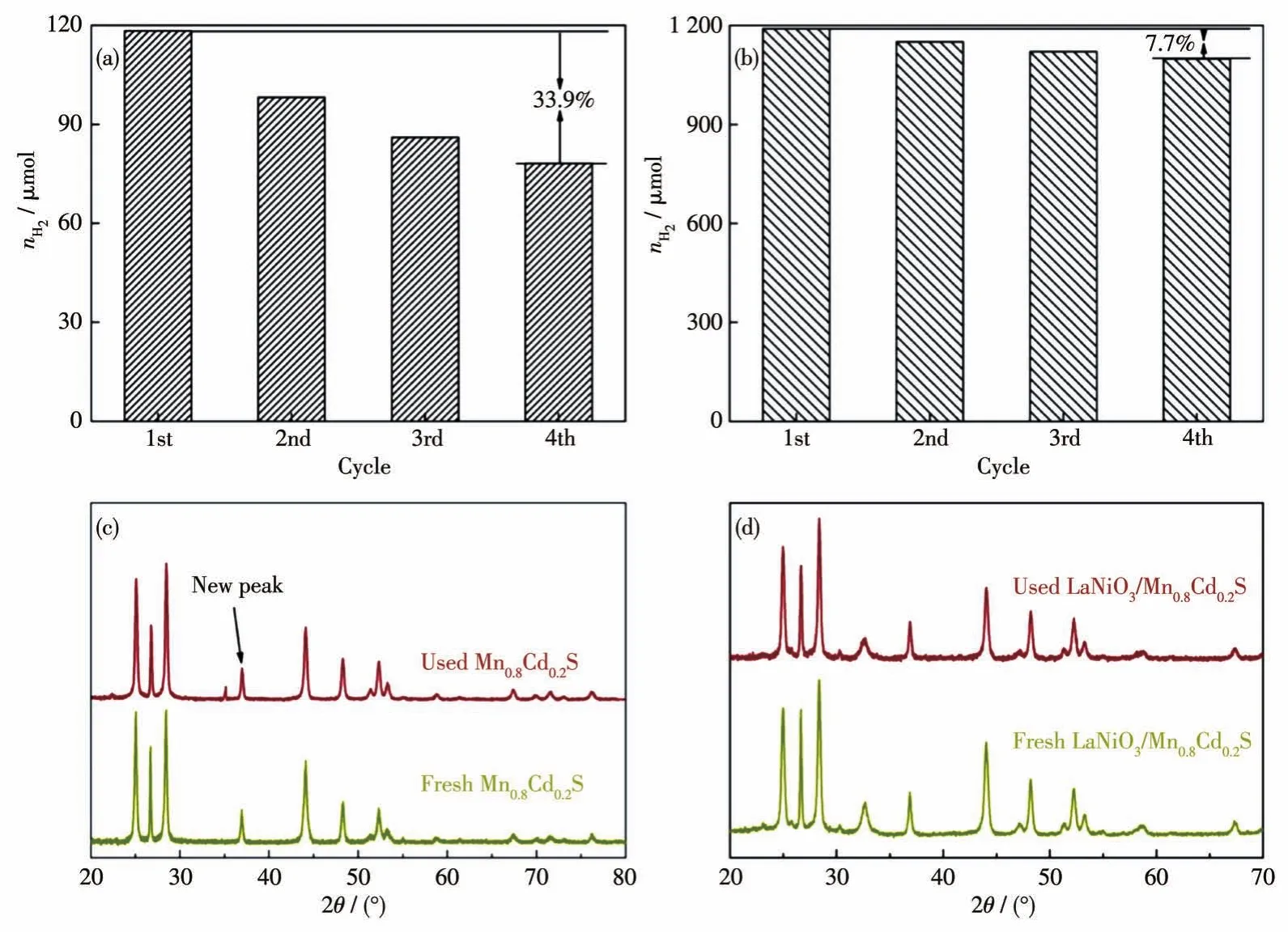
图11 Mn0.2Cd0.8S(a)和LaNiO3/Mn0.2Cd0.8S异质结(b)光催化剂的产氢稳定性测试;循环反应前后Mn0.2Cd0.8S(c)和LaNiO3/Mn0.2Cd0.8S(d)光催化剂的XRD图Fig.11 Cycling runs of Mn0.2Cd0.8S(a)and LaNiO3/Mn0.2Cd0.8S heterojunction(b)photocatalysts for photocatalytic H2evolution;XRD patterns of the used and fresh Mn0.2Cd0.8S(c)and LaNiO3/Mn0.2Cd0.8S heterojunction(d)photocatalysts
3 结 论
通过原位生长的方式制备出LaNiO3/Mn0.2Cd0.8S异质结光催化剂并将其用于光解水产氢反应。相较于CdS和Mn0.2Cd0.8S,LaNiO3/Mn0.2Cd0.8S异质结光催化剂的光解水产氢活性分别提高了25倍和10倍。电化学实验和荧光光谱证实,LaNiO3/Mn0.2Cd0.8S异质结光催化剂中Mn2+离子的引入和异质结构的构筑有利于光生电子-空穴的分离,从而有利于光解水产氢活性的提高。根据LaNiO3能带结构和LaNiO3/Mn0.2Cd0.8S异质结光催化剂的循环测试结果,证实了LaNiO3/Mn0.2Cd0.8S异质结光催化剂中直接Z型异质结构的构筑。该方法能够极大地提高CdS光解水产氢活性,同时有效地抑制其光腐蚀现象,为新型光解水产氢催化剂的设计、合成提供了一种新的思路。
猜你喜欢
杂志排行
无机化学学报的其它文章
- Synthesis,Structures and Catalytic Activity in Knoevenagel Condensation Reaction of Cu(Ⅱ)/Co(Ⅱ)/Ni(Ⅱ) Coordination Polymers Based on Ether-Bridged Tetracarboxylic Acid
- Synthesis and Luminescence Properties of Double Perovskite Ca2Gd1-xTaO6∶xTb3+Green Phosphors
- Carbonized MoS2/S-Doped g-C3N4Heterojunction:Synthesis and Catalytic Degradation Mechanism of Rhodamine B under Visible Light
- I-Assisted Synthesis Erythrocyte-like Bi2WO6with Excellent Adsorption and Photocatalytic Activity
- Preparation of Li2Ni2(MoO4)3@C Composite as High-Performance Anode Material for Lithium-Ion Batteries with High Initial Coulombic Efficiency
- 单分散共价有机框架纳米颗粒的室温快速制备
