C3N4负载CoB催化剂的制备及催化硼氢化物水解制氢性能研究
2021-11-04张迪王雪王艳
张迪,王雪,王艳
科学研究
C3N4负载CoB催化剂的制备及催化硼氢化物水解制氢性能研究
张迪,王雪,王艳*
(沈阳师范大学,辽宁 沈阳 110034)
采用化学沉积的方法在g-C3N4基底材料上制备出二元非贵金属Co-B催化剂,通过调节制备催化剂过程中还原剂浓度条件对样品进行优化,探究该体系的最佳还原剂浓度。结果表明:当还原剂的浓度值为0.6 mol·L-1时,所制备的Co-B/g-C3N4催化剂在硼氢化钠(NaBH4)水解制氢过程中表现出了较高的催化活性,其放氢速率为5 058.5 mL·min-1·g-1。
化学沉积法; 非贵金属; 硼氢化钠; 制氢
众所周知,碳和氮是地球环境中含量最丰富的两种化学元素,氮化碳的研究可以追溯到高分子聚合物氰脲酰胺[1]。此后,一些学者通过理论计算对C3N4的晶体结构进行了研究。推测出C3N4结构中存在5种结构,而g-C3N4则是唯一一个软质相,并且在常温下g-C3N4是5种结构中最稳定的一种。因为在g-C3N4的结构中C和N之间有很强的共价键而作为一种特殊的共轭体系聚合物,因此,与其他聚合物相比,它具有良好的性能稳定性。g-C3N4的结构在600 ℃以下几乎不会有明显变化,但它超过了600 ℃后,C3N4开始分解,结构也发生变化。它在750 ℃左右完全分解,说明g-C3N4具备良好的热稳定性。除了热稳定性,C3N4也有很好的化学性质,在常温常压下,几乎不溶于普通溶剂(如水、丙酮、乙醇等)。这种高稳定性是使得g-C3N4成为一种高效的催化剂先决条件。
同时,随着煤炭、石油和天然气等化石能源的不断消耗以及对生态环境的严重破坏,人们渴望绿色能源的呼声越来越强烈。氢气作为一种新能源,以自身清洁、可再生、高效等独特的优势在新能源中占据着重要的地位。氢能源产业还不具有经济性,氢气的储存和制取问题阻碍了氢能的大范围使用,这是利用氢作为替代能量载体的主要技术障碍[2-5]。如果要实现广泛应用,首先要在源头上减少应用。目前的储氢材料大体两类,一类是化学储氢材料,另一类是物理吸附储氢材料。物理吸附储氢材料就是利用物理吸附将氢气储存在纳米材料中。化学储氢材料包括有机液体储氢材料、储氢配合物与氧化物材料和硼氢化物类储氢材料等。硼氢化钠[6]是目前最受关注的新型化学硼氢化物储氢材料之一,硼氢化钠分子式为NaBH4,白色晶体,是常用的还原剂之一。硼氢化钠在水解制备氢[7]时表现出具有良好的稳定性能,氢气化学性质比较温和,在室温的条件下能催化水解制氢[8],反应原理如下:
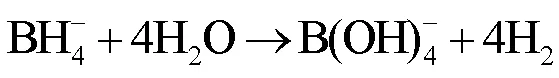
在这个供氢体系中,催化剂是关键材料,研制出性价比高、稳定性高的催化剂成为催化供氢技术的研究重点。目前,催化NaBH4的催化剂大致可以分为三类:贵金属催化剂体系、贵金属与非贵金属复合催化剂体系和非贵金属催化剂体系。目前,贵金属催化剂有Pt、Ph、Ru、Pd、Ir等纳米材料催化剂[9-10],这些贵金属纳米材料催化剂对硼氢化物催化制氢均能有良好的效果。这些贵金属纳米材料催化剂对硼氢化物催化制氢均能有良好的效果,但其价格太过昂贵,不适合工业生产和日常生活需要,这阻碍了其广泛发展;为了降低生产成本,研究人员将贵金属和非贵金属进行组合形成复合催化剂即贵金属与非贵金属复合催化剂体系,这种形式的催化剂在一定程度上提高了储氢材料催化放氢的速率,虽然加入了非贵金属元素使其成本降低,但是由于仍然存在贵金属,必然会增加催化剂的成本,导致催化制氢成本增加。因此,要想从根本上解决制氢成本问题,只有完全使用非贵金属催化剂代替贵金属催化剂催化硼氢化物水解制氢才能实现氢能的广泛应用。
非贵金属Co、Ni、P、Fe及其合金等催化剂在一定条件下也能表现出良好的催化活性,且能够催化硼氢化物水解制氢,最重要的是得到这些非贵金属的成本明显低于Pt、Pd等贵金属催化剂的成本。同时,非贵金属元素之间的协同作用必定会增加表面缺陷,增加表面吸附能力,影响硼氢化物微结构,促使催化剂的催化性能有较大的提高,这对硼氢化物水解制氢的应用具有重大意义。但是非贵金属催化剂相比于贵金属催化剂其放氢速率及放氢量还可进一步提高,反应活化能还可进一步降低,并且非贵金属单质的抗氧化性不强,催化剂稳定性差,经过我国科研工作者在该领域进行的多方面研究得到非贵金属磷化物和硼化物催化剂可以有效增强催化剂的稳定性,提高催化效率。
根据以上结论,本实验具有以下研究特色:(1)本实验采用的元素均为非贵金属元素,对比以往的贵金属催化剂和贵金属与非贵金属复合催化剂,成本降低很多。同时,非贵金属元素之间的协同作用会增加表面缺陷,增加表面吸附能力,影响硼氢化物微结构,促使催化剂的催化性能有较大的提高,这对硼氢化物水解制氢的应用具有重大意义。(2)与其他催化剂相比,石墨相氮化碳拥有独特的半导体能带结构和热稳定性。因此当研究出廉价且催化性能高、稳定性好的催化剂时,便可以广泛地应用于人们的生活中,这会使生活更便捷、环境更友好。
1 实验部分
1.1 0.1g g-C3N4催化剂的制备
称取适量三聚氰胺于陶瓷坩埚中,放入管式炉中设置程序升温5 ℃·min-1升温到550 ℃保持4 h,降至室温时研磨干燥备用。
以g-C3N4为基底材料,首先称取0.1g g-C3N4基底与适量去离子水结合,置于超声波清洗器中
30 min,以获得颗粒均匀的乳浊液。将获得的乳浊液置于磁力搅拌器上,加入CoCl2·6H2O,C2H5NO2,调节pH至12.00后继续搅拌30 min。待温度在25 ℃稳定后,将一定量的还原剂NaBH4加入溶液中。经过不间断搅拌1 h后将所得样品离心,并在烘箱中干燥一整晚,即得到催化剂。
1.2 催化NaBH4制氢性能测试
Co-B/g-C3N4催化剂催化NaBH4水解制氢性能测试实验在圆底烧瓶中进行,所释放出的氢气用水置换法测定。首先配制质量分数为4.7% NaBH4水溶液10 mL于圆底烧瓶中,通过恒温水浴调节至298 K,待温度稳定后加入所制备的Co-B/g-C3N4催化剂进行放氢性能测试,并记录相对应气体的体积。放氢速率的单位为mL·min-1·g-1,表示在单位质量(g)催化剂的作用下,每分钟(min)放出氢气的体积(mL)。
2 结果与讨论
2.1 还原剂浓度值的影响
将在不同还原剂浓度下沉积制备出的Co-B/g-C3N4催化剂用于NaBH4在298 K时的水解制氢。图1显示了还原剂浓度为0.5 mol·L-1时对制备的催化剂催化性能的影响。如图所示,放氢速率为3 698.8 mL·min-1·g-1。
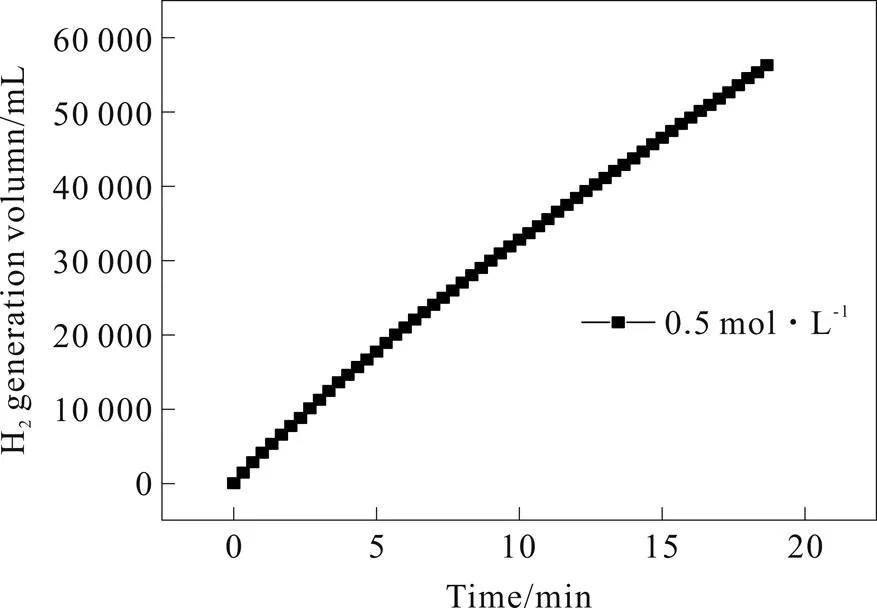
图1 当NaBH4浓度为0.5 mol·L-1时沉积的Co-B/g-C3N4催化剂对NaBH4水解的催化活性
如图2所示,随着还原剂值从0.5 mol·L-1增加到0.6 mol·L-1,放氢反应速率逐渐增加。当还原剂浓度为0.6 mol·L-1时,放氢反应速率最高,为5 058.5 mL·min-1·g-1。
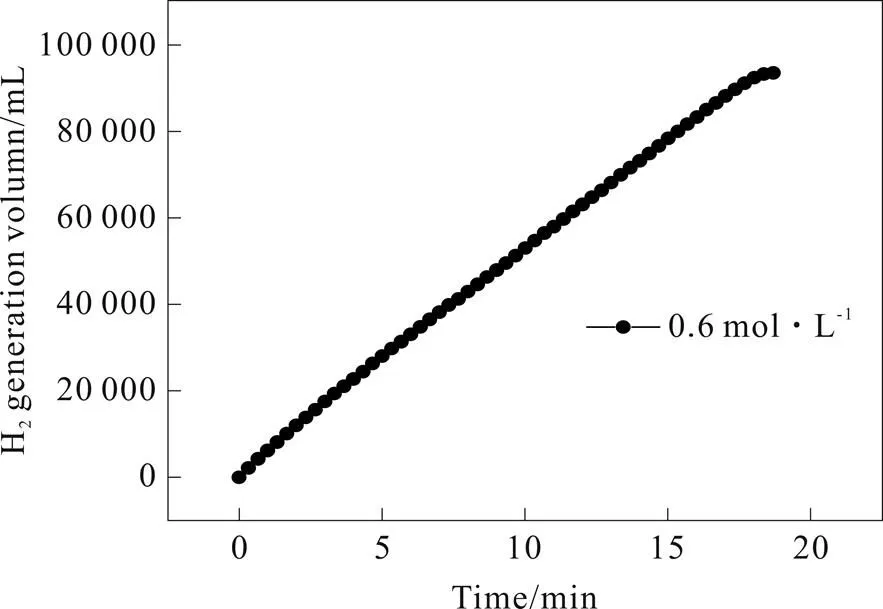
图2 当NaBH4浓度为0.6 mol·L-1时沉积的Co-B/g-C3N4催化剂对NaBH4水解的催化活性
随后,随着还原剂值的进一步增加,氢气生成的速率反而降低,为2 547.7 mL·min-1·g-1,如图3所示。上述结果表明,制备Co-B/g-C3N4催化剂时应当要求适当的还原剂浓度值以达到最佳的催化活性。
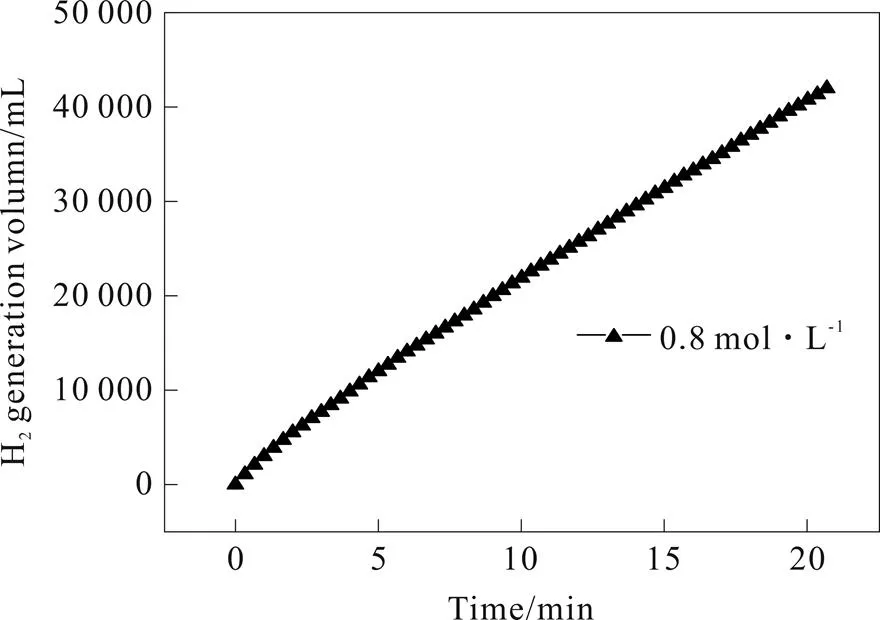
图3 当NaBH4浓度为0.8 mol·L-1时沉积的Co-B/g-C3N4催化剂对NaBH4水解的催化活性
表1总结了其他Co基和贵金属催化剂体系催化NaBH4水解制氢反应的速率情况,可以看出,制备的Co-B/g-C3N4催化剂在催化NaBH4水解制氢过程中产生了较高的速率,该值明显高于部分钴基催化
剂[12-15,17],甚至是部分贵金属催化剂[11,16]。
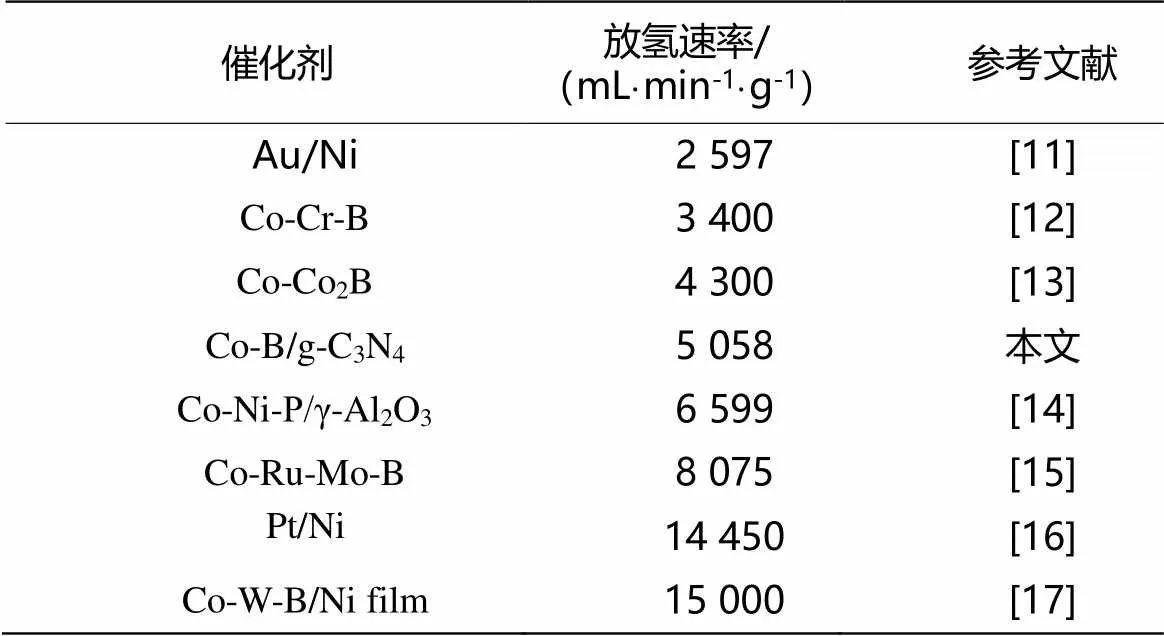
表1 不同催化剂催化NaBH4水解反应的主要参数对比
3 结 论
本文通过简单的化学沉积的方法制备出Co-B/g-C3N4催化剂。结果表明,当温度为25 ℃,沉积时间1h,pH为12.00时,Co-B/g-C3N4在NaBH4水解反应中表现出较高的催化活性。其催化NaBH4水解的最佳放氢速率为5 058.5 mL·min-1·g-1。
[1]GEICK R, PERRY C H, RUPPRECHT G. Normal Modes in a Hexagonal Boron and Nitride[J].., 1966, 146: 543-547.
[2]HE T, XIONG Z, WU G, et al. Nanosized Co- and Ni-catalyzed ammonia borane for hydrogen storage[J].,2009,21:2315-2318.
[3]ZHU Q L, XU Q. Liquid organic and inorganic chemical hydrides for high-capacity hydrogen storage[J].., 2015, 8: 478-512.
[4]LI S, LU Y, GUO L, et al, Hydrogen production by biomass gasification in supercritical water with bimetallic Ni-M/cAl2O3catalysts M=Cu, Co and Sn[J].,2011,36:14391-14400.
[5]QI K, CHENG B, YU J, et al, Review on the improvement of the photocatalytic and antibacterial activities of ZnO[J]., 2017,727:792-820.
[6]余丹梅, 赵家雄, 王丽, 等. 硼氢化钠合成与制备方法的发展现状[J]. 电源技术, 2008, 132 (3):191-193.
[7]徐东彦, 张华民,叶威. 硼氢化钠水解制氢[J]. 化学进展, 2007, 19 (10): 1598-1605.
[8]王书明, 蒋利军, 刘晓鹏, 等. 硼氢化钠催化水解供氢的研究[J]. 电源技术研究与设计, 2006, 130 (10): 810-812.
[9]XU D, ZHANG H, YE W. Hydrogen generation from hydrolysis of alkaline sodium borohydride solution using Pt/C catalyst[J]., 2007, 8 (11): 1767-1771.
[10]ZHAO J, HUA M, CHEN J. Improved hydrogen generation from alkaline solution using carbon-supported Co-B as catalysts[J]., 2007, 32 (18): 4711-4716.
[11]WANG X F, SUN S R, HUANG Z L, et al. Preparation and catalytic activity of PVP-protected Au /Ni bimetallic nanop-articles for hydrogen generation from hydrolysis of basic NaBH4solution[J]., 2014, 39 (2):905-916.
[12]PATEL N, FERNANDES R, MIOTELLO A. Promoting effect of transition metal–doped Co–B alloy catalysts for hydrogen production by hydrolysis of alkaline NaBH4solution[J].,2010,271: 315-24.
[13]VERNEKAR A A, BUGDE S T, TILVE S. Sustainable hydrogen production by catalytic hydrolysis of alkaline sodium borohydride solution using recyclable Co-Co2B and Ni-Ni3B nanocomposites[J].,2012,37: 327-34.
[14]LI Z, LI H L, WANG L N, et al. Hydrogen generation from catalytic hydrolysis of sodium borohydride solution using supported amorphous alloy catalysts (Ni-Co-P/γ-Al2O3)[J].,2014,39: 14935-41.
[15]WANG W, ZHAO Y, CHEN D, et al. Promoted Mo incorporated Co–Ru–B catalyst for fast hydrolysis of NaBH4in alkaline solutions[J].,2014,39: 16202-11.
[16]KONG D C, G J, XIANG S, et al. Preparation of colloidal Pt/Ni bimetallic nanosols and their catalytic activities for hydrogen generation from hydrolysis reaction of sodium borohydride[J]., 2013, 34 (10): 2377-2382.
[17]DAI H, LIANG Y, WANG P, et al. High–performance cobalt–tungsten–boron catalyst supported on Ni foam for hydrogen generation from alkaline sodium borohydride solution[J].,2008,33: 4405-12.
Preparation of C3N4Loaded CoB Catalyst and Its Catalytic Performance forthe Hydrolysis of Borohydride to Hydrogen Production
(Shenyang Normal University, Shenyang Liaoning 110034, China)
A binary non-noble metal Co-B catalyst was prepared on g-C3N4substrate by chemical deposition method. The sample was optimized by adjusting the concentration of reducing agent in the preparation process of the catalyst.The results showed that,when the concentration of reducing agent was 0.6mol·L-1, the prepared Co-B/g-C3N4catalyst exhibited high catalytic activity during the hydrolysis of sodium borohydride (NaBH4) to hydrogen production, and the hydrogen desorbed rate was 5058.5 mL·min-1·g-1.
Chemical deposition method; Non-precious metals; Sodium borohydride; Hydrogen production
国家自然基金面上项目(项目编号:22075186)。
2021-08-04
张迪(1997-),女,辽宁省朝阳市人,2019年毕业于沈阳师范大学化学(师范)专业,研究方向:物理化学。
王艳(1980-),女,副教授,博士,研究方向:新能源材料。
TQ032.41
A
1004-0935(2021)10-1437-04
