胭脂鱼核连蛋白2/Nesfatin-1基因克隆及其在间脑与肝胰脏中的差异表达
2021-11-02苏时萍李卿青谢启明刘帆张君李西雷
苏时萍,李卿青,谢启明,刘帆,张君,李西雷
(安徽农业大学动物科技学院,合肥 230036)
核连蛋白2(nucleobindin-2,NUCB2)经激素原转化酶作用于特定位点后,可裂解产生82个氨基酸的神经肽Nesfatin-1,又称厌食肽[1]。有研究发现,Nesfatin-1发挥主要生物学功能的区域为第23—53氨基酸片段,称为M30[2]。至今,前体NUCB2 已在金鱼(Carassius auratus)[3]、斑马鱼(Danio rerio)[4]和西伯利亚鲟(Acipenser baerii)[5]等鱼类中被成功克隆。NUCB2主要分为信号肽、Nesfatin-1、Nesfatin-2和Nesfatin-3 4 个氨基酸区域,且在人(Homo sapiens)和小鼠(Mus musculus)间有较高的保守性[6]。Nesfatin-1 主要分布于人和其他动物的中枢神经系统如下丘脑室旁核、弓状核、视上核、下丘脑外侧区等部位[7-9],在食道、胃、肝胰脏、肠道、卵巢、心脏等的外周组织中也有丰富表达[3,10-11]。有研究表明,Nesfatin-1 除具有中枢性主动抑制摄食和生殖调控作用[12-13]外,还具有调控葡萄糖代谢[14]、脂肪代谢[13,15]、胃肠道运动[12,16]等重要的生物学功能。对金鱼和斑马鱼禁食后发现,Nesfatin-1 在二者脑中的表达量降低,而在其肝胰脏中的表达量显著增加[3-4],证明Nesfatin-1 在中枢抑制摄食作用下和在被动缺食情况下,会诱发鱼类肝胰脏Nesfatin-1 的高表达,从而促进血糖升高,缓冲体内由食物缺乏造成的代谢压力。
中国胭脂鱼(Myxocyprinus asiaticus),是胭脂鱼属在亚洲的唯一种,为我国Ⅱ级保护动物,仅分布于长江水系和闽江水系[17]。中国胭脂鱼是一种古老的鱼类,在鱼类系统分类学和动物地理研究上有重要的科研价值,并具有极高的经济价值。近年来,环境因素导致胭脂鱼自然种群数量急剧下降,其主要的保护措施是人工放流[18]。虽然胭脂鱼人工驯养与繁殖已取得成功,但由于亲本培育与人工繁殖技术不太成熟,相关理论研究也比较缺乏,造成人工苗种产量不稳定。本研究在克隆中国胭脂鱼NUCB2基因序列、分析其核酸序列和相应的氨基酸序列的基础上,应用实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction,qPCR)技术对Nesfatin-1 在胭脂鱼快速生长期(3龄)和性成熟期(6 龄)的间脑和肝胰脏中的表达变化进行检测,目的是探索Nesfatin-1 在胭脂鱼快速生长期和性成熟期的时空表达差异,为全面研究和揭示鱼类NUCB2 基因的生物学功能提供基础信息,也为深入研究Nesfatin-1 对鱼类不同生长发育阶段调控作用的差异性提供基本素材,为后续进一步完善胭脂鱼亲本培育技术提供基本信息资料。
1 材料与方法
1.1 试验材料
本试验所用3 龄[(2.1±0.29)kg]和6 龄[(5.32±0.47)kg]各6尾的雌性胭脂鱼均采自中国水产科学研究院长江水产研究所(湖北省荆州市)养殖基地。解剖前用0.05%的鱼用麻醉剂间氨基苯甲酸乙酯甲磺酸盐(MS-222)(美国Sigma-Aldrich公司)浸泡麻醉5 min,取供试的12 尾胭脂鱼左半侧脑和肝胰脏组织,分别浸没于含RNAstore[天根生化科技(北京)有限公司]无核酸酶冻存管中,先后分别于4 ℃与-20 ℃条件下保存24 h后,置于-80 ℃冰箱中保存,用于总RNA 提取;将摘取的右半侧脑和剩余的肝胰脏组织置于4%多聚甲醛(北京索莱宝科技有限公司)中,固定24 h后,分别转入30%蔗糖溶液和80%乙醇溶液中,于4 ℃条件下保存,待用。
1.2 试验方法
1.2.1 总RNA 的提取与第1 链cDNA 的合成
使用RNAiso Plus 试剂盒(日本TaKaRa 公司),按其说明步骤,分别从胭脂鱼脑和肝胰脏组织中提取总RNA,经超微量分光光度计(北京凯奥科技发展有限公司)和1%琼脂糖凝胶电泳检测浓度和完整度后,用PrimeScriptTMRT 试剂盒(日本TaKaRa公司)合成cDNA,待用。根据SMARTer®RACE 5′/3′试剂盒和3′-Full RACE Core Set with PrimeScriptTMRTase试剂盒(日本TaKaRa公司)操作说明,以RNA为模板反转录合成各自第1 链cDNA,作为后续cDNA 末端快速扩增(rapid amplification of cDNA ends,RACE)的模板。
1.2.2 NUCB2 基因的完整cDNA 克隆
根据NCBI(https://www.ncbi.nlm.gov/pmc)中已知的斑马鱼NUCB2(NM_201493.1)序列,由Primer Premier 5.0软件设计同源引物NUCB2-F和NUCB2-R(表1),扩增胭脂鱼NUCB2 的部分序列,经1%琼脂糖凝胶电泳后,用凝胶回收试剂盒[天根生化科技(北京)有限公司]回收纯化DNA并测序。根据已测序列,使用Primer Premier 5.0软件设计5′和3′的RACE 引物NUCB2-5R 和NUCB2-3F(表1),依据上述方法中所得的cDNA 为模板,按照SMARTer®RACE 5′/3′试剂盒和3′-Full RACE Core Set with PrimeScriptTMRTase 试剂盒操作说明完成后续聚合酶链反应(polymerase chain reaction, PCR)扩增,获得胭脂鱼NUCB2的5′和3′序列。将RACE PCR扩增片段回收纯化后,连接到pMD19-T 载体(日本TaKaRa公司)上,转化至大肠埃希菌DH5α感受态细胞[天根生化科技(北京)有限公司]中,然后涂布于含有氨苄青霉素、5-溴-4氯-3-吲哚-β-D-吡喃半乳糖苷(5-bromo-4-chloro-3-indolyl-β-D-galactoside,X-Gal)、异丙基-β-D-硫代半乳糖苷(isopropyl-β-D-thiogalactopyranoside, IPTG)[天根生化科技(北京)有限公司]的LB(Luria-Bertani)培养基上,挑取白色阳性单菌落进行测序。各序列经验证后,用Contig Express 软件进行拼接,得到胭脂鱼NUCB2完整cDNA 序列。最后设计扩增完整开放阅读框(open reading frame, ORF)的引物NUCB2-cF 和NUCB2-cR(表1)来验证胭脂鱼NUCB2基因cDNA的完整性。本试验涉及的引物合成与核酸测序均由上海桑尼生物科技有限公司完成,所涉及的引物见表1。
1.2.3 NUCB2 序列分析
对于获得的胭脂鱼NUCB2完整cDNA序列,首先通过NCBI BLAST(http://www.ncbi.nlm.nih.gov/BLAST)对比其核苷酸序列的一致性,再由NCBI ORF finder 在线分析工具(https://www.ncbi.nlm.nih.gov/orffinder/)预测胭脂鱼NUCB2 的完整开放阅读框,找出起始密码子和终止密码子等基本生物学信息,并用NCBI BLASTP(https://blast.ncbi.nlm.nih.gov/Blast.cgi)对比氨基酸一致性;运用SignalP 4.1 服务器(http://www.cbs.dtu.dk/services/SignalP/)在线预测氨基酸序列的信号肽和前肽裂解位点;用ExPASy-ProtParam工具(https://web.expasy.org/protparam/)在线预测NUCB2 总分子量、理论等电点(isoelectric point, pI)、多肽疏水性和蛋白质组成;用ProP 1.0(http://www.cbs.dtu.dk/services/ProP/)在线预测是否存在前肽裂解位点;运用Clustal X和DNAman软件对序列进行多重比对,使用MEGA 5.0 软件的邻接(neighbor joining,NJ)法构建系统进化树。
1.2.4 实时荧光定量PCR
按照1.2.1 节的方法提取胭脂鱼肝胰脏和脑组织总RNA,根据TransScript All-in-One cDNA supermix for qPCR 试剂盒(北京全式金生物技术有限公司)说明完成第1 链cDNA 反转录,用GoTaq qPCR Master Mix(美国Promega 公司)完成后续qPCR试验。根据序列同源性,选择18S作为参考基因,相关引物见表1。使用荧光定量PCR仪[赛默飞世尔科技(中国)有限公司]进行扩增反应。每个组织均重复试验3 次,基因的mRNA 相对表达量应用2-ΔΔCT法进行分析计算。

表1 引物序列及作用Table 1 Primer sequences and function
1.2.5 免疫组织化学分析
将肝胰脏组织切成5 μm的薄片,由武汉塞维尔生物科技有限公司完成。将胭脂鱼脑组织块从30%蔗糖中捞出,用0.01 mol/L 磷酸缓冲液(phosphate buffered solution,PBS)冲洗以去除多余液体,然后放在滤纸上吸干水分,腹面向上,进行间脑修整,把修整后的间脑平整地放在含已经冻凝的OCT包埋剂(聚乙二醇和聚乙烯醇水溶性混合物)托盘上,滴加OCT,以覆盖整个组织为准,再放入CMl900恒温冷冻切片机(德国Leica公司)操作台上冷冻15 min;然后将放有组织块的托盘放在冷冻探头上,调整角度,对脑组织进行匀速冠状切片,厚度为40 μm;用勾线笔轻挑起切片并放入盛有冷的0.01 mol/L PBS(pH 7.4)的6 孔板中,平衡30 min 后放入4 ℃冰箱中保存,1个月内分析完成。
将肝胰脏组织切片用梯度乙醇脱蜡、复水后,放入含有0.1 mol/L、pH 6.0 的柠檬酸修复液的盒中(修复液没过切片),然后放入微波炉中以100 W功率保持修复液微沸15 min,充分修复后,取出切片,自然冷却20~30 min至室温,待用。用钝性柔和的小钩(自制针灸针)从6 孔板中捞取5 个脑冰冻切片,轻放入24 孔晶体板的一个小孔内,每孔加0.01 mol/L PBS 500 μL,浸泡5 min,然后依次转入另外3孔,洗涤3 次。分别向脑组织和肝胰脏组织切片上滴加1%辛基酚聚氧乙烯醚(Triton)和10%山羊血清,孵育20 min 后,弃血清,滴加Nesfatin-1(美国R&D 公司)一抗(1∶100),置于湿盒内4 ℃孵育过夜,弃一抗,用PBS 洗5 次,每次5 min,然后滴加0.3%Triton-Alexa Fluor®488 驴抗山羊IgG(H+L)(英国Abcam 公司)二抗(1∶200),于37 ℃避光孵育2 h后,避光洗5次,每次5 min。用丙三醇溶液进行封片,在相同的电压和激光强度下,参照BERNIER等[19]的方法对胭脂鱼间脑核团在FV10-ASW2.0 激光共聚焦显微镜(日本奥林巴斯公司)下进行定位观察并拍照;阴性对照分别是与一抗同源的IgG,荧光标志物对照是PBS加二抗。通过预吸收法[20]进行Nesfatin-1抗体特异性试验。根据克隆的中国胭脂鱼Nesfatin-1 的基因序列(GenBank 登录号:MK962319),设计特异性引物来扩增目的基因序列(编码Val24—Leu105,N-末端),用双酶切法将其构建到原核表达载体PET32a 上,将重组载体命名为PET32a-Nesfatin-1,进而转入大肠埃希菌Rostta(DE3)中进行蛋白表达,并利用镍柱进行蛋白纯化,通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDA-PAGE)进行鉴定。最后,以验证后的胭脂鱼Nesfatin-1蛋白与一抗Nesfantin-1进行孵育、吸收,其被完全吸收的质量浓度为38.2 mg/mL。
1.3 数据统计与分析
试验所得数据用平均值±标准差表示。mRNA表达量以18S为内参基因,结果为相对表达量。用SPSS 19.0 统计软件对Nesfatin-1 在3 龄和6 龄胭脂鱼脑和肝胰脏内的相对表达量进行单因素方差分析,P<0.05 表示差异有统计学意义,P<0.01 表示差异有高度统计学意义。
2 结果
2.1 中国胭脂鱼NUCB2 基因全长序列分析及蛋白质结构预测
由NCBI ORF finder 在线分析工具预测得到:NUCB2 cDNA 全长2 090 bp,由长99 bp 的5′非翻译区、1 449 bp 的开放阅读框和542 bp 的3′非翻译区组成,其中,3′非翻译区还含有典型的AATAAA加尾信号。该蛋白由482 个氨基酸残基编码组成。用SignalP 4.1 服务器预测发现,NUCB2 有一个由23 个氨基酸组成的信号肽区(图1)。用ExPASy-ProtParam 工具预测表明,NUCB2 分子量为56 632.07,理论等电点(pI)为4.96,亲水性平均值为-1.141(小于0),说明其为亲水蛋白。NUCB2蛋白组成中谷氨酸(Glu,E)最多,占13.7%,其次是亮氨酸(Leu, L),占10.0%,未见吡咯赖氨酸(Pyl,O)和硒半胱氨酸(Sec,U)。用ProP 1.0预测的结果显示,赖氨酸(Lys,K)106-精氨酸(Arg,R)107和赖氨酸(Lys, K)179-精氨酸(Arg, R)180 可能是2 个潜在的前肽裂解位点,它们将除信号肽区外的NUCB2区域分割成长度为82个氨基酸的Nesfatin-1(24~105)、71 个氨基酸的Nesfatin-2(108~178)和302 个氨基酸的Nesfatin-3(181~482)3 个功能区域。

图1 中国胭脂鱼NUCB2的核苷酸和氨基酸序列分析Fig.1 Nucleic acid and amino acid sequence analysis of NUCB2 in Myxocyprinus asiaticus
2.2 NUCB2 同源性比对分析
多重序列比对结果(图2)显示,胭脂鱼NUCB2和其他物种NUCB2 序列均含有20~35 个氨基酸序列的信号肽区域,均有2 个前肽裂解位点将其后序列分割成Nesfatin-1、Nesfatin-2 和Nesfatin-3 3个结构域。在这3个结构域中,长度为82个氨基酸的Nesfatin-1 在第37—49、77—79 号位点连续不保守;在Nesfatin-2 中,鱼类和哺乳类的氨基酸比其他2 个区域更为保守,但哺乳类在第17、18 号位点氨基酸缺失,导致这一区域的鱼类均有71 个氨基酸,而哺乳类的氨基酸只有69个;Nesfatin-3是3个结构域中氨基酸数量最多且差异最大的,从405 号位点以后氨基酸序列不一致,到410 号位点后在哺乳类中均出现一段无氨基酸的对比空白(以人序列为参考)。

图2 中国胭脂鱼NUCB2氨基酸序列同源性比对Fig.2 Homology alignment of NUCB2 amino acid sequences in M.asiaticus
2.3 NUCB2 进化树分析
选取NCBI中已知的NUCB2氨基酸序列,利用MEGA 5.0 邻接法(NJ 法)与胭脂鱼NUCB2 推测的氨基酸序列进行系统发育分析。结果表明,鸟类和哺乳类聚为一支,鱼类中同属鲈形目的罗非鱼(Oreochromis niloticus)和青鳉(Oryzias latipes)聚为一支,胭脂鱼NUCB2 先与斑马鱼(D.rerio)聚为一小支,再与同为鲤形目的白鱼(Anabarilius grahami)、重口裂腹鱼(Schizothorax davidi)和银鲫(Carassius gibelio)聚为一大支(图3)。
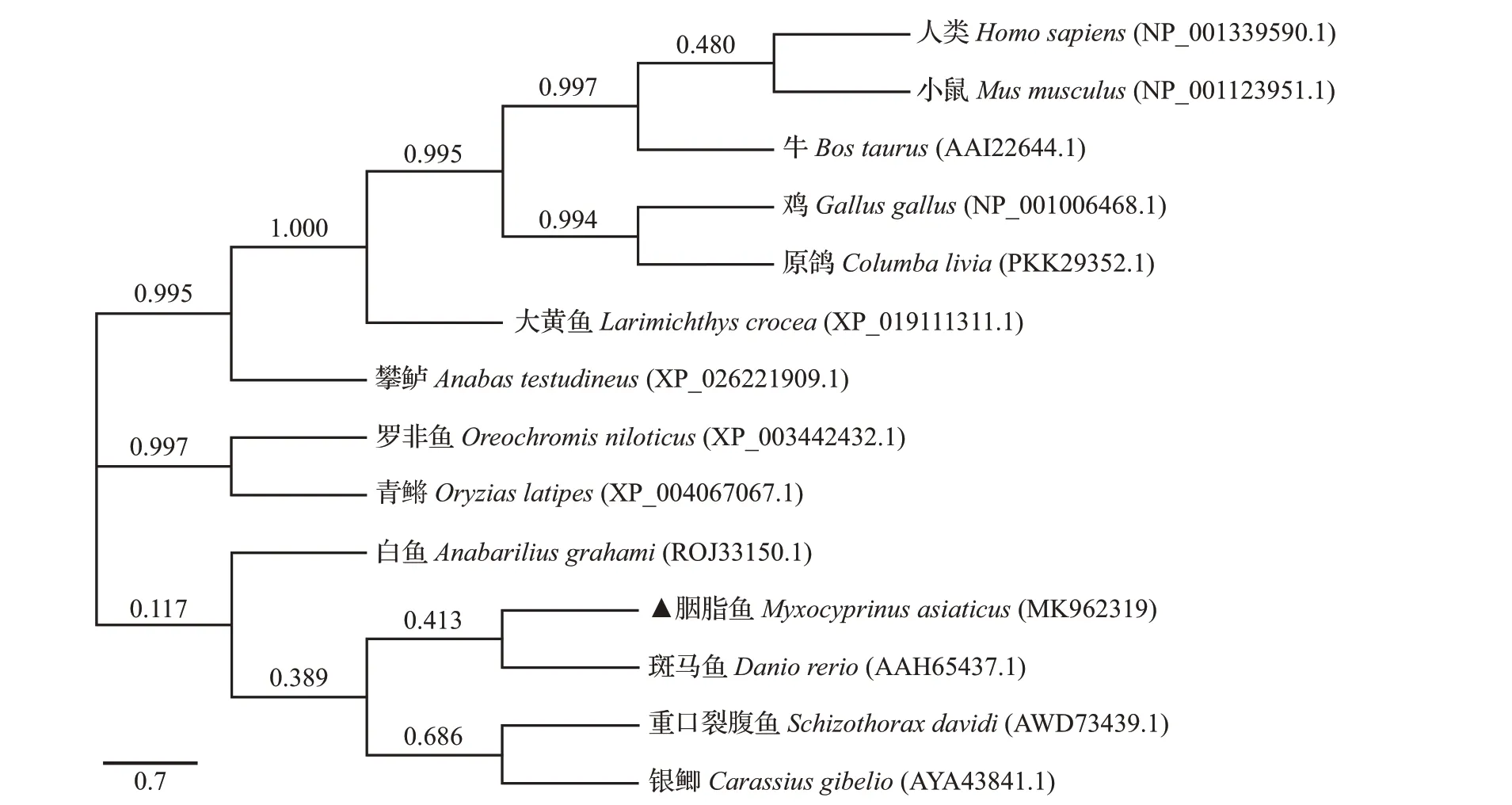
图3 基于不同物种NUCB2氨基酸序列构建的系统发育树Fig.3 Phylogenetic tree based on multiple alignments of NUCB2 amino acid sequences from various species
2.4 Nesfatin-1在胭脂鱼脑和肝胰脏中的差异表达
由图4 可见:在胭脂鱼3 龄和6 龄2 个阶段,Nesfatin-1在脑中的转录表达均极显著低于在肝胰脏中的表达(P<0.01),而Nesfatin-1 在肝胰脏或脑中的转录未表现出明显的年龄差异(P>0.05)。以原核表达的胭脂鱼Nesfatin-1蛋白为抗原,经SDSPAGE鉴定表明,其抗体具有特异性(图5)。免疫荧光结果(图6)显示:Nesfatin-1 蛋白表达在3 龄和6龄胭脂鱼的肝胰脏中均呈强阳性反应(图6A),而在间脑内的几个核团区均呈弱阳性反应(图6C);在肝胰脏中,Nesfatin-1主要由米粒状的胰腺细胞分泌,而在肝细胞中未见有阳性反应(图6B);在控制摄食区的间脑中,在结节外侧核、室周前核和室前核的少数大神经元细胞中有Nesfatin-1 分泌,而在小神经元细胞中未见有阳性反应(图6C和图6D)。
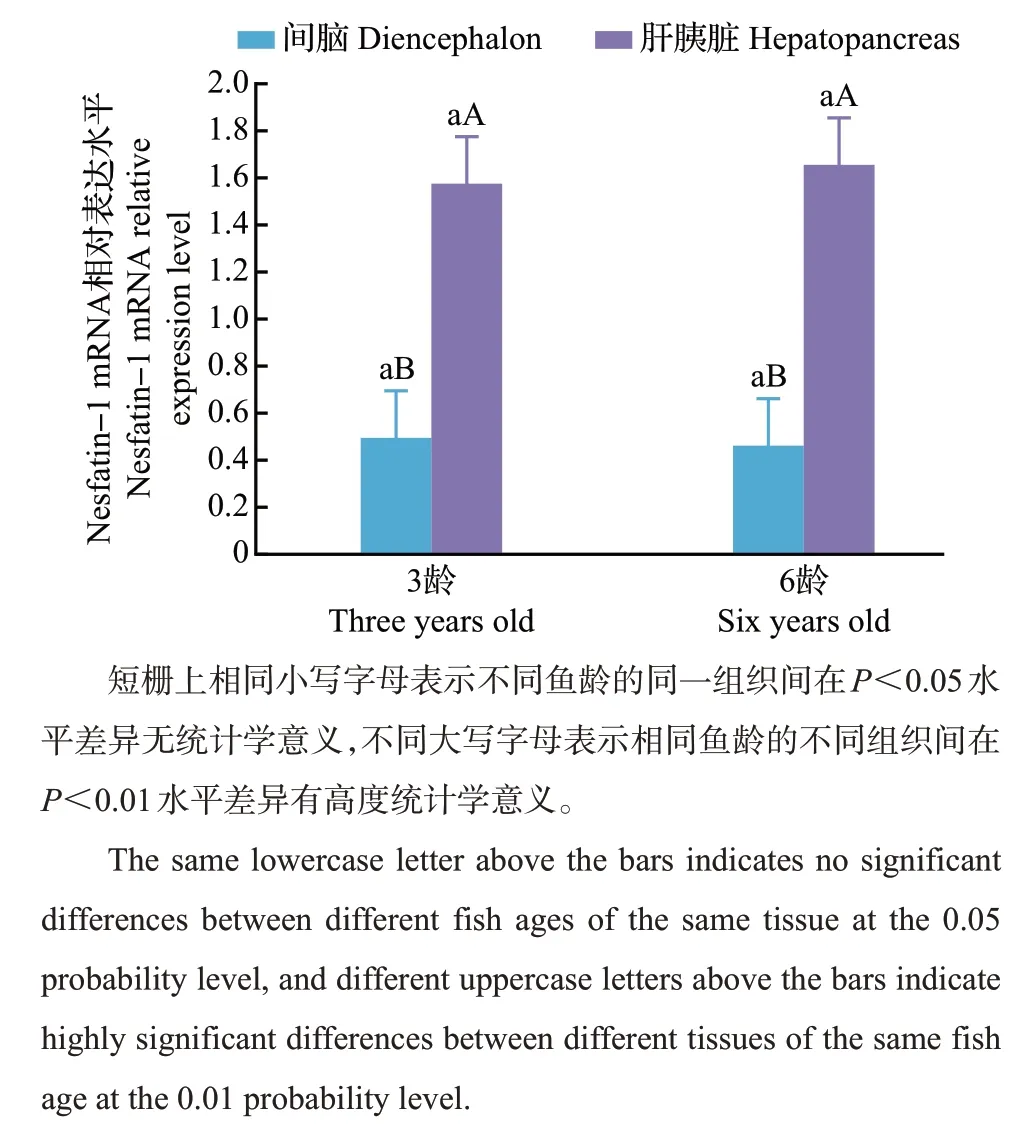
图4 Nesfatin-1 mRNA在2个发育期胭脂鱼间脑和肝胰脏中的相对表达水平Fig.4 Relative expression levels of Nesfatin-1 mRNA in the diencephalon and hepatopancreas of two developmental stages of M.asiaticus

图5 胭脂鱼Nesfatin-1原核表达蛋白的SDS-PAGE鉴定Fig.5 SDS-PAGE identification of prokaryotic expression protein Nesfatin-1 of M.asiaticus
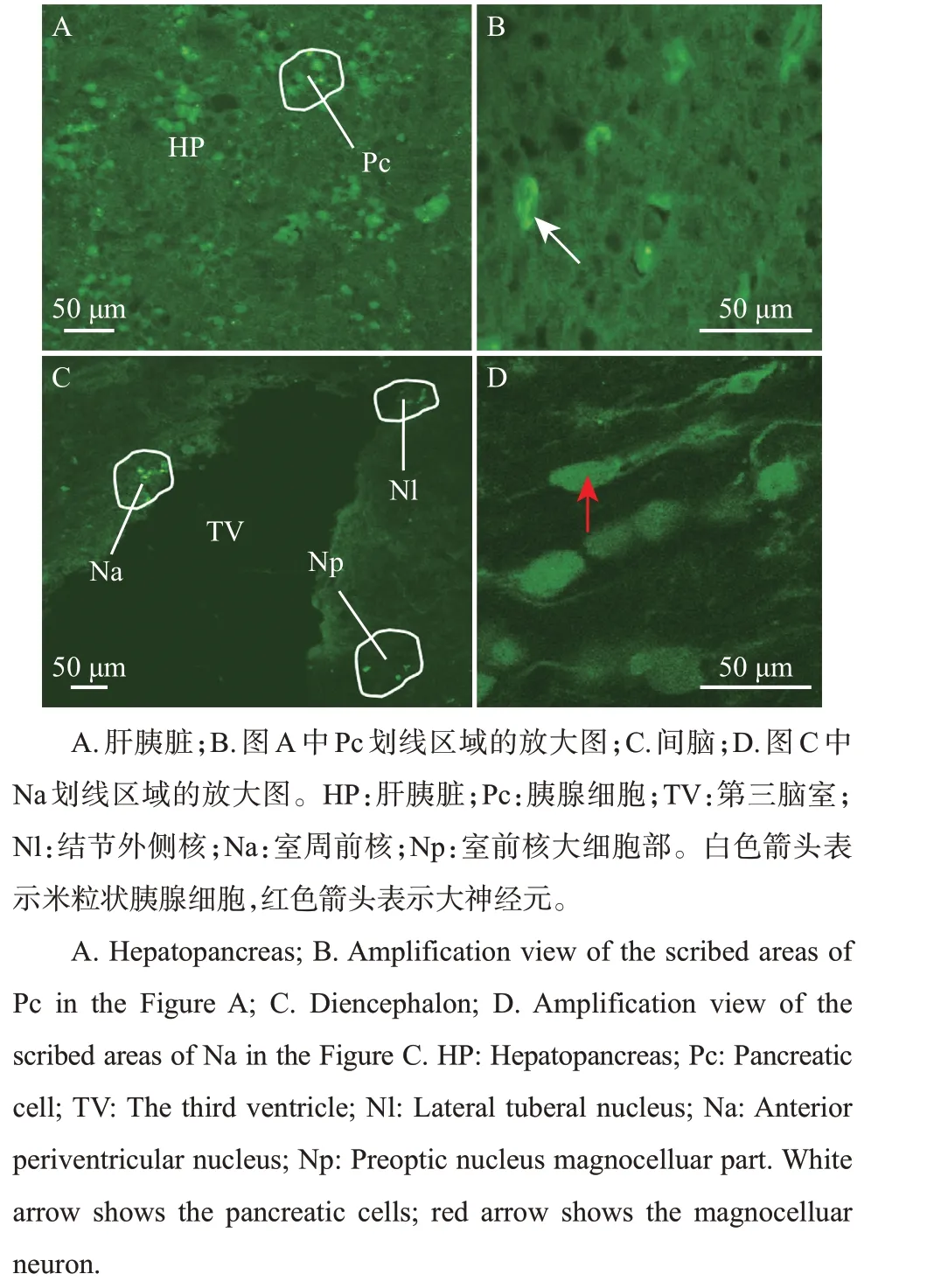
图6 Nesfatin-1在中国胭脂鱼间脑及肝胰脏中的分布Fig.6 Distribution of Nesfatin-1 in diencephalon and hepatopancreas of M.asiaticus
3 讨论
本研究克隆了中国胭脂鱼NUCB2 基因的完整cDNA序列(MK962319)。通过核酸序列比对发现,胭脂鱼NUCB2 的核酸序列与银鲫(C. gibelio)、斑马鱼(D.rerio)、重口裂腹鱼(S.davidi)的一致性分别高达88.40%、87.58%和85.50%,与鸟类和哺乳类相似度较低。氨基酸一致性对比得出,胭脂鱼NCUB2 与斑马鱼的一致性高达85.69%,与重口裂腹鱼和银鲫的一致性分别为85.28%和83.88%。从系统发育树也可以看出,胭脂鱼与鲤形目鱼类聚在一起,在鲤形目中NUCB2 核酸和氨基酸具有高保守性,推测其生物学功能在鲤形目中也高度保守。
胭脂鱼NUCB2 的氨基酸序列中有2 个前肽裂解位点和1个信号肽,将整个基因分成4个区域,这与已知的其他脊椎动物的NUCB2结构相同。胭脂鱼NUCB2在进化树中与哺乳类和鸟类不聚集,但氨基酸多重序列比对结果显示,它们在Nesfatin-1 区域都有82个氨基酸,且在Nesfatin-124-53(M30)核心功能区域[2]中,人类、牛(Bos taurus)、小鼠等哺乳动物和鸟类M30 区域仅在Nesfatin-135和Nesfatin-1392个位点中度保守,在Nesfatin-145位点不保守,其余位点均高度保守[20-23],支持了NUCB2的M30区域在脊椎动物中高度保守,且可能存在诸多相似生理功能的观点。在鱼类中,鲤形目鱼类的M30区域完全一致,但与鲈形目存在7 个不保守位点和3 个中度保守位点。M30 区域在哺乳类和鱼类中氨基酸序列的各自保守性和差异性,说明Nesfatin-1 在哺乳类和鱼类中的功能存在共性,也存在一定的物种特异性。
上述基因结构分析证明,Nesfatin-1 的摄食抑制功能具有明显的物种、组织和时间特异性。自OH-I 等[1]第一次发现脑注射Nesfatin-1 对鼠摄食的抑制作用后,随着对Nesfatin-1 生理功能的深入探究,发现其在多种动物的中枢器官和外周器官中广泛表达,表明Nesfatin-1 可能具有除抑制摄食外的多种生物学功能[14,24-25]。如糖代谢调节功能,在雌鼠体外试验中,随着葡萄糖浓度升高,其胃细胞中Nesfatin-1 浓度升高[26];在金鱼肠细胞体外试验中,随着葡萄糖浓度上升,Nesfatin-1下调表达[15]。证明Nesfatin-1在脊椎动物糖代谢调节中具有明显的物种和组织特异性。对大鼠禁食后再饲喂,Nesfatin-1在其脑组织中的表达呈现明显的先降后升变化,而在肝脏中的表达则明显上升[27];对金鱼禁食后发现,其脑部Nesfatin-1表达下降,但在肝脏中Nesfatin-1则呈显著上调表达[3],显示Nesfatin-1 的抑制摄食功能主要依赖于中枢调节,而肝脏则可能是对外源饥饿的条件刺激进行反馈调节的主要器官,即Nesfatin-1的代谢调节具有明显的组织特异性。同时,本研究结果也证实,Nesfatin-1在胭脂鱼脑和肝胰脏中存在明显的时空表达差异。
有研究发现,Nesfatin-1与性腺发育相关,特别是对启动初情期的调控有一定的作用,如在初情期雌性小鼠的卵巢和卵泡中检测到Nesfatin-1蛋白的表达,在初情期雌性大鼠(Rattus norvegicus)中,Nesfatin-1在下丘脑上调表达[12],证明Nesfatin-1对鼠初情期性腺发育有促进作用。然而,对金鱼和斜带石斑鱼(Epinephelus coioides)腹腔注射Nesfatin-1,显著降低了其性激素的分泌[25,28],表明在初情期鱼类中外周性Nesfatin-1 起主要作用,负责此阶段性腺发育过程中的能量累积,并对中枢性Nesfatin-1 促性腺发育功能起一定的负反馈调节作用。本研究中,Nesfantin-1在初情期(6龄)和初情期前期(3龄)胭脂鱼体内表达均是外周性高于中枢性,与上述结果类似。此外,Nesfatin-1在快速生长期(初情前期和初情期)胭脂鱼的胰腺细胞中大量分泌,发挥重要的刺激代谢的作用,可能是为了满足快速生长期大量的能量累积需求;而其在间脑中的分泌位置比较广泛,且表达量比较低,说明此阶段中枢性Nesfatin-1 的功能也比较复杂,其抑食作用和促生殖作用可能由不同的脑功能区进行控制,其准确的功能定位有待深入探究。
在脊椎动物中未见对Nesfatin-2 和Nesfatin-3特定功能的研究。本试验中多重序列比对结果显示,Nesfatin-2 在脊椎动物中的高保守性区域也是一段古老的区域,说明它在脊椎动物中的生物学功能也可能是保守的。而Nesfatin-3 在405 号位点前保守性较高,直到第410号位点,哺乳动物相较于鱼类出现了一段氨基酸空白,这一段空白可能揭示了Nesfatin-3 在生物从低等进化到高等的过程中,氨基酸数量开始减少,功能可能也随之发生改变。
4 结论
本研究克隆了中国胭脂鱼的NUCB2 基因的完整序列,并通过基因序列和氨基酸序列分析,发现其核酸序列在鱼类中高度保守,与羊膜动物的保守性较低,但其核心序列M30/Nesfatin-1 却有高度保守性;另外,根据不同断裂位点,分析得出Nesfatin-2和Nesfatin-3 2个肽段,其生物学功能还有待进一步研究。同时发现,核心肽Nesfatin-1 在中国胭脂鱼生长期和性成熟初期的中枢和外周组织中存在明显的表达和分布差异,但时间差异不明显,可能与生长期与性成熟初期均为胭脂鱼大量摄食期有关,更科学的生长期划分还需要以其他鱼类为对象进一步深入研究,以免造成长江胭脂鱼资源损耗。
