儿童耳前瘘管切除术不同手术方式的疗效观察*
2021-11-02夏忠芳夏志杰汪在华
李 隽,夏忠芳,姚 薇,夏志杰,张 艳,黄 珊,汪在华
华中科技大学同济医学院附属武汉儿童医院耳鼻咽喉科,武汉 430016
先天性耳前瘘管是第一、二鳃弓小丘样结节在胚胎发育时融合不全,由上皮细胞内陷所形成,是临床最常见的儿童头面部发育畸形。1864年,学者Heusinger首次对先天性耳前瘘管病例进行报道,文献报道其患病率约为10%~14%[1],如瘘管没有感染,一般无需特殊处理,一旦合并瘘管感染,手术切除则是首选治疗方案。
耳前瘘管临床特征多样,瘘口可位于耳轮脚前,也可见于外耳道、耳轮后上边缘、耳垂、耳屏、耳轮脚起始部和耳廓的上部或背侧区域。反复的瘘管感染史和手术切排史,导致术区皮肤条件好坏不一,瘘口周围皮肤常呈发红、瘢痕、肉芽增生甚至瘘道形成等改变。针对复杂的瘘管情况,为了能既完全切除瘘管,同时又能对瘘口周围的炎性创面进行Ⅰ期修复,国内外医生进行了不同手术方式的探索,但针对儿童患者不同手术方式的研究鲜见。本研究回顾性分析我院2016年1月至2019年12月收治的行先天性耳前瘘管切除术的病例,从手术路径、切口方式和软骨处理等多个手术环节比较儿童耳前瘘管切除术不同手术方式的应用,并首次结合瘢痕评分量表(Stony Brook Scar Evaluation Scale,SBSES)[2]评估术后切口的美观度,综合分析儿童耳前瘘管切除不同手术方式的术后效果,为临床手术方案设计提供依据。
1 资料与方法
1.1 一般资料
回顾分析2016年1月~2019年12月武汉儿童医院耳鼻咽喉头颈外科收治的入院行耳前瘘管切除术的先天性耳前瘘管患儿资料。患儿年龄4个月~16岁,平均(5.1±3.2)岁;右侧56耳,左侧78耳,共134耳,术前均有瘘管合并感染史。
1.2 手术方法
所有患儿均在急性期炎症控制后全麻下进行手术。常规消毒铺巾,切口周围皮下注射副肾盐水(0.01 mg/mL),尤其是耳轮脚及其周围,包括耳甲艇和三角窝,以及炎性皮肤区域。耳前组织切除法沿瘘口注入适量美兰。
1.2.1 耳前组织切除法 沿瘘口周行梭形切口,用眼科剪根据染色指示沿瘘管周平行于切口方向将周围组织与皮肤分离,如果瘘管周围有肉芽组织,要注意分离区域应在肉芽外周,解剖瘘管壁与耳轮脚软骨粘连处,必要时将该区域软骨膜或部分软骨组织一并切除(图1A、1B),术区深达颞筋膜浅层。瘘管完全摘除后,可见一个以颞浅筋膜为底、腮腺顶为前下界,耳轮脚软骨暴露为后界,耳屏软骨前间隙为后下界的区域(图1C)。间断缝合皮下组织和皮肤,术区加压包扎。

A:一并切除瘘管基底部与耳轮脚软骨粘连处的软骨膜或部分软骨组织;B:完整摘除的瘘管组织;C:瘘管完全摘除后,可见一个以颞浅筋膜为底的、腮腺顶为前下界,耳轮脚软骨暴露为后界,耳屏软骨前间隙为后下界的区域。图1 耳前组织切除法Fig.1 The supra-auricular approach for preauricular sinuses
1.2.2 瘘管解剖法 仅在瘘口周切口区域皮下注射少量副肾盐水,沿瘘口导入留置针头导丝(图2A),用止血钳或缝线将导丝绑定(图2B)。沿瘘口行梭形切口,钝性分离瘘管周皮下组织,边分离边牵拉和导丝固定在一起的瘘管(图2C),游离部分瘘管后,用眼科剪沿瘘口纵行剖开瘘管但不要超过导丝的最远端(图2D),将导丝逐渐深入到瘘管远端,固定,再沿瘘管壁游离部分瘘管,直到暴露瘘管盲端(图2E),完整摘除瘘管。耳前瘘管多有数个分支,术中注意每个分支,遇肉眼判断不清,可在显微镜下识别盲端和分支口,确保瘘管完全摘除。

A:沿瘘口导入留置针头导丝;B:用止血钳或缝线将导丝绑定;C:沿导丝指示,游离瘘管;D:沿导丝纵行剖开管腔,逐渐深入进一步游离瘘管到远端;E:沿管腔游离至暴露瘘管盲端。图2 瘘管解剖法Fig.2 The sinusectomy approaches for preauricular sinuses
1.2.3 切口类型 Ⅰ型,以瘘口为中心的单一梭形切口(图3A);Ⅱ型,包含瘘口和炎性皮肤的大梭形切口(图3B);Ⅲ型,分别在瘢痕区与瘘口周作平行的双梭形切口(图3C);Ⅳ型,上述3型切口切除病变联合皮瓣转移修补创面。皮瓣的设计可依据创面的具体情况而定[3-4],如向上沿颅耳沟延长原切口,减少创面上部的张力,沿耳屏上切迹延长切口下端,同时制作三角皮瓣,修补创面下部的缺损;另可在耳屏前作一顶角向下,蒂在耳屏前的三角皮瓣,向上转移皮瓣修补耳前创面(图3D)。
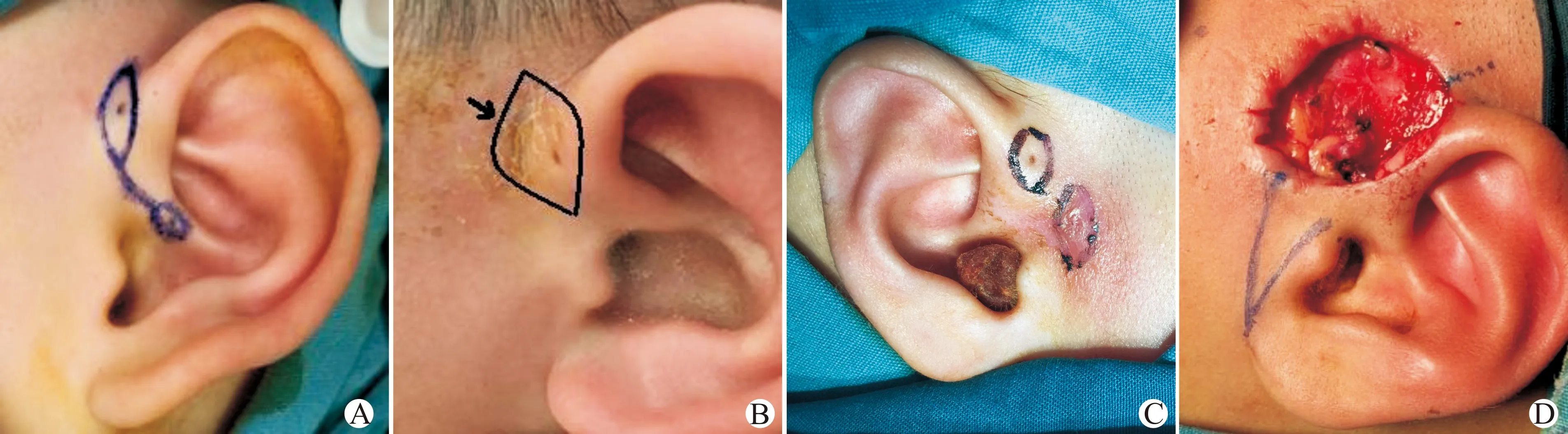
A:Ⅰ型切口,沿瘘口作单一梭形切口;B:Ⅱ型切口,包绕瘘口和炎性皮肤在内的大梭形切口;C:Ⅲ型切口,沿瘘口和炎性皮肤作平行的双梭形切口;D:Ⅳ型切口,切除病变后作三角皮瓣转移修补创面。图3 4种切口类型Fig.3 Four kinds of incision
1.2.4 软骨处理 切除与瘘管壁紧密粘连软骨膜或部分耳廓软骨;或仅分离瘘管组织和软骨,不处理耳廓软骨保留软骨完整结构。
1.3 斯托尼布鲁克瘢痕评估量表(SBSES)评估切口愈合美观度
SBSES评分细则见表1。得分0~5分,评分越高,瘢痕越小,切口越美观(图4)。

表1 斯托尼布鲁克瘢痕评估量表Table 1 Stony Brook Scar Evaluation Scale
1.4 统计学方法


术后1年,患儿切口愈合美观,与周围皮肤颜色一致,无瘢痕,耳廓形态正常图4 术后1年切口愈合情况Fig.4 Wound healing one year after operation
2 结果
2.1 不同手术方式术后并发症的比较
78耳采用耳前组织切除法,56耳采用瘘管解剖法。Ⅰ型切口44耳、Ⅱ型切口39耳、Ⅲ型切口17耳、Ⅳ型切口34耳;软骨处理75耳,未处理软骨59耳。术后随访12个月,复发5耳(3.7%);伤口感染延迟愈合4耳(3.0%);暂时性面瘫1例(0.7%)。并发症的总体发生率为7.46%,具体见表2。比较不同手术路径、切口类型和软骨处理与否发生并发症的情况(表3):不同手术路径的并发症发生率差异无统计学意义(P>0.05);不同切口类型的并发症发生差异具有统计学意义(P<0.05);软骨处理与否的术后复发率差异具有统计学意义(P<0.05)。

表2 术后并发症患者情况列表Table 2 Profile of the patients with postoperation complication

表3 不同手术方式发生并发症的比较Table 3 Comparison of complication rates between different surgical methods
2.2 不同手术方式切口外观的比较
总体134耳SBSES评分(3.239±1.264),不同手术方式SBSES评分详见表4。SBSES评分与手术路径,切口类型,软骨是否处理均有关。瘘管解剖法较耳前组织切除法SBSES评分高;软骨未处理组SBSES评分高于处理组;不同切口比较,Ⅰ型切口SBSES评分最高,Ⅱ型、Ⅲ型切口评分较低,差异有统计学意义(均P<0.05)。

表4 不同手术方式的SBSES评分比较Table 4 Comparison of the SBSES score between different surgical methods
3 讨论
耳前瘘管切除术临床上应用最广的手术路径是耳前组织切除法,又称耳上路径,由Prasad等[5]于1990年提出,手术设计是依据耳前瘘管的组织发生原理,走行于颞肌筋膜浅面、耳轮软骨前,皮肤下之间的区域。经典的耳前路径是瘘口梭形切口顶端沿耳轮脚向上、向后延长至耳后沟,从耳后切口暴露颞肌,沿颞肌筋膜浅层向耳前分离,完全切除包括瘘管在内的皮下整块耳前软组织,属于扩大范围的瘘管切除[6-7]。对此手术路径,国内外学者均有研究报道,认为大大提高了耳前瘘管的手术效果,尤其是对于难治性耳前瘘管的病例[1,7]。此种技术不强调术中识别瘘管的走行和细小分支,而注重解剖层次的分离,故本次研究中的二次手术病例均采用此路径,术后未再复发,疗效满意。但是对于儿童患者,尤其是1岁以内的婴幼儿,头面部体积较小,解剖结构之间间距相对较窄,手术操作空间狭小,而该手术路径中需分离的组织范围较广,故容易损伤周围组织,如神经、肌肉和血管。本研究所有病例中唯一1例术后发生面神经损伤的即是采用的此手术路径(表2),患儿术后出现额纹不对称,术侧变浅及术侧闭眼困难,3个月后逐渐恢复。分析原因考虑为术中向前下分离耳前组织时进入了腮腺实质导致面神经分支损伤,所以对于儿童患者采用耳前组织切除法时尤应注意解剖层次的识别。本研究采用的另一手术路径为瘘管解剖径路,由Baatenburg de Jong报道[8],术中采用探针或示踪剂如美兰标记瘘管管腔,沿管腔解剖切除瘘管,必要时可使用显微镜或手术放大镜辅助识别瘘管走形[9]。由于术中既要解剖管腔内部又需分离管外组织,故又被称为Inside-out技术[8]。术后复发是瘘管解剖路径最有争议的地方。从病理学角度分析术后复发的原因是瘘管上皮组织的残留,由于瘘管走行的不定型性和分支数量的不确定性使得术中追踪瘘管的难度增加,尤其是向下和深面延伸的分支;对于感染较重的病例,如术前曾有脓肿形成,术区形成了瘢痕、肉芽,改变了瘘管原有的走行,增加了术中识别瘘管的难度。不论是采用美兰、探针、还是辅助显微镜等,都很难辨识和确定需切除边界。而瘘管解剖路径是以瘘管走形为术中指示,因此对于反复感染或有脓肿切排史的病例采用该路径有一定的局限性。El-Anwar等[10]综合分析了17个不同研究中心共计1270耳关于耳前瘘管切除术的报道,比较这两种路径并发症的发生情况。结果显示瘘管解剖法径路的术后复发率明显高于耳前径路,术后伤口感染、裂开和瘢痕形成的报道也多于耳前组织切除法,认为瘘管解剖法较耳前组织切除法并发症发生率更高。本研究中术后复发共5例,其中4例是采用瘘管解剖路径(表2),也显示瘘管解剖路径存在术后复发的风险,但是两种手术路径在总体并发症的发生率上未见统计学差异(P>0.05),与El-Anwar等结论不同。分析原因可能是El-Anwar研究中的两种手术路径的比较来自于不同的医疗机构,每个机构只采用其中一种手术路径,不同机构之间术者存在技术偏向和技巧差异;而本研究是在同一机构内针对对两种手术路径进行观察排除了术者差异的干扰。
随着人们对生活质量的要求越来越高,耳前瘘管切除术作为颜面部手术,术后切口愈合的美观情况也是儿童患者十分关注的问题。耳前组织切除路径切除病变后,术区常遗留一个较大的腔隙,术中需分离周围的皮下组织和肌肉进行缝合来封闭术腔和软骨创面,有时需要上引流条和加压包扎避免术区死腔形成,切口容易感染,伤口缝合张力较大[11]。本研究结果中耳前组织切除法SBSES评分低于瘘管解剖法,提示切口愈合美观较瘘管解剖法欠佳。而对于儿童患者选择手术方案时应考虑手术创伤问题,相对于耳前组织切除法,瘘管解剖法的切除范围要小一些,手术创伤小,术后切口的SBSES评分较高(表4),切口愈合美观度高。可见两种手术路径均可应用于儿童耳前瘘管切除术,各有优劣,设计手术方案时应根据不同手术路径的特点选择适应症。
降低复发率除手术路径的选择,是否需要处理耳廓软骨也是存在争议的问题。Gur等[12]和Chvez Delgado等[13]确认软骨切除后复发率降低,Yeo等[14]则认为不影响复发,但是术中处理软骨,术后可能会影响耳廓外型,并有增加术后感染耳廓软骨膜炎的风险。术后复发率国内外报道差异较大,为0~43%[1]。国内学者也在探索既保留软骨又降低复发的方法,提出以耳轮棘为标志的精细解剖技巧,但是复发率仍有4%[15]。本研究软骨处理组复发率为0%;软骨未处理组为8.47%,软骨未处理组复发率明显高于软骨处理组,提示处理与瘘管粘连的耳廓软骨是控制术后复发的有效措施。虽然本研究中软骨处理组并未出现耳廓软骨膜炎的并发症,但是软骨处理组SBSES评分低于软骨未处理组,提示耳廓软骨切除对切口美观存在影响。
先天性耳前瘘管患儿瘘口部位的多样性和术区皮肤条件的复杂性使耳前瘘管切除术的切口设计显得尤为重要。国内外医生报道了多种切口和修复方法[16],包括连同炎性皮肤一起切除的单梭形切口、双梭形切口[17-18]和皮瓣转移的技术[3-4]。本研究观察了目前常用的4种耳前瘘管切除术切口类型临床应用效果并进行比较分析,结果显示切口类型与并发症的发生存在统计学相关性,连同瘘口和炎性皮肤作的大梭型切口(Ⅱ型)并发症发生率最高。除复发以外,伤口感染、伤口延迟愈合是手术后经常需要面对的并发症。耳前瘘管切除术后伤口感染的原因主要是瘘管分支末端残留和前期感染形成的炎性组织未彻底剔除[14]。没有彻底剔除紧贴皮下的炎性病变即缝合切缘,残留皮下的炎性病变容易导致伤口感染、裂开。本研究中术后感染病例有75%(3/4)是采用的Ⅱ型切口(表2)。分析原因Ⅱ型切口的切缘容易在炎性组织的皮肤上(图3B)。Ⅲ型切口由于在瘘口和炎性皮肤区域分别作梭形切口,有利于彻底切除远端的炎性皮肤及瘢痕(图3C)。但是Ⅱ型和Ⅲ型切口共同特点是皮肤组织缺损较大,切口缝合时张力较大,故SBSES评分较低(表4),显示该两种切口术后瘢痕明显。所以对于皮肤缺损太大的创面,可设计采用周围皮瓣转移(Ⅳ型)的方法进行修补(图3D)。本研究结果显示Ⅳ型切口较其它类型切口并发症较低(表3),SBSES评分较高(表4),有显著性差异,说明该类型切口既有助于彻底切除病变,又让创面愈合相对美观。
综上所述,儿童耳前瘘管切除术手术路径的选择应根据不同手术方式的特点结合患儿的临床特征进行;手术方案的设计在彻底切除瘘管减少复发的基础上应兼顾减少手术创伤及考虑术后美观效果。
