食物过敏:从致敏机理到控制策略
2021-10-31傅玲琳王彦波
傅玲琳,王彦波
(浙江工商大学食品与生物工程学院,浙江 杭州 310018)
过敏性疾病是一种严重影响人体健康的全球性问题,引起机体过敏的原因众多,其中食物过敏占有不容忽视的比重。食物过敏是指由机体免疫系统对某些食物蛋白质的超常反应,发病时可累及周身多个系统,如皮肤、呼吸道、胃肠道和中枢神经系统,严重时可导致过敏性休克甚至危及生命。近些年来,世界范围内食物过敏的发病率呈逐年上升趋势,食物过敏已经成为全球关注的食品安全和公共卫生问题,被称为继哮喘之后的“第二波”过敏流行病[1]。在欧美、澳大利大等西方国家,食物过敏在成人中的患病率约为2%,而在儿童中则高达8%[2]。大量研究发现,食物过敏的发病率上升可能与基因、环境以及二者的相互作用(如表观遗传)有关,考虑到短时间内遗传基因不会发生显著变化,环境和饮食因素被认为是导致食物过敏风险上升的主要原因[2]。根据发病机制的不同,食物过敏可以分为免疫球蛋白(immunoglobulin,Ig)E介导、非IgE介导和混合介导的反应,其中IgE介导食物过敏的机制较为清楚,主要包括致敏阶段和效应阶段,即机体首次暴露致敏原产生特异性IgE(specific IgE,sIgE),sIgE与肥大细胞和嗜碱性粒细胞上的受体结合使机体致敏,当致敏原再次进入体内时,通过与上述细胞表面的sIgE结合发生交联,激活胞内的酶系统,促进多种炎性介质的释放,引发一系列生理反应[3-5]。
根据世界卫生组织(World Health Organization,WHO)和联合国粮食与农业组织(Food and Agriculture Organization of the United Nations,FAO)的统计,90%以上的食物过敏反应是由牛乳、鸡蛋、大豆、花生、小麦、坚果、鱼类和甲壳α纲类动物以及相应制品引起的,这8 类食物因此也被称作“Big Eight”[6-7]。2021年2月,最新的WHO/FAO食物致敏原风险评估专家咨询会上提出,综合考虑每种食物引起超敏反应的发生几率、严重程度和潜在风险,芝麻或将取代大豆成为新的八大类之一[8]。除八大类以外,其他种类的食物,如某些水果、蔬菜、昆虫和谷物等也可能是特定国家或地区的常见致敏食物。近年来,随着人们对黏膜免疫系统、口服免疫耐受以及肠道共栖微生物的逐渐认识,有关食物过敏的机理研究也在不断深入。但是,目前对于食物过敏最有效的治疗手段仍是严格避免接触致敏原。随着食品工业的快速发展,使用的原料越发复杂和多样,饮食回避对于易感人群难度较大,且易造成人体营养素的缺乏与失衡。一方面,日益严峻的食物过敏问题需要切合实际的风险评估和标识措施;另一方面,各类易感人群的营养需要也为低敏食品体系的研究提出了挑战。
食物过敏现已成为食品行业亟需面对和解决的食品安全问题。基于此,本文将围绕食物过敏的研究现状,从食物过敏的流行病学特征与分子机制、食物致敏原的识别与评价,以及食物过敏的诊断与控制等方面逐一展开,系统回顾最新研究进展并提出展望,以期为食物过敏的预防与控制,以及保障食物致敏原安全提供一定借鉴。
1 食物过敏的流行病学与致敏机制
1.1 中国食物过敏的最新流行病学特征
食物过敏的流行病学调查在美国、加拿大和欧洲一些国家已经有了较为全面的数据。但是在我国,尚无针对普通人群开展的食物过敏流行病学研究,仅有部分区域性或针对特定年龄段的调查数据可供参考。其中区域性的横断面研究主要集中在省会城市和南方地区,如温州(浙江)[9]、重庆[10]、广州(广东)[11]、北京[12]、上海[13-14]和香港[15]等地,并且针对的多是婴幼儿、学龄前和学龄段儿童,尚无有关成人或全年龄段人群的食物过敏流调报告。如表1所示,通过问卷调查或病史初筛,自述/父母报告的食物过敏发病率范围较大,为4.80%~21.13%,结合皮肤点刺(skin prick test,SPT)和/或血清学特异sIgE和/或开放性食物激发确诊的发病率为0.34%~18.0%。除横断面调查外,也有少数研究针对门诊过敏病人和超敏报告事件进行了统计[16-20],其中规模最大的是一项2017年我国南方地区过敏性疾病患者血清sIgE检测结果(n=39 813)的回顾性分析,该项报告发现过敏食物中阳性检出率最高的是虾(19.2%),其次是蟹(15.5%)和鸡蛋白(9.9%)[20]。

表1 中国人群食物过敏的横断面流行病学调查数据Table1 Cross sectional epidemiological survey data of food allergy in China
尽管有关食物过敏的横断面研究十分有限,但从已有的数据中仍可对我国食物过敏的流行病学特征窥知一二。1)发病率总体呈上升趋势。一项针对温州地区2 岁及以下儿童的3 次横断面调查显示(1999、2009年和2019年;n=1 228),该年龄段儿童的食物过敏发病率呈逐年上升趋势:1999年为3.5%,2019年上升为11.1%;其中最常见的牛乳过敏在1999—2019年间的发病率由1.6%上升为5.7%(P=0.004)[10]。2)可能存在城乡、地域和民族差异。有关城乡地区的发病情况,一项北京6~11 岁小学生的随机抽样调查(n=10 672)发现,该地区城市儿童食物过敏的父母报告率为11.90%,显著高于郊区儿童的8.2%(P<0.001)[12];但另一项广州市区及韶关农村学龄儿童的研究(n=11 432)发现,结合问卷答案和SPT或sIgE检查,两地食物过敏的发病率并无显著差异(P=0.872)[11]。此外,袁娟丽等对我国南北方人群携带的乳糜泻人类白细胞抗原(human leukocyte antigen,HLA)易感基因进行研究发现,我国南方人群和女性群体罹患乳糜泻的风险可能更高[21]。针对民族差异性,Zhou Chunyan等通过对我国新疆地区患有胃肠不适症的患者进行筛查(n=2 277),发现汉族人患乳糜泻的比率显著低于维吾尔族、哈萨克族和回族人群[22]。3)最常见的过敏食物与西方国家存在异同。由表1不难看出,我国食物过敏人群主要对牛乳、鸡蛋(白)和虾蟹过敏,而西方国家发病率较高的花生和坚果过敏在我国并不常见,WHO列举的“八大类”致敏原在我国并不完全适用;此外,水果类食物例如桃子和芒果也是我国人群的常见致敏原。当然,由于缺乏全国范围内的规范性调查结果,以上几点只是笔者的初步判断,并且只能部分代表婴幼儿和未成年儿童群体,但是相信随着政府和业内专家对食物过敏疾病的日渐重视,我国普通人群的食物过敏流行病学数据将逐渐得到完善和补充。
1.2 食物过敏的分子机制
针对食物过敏的分子机制,比较清楚的是IgE介导型的免疫学机理。正常情况下,机体免疫系统能够正确区分致病性抗原与无害的环境抗原,如食物中的营养物质。这一免疫耐受的形成过程最初与肠道相关淋巴组织(gut-associated lymphoid tissue,GALT)密切相关。一系列细胞参与了免疫耐受的诱导过程,包括抗原从肠腔转移到固有层和淋巴组织,进而被呈递并诱导相应的T细胞反应,最后免疫效应细胞归巢回到肠道等[4]。简单来说,进入机体的变应原经胃肠消化后可能通过细胞旁途径、肠上皮细胞胞吞作用和M细胞的内吞等方式透过肠上皮屏障。透过屏障后,变应原可经固有层中传统的抗原递呈细胞(antigen-presenting cells,APCs)如树突状细胞(dendritic cells,DCs)摄取,或经非传统的APCs,如库普弗细胞和浆细胞样DCs处理后迁移进入肠系膜淋巴结(mesenteric lymph node,MLN),然后被摄取的蛋白/多肽进一步降解并通过主要组织相容性复合物类(major histocompatibility complex,MHC)分子呈递给初始T细胞,激活T细胞免疫反应[5]。其中,CD103+DCs是促进黏膜耐受形成的主要DC亚群之一[23],该类细胞产生的转化生长因子-β(transforming growth factor-β,TGF-β)和视黄酸,可诱导初始T细胞分化为特异性叉头状P3(FOXP3+)调节性T细胞(regulatory T cells,Treg)[24]。此外,视黄酸也可诱导Treg细胞表达整合素α4β7,诱导其他Treg细胞归巢到肠道,抑制免疫反应[25-26]。与此同时,视黄酸和DCs的相互作用在次级淋巴组织中也可诱导B细胞向分泌IgA的浆细胞分化,最终达到IgA抗体的类别转换。
在食物过敏患者体内,这一口服耐受的形成过程遭到了破坏。一般认为,致敏过程中肠上皮屏障的损伤导致了变应原的透过量增加,同时诱导上皮细胞因子,如白介素(interleukin,IL)-33、IL-25和胸腺基质淋巴细胞生成素(thymic stromal lymphopoietin,TSLP)的分泌,这些细胞因子可上调DCs上的OX40配体(OX40L)。DCs进一步诱导初始T细胞向Th2细胞分化,释放可招募嗜酸性粒细胞的细胞因子IL-5,并促进B细胞类别转换产生IgE(通过IL-4和IL-13)[4-5,27]。形成的sIgE与组织中肥大细胞和嗜碱性粒细胞表面上的FcεRI受体结合,再次接触致敏原时发生脱颗粒反应,激活胞内的酶系统释放一系列活性介质,引起局部或全身性的变态反应。图1汇总并展示了致敏过程中肠道内Th2细胞介导的变应原免疫反应。

图1 致敏过程中肠道内Th2细胞介导的变应原免疫反应[4]Fig. 1 Th2 cell-mediated inflammatory response to oral allergens in the gut during sensitization process[4]
另一方面,肠道微生态在调节机体对致敏原的免疫反应中起着关键作用[28]。研究发现,食物过敏和健康人群的肠道微生态组成存在明显不同,这些差异出现在过敏症状之前,且在婴幼儿和儿童时期更为明显:例如,患有鸡蛋过敏的儿童其肠道菌群的α-多样性更高,且毛螺菌科和瘤胃菌科的类群丰度更高[29]。而与健康组相比,食物过敏的婴儿肠道菌群的多样性没有差异,但厌氧菌和自养型芽孢杆菌的相对丰度有所减少,拟杆菌和芽孢杆菌的相对丰度有所增加[30]。再如,在患有牛乳过敏的婴儿中,与持续性过敏组相比,8 岁后过敏症状得到缓解的个体其早期(3~6 岁)肠道菌群中梭菌属和拟杆菌属的水平更高[31]。更直接的是,通过将健康婴儿的粪便菌群移植到无菌小鼠上,可以缓解这些小鼠摄入牛乳后的过敏反应,但是从牛乳过敏的婴儿移植的粪便菌群则没有这一能力[32-33]。以上证据有力地表明了食物过敏与肠道微生态间的因果关联。有关微生态参与调控的食物过敏机制仍在不断探索阶段,目前报道的作用主要包括:调节肠道细胞功能,提升肠道屏障特性;生成代谢产物(如乙酸、丁酸和丙酸等短链脂肪酸)参与免疫调控;以及促进和维护机体口服耐受等[34-36]。笔者前期研究发现,与健康人群相比,食物过敏患者在肠道菌群的组成和功能上存在显著差异,进一步经代谢组学和通路富集分析发现,过敏患者体内肠道微生物的若干关键代谢通路得到了调控,尤其是氨基酸代谢水平发生了显著变化,多种氨基酸的合成增强,降解减弱;与此同时,特征氨基酸(如异亮氨酸)的变化程度与患者的临床和免疫学指标密切相关。菌群来源的氨基酸代谢物可能与食物过敏的发生有关,但这其中涉及的免疫信号通路和分子机制有待进一步的研究。
1.3 食物过敏发生的机体风险因素
目前,尚不清楚是哪些原因导致人体内由DCs和Treg细胞介导的口服耐受过程转变为了由Th2细胞介导的食物过敏反应。研究人员指出,一些可能诱发食物过敏的风险因素包括家族病史、性别、种族、基因多态性、接触细菌的时间和途径、膳食习惯的改变和早期皮肤暴露等[37]。关于先天遗传因素的作用可详见Lack[37-38]、Sicherer[2]等的报道,此处笔者将针对后天性因素进行详细阐述。
Strachan在1989年提出了著名的“卫生学假说”(Hygiene hypothesis),认为儿童早期缺乏对传染源、细菌和寄生虫的接触,导致机体免疫系统没有得到足够的锻炼,增加了其对过敏性疾病的易感性。进一步研究发现,过敏性疾病的增加更有可能是由于现代化的环境和生活方式使得人们接触共生有益菌的机会变少,而这些共生菌能够帮助宿主免疫系统建立正确的调控途径避免发生紊乱,即发展形成了“老朋友假说”(old friends hypothesis)。目前已发现支持这一假说的流行病学证据,如孕妇产前避免食用抗生素、孕期摄入膳食纤维(调控肠道微生态平衡)、阴道分娩、母乳喂养、幼儿时期接触动物等均能在一定程度上降低儿童发生过敏性疾病的几率[37,39-41]。
近30 年来,饮食结构的显著变化使得研究学者们怀疑,某些宏量和微量营养素的摄入可能与日益增加的食物过敏状况有关,这里有4 个假说值得深思:VD水平、膳食脂肪的来源、抗氧化剂的减少和伴随有害产物的摄入。首先,VD假说认为,体内VD的不足或过量(主要是日照时长、纬度、出生季节和膳食摄入导致的)是哮喘和过敏发生率增加的原因。例如在美国和澳大利亚,与靠近赤道的地区相比,远离赤道的地区人群发生食物过敏的可能性更高[42,43],再如Nwaru等[44]发现,母亲在怀孕期间VD的摄入量与婴儿较低的食物过敏风险有关;另一方面,也有几项队列研究发现婴儿期间补充VD增加了人群罹患食物过敏的几率[45-46]。有关VD与食物过敏的关系尚未得到一致的结论,有人提出,二者之间可能存在一种“U形”关系,即VD过少或过多均会增加食物过敏发生的风险[47-48]。从机制上看,VD的活性形式1,25-二羟VD参与着多种免疫细胞的调节,如T细胞、DCs和Treg细胞等,VD也可能通过影响下游基因的表达、作用于表观遗传(如DNA甲基化)和调节肠道菌群组成等方式影响免疫系统的平衡[49]。第二,膳食脂肪的来源,研究认为动物脂肪消耗量的减少以及人造奶油和植物油使用量的增加加剧了食物过敏的发生。这主要是与ω-6系多不饱和脂肪酸(如亚油酸)的摄入降低、ω-3系多不饱和脂肪酸(如二十碳五烯酸)的摄入升高有关。ω-6系脂肪酸可以合成前列腺素E2(prostaglandin E2,PGE2),而ω-3系脂肪酸则会抑制PGE2的合成。PGE2能抑制T细胞产生IFN-γ,导致B细胞产生IgE,诱发食物过敏的发生[37,50]。第三,抗氧化剂假说,这个假说认为新鲜水果和蔬菜的食用量减少降低了膳食抗氧化剂的摄入,如VC、VE、β-胡萝卜素、硒和锌等,这可能是导致机体过敏的原因之一[38,51]。关于这一观点的争议较大,并且有关食物过敏的证据尚不完善,此处不再详述。第四,伴随有害产物的摄入,该假说认为在食品原料及在加工、储藏过程中引入的特定有害物质可能诱发食物过敏。例如,一项研究分析了南非食物过敏队列中儿童的环境风险因素,发现快餐的摄入和油炸烹饪方式与过敏的发生有关[52]。再如Wang等[53]经Meta 分析发现,人群摄入快餐的频率与哮喘和喘鸣样症状的发病有密切关系。这一现象可能与油炸食品中广泛存在的糖基化终末产物(advanced glycation end-products,AGEs)有关。AGEs是一类蛋白质、多肽和脂类与还原糖反应生成的多种高度异质产物的总称,它们具有改变致敏原表位结构、激活炎症细胞通路和Th2型偏向分化的特点,这些物质可能通过变应原相关/无关的多种途径诱发食物过敏[54-56]。近期发表在Cell上的观点进一步支持了该假说,提出了“食物过敏是机体食品质量控制体系(food quality control system,FQCS)的异常激活”[57]。该观点认为,FQCS通过监视食物成分来消化和吸收有益的营养物质并排出有害物质。但当环境或食物中存在某些能够有效诱发机体FQCS的有害物质(如加工产物、防腐剂、有毒的植物次生代谢物等),可能使得免疫系统对同时摄入的食物蛋白质高度敏感,从而诱发免疫反应。以上有关膳食习惯与食物过敏的关联可以总结为“营养免疫调节假说”(nutritional immunomodulation hypothesis),即认为现代饮食和环境的急剧变化导致某些具有免疫调节潜力的因素影响了食物过敏的发生[2]。
另一方面,早期皮肤暴露是诱发食物过敏的重要风险因素。Fox等据此提出了“双重致敏原暴露假说”(dual allergen exposure hypothesis),认为经口致敏可以促进免疫耐受的形成,但是经皮肤致敏则会干扰口服耐受。受损的皮肤屏障导致的变应原早期暴露和持续性炎症可能诱发和加剧食物过敏[58]。已经有越来越多的证据支持这一观点,例如在丝聚蛋白(具有维持皮肤屏障的功能)突变的人群中观察到了更高的食物过敏发生率[59];再如在患有特异性疾病的婴儿中,花生过敏的发病率与环境粉尘中检出的花生含量密切相关等[60]。在动物模型中,将小鼠破损的皮肤暴露于卵清蛋白或花生提取物,其体内产生了相应的sIgE并诱发了Th2型免疫应答[61-62]。有关皮肤暴露致敏的具体机制还在研究中,已有观点认为:受损的皮肤上皮细胞可释放多种炎性因子,如IL-25、IL-33和TSLP,它们作用于DCs和其他细胞,诱导形成局部的Th2偏向型免疫反应,进一步转移到肠道,通过效应细胞归巢和肠道肥大细胞聚集等方式诱发食物过敏[37,63]。
2 食物致敏原的识别与评价体系
2.1 什么使食物蛋白质成为致敏原?
食物致敏原的定义是可由特定免疫细胞识别并引发产生特定症状的食物蛋白种类。截止目前,经WHO和国际免疫学会联合会(International Union of Immunological Societies,IUIS)致敏原命名小组委员会命名的食物致敏原共有370余种,涵盖了包括“八大类”食物在内的125 种食物。
致敏原结构中决定其被免疫系统识别的片段称为表位,即表位是变应原中参与抗体结合的部分。根据结合受体的不同,表位可分为T细胞表位和B细胞表位;根据结构的不同,表位又可分为线性表位和构象表位。其中,线性表位是由多肽链上连续的氨基酸组成的,构象表位是由空间上临近但一级序列不连续的氨基酸组成的[64]。目前,针对表位长度的观点不甚统一,但考虑到MHC II类分子对不同链长肽段的亲和程度,抗原表位的合适长度一般为10~25 个氨基酸。表位是机体识别致敏原的物质基础,因此有相当一部分研究致力于鉴定不同食物致敏原的表位结构,近年来也发展形成了一系列集成化、高通量化的表位定位技术,如多肽芯片技术、质谱技术、表面等离子体共振和噬菌体展示技术等[65]。明确致敏原的表位一方面可以帮助理解抗原-抗体相互作用的结构基础;另一方面,也可为食物过敏病患者的血清学诊断提供重要信息。如通过比较不同鸡蛋过敏儿童血清对卵类黏蛋白表位的识别能力,Järvinen等发现持续过敏患者的血清抗体较暂时性过敏患者可以识别更多的致敏原表位,针对其中特异性表位的结合抗体或可作为持续性食物过敏的筛查工具[66]。
食物中的蛋白质数量非常庞大,但只有其中少部分的蛋白质成为了食物致敏原。研究人员通过比较不同类食物致敏原的结构和生化特性,发现致敏原具有如下共同特征:1)含量丰富。食物中的致敏原通常为其中丰度较高的蛋白质,相较那些含量较低的蛋白组分,免疫系统有更多的机会接触到这些高丰度蛋白引发免疫反应[67];2)稳定性高、不易消化。许多食物致敏原耐热和酸碱,且不易被消化酶降解,具有较强的化学稳定性和抗消化性,它们经烹饪或胃肠消化后仍能保持一定的结构完整性,被认为是能够刺激肠屏障发生特异性反应的重要因素[68];3)蛋白质结构的特殊性。许多致敏原含分子内二硫键,破坏这些二硫键会改变蛋白质的结构和稳定性,降低表位结合sIgE的能力;此外,大部分致敏原属于糖蛋白,蛋白质翻译后修饰,尤其是糖链的修饰被认为与致敏原的免疫识别有关。虽然已有研究鉴定了其中部分蛋白的糖链结构,但其与致敏原抗原表位的特异性和参与的致敏识别机制尚不十分明确[67,69]。4)与已知致敏原的同源性[70]。相当一部分致敏原之间存在序列同源性,例如一些果蔬类致敏原与吸入性致敏原(如花粉)存在不同程度的同源性,这些变应原之间的免疫交叉反应可能导致机体对多种食物过敏。根据这一特征,未知蛋白与已知致敏原的序列或结构相似性常是判定其安全性和潜在致敏性的指标之一。值得注意的是,以上提到的各种致敏原特征均存在例外,例如鳕鱼主要致敏原Gal d 1(属小清蛋白)的丰度较低,不到其肌肉组织湿质量的1%[71];猕猴桃致敏原Act c 1、桃致敏原Pyr c 1和苹果致敏原Mal d 1等化学性质不稳定,极易被胃蛋白酶消化[72];再如有些致敏原不含糖基,也并非每位花粉症患者都对某种水果或蔬菜过敏等等。使食物蛋白质成为致敏原的原因还未完全揭示。食物本身是十分复杂的基质,除了含有致敏原外,还有很多非致敏组分,如其他蛋白质、脂质、添加剂和食品加工伴随产物等。以脂质为例,膳食中的脂肪可能作为助剂诱发炎症和Th2偏向型免疫响应,同时可能会降低蛋白质的消化率,增加肠道屏障的通透性[73]。目前针对食物致敏原的研究大多集中在蛋白质分子本身,除此之外,食物复杂基质的影响、内外源有害物质的协同作用(例如前述的FQCS)以及特定人群的饮食习惯和地域差异等都可能是导致某种特殊致敏原出现的潜在因素。
2.2 食物致敏原的致敏性评价手段
准确的食物致敏原评价方法有助于过敏相关免疫机理的研究,也是研发预防和治疗食物过敏手段的必要途径。根据体系的不同,食物致敏原的评价手段可以分为体内、体外和生物信息学比对方法。
2.2.1 体内评价方法
体内评价是研究食物潜在致敏性最直接、准确的方法。考虑到人体激发实验的难度和风险性,致敏原的体内评价手段多采用龋齿类动物过敏模型,常见的有BALB/c、C3H/HeJ、A/J和C57BL/6等小鼠,以及Wistar和Brown Norway(BN)等大鼠[74-75]。除此之外,也有少数研究利用狗、猪和斑马鱼构建食物过敏动物模型[75-77]。理想的动物模型应具有和人体相似的黏膜免疫机制、胃肠消化和肠道生理特征,并且具有一定的易感性,可以形成类似机体内发生的免疫效应过程和临床过敏症状。其中,BALB/c小鼠是近交高应答IgE品系,C3H/HeJ小鼠是Toll样受体4基因突变型,二者广泛应用于食物过敏模型的构建;C57BL/6常被用作吸入性过敏反应的相关研究;BN大鼠是高免疫球蛋白应答品系,可以在不使用佐剂的情况下产生致敏原特异性应答,但是其效果易受环境、年龄及亚临床感染的影响[74,78]。值得指出的是,不同种类和品系的鼠类对同一种食物致敏原的识别方式和敏感程度存在差异,因此需要根据研究目的和致敏原特性有目的地进行选择和评价。
在食物过敏动物模型中,除类型和品系的选择外,动物对致敏原分子的易感性,致敏原的给予剂量、频次、致敏途径和佐剂的使用均会影响动物免疫反应的形成方向(致敏/耐受),进而决定模型的构建是否成功。其中,致敏原的致敏途径有口服灌胃、腹腔注射和皮下注射等。表2以对虾致敏原原肌球蛋白刺激BALB/c小鼠为例,列出了2 种主要致敏途径的致敏剂量、周期和优缺点。可以看出,致敏原的口服给药符合实际生活中食物经口摄入过敏的情况,但易产生免疫耐受,一般需要借助黏膜佐剂(如霍乱毒素(cholera toxin,CT)或其亚单位)破坏免疫耐受,诱导食物过敏反应;相比较下,致敏原的腹腔注射作用部位靠近黏膜,在佐剂(如弗氏佐剂和氢氧化铝)的帮助下,更易引起黏膜免疫反应,致敏效果好、成功率高,但是致敏原未经胃肠消化,因而不能反映食物进入机体的真实情况[79]。鉴于此,一部分研究会使用多种途径组合的方式以获得最佳的刺激效果,如采用腹腔注射致敏联合灌胃激发的方式建立过敏模型[80-81]。经激发后,刺激物的致敏性可以通过不同的指标评价,常见的如动物的体温、体质量和过敏症状评分,血清学特异性抗体、活性介质和细胞因子的水平,以及免疫细胞的功能和分化等。

表2 不同致敏途径构建BALB/c小鼠过敏模型的对比[79]Table2 Comparison of the establishment of food allergy model in BALB/c mice by different sensitization routes[79]
2.2.2 体外评价方法
致敏原的体外评价方法具有操作性强、通量高、周期短、安全可行等优势。常用的体外评价手段有血清学和细胞学两种。血清学方法一般是基于“致敏原表位-特异性抗体结合”的原理进行评价,主要包括放射过敏原吸附实验(radioallergosorbent test,RAST)、酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)、斑点印记杂交(Dot blot)和免疫印记法(Western blot,WB)等。其中ELISA因特异性好、灵敏度高,常被用作食物致敏原的评价和定性定量分析,主要有间接法、竞争法和双抗体夹心法等,Dot blot的原理近似于间接ELISA,而WB主要用于评价复杂混合物,联立二维电泳和蛋白质谱可以达到分析、鉴定粗蛋白组分中抗体结合蛋白的目的。值得指出的是,以上血清学方法依赖于“致敏原-抗体”的特异性结合,易受食物基质和抗体识别特性的影响出现假阳/阴性,往往需要进一步的验证[82]。
在IgE介导的食物过敏反应中,致敏原表位与肥大细胞或嗜碱性粒细胞表面的sIgE抗体结合,引起细胞脱颗粒并释放活性介质(如组胺、类胰蛋白酶和β-氨基己糖胺酶),作用于特定组织和器官引起过敏症状。因此可以通过评价免疫细胞的相应变化研究食物的致敏能力,即细胞脱颗粒实验。已经有若干个细胞模型被用于食物致敏原的评价,如人肥大细胞(HMC-1和LAD2)和嗜碱性粒细胞,以及大鼠嗜碱性粒细胞(RBL-2H3)等。其中HMC-1和LAD-2是两类商业化的人肥大细胞系,人嗜碱性粒细胞可由患者外周血分离得到;RBL-2H3是大鼠嗜碱性粒细胞肿瘤株亚系,经人源化处理的RBL-2H3呈现了理想的人IgE结合能力,并且具有与人嗜碱性粒细胞类似的功能和介质释放特点[83]。上述细胞(系)经与患者血清中的sIgE结合后,再次暴露于致敏原发生脱颗粒,通过细胞形态学的改变、活性介质和细胞因子的释放评价食物的致敏能力[75,84]。该类方法更好地重现了体内IgE-介导的细胞生物学变化,是传统血清学方法的有力补充,但是其结果易受细胞状态、分散形式和操作条件的影响,进一步应用需要进行必要的方法学标准化。
由于食物过敏的复杂性,单一细胞模型往往不能很好地模拟体内免疫环境,共培养技术通过将2 种及以上的细胞培养于同一环境中,实现了细胞间信息和物质的沟通,具有更好地反映体内环境的优点。笔者前期利用Tranwell小室将肠道上皮细胞CMT93、小鼠脾脏来源DCs和T细胞进行共培养,成功构建了肠道三维细胞模型(图2)。以卵白蛋白为典型致敏原进行刺激发现,与传统平面培养相比,三维细胞模型中各个信号通路的基因表达得到了显著调控,且体系中初始T细胞向Th2细胞分化的现象更为明显。Transwell共培养系统更好地模拟了体内肠道黏膜免疫的微环境,适用于致敏原评价、抗过敏因子筛选和食物过敏机制等方面的研究。
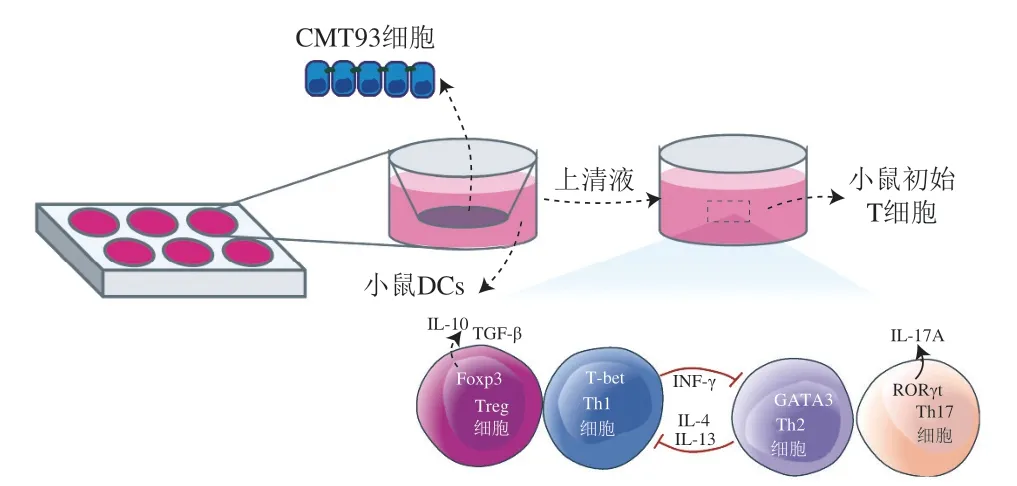
图2 肠道三维细胞模型图示Fig. 2 Illustration of the three-dimensional cell model of small intestine
2.2.3 “高通量生物信息预测-体外验证”表位研究方法
生物信息学是整合了生物学、数学、统计学和计算机科学来阐明和理解生物学大数据的学科。作为一种低成本、高通量的手段,常被用作致敏原评价初期的筛选工具,主要体现在转基因食品的安全性评估和致敏原表位的预测研究上。从本质上看,生物信息学分析是通过将目标蛋白与致敏原数据库进行同源比对,根据基因或蛋白序列的同源性对研究对象的致敏性进行评价。可提供致敏原信息的数据库包括Allergome(www.allergome.org,目前最完善的过敏原数据库)[85]、美国国家生物技术信息中心(National Center of Biotechnology Information,NCBI)、Uniprot蛋白数据库、国际免疫学会联合会(International Union of Immunological Societies,IUIS)(http://www.allergen.org)、致敏原搜索引擎AllergenOnline和致敏原结构数据库(structural database of allergenic proteins,SDAP)等[86-87]。
在致敏原评价方面,近年来得到广泛关注的是生信分析在表位预测中的应用,包括线性表位和构象表位的预测[65,88]。最常见的是致敏原B细胞线性表位的预测,代表性软件/网站有BepiPred[89-90]、DNAstar[91]、ABCpred[91]、AntheProt[92]、BcePred[93]和Immunomedicine Group[94]等。这些工具多是基于蛋白质氨基酸残基和多肽链的理化性质,如亲/疏水性、可及性、柔韧性、电荷分布和二级结构等(或结合多种指标得出的抗原指数)对目标蛋白进行表位预测。由于以上各种软件单独使用均有一定的局限性,实际操作往往结合3 种以上的工具进行综合分析,后续再利用其他评价方法进行验证。由此发展形成的“高通量生信预测-体外验证”表位研究方法[82,95],相较传统的肽扫描技术具有耗时短、成本低、通量高的优势,在食物致敏原的表位定位中得到了广泛应用,如对虾原肌球蛋白和精氨酸激酶[96]、大豆β-伴大豆球蛋白[97-98]和脉红螺副肌球蛋白[99]的表位研究等。图3所示为该体系的基本流程和研究策略。

图3 “高通量生物信息预测-体外验证”表位研究策略[96]Fig. 3 Research strategy for allergenic epitopes by high-throughput immunoinformatics coupled with in vitro verification[96]
相对于线性表位的预测,构象表位的预测研究进展相对缓慢,但也已有一些基于致敏原结构信息的预测工具,如SEPPA[100-101]、DiscoTope[102]、EPSVR和EPCES[103]等。除表位预测外,生物信息学工具也可通过已知的表位信息预测相似致敏原之间的交叉反应,联合突变肽技术还可筛选出表位中影响IgE结合能力和致敏性的关键氨基酸[96]。其他有关食物致敏原的表位研究手段,详见Zhou Fanlin等的报道[65],此处不再详述。
2.3 食物致敏原的确证与检测
实施食物致敏原标签制度是避免食物过敏的有效措施之一。目前,已颁布强制性食品致敏原标识措施的国家/地区有美国、欧盟、加拿大、日本、澳大利亚和新西兰等[104]。我国GB 7718—2011《食品安全国家标准 预包装食品标签通则》中规定:食品中可能含有八大类食物致敏原时,宜在配料表中使用容易辨识的名称,或在邻近位置加以提示[105]。2019年12月,食品安全国家标准审评委员会发布了该标准的征求意见稿,沿用了GB 7718—2011版中规定的致敏物质目录,但拟将其中致敏原标识的相关条款由推荐性转为强制性标识。
致敏原管理的程序一般包括识别、评估、标识及相应的控制措施。在整个过程中,建立灵敏可靠的致敏原检测方法至关重要。目前已有多种技术可用于检测加工或未加工食品中的致敏原含量,根据目的物的不同可分为针对蛋白质或针对DNA的检测,根据检测原理的不同可分为基于免疫学、基于分子生物学、基于质谱技术和基于生物传感器的检测方法等。
免疫学方法,即利用特异性抗体检测目标蛋白,使用的抗体有单克隆抗体和多克隆抗体两类。传统的免疫学方法如ELISA和WB的原理在2.2.2节已有介绍,此处不再赘述。其中,ELISA是食品工业最常用的致敏原定量手段,具有易操作、灵敏度好、检测限(limit of quantitation,LOD)理想等优势,但也存在一定缺陷:如抗体的交叉反应易出现假阳性,食物基质效应的影响,此外致敏原在食品加工过程中发生反应可能掩盖其部分抗原性,导致ELISA的结果产生偏差[106-107]。目前已有大量商品化的ELISA试剂盒可供各类致敏原检测使用,但是多数试剂盒是针对单一致敏原/致敏食物设计的,针对不同种类原料进行多靶标检测的体系尚多处于研究阶段。侧流免疫层析技术是另一类常见的免疫学检测方法,其原理与ELISA相似,具有可视性强、成本低、易操作、易携带等优点。传统的侧流免疫层析依赖于肉眼观察,灵敏度较低,仅能进行半定量或定性分析,但是随着高灵敏标记物、新型层析膜和检测设备的应用,侧流层析检测系统正由传统的定性检测向精准定量检测转变[108-109]。
分子生物学方法主要是指聚合酶链式反应(polymerase chain reaction,PCR)、实时荧光定量PCR法(quantitative real-time PCR,qPCR)和环介导等温扩增技术(loop-mediated isothermal amplification,LAMP)。该类手段分析的是致敏原/致敏食物的特征DNA序列,与蛋白质相比,DNA的稳定性更高且不易受表型变异的影响,随着越来越多致敏原的DNA序列被报道出来,依赖DNA的致敏原检测技术得到了快速发展[110]。传统的PCR法,检测灵敏度有限且只能提供定性结果。相比之下,qPCR可在扩增阶段实现目标蛋白DNA的实时检测,具有操作简便、灵敏度高、重复性好的优势,可以作为定量食物致敏成分的有力手段。通过使用不同的荧光探针建立多重qPCR,还可实现多种食物致敏原的同时检测[111]。LAMP法则是基于恒温核酸扩增技术,通过高度特异的颜色/浊度变化进行判定,无需热循环仪器,更适合现场或条件一般的情况下进行快速检测。值得指出的是,依赖DNA的分析手段可能受食品中抑制剂的影响出现误差,提取前加入内标物可帮助提高定量结果的可信性[110]。研究人员通过比较检测同一种致敏原的市售ELISA试剂盒与qPCR试剂盒,发现两种检测方法的结果较为一致,qPCR的特异性更好但ELISA的灵敏度更高,并且两类产品均会受到样品基质效应和加工处理的影响[112-113]。此外,由于PCR类技术并不直接检测蛋白,无法直接反映样品中致敏原的含量,其结果转换为蛋白含量的校准参数也备受争议,另外该手段也不适用于乳类和蛋类样品中的致敏原分析[114-115]。
质谱类技术以高分辨率、高灵敏度和高通量的独特优势,在食物致敏原的识别与检测领域备受关注。该技术克服了免疫学方法通量低和易有交叉反应的弊端,也避免了PCR类方法不能直接检测致敏蛋白的缺陷。食物致敏原的质谱类确证技术可分为“top down”和“bottom up”两类:其中“top down”指的是将完整蛋白离子化后进行质谱检测,最常见的是基质辅助激光解析电离-飞行时间质谱(matrix-assisted laser desorption ionizationtime of flight,MALDI-TOF),但是该方法提供的信息比较有限;另一类“bottom up”是现在主流的分析手段,其原理是利用特异性的酶或其他水解方法将蛋白质切割为小分子质量多肽混合物,利用色谱柱将混合物分离后进行一级或多级质谱的测定,再将得到的数据与蛋白质数据库比对,从而确证目标蛋白[116]。在此基础上建立的致敏原定量方法主要是采用多反应监测的方式(multiple reaction monitoring,MRM),通过选择合适的目标物特征肽段和内标物,实现致敏原的绝对精准定量和多靶标检测。常见的此类技术包括三重四极杆质谱(triple quadrupole mass spectrometer,QqQ-MS)、四极杆飞行时间质谱(quadrupole time-of-flight mass spectrometry,Q-TOF-MS)和四极杆-线性离子阱质谱(quadrupole-linear ion trap tandem mass spectrometry,Q-LIT-MS)等[117]。其中QqQ-MS检出限较低,在食物致敏原分析领域较为常见;此外,在这类方法基础上形成的同位素稀释质谱法已被定义为国际上食品安全检测最精准的仲裁检测方法,具有灵敏度高、特异性强、不易受基质干扰等优势,其在致敏原确证和检测领域的应用正处于积极探索阶段。当然,质谱类检测方法的缺点也比较明显,除了设备和操作要求高、成本昂贵外,基质效应和食品加工可能导致目标物提取不完全,因此这类技术通常会选择不同的基质以考察方法的适用范围,同时优化前处理方法实现致敏原的有效提取等。
最后一类基于生物传感器的检测方法主要是指利用分子识别元件特异性地结合待测致敏原,发生反应后产生的信号通过转换器转变为可以定量处理的光学和电学等信息[118]。生物传感器的种类非常丰富,常见的用于食物致敏原分析的类型有表面等离子共振传感器(surface plasmon resonance,SPR)、电化学免疫传感器和压电免疫传感器等;他们根据识别元件的类型也可分为免疫传感器、核酸传感器和适配体传感器[119-120]。有关不同传感器的原理、特点和应用形式可详见若干前人综述[119-122]。其中,SPR是基于表面折射率敏感变化的一类分析技术,当目标物与传感器芯片结合形成复合物时,反映为传感器表面性质的改变可对致敏原进行定量检测[123]。该类方法具有简单、快速、无需标记、灵敏度高等优势,进一步通过与纳米材料和免疫磁珠相结合,SPR在致敏原确证与检测领域的应用日渐拓展。如Zhou Jinru等将抗体固定在金膜传感器芯片上检测水产品中的原肌球蛋白,检测时间仅为3 min, 检测限为1.0 μg/mL[124]。另一类电化学免疫传感器主要是利用电化学方法对免疫反应进行监测,具体可分为电流型、电位型、阻抗型和伏安型传感器4 类[119]。与其他种类的传感器相比,电化学传感器具有较高的小型化潜力。其中,如Fu Linglin等采用离子交换色谱联立毛细管电泳检测鱼中的小清蛋白,最优条件下检测时间为2.8 min,LOD为0.71 μg/mL[125]。目前,大部分用于定量食物致敏原的生物传感器还处在实验室研究阶段,这类技术的产业化推广无疑会为现有的检测手段提供有力补充。
总体来说,各类检测方法都有其独特的优势,目前尚没有一种方法可以集合各种技术的优势,实现致敏原的精准定量和高效分析(表3)。综合不同方式的特点,笔者认为未来食物致敏原的检测技术可以从以下几个方面着手:1)开发有效的样品前处理方法以实现蛋白的高效提取和纯化,联合背景抑制和/或信号放大手段,避除基质的影响;2)提高分析的特异性,如开发高特异性抗体、筛查稳定特征肽段和适配体等,最大限度地降低交叉反应现象;3)开展基于多种致敏食物的高通量检测手段,特别是针对未知蛋白的非靶标确证技术;4)研究适用于不用场所的快速检测方法和便携设备等。

表3 食物致敏原定量检测方法的优劣势对比Table3 Comparison of different methods for food allergen quantification
3 食物过敏的诊断与控制
3.1 食物过敏的诊断:传统与新兴诊断技术
食物过敏可以分为IgE介导和非IgE介导的反应两类,其中非IgE介导的类型因发病机制不明确、病程缓慢且临床表现各异,现今缺乏公认的诊断标准[126],本文将主要针对IgE型食物过敏的诊断展开探讨。临床上,医生在询问患者病情和家族过敏史,确定其为食物过敏引起的不良反应后,可以通过食物激发(oral food challenge,OFC)、SPT和饮食回避等体内方法,联合血清sIgE的检测等体外方法进行确证。
OFC实验包括开放性食物激发实验、单盲安慰剂对照食物激发实验和双盲安慰剂对照食物激发实验(double-blind placebo-controlled food challenge,DBPCFC)。开放性食物激发实验,即使用天然形态的食物激发,医患双方均知情,主要用于婴幼儿及少儿群体的食物过敏诊断;单盲安慰剂对照食物激发实验,通过制备食物胶囊等掩盖受试食物的性状和气味,同时设置安慰剂,医生知情但患者不知情,可以帮助排除患者心理因素的影响;DBPCFC,即制备食物胶囊和给予激发时,医患双方均不知情,是目前国际公认的食物过敏诊断“金标准”[2,127-128]。虽然OFC是食物过敏最准确的诊断方法,但是该实验程序复杂,必须在有专业医务人员和设施准备充分的条件下进行,不规范操作可能引起严重的过敏反应[129]。相比之下,SPT通过采用食物提取物/新鲜食物进行局部皮肤表层的侵入刺激,根据产生的风团和红晕反应进行判断,具有操作简单、灵敏度高、安全性好的优势,阴性结果准确率大于90%,但需注意该方法的特异性不高,并且由于没有统一标准化的测试物,不同机构间SPT结果95%阳性的预测值存在一定差异[130]。此外,饮食回避则是通过短期回避暴露的可疑食物,后期观察临床症状的变化辅助明确食物过敏的种类,但是饮食回避易受患者机体状况和其他因素的干扰,不能作为食物过敏的确诊依据。另一方面,血清sIgE水平是反映机体识别致敏原的客观指标,检测血清sIgE水平是常用的食物过敏体外诊断方式,其中ImmunoCap系统是目前较为广泛使用的致敏原检测系统,可提供多达600 种食物抗原的sIgE分析。有报道称,联合SPT和血清sIgE检测可显著提高食物过敏诊断的准确率,阳性预测值高达92%[131]。
近年来,在已有诊断技术的基础上,逐渐发展出现了一系列新兴的检测方法,包括致敏原成分诊断(components-resolved diagnosis,CRD)、嗜碱性粒细胞激活和肥大细胞激活实验等。简单来说,CRD是使用单一致敏原成分替代原有粗提物进行诊断的方法,例如使用Ara h 2和Ara h 6诊断花生过敏,使用Cor a 9和Cor a 14诊断榛子过敏,使用Jug r 1诊断核桃过敏,使用Ana o 3诊断腰果过敏等[132-134]。CRD在区分花粉症与食物过敏的诊断上很有意义,因为许多植物花粉与食物间存在交叉反应性,如榛子Cor a 1与桦树Bet v 1会有交叉反应,以Cor a 9和Cor a 14取代榛子粗提物可以帮助判断患者是因榛子还是桦树花粉引起的过敏。Flores Kim等通过汇总分析有关牛乳、鸡蛋、花生和虾等过敏食物的CRD研究发现,选用特定致敏原取代原有粗提物可显著提升诊断的特异性,但灵敏度却有所降低;此外由于各项研究结果的差异性,CRD的进一步应用需要确定合适的诊断阈值、风险评估控制和方法成本效益等[133]。另一方面,肥大细胞和嗜碱性粒细胞是IgE型变态反应的效应细胞,经与致敏原结合发生脱颗粒,释放活性介质引起过敏症状(原理详见2.2.2节叙述)。Ford等研究发现牛乳过敏与耐受患者嗜碱性粒细胞表面CD203的表达存在显著差异,且与临床过敏症状的严重程度有关[135]。Bahri等将人原代肥大细胞用于花生过敏的诊断,发现活化后细胞表面标志物的表达(CD63和CD107a)、前列腺素D2及β-己糖胺酶的释放可显著区分过敏患者,其诊断效果比CRD法更精确[136]。
随着分子生物学、蛋白组学和基因组学的不断发展,研究人员也提出了一系列可能辅助食物过敏诊断的新型标志物,主要涉及免疫细胞、体液和基因等方面,此处笔者不再赘述,部分内容可详见Eiwegger等[132]的报道。值得指出的是,近年来,机器学习和人工智能在医学领域显示出了独特的生命力,或可为食物过敏的精确诊断和处理提供有力方案。图4汇总了食物过敏新型诊断方法及发展趋势。

图4 食物过敏新型诊断方法及其发展趋势[132]Fig. 4 Novel approaches in diagnosing food allergy and future trends[132]
3.2 食物过敏的口服免疫耐受治疗与限制
针对食物过敏的处理,临床上没有一致认可的治疗手段,口服免疫疗法(oral immunotherapy,OIT)是其中比较公认有效的治疗措施。OIT是指通过有意的低剂量、长时间暴露于致敏原,不断刺激机体对致敏原的耐受能力,诱导患者逐渐达到对特定食物致敏原的耐受或持续无应答的效果,属特异性致敏原免疫治疗(allergenspecific immunotherapy,ASIT)的一种。临床OIT治疗分为3 个阶段:1)单日剂量递增阶段,在临床监护下通过短时间内暴露梯度浓度致敏原,确定患者的个人最高耐受剂量;2)连续剂量递增阶段,保证受试者不发生严重不良反应的前提下,每1~2 周增加一次口服剂量,持续3~9 个月甚至更长时间,直至达到目标耐受剂量;3)维持阶段,患者每日自行服用安全耐受剂量并定期追踪复查,该阶段通常持续数月到数年不等[137-138]。实际操作OIT时使用的食物和载体类型可能各异,有些使用现成的市售食品(如液态奶或花生粉),有些则使用特别处理的产品,如脱水蛋清或水解蛋白[138]。
临床OIT治疗后一般通过口服食物激发试验评估其有效性,根据患者阈值提高的程度和维持的时长判定属于暂时性脱敏还是持续无应答。大多数在治疗期间实现脱敏的受试者停止治疗后,只有少数能实现持续无应答[138]。目前有关OIT治疗食物过敏的研究主要集中于花生、牛奶和鸡蛋这3 类最常见的过敏食物。尽管多数报道指出,受试者经OIT治疗后可在不同程度上提高其对目标致敏原的耐受性,但是有关OIT对过敏病人长期生活质量(quality of life,QOL)改善的数据并不一致。如Epstein-Rigbi 等追踪了191 位4~12 岁接受OIT治疗的儿童,通过食物过敏生活质量问卷调查发现,受试者在治疗期间直至达到维持阶段的QOL显著提高,且在治疗结束6 个月后持续有提升效果[139];但另一项发表在《柳叶刀》上的研究却发现花生过敏人群在OIT治疗后发生过敏和不良反应的风险比未接收治疗的患者高出3 倍,且在少数评估QOL的实验中,两组患者并不存在差异[140]。
2020年1月底,美国食品药品监督管理局(food and drug administration,FDA)批准了全球首个治疗食物过敏的OIT制剂——Aimmune Therapeutics公司的PALFORZIA,适用于4~17 岁诊断出花生过敏的儿童,可减轻意外摄入花生后的不良反应,包括过敏性休克。目前,大多数OIT疗法仍然处于临床研究阶段,且有许多问题尚未解决:首先,口服抗原的剂量和疗程时间难以确定,维持期后患者依赖于食物的长期摄入,耐受程度可能随时间的延长逐渐下降,另外,某些致敏原的耐受剂量与致敏剂量间范围较窄,掌握不当可能引发严重不良反应;其次,OIT疗法的免疫机制尚未明确,脱敏治疗成功的生物标记物有待确定。初步认为Th1细胞的激活、Th2细胞的凋亡及失活以及Treg细胞的变化与OIT的机制有关,但是其深层次的脱敏过程及与健康状态下免疫耐受的差别值得深究[4,141];最后,OIT联合疗法是近年来出现的新热点,例如OIT结合使用奥马珠单抗或益生菌在部分研究中发现有理想的脱敏效果,但是其疗效和安全性有待进一步确定[142-143]。
3.3 消减食物致敏原的新型加工技术
食品在加工过程中会经历一系列物理、化学和生物学变化,引起包括蛋白质在内的各种成分发生改变。这一过程中,致敏原结构的变化可能引起表位的改变,原有的表位被破坏/掩盖致敏性降低或者形成新的表位致敏性增强[144-145]。近年来,使用新型加工技术消减致敏原制备低敏性食品的研究备受关注。根据原理的不同,可将这些手段分为化学修饰、物理加工和生物处理方法。本文将主要围绕其中的物理和化学修饰加工技术进行介绍(图5)。

图5 消减食物致敏原的新型加工技术及其优劣性Fig. 5 Classification, and pros and cons of novel processing techniques for reducing food allergens
化学修饰方法主要包括蛋白酶酶解、非酶糖基化和交联酶处理等。其中蛋白酶酶解是最为广泛使用的致敏原消减手段,利用酶的水解作用断解肽链,破坏致敏原的线性和构象表位,生成的短链肽难以再与肥大细胞/嗜碱性粒细胞表面的sIgE发生交联反应。在传统酶解工艺的基础上,研究人员近期发现,靶向酶解致敏原B细胞表位但保留其T细胞表位可能是一种理想的食物脱敏手段。Ueno等通过蛋白酶种类和酶解条件的摸索[146],发现利用Alcalase在碱性条件下水解αS1-酪蛋白,得到的产物免疫原性被大幅消减,但其抗原性得到了部分保留,可以作为肽类口服免疫疗法制剂使用。除蛋白酶酶解外,非酶糖基化也是一种有效的降敏加工方式,其原理是利用还原糖(或其降解产物)与蛋白质自由氨基间发生美拉德反应,通过侧链接枝和共价交联,改变致敏原结构、掩盖致敏原表位[147]。如Fu Linglin等利用核糖、低聚半乳糖和壳寡糖与虾原肌球蛋白发生美拉德反应,产物的抗原性最高可降低60%,且蛋白质接枝度、二级结构含量和产物的sIgE-结合能力具有一定相关性[148]。此外,谷氨酰胺转移酶等交联酶的使用能催化蛋白质发生链内/间交联反应,也可在一定程度上改变蛋白质构象,达到消减致敏原的目的[149]。总体上,以上化学修饰方法具有易操作、成本低和效率高的优势,但是其缺点也比较突出,例如酶解易产生苦味肽,也易造成蛋白质加工功能的损失,影响食品的感官和质构;糖基化和交联反应较难控制,生成的有害伴随产物(如晚期糖基化终末产物)存在潜在安全风险等。
另一方面,物理消减手段近年来逐渐受到研究学者们的重视,常见的如超声、超高压、低温等离子体、辐照、微波和脉冲电场等[150-151]。从原理上看,物理加工方式多是利用某种物理场的作用,诱导蛋白质发生构象变化,进而影响致敏原的表位结构。例如大豆分离蛋白经低温等离子体处理后,蛋白质与溶液中的活性粒子发生反应,二级结构和构象结构发生改变,经特定条件处理后蛋白的抗原性降低可达75%[152]。关于物理加工手段消减食物致敏原的报道请详见Ekezie等的汇总[153]。物理加工方法因不涉及化学试剂安全性较高、使用集成化设备也更适合大规模生产,但是由于各种物理场-致敏原相互作用的机制尚未明确,处理过程中“曝露条件-构象变化-致敏性”的构效关系也尚未明晰,上述技术处理后产物的抗原性变化趋势高低不一;此外,物理加工手段无法破坏蛋白质的线性表位,因而无法完全消除受试食品的致敏性。除了涉及物理场的加工技术外,近年来还出现了一类利用蛋白质-小分子互作构建低敏蛋白的报道,主要是致敏原与多酚间的相互作用,其原理是利用分子间的非共价作用力,如氢键、范德华力和疏水相互作用改变体系中致敏原的构象结构,进而影响其抗原性。已报道的“致敏原-多酚”低敏互作物如“花生Ara h 2-绿原酸”[154]、“乳清分离蛋白-茶多酚”[155]和“醇溶蛋白-越橘属多酚”[156]体系等。
总之,食品加工是通过改变蛋白质结构(一级或构象结构)改变致敏原表位(表位结构或可及性),进而影响其抗原性的。不同的加工手段对致敏原造成的影响各异,作用的对象和机理也各不相同,需要根据处理对象和应用需求有针对性的选择。另外,值得指出的是,目前有关各类加工技术,尤其是物理手段对致敏原免疫活性的影响研究较为初步,在不同处理过程中涉及的具体抗原表位和关键信息需要得到解析。
3.4 基于肠道菌群调控的食物过敏调控手段
近年来,越来越多的证据表明,肠道菌群可以通过与宿主黏膜免疫系统的复杂相互作用调节机体免疫。益生菌作为一类对宿主有益的活性微生物,经口服等方式摄入后,定植于人体肠道,改善机体微生态平衡和肠道菌群结构,具有治疗和预防过敏性疾病的作用。目前有关益生菌缓解过敏的研究,多数关注于乳杆菌属(Lactobacillusspp.)和双歧杆菌属(Bifidobacteriumspp.)[157],并且主要集中在湿疹和哮喘两类过敏性疾病,少数有涉及食物过敏人群的干预实验[158]。Kuitunen等对891 名新生儿进行了长达5 年的随访,发现混合益生菌干预(含乳酸杆菌、双歧杆菌和丙酸杆菌)在全队列中没有预防湿疹等过敏性疾病的效果,但在剖腹产婴儿中可显著降低IgE介导的湿疹和食物过敏反应的累积发病率[159]。另一项采用短双歧杆菌和嗜热链球菌发酵的牛乳干预高风险儿童的研究发现(n=129),干预1 年后幼儿牛乳过敏的发病率虽然没有显著变化,但是SPT的阳性率和发生呼吸道和消化道不适症状的几率有所降低[160]。Tan-Lim等通过分析9 项利用益生菌干预牛乳过敏儿童(n=895)的随机对照实验发现,食用益生菌可能起到缓解过敏性湿疹症状的作用,但是无法确定对口服耐受是否有影响,并且由于各项研究结果的异质性较高,该项Meta分析的结论有待进一步确认[161]。
益生菌调节黏膜免疫系统的机制主要涉及肠道黏膜屏障的修复、微生态结构的改变、调节性T细胞和辅助性T细胞平衡的调节、免疫细胞功能及表型的调控、sIgE抗体的类别转换等[157,162-163](图6)。如Fu Linglin、赵淑淑等对虾原肌球蛋白过敏的小鼠模型进行经口灌胃乳酸菌或双歧杆菌处理,发现益生菌干预可在不同程度上缓解小鼠的过敏症状,改善肠道屏障状态,降低血清中sIgE的水平等,其机制可能是通过诱导Treg细胞的形成抑制Th0细胞向Th2方向分化倾斜,达到将特异性抗体同型向耐受模式转换的目的[164-167]。类似地,在对花生过敏的小鼠模型中,饲喂混合益生菌制剂VSL#3可诱导小肠上皮细胞产生TGF-β,调节FOXP3+Treg细胞的产生,抑制Th2型细胞因子的释放和炎症反应,缓解食物过敏[168]。Schiavi等也发现VSL#3能够减轻小鼠模型中对虾原肌球蛋白引起的全身和局部性过敏反应[169]。尽管现有研究针对益生菌缓解食物过敏的机制进行了探索,但是有关益生菌调控肠黏膜免疫的机理还有许多问题没有解决。例如,以上提及的理论似乎无法解释不同益生菌菌株在作用效果上的差异,也无法说明不同体质人群摄入益生菌后缓解程度各异的原因。一方面,益生菌可能直接作用于免疫系统调节DCs的活性和T细胞类群的分化趋向发挥作用;另一方面,益生菌介导的肠道共生菌及其代谢物的改变,特别是短链脂肪酸(如乙酸盐、丙酸、丁酸及其盐类)含量的变化,在维持肠道固有层中FOXP3+Treg细胞的比例和调节免疫应答等方面也有重要作用。针对“膳食成分-肠道微环境-宿主免疫”之间的复杂网络关系还有许多问题尚未得到解答。

图6 益生菌缓解食物过敏的潜在机制[157]Fig. 6 Potential mechanisms of probiotics in the regulation of allergic responses[157]
3.5 食物过敏标识的风险评估
食物致敏原是造成食物过敏风险的主要不可控因素,实施致敏原风险评估与管理对于保护食物过敏患者的权益和健康至关重要。简要来说,致敏原风险评估的目的在于明确食品中有意加入和无意带入的致敏原导致过敏患者发生不良反应的风险;而致敏原风险管理则是通过相关法律法规的制定、食物致敏原的标识与标准化以及污染食物的确证与控制等措施实现的[170]。标准化的风险评估流程分为4 个步骤,即危害识别、危害特征描述、暴露评估和风险特征描述[171]。危害识别指的是包含致敏原的食物,如前述的八大类以及各地区的其他常见致敏食物(基于流行病学调查确定);危害特征描述,即需要确定人群的致敏阈值,这是风险评估的重要参考数据。其中比较公认的是由澳大利亚和新西兰过敏原管理局制定的自愿附带微量致敏原标签体系(voluntary incidental trace allergen labeling,VITAL)。该体系是由专家组成员通过分析高质量的已发表文献、未发表的临床数据和FARRP开展的研究,经统计学建模后得出主要易致敏食物的剂量-反应效应,最后基于ED01(eliciting dose 01)(每100 位过敏患者中会有1 人发生过敏反应,即保护99%的消费者,下同)或ED05原则提出的参考剂量[172-173]。VITAL体系在2007年被首次提出,现已升级至3.0版本,其中不仅涵盖了更新的致敏阈值清单,还包括风险审查等系列指导意见[174]。暴露评估是风险评估的第三阶段,通过排查市售常见致敏食物及其加工产品中致敏原的含量,结合问卷调查中居民膳食的相关数据,明确易过敏人群可能摄入的各类致敏食物的剂量,并据此建立概率评估模型。最后,风险特征描述则是基于以上三部分的结果进行总结评估,为过敏食物标识清单等管理措施提供参考依据。
在我国,由于受到流行病学数据、致敏阈值和暴露评估数据的限制,食物过敏标识的风险评估还处在初步研究阶段。不过相信,随着我国普通人群流行病学数据的不断补充、食物过敏临床诊断的日益深入,以及食物致敏原评价和确证技术的逐渐改进,符合我国国情的食物致敏原标识与风险管理将逐步得到完善。
3.6 国内外低/无敏食品及产业展望
目前,国内外有关低敏或无敏食品的开发研究中,技术成熟且已实现产业化发展的主要有无麸食品和婴幼儿食品两类。其中,无麸食品是指不含麸质的食品,适用于乳糜泻及麸质过敏患者,同时也被推荐给运动员和患有桥本病和自闭症的人群食用。麸质,又称谷蛋白,是一类存在于小麦、黑麦和大麦中的储藏蛋白,主要由麦谷蛋白和麦醇溶蛋白组成,是小麦及其制品中的主要致敏原。天然存在的可用于制作无麸食品的原料主要来自于特定谷物、假谷和豆类,如大米、小米、玉米、木薯、荞麦、藜麦和羽扇豆等[175-176],此外也可添加蔬菜,如南瓜、胡萝卜和菠菜等[177]。无麸食品在西方国家的普及度较高,但不同地区的标准有所差异,如美国FDA规定生产企业在其食品所含麸质低于20 mg/kg的情况下可标注“无麸质”(“gluten-free”或“no gluten”),欧盟(Commission Regulation (EC) No. 41/2009)、加拿大、阿根廷和国际食品法典委员会标准(Codex Standard 118-1979)对“无麸质”的限量要求与FDA相同,但澳大利亚和新西兰(Australia New Zealand Food Standards Code-Standard 1.2.8)的规定更为严格,要求“无麸质”标签产品“不得检出”麸质,即含量低于已知方法的最低检出限7 mg/kg。目前,我国尚未出台有关“无麸质”的食品标准,但已有几项关于麸质致敏原检测的标准相继发布(SN/T 1961.11—2013《出口食品过敏原成分检测 第11部分:实时荧光PCR方法检测麸质成分》和SN/T 4286—2015《出口预包装食品麸质致敏原成分风险控制及检验指南》)。
据统计,乳糜泻在欧美白种人中的发病率约为1%甚至更高,且在1990—2010年间呈逐年上升趋势[178-179];我国人群中乳糜泻的发病率尚不明确,但部分省份16~25 岁群体血清学筛查的阳性率高达2%[180],考虑到我国尤其是北方地区人群的基因易感性较高,且麸质过敏症状较为“隐性”不易察觉,我国人群中麸质过敏的暴露风险不容小觑[181-182]。除麸质过敏患者外,追求无麸质饮食的健康人群也在不断扩张,这使得全球范围内的无麸质食品产业迅速增长。据权威统计机构Statista公布的数据,2020年全球无麸质食品的销售额约为56亿 美元,2025年预计增长达到83亿 美元[183]。目前,无麸饮食作为一种新兴的饮食理念受到许多商家和消费者的推崇,但是与含麸食品相比,无麸食品在营养价值和感官品质上存在一定缺陷:首先,无麸食品一般抗性淀粉和膳食纤维含量偏低,且易存在VB、VD和铁、锌等矿物质的缺乏,加工后的无麸食品也可能含有较高的油脂、饱和脂肪酸和盐[184-185]。如Allen等[185]通过调研英国零售市场上常见的无麸面包信息,发现仅有5%的产品按照要求进行了4 种营养素(钙、铁、烟酸和硫胺素)的强化,而28%的产品仅对钙和铁进行了强化。其次,由于不含面筋蛋白,无麸原料制成的面团在黏度、弹性、保水性和吸水率等物性特征上并不理想,导致最终产品在感官特性上存在不足[175]。如何开发出更加营养健康、安全美味的无麸食品是未来研发的主要方向:一方面,需要综合关注无麸食品配方的营养素含量,对缺乏或过量的宏/微量营养成分进行补充和改良;另一方面,外源添加功能性成分(如多糖和蛋白胶体),同时控制好粉料性质、面团制作和发酵工艺,也是提高无麸质食品品质的有效手段[186]。
近年来,低敏/无敏婴幼儿食品产业一直稳步发展,主要包括婴幼儿配方奶粉和营养米粉等辅食。牛乳过敏是婴幼儿最常见的食物过敏种类,低敏/无敏配方奶粉是通过将牛乳蛋白部分或全部水解为小分子肽段和氨基酸,破坏天然牛乳蛋白的表位结构,大大降低其致敏性。市面上常见的低敏婴幼儿配方奶粉主要包括游离氨基酸型、深度水解型和部分水解型,也有采用(酶解)大豆蛋白替代乳清粉或全部乳粉的类型,但需注意这些产品可能在部分牛乳过敏儿童中发生免疫交叉[187-188]。此外,主打“低敏”概念的营养米粉等辅食则是通过使用不易过敏的食品原料进行生产,因此制得的产品致敏风险较低。
除了以上提及的两类食品外,其他种类的低敏/无敏食品大多处于初步研究阶段,离产业化发展还有一段距离,但是相信,随着未来国内和国际食品市场的不断细分和行业内对食物过敏问题的日益重视,专门为不同食物过敏患者和易感群体设计的低敏和无敏食品将会不断涌现出来。
4 结 语
当前,食物过敏的发病率逐年攀升,这给社会、家庭及个人带来了严重负担。现代饮食习惯和生活方式的改变正潜移默化地影响着人群对过敏性疾病的易感性,同时,食品工业的快速发展,涉及的原料和产品日益增多,饮食规避对于食物过敏患者也将越来越困难。食物过敏已经成为食品行业必须面对和解决的食品安全问题。一方面,为了更好地了解我国食物过敏人群的特点,亟需开展针对全年龄段普通人群的流行病学调查,利用遗传学、表观遗传学、微生物学和多组学技术,联合生物信息学手段,系统研究可能诱发食物过敏的风险因素和免疫学机制;另一方面,为了进一步保障易感人群的健康和生活质量,相关人员应继续探索各类致敏原的高效分析手段,建立体内外评价方式,开发靶向消减技术,并积极推进低敏/无敏食品产业的发展等等。此外,考虑到肠道菌群失调与食物过敏的密切关联,有关肠道微生物调节食物过敏的机制,以及利用益生菌或益生元缓解食物过敏的功效研究也需进一步的探索、验证与实践。
