活性炭催化热解纤维素协同制备酚类和合成气
2021-10-31苏银海张书平刘凌沁熊源泉
苏银海,张书平,刘凌沁,熊源泉
(1南京理工大学新能源学院,江苏江阴 214443;2南京理工大学能源与动力工程学院,江苏南京 210094;3能源热转换及其过程测控教育部重点实验室,东南大学能源与环境学院,江苏南京 210096)
引 言
苯酚是一种重要的基础化工原料,在化工合成中有着诸多应用,常被用于酚醛树脂、酚酞以及各种药品的生产合成。目前工业生产中的苯酚主要来自化石燃料中提炼的异丙苯合成[1],但合成效率不高,且化石资源不可再生。因此,以绿色可再生的生物质为原料获取酚类化合物极具意义。快速热解技术是一种将固体生物质转化为液态生物油的有效方法[2]。但直接热解生物油含水率较高(通常为15%~50%(质量)),且有机组分复杂[3],一般由数百种化合物组成。有机组成又可分为难以检测的有机大分子和可检测的小分子化合物,一般认为只有生物油中的小分子组分具有较高的潜在利用价值。生物油中的酚类物质主要来自于木质素的热分解,只占可检测组分的20%~30%[4],这给酚类的分离提纯带来了很大的困难。此外,木质素是一种具有复杂空间网状结构的无序大分子,由三种苯并烷基单体(愈创木基、紫丁香基和对羟苯基)通过C—C键和C—O键连接而成[5]。因而生物油中的酚类物质通常包含多种甲基、甲氧基、乙基单酚,组成的复杂性进一步降低了生物油的可利用价值[6]。
通过选用合适的催化剂调控生物质热解路径,选择性地提高生物油中某一种或某一类化学品含量的工艺称之为催化热解[7]。研究发现多种催化剂能够有效提升生物油中酚类的富集度。如碱性催化剂通过促进木质素中醚键的断裂,增加生物油中酚类组分的含量[8-11]。Lu等[12]发现向生物质中浸渍一定量的磷酸同样可以提高酚类组分收益率。当浸渍量为7.42%(质量)时,单酚类物质最大峰面积百分比为42.8%。进一步研究发现[13],氢气气氛有利于酚类物质的富集。550℃时,氢气气氛协同作用下,苯酚产率高达5.3%(质量)。Bu等[14]发现磷酸法制备的活性炭能够高选择性地富集单一苯酚。进一步研究表明,非原位催化相比于原位催化有着更高的苯酚选择性[15],且活性炭催化剂能够重复使用3~4次[16]。Su等[17]在研究中发现活性炭催化后的生物油中水含量可达约96%(质量),水分剩余有机组分以酚类小分子为主。
上述研究侧重于通过催化作用促进木质素组分的裂解来提高单酚化合物收益率。但生物质主要组分除了木质素,还有纤维素和半纤维素[18]。常规认知中,酚类物质主要来自于木质素的催化转化,纤维素在热解过程中很难向苯酚转化。但Zhang等[19]通过实验发现纤维素热解生成的葡萄糖单体,经活性炭催化转化后可获得高纯度的苯酚。同时,热解气中还会生成高浓度的CO。合成气(CO+H2)是一种极具价值的基础工业原料,在能源和化工行业中有着诸多应用。既可以直接作为燃料用于燃烧发电,也可以通过化学合成转化为各种化学品。根据H2/CO的摩尔比合成气有不同的用途。摩尔比<1时,可用于合成酸类;摩尔比≈2时,可用于合成醇类;摩尔比>3时,可用于氢源与氮气反应合成氨。因此,本文着重于探讨纤维素向苯酚和CO转化的可能性及影响因素。文中利用自行制备的磷酸法活性炭作为催化剂,利用固定床催化热解反应器研究生物质灰分中的钾元素、催化剂/纤维素质量比以及催化热解温度对纤维素向苯酚和CO同时转化的影响,并对纤维素的催化转化路径进行简要分析。
1 实验材料和方法
1.1 实验材料
实验用到的材料包括纤维素、木粉、磷酸、乙酸钾、乙醇和无水硫酸钠。其中,微晶纤维素为热解原料,呈现白色粉末状,购自Aladin公司。杨木粉由连云港某木材加工厂提供,筛取0.3~0.6 mm颗粒用于制备活性炭催化剂。活化剂为磷酸(分析纯,85%(质量))。灰分对纤维素热解的影响采用乙酸钾(分析纯)模拟,所用吸水剂为无水硫酸钠(分析纯),所用溶剂为无水乙醇(分析纯),均购自成都市科隆化学品有限公司。实验前,将纤维素和杨木粉置于通风干燥箱中105℃干燥,表1为纤维素和杨木粉的燃料特性分析(干燥基),热值采用弹筒热值仪测量。
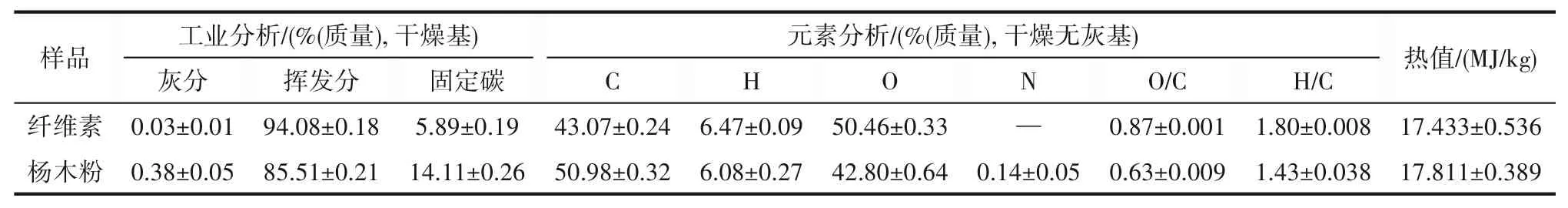
表1 纤维素和杨木粉的燃料特性分析Table 1 Fuel characteristics analysis of cellulose and poplar wood
1.2 活性炭催化剂的制备及表征
实验所用活性炭催化剂以杨木粉为原料,采用磷酸活化法制备。流程如下:将20 g杨木粉和20 g磷酸(85%(质量))依次加入300 ml去离子水中,室温磁力搅拌24 h。随后,置于通风干燥箱110℃下干燥36 h。将干燥后的混合物取出,氮气气氛下,以10℃/min升温至600℃煅烧90 min。待反应物自然冷却后取出,使用去离子水反复洗涤浸泡至中性。干燥后,研磨筛取0.1~0.3 mm颗粒备用。
活性炭催化剂的孔隙结构采用N2自动吸附/脱附分析仪(Micromeritic USA ASAP 2020M)检测,表面形貌特征通过配备X射线能量色散谱(EDS,AZtec,Oxford,UK)的扫描电子显微镜(SEM,SU3500,Hitachi,Japan)进行观察,表面官能团分布由傅里叶变换红外光谱分析仪(Bruker Vector 22)获得。
1.3 催化热解实验流程
实验系统示意图如图1所示,所用催化热解装置为固定床。固定床反应器从上至下划分为三部分:顶部冷却段、中部热解段和底部催化重整段。每组实验前,在催化段中垫入石英棉,并将活性炭催化剂均匀装载至石英棉上。称取热解原料(纤维素)约2 g装入石英吊篮中,实验开始前吊篮位于反应器顶部冷却区。将气路连接完整,并通入200 ml/min氮气吹扫10 min后,将反应器加热至预设热解温度。温度稳定后,将石英吊篮快速推入热解区,保持15 min。纤维素热解过程中释放的挥发分被载气携带,经催化剂层催化重整,最终以气态形式进入冷凝装置。液相产物经由冰水混合物冷凝收集,不可冷凝气相组分经过滤吸水后,由气体采样袋收集。催化反应结束后,将石英反应器从电加热炉中移出,风冷降至室温后取出热解焦和反应后的催化剂,称取两者质量。液相产物质量为反应前后冲击瓶的质量差;催化剂积炭量由反应前后催化剂的质量差计算;气相产物先由煤气分析仪检测各组分体积分数,根据载气量计算出体积产量,并由气体摩尔体积公式计算气相产物质量。产物质量平衡为热解三相产物质量与积炭量之和与热解原料质量的比值。对比组实验中,以石英砂代替催化剂,其他条件相同。所有实验均进行三次,取平均值。

图1 催化热解实验装置示意图Fig.1 Schematic diagram of experimental equipment for catalytic pyrolysis
1.4 催化热解产物的分析
冷凝收集到的生物油加入一定量无水硫酸钠静置过夜吸除水分,过滤后以无水乙醇为溶剂进样测试。有机物组分由气相色谱/质谱联用仪(GC/MS)测定,型号为Agilent 7890A/5975C,配VMS毛细管柱,载气氦气(流速1 ml/min),进样口温度230℃,进样量1μl,分流比5∶1,溶剂延时4.5 min。进样时,初温设置为40℃,保持3 min,以5℃/min升温至180℃,再以10℃/min升温至230℃,保持温度2 min。谱图离子峰对应的有机物种类,通过与美国国家标准和技术研究所(NIST)标准谱库鉴别。实验前将所有生物油样品定容至10 ml,因此文中使用单酚物质的离子峰面积近似代替真实产率,峰面积比代表相对含量。催化热解主要产物苯酚的真实质量产率采用外标法测定[20]。
气相产物的组成采用煤气分析仪(德国,MRU,VARIO PLUS)检测。主要分析热解气中的CO、H2、CO2和CH4,含量较低的C2、C3和C4组分忽略,默认剩余组分为载气N2。气相产物总体积由载气体积除以载气体积百分比求得。主要气体组分的相对体积含量(Ai,%(体积))由式(1)计算:

主要气体组分的单位质量体积产率(Vi,ml/g)由式(2)计算:

式中,Ai是组分i的体积分数(包括CO、H2、CO2和CH4),%;V为全部气态产物的总体积(包含载气N2),ml;m为纤维素质量,g。
合成气有效组分相对体积含量(%(体积))和单位质量体积产量(ml/g)分别由式(3)和式(4)求得:

气相产物的低位热值(LHV,MJ/m3)由式(5)求得[21]:
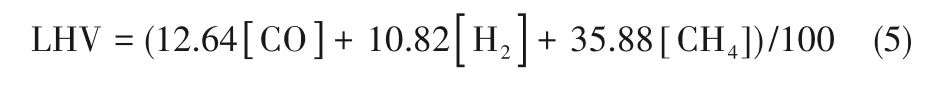
2 实验结果与讨论
2.1 活性炭催化剂的表征
活性炭催化剂孔隙结构如图2(a)所示,等温氮气吸附/脱附曲线为典型的I型曲线。在低压段呈现快速上升趋势,表明所制备的催化剂具有丰富的微孔结构。在中压段(相对压力介于0.3~0.8)存在迟滞回环,这表明所制备的催化剂还具有一定的中孔结构。图2(a)中的孔径分布曲线显示活性炭在1~4 nm间有着密集的孔隙分布,为典型的埃孔碳。根据吸脱附结果,计算得到的BET比表面积和平均孔径分别为1451.43 m2/g和2.219 nm。图2(b)中的红外谱图提供了热解焦和活性炭催化剂的表面官能团的详细信息,其中热解焦为同温度下热解的杨木粉。由图可见,两者红外谱图区别明显。表明活化过程赋予了催化剂独特的表面结构。700和1550 cm-1处对应着芳香环中—C C和—C—H键拉伸振动,对应着催化剂较高的碳化程度[22]。1050和1150 cm-1处吸收峰分别代表磷酯结构中的P O键和C—O—P结构[23]。这表明活化过程将丰富的含磷官能团引入了活性炭表面,结合NH3-TPD谱图[图2(c)]在300~400℃温度区间较为显著的吸收峰[24],可认为所制备的活性炭为一种具有中等酸强度的多孔固体酸催化剂。
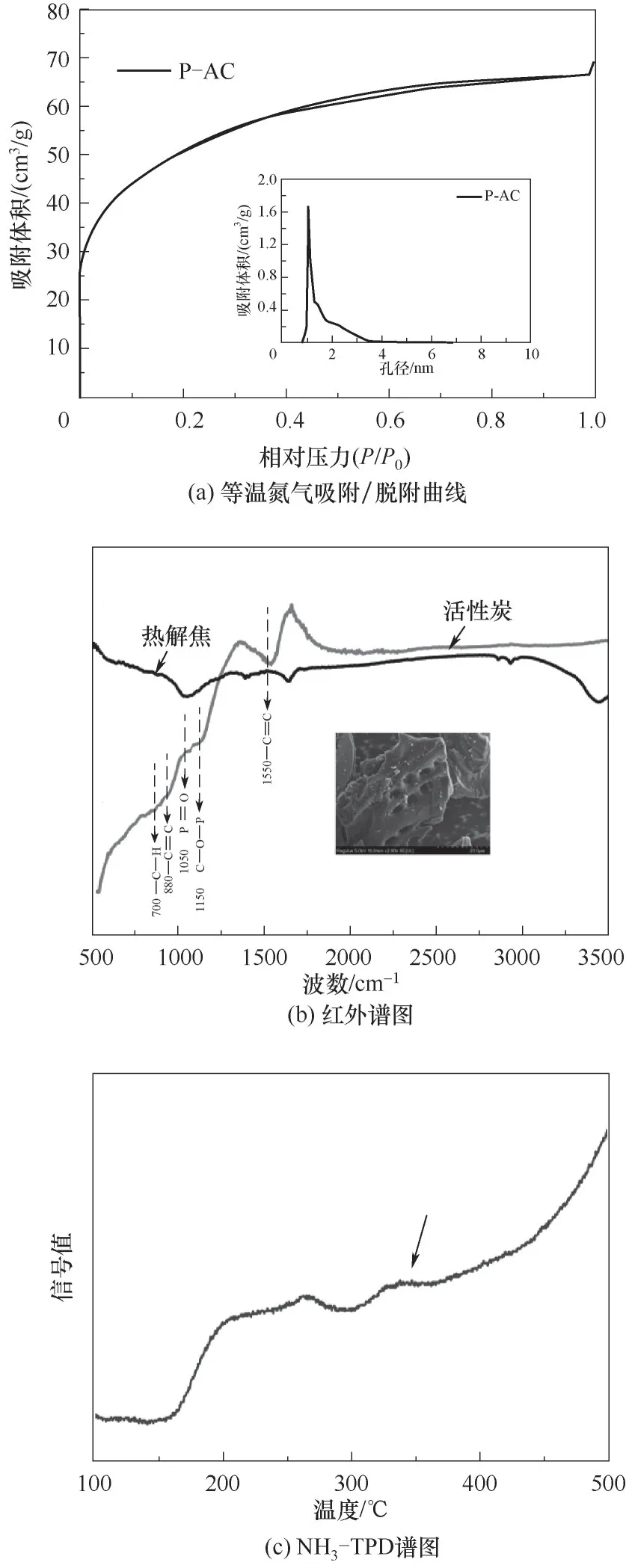
图2 活性炭催化剂的表征Fig.2 Characterization of activated carbon catalyst
2.2 钾对催化热解产物的影响
图3给出了热解温度为450℃、催化剂比例为1∶1时,纤维素催化热解产物的质量分布和离子色谱图。图中C和KC分别表示未浸渍和浸渍钾的纤维素催化热解实验结果,C-N和KC-N分别表示直接热解的未浸渍和浸渍钾的纤维素。钾浸渍样品制备:纤维素中加入1%(质量)乙酸钾和一定量去离子水,混合均匀,60℃通风干燥过夜。图3(a)中热解焦质量分布的变化表明钾的加入和催化重整过程均会在一定程度上促进热解焦产率的上升。这一现象与文献报道一致,前者主要来自于钾对热解挥发分的二次裂解作用[25]。后者则是由于催化剂层增加了热解过程中的流动阻力,延长了热解挥发分与热解焦接触时间,导致焦催化的二次裂解作用增强[22]。这一现象同样反映在生物油和热解气的变化规律中。以C-N和KC-N为例,钾的二次裂解作用导致KC-N中生物油产率下降,热解气产率上升。但在C和KC中,生物油和热解气的质量分布主要由催化重整过程决定。经催化重整后,生物油产率从直接热解生物油中的50%(质量)左右大幅下降至35%(质量)左右,而热解气变化规律则相反。这可能与钾导致的热解挥发分组分的改变相关。

图3 钾对纤维素催化热解产物质量分布的影响(a)及典型离子色谱图(b)Fig.3 Effects of potassium on mass distribution of catalytic pyrolysis products from cellulose(a)and typical ion chromatograms(b)
图3(b)中给出了GC/MS测得的离子色谱图,图中离子峰1、2、3、4分别代表苯酚、2-甲基苯酚、3-甲基苯酚和糖类。直接热解组C-N和KC-N中明显观察到代表糖类的离子峰4以及大量代表其他小分子含氧组分的离子峰,但代表单酚类的离子峰强度较低。催化热解组C和KC与此相反,谱图中主要呈现代表苯酚、2-甲基苯酚、3-甲基苯酚的三组离子峰,其中以峰1最为显著。以上现象说明经过活性炭的催化重整,生物油中的小分子含氧组分向单酚类组分富集。此外,钾的存在明显改变了生物油的组成。对比直接热解组C-N和KC-N,添加了钾后,代表糖类组分的离子峰4明显削弱,而代表其他小分子含氧组分的诸多离子峰均出现不同程度的增长。催化实验组C和KC中,钾的存在一定程度上降低了苯酚离子峰的强度,增加了2-甲基苯酚、3-甲基苯酚的峰强。
2.2.1 钾对生物油化学组成的影响GC/MS检测结果经分析整理以柱状图的形式绘制在图4中。如图4(a)所示,纤维素直接热解主要产生糖类组分,CN中糖类相对含量约为48.52%。钾在热解过程中的催化裂解作用会导致糖类组分脱水降解为酸类、酮类、呋喃类、酯类等物质[25-26]。因此,KC-N中糖类相对含量下降到19.20%,而其他小分子含氧组分所占百分比均有不同程度提高。经活性炭催化后,生物油中有机组分转化为以苯酚为主的酚类物质。从酚类占比来看,钾的添加有利于酚类相对含量的提高。C中酚类的相对百分含量为62.31%,KC中增加到81.71%。具体到每种单环苯酚,如图4(b)所示,钾浸渍后苯酚和2/3-甲基苯酚的相对含量均得到了不同程度的提高。C中苯酚和2/3-甲基苯酚的相对含量分别为45.37%、7.93%和9.01%,而KC中苯酚和2/3-甲基苯酚的相对含量分别为50.71%、10.66%和20.34%。但图4(c)中的峰面积数值表明,虽然钾促进了酚类富集度的上升,但苯酚的实际峰面积是下降的。这可能是因为钾的添加使得其他小分子含氧有机物含量下降幅度更大,造成了苯酚含量的相对上升。外标法定量的苯酚质量产率在图4(d)中给出。催化生物油C中苯酚的质量产率为1.78%。浸渍钾之后,苯酚质量产率下降到1.68%,钾的存在并不利于生物油中苯酚的富集。

图4 钾对纤维素热解油组分的影响Fig.4 Effects of potassium on the bio-oil composition of cellulose
2.2.2 钾对热解气组成的影响 如图5(a)所示,纤维素直接热解气主要由CO、CO2和CH4组成,H2含量很低,可以忽略不计。经活性炭催化后,热解气中CO的含量大幅度上升,CO2和CH4含量均出现不同程度的下降。热解气C中CO体积分数高达69.21%,H2为0.79%。而在热解气C-N中CO含量仅为36.15%(体积)。分析图5(b)中各组分气体实际体积产量发现,体积分数的变化主要由CO体积产量的大幅增加导致。热解气C-N中CO体积产量仅为56.58 ml/g,C中高达169.95 ml/g。伴随着热解气中有效组分的增加,低位热值(LHV)从热解气C-N中的12.08 MJ/m3增加至C中的12.93 MJ/m3。但钾的添加会造成热解气品质的明显下降,浸渍钾的样品中CO的体积分数大幅下降,CO2相对含量明显上升。对体积产量的分析发现,加入钾之后,CO2的体积产量显著增加,这是导致CO体积分数下降的主要因素。但钾对不同实验组中CO体积产量的影响有一定区别。在催化热解组中,钾导致了热解气KC中CO产量的下降。但在直接热解组中,热解气KC-N的CO产量却出现了上升。这可能是因为钾导致了挥发分组分的改变,并进一步影响了挥发分在催化剂表面的化学反应路径[27]。
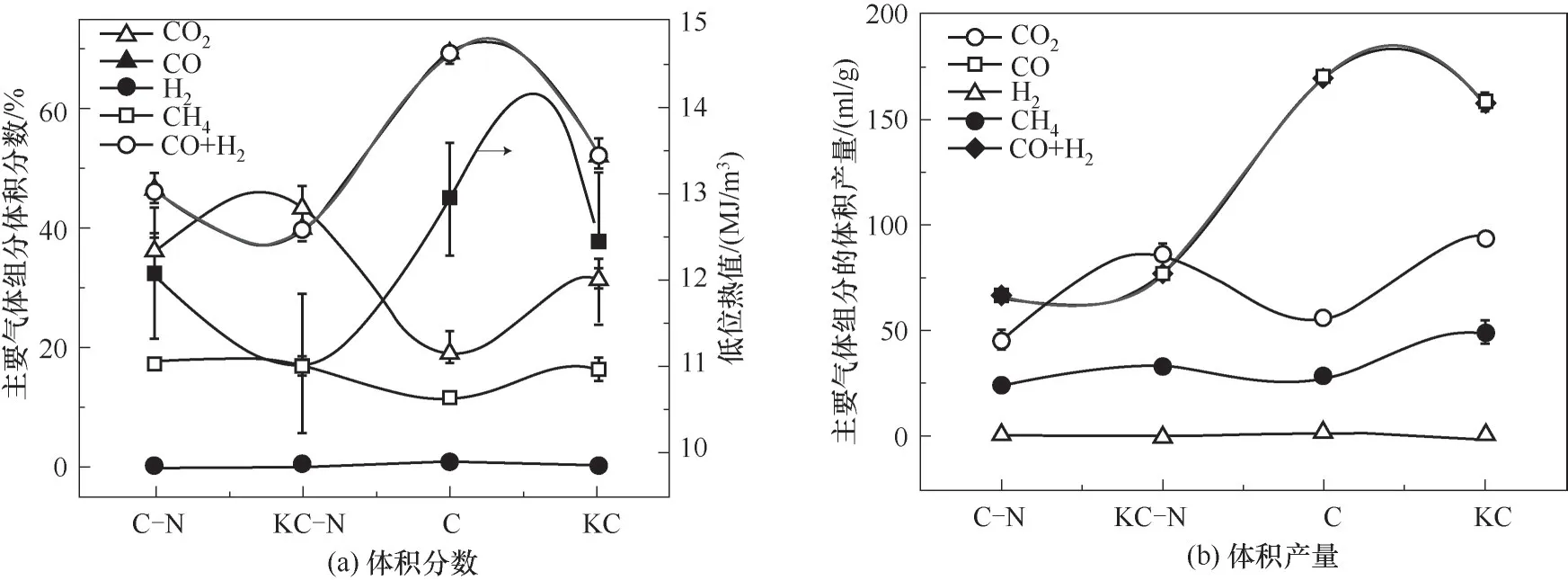
图5 钾对纤维素热解气组分的影响Fig.5 Effects of potassium on the syngas composition
2.3 催化剂/纤维素质量比对催化热解产物的影响
催化剂/原料质量比对催化反应产物有着明显影响。研究催化剂/纤维素质量比时,设定催化热解温度为450℃,分别研究催化剂/纤维素质量比为0.6、0.8、1.0和1.2时生物油和热解气的组成,相应的热解产物标记为C0.6、C0.8、C1.0和C1.2。
2.3.1 催化剂质量比对热解产物质量分布和生物油化学组成的影响 如图6(a)所示,随着催化剂比例的上升,流动阻力进一步增大,热解焦产率呈现微弱的上升趋势。但纤维素热解焦产率通常较低,实验中约为18%(质量)。催化剂比例上升时,生物油产率先增加后下降,在C0.8中取得最大值36.63%(质量)。而热解气呈现先下降后上升的相反趋势,C0.8处最小值为40.69%(质量)。催化剂比例的变化对积炭量基本没有影响,其数值在4%(质量)附近波动。
催化剂比例显著影响着生物油中酚类物质的富集度。图6(b)中,催化剂比例为0.6和0.8时,催化反应不够充分,生物油中酚类的富集度约为30%。生物油中存在大量的其他含氧小分子有机物,如酮类、呋喃类等。当催化剂比例从0.8增加到1.0时,酚类物质相对含量从32.01%翻倍至62.31%,比例为1.2时进一步增加到71.29%。从图6(c)中酚类的具体组成来看,生物油中的酚类主要由苯酚、2-甲基苯酚和3-甲基苯酚组成。这三种单酚物质的相对含量随着催化剂比例上升迅速增加,其中苯酚的含量占主导地位。在C1.0和C1.2中,苯酚的相对百分含量分别为45.37%和51.63%。可见在适宜的催化条件下,纤维素能够催化转化为高纯度的苯酚。催化剂比例为0.6和0.8时,由于催化作用不足,还存在少量其他单酚类组分,如对苯二酚、2,5-二甲基苯酚、2,4-二甲基苯酚和3,4-二甲基苯酚等。主要单酚组分的峰面积绘制在图6(d)中。由图可见,随着催化剂比例的上升,2/3-甲基苯酚峰面积持续下降。但催化剂比例过高,可能存在过度催化现象,导致C1.2中苯酚峰面积低于C1.0。因此催化剂/纤维素质量比为1∶1更适合生物油中苯酚的富集。

图6 催化剂/原料质量比对纤维素催化热解的影响Fig.6 Effects of catalyst/feedstock mass ratio on catalytic pytolysis of cellulose
2.3.2 催化剂质量比对热解气组成的影响 与生物油中苯酚的富集度不同,图7(a)中热解气中CO、CO2和CH4的体积分数呈现波动式变化。CO在C1.0中取得最大值69.21%(体积),对应的CO2和CH4的体积分数为18.57%和11.43%。但从体积产量看,CO的体积产量随催化剂比例的增加,呈现上升趋势。在C0.6、C0.8、C1.0和C1.2中,CO体积产率分别为158.01、161.01、169.95和182.20 ml/g。综合考虑体积分数和体积产率后认为,催化剂/纤维素质量比为1∶1,最适宜热解气中CO的富集。
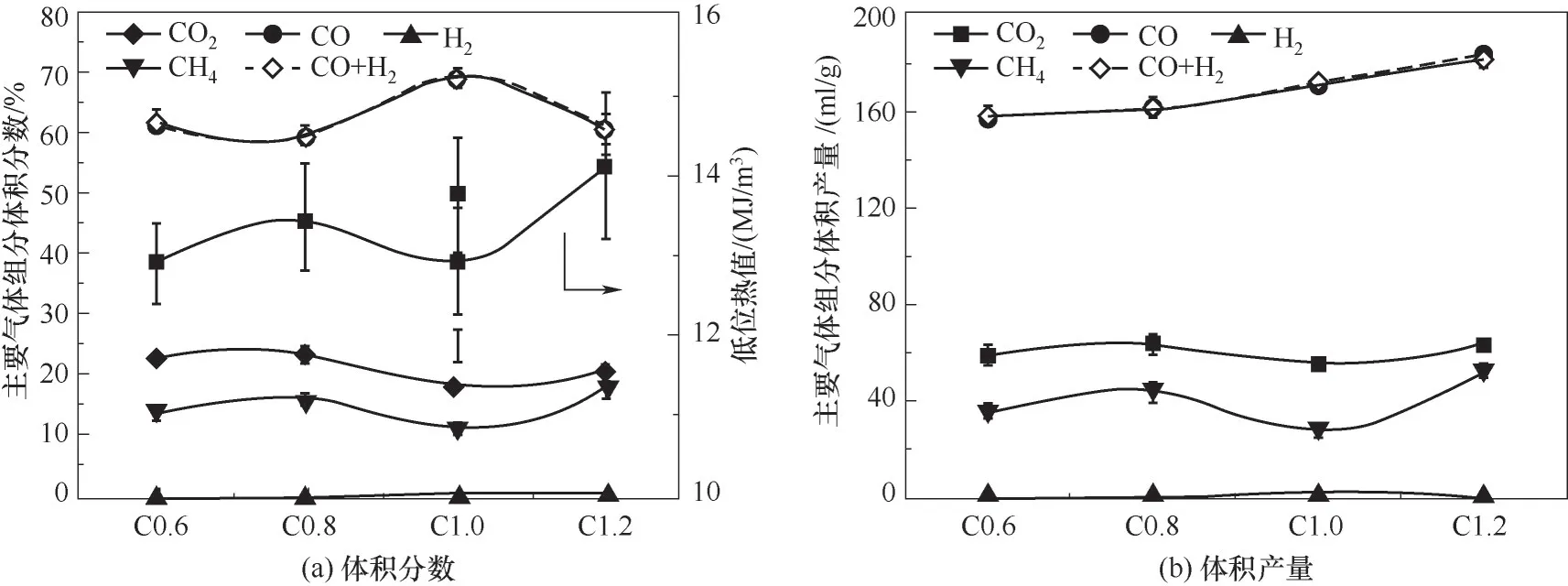
图7 催化剂/原料质量比对纤维素热解气组分的影响Fig.7 Effects of catalyst/feedstock mass ratio on the syngas composition
2.4 热解温度对催化热解产物的影响
研究催化热解温度时,固定催化剂/纤维素质量比为1∶1,分别研究催化热解温度为400、450、500和550℃时生物油和热解气的组成,相应的热解产物标记为C400、C450、C500和C550。
2.4.1 催化热解温度对热解产物质量分布和生物油化学组成的影响 如图8(a)所示,热解焦、生物油、热解气和积炭质量明显受催化温度影响。随着催化温度的上升,热解焦、生物油和积炭呈现线性下降趋势,而热解气产率呈现上升趋势。即催化温度上升,裂解作用增强,导致产物趋向于由生物油向热解气转化。C450和C550中,热解焦、生物油、热解气和积炭量分别为18.55%(质量)、33.09%(质量)、43.99%(质量)和4.37%(质量),以及13.63%(质量)、24.36%(质量)、63.12%(质量)和-1.12%(质量)。值得注意的是C550中,催化剂积炭量出现了负值。通过上文元素分析可知,纤维素的含氧量较高,约为50%(质量)。因此,在纤维素的催化重整过程中可能同时存在着纤维素中氧元素对碳基体的氧化烧蚀现象和酸位点表面积炭覆盖现象。催化重整温度的升高,纤维素中氧元素对催化剂碳基体的氧化烧蚀作用增强,导致氧化烧蚀量超过酸位点积炭覆盖量,最终引起积炭量为负值。
图8(b)给出了催化生物油中各组分相对含量随温度的变化。由图可知,催化温度上升有助于纤维素热解产生的小分子含氧有机物向酚类物质的转化。C400中酚类相对含量仅在40%左右,催化温度升高后的C450、C500和C550中相对含量分别为62.31%、56.32%和62.99%。但过高的温度会导致多环芳烃富集度增加,不利于生物油品质提高,如C550中多环芳烃相对含量为30.29%。如图8(c)所示,生物油中同样仅含有三种单酚类物质,C400、C450、C500和C550中苯酚的相对含量分别为27.65%、45.37%、40.25%和62.99%。由于过高的催化温度,C550中2/3-甲基苯酚完全消失。图8(d)中苯酚的峰面积显示,其最大质量产率出现在C450样品中。尽管C550有着最大的苯酚富集度,但峰面积却仅有C450的1/3略多。可认为450℃为最适宜纤维素催化热解富集苯酚的温度。

图8 热解温度对纤维素催化热解的影响Fig.8 Effects of pyrolysis temperature on catalytic pytolysis of cellulose
2.4.2 催化热解温度对热解气组成的影响 如图9(a)所示,随着热解温度的上升,CO的体积分数先上升后下降,在C450处取得最大值,其数值依次为66.43%、69.21%、65.79%和62.05%。但温度超过500℃时,热解气中的H2占比迅速增加,因而总的合成气有效组分占比不降反升。同时,热解气中的CH4占比也呈现增长趋势,而CO2则呈现线性下降。热解气的总热值从C400的10.15 MJ/m3持续增长至C550的15.33 MJ/m3。通过对图9(b)中实际产量的分析发现,气体组分浓度的变化主要来自于CO和H2体积的快速增加,而CO2的实际降幅并不大。在最适宜的热解制油温度450℃时,热解气中CO的含量和产率分别为69.21%(体积)和169.95 ml/g,热值为12.93 MJ/m3。
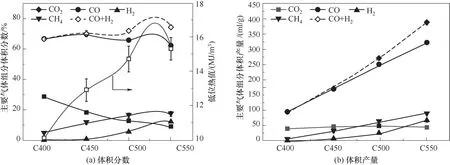
图9 热解温度对纤维素热解气组分的影响Fig.9 Effects of pyrolysis temperature on the syngas composition
2.5 反应机理探讨
相关文献报道[17,22],苯酚的生成路径与纤维素在分子筛催化作用下发生的“烃池”反应具有相似性,具体的催化转化路径绘制在图10中。如图所示,热解过程中纤维素生成以糖类为主的挥发分发生烃池反应先转化为含氧小分子,这些含氧小分子在催化剂表面发生脱水反应,转化为呋喃环类六碳化合物[28]和糠醛、1,2-环戊酮等五碳化合物[19]。其中,六碳化合物进一步脱氧环化转化为2-甲基-2-环戊烯-1-酮等环状化合物,这一过程伴随着H2O和少量的H2释放。而多个五碳类化合物在酸位点表面发生一系列Diels-Alder反应加成为芳香环类中间体,这一过程中伴随着H2O、CO和CH4的释放。两者生成的芳香环中间体进一步脱氧脱羰基转化为苯和甲苯[29]。生成的苯环类化合物与活性炭表面酸位点上的氧原子结合,随后热解挥发分含有的过热水蒸气中的氧与催化剂酸位点中的氧发生交换[30]。苯及甲苯获得了酸位点中的氧原子,脱离表面酸位点,最终生成苯酚和甲基苯酚[31]。而当热解过程中存在钾元素时,挥发分中的糖类优先裂解为以酮类和呋喃类为主的二次裂解产物[32-33]。并在这一过程中伴随着CO2的释放[34],引起气液相产物品质的同时下降。以上反应路径主要参照分子筛酸位点反应机理,具体路径有待后续进一步的机理实验验证。

图10 活性炭催化热解纤维素制备苯酚和CO机理Fig.10 Mechanism of preparing of phenol and CO by the catalytic pyrolysis of cellulose with phosphoric activated carbon
3 结 论
(1)纤维素热解挥发分经活性炭催化转化后,液相产物向苯酚富集,气相产物向CO富集。
(2)钾会导致挥发分中糖类物质提前降解,进一步引起热解产物品质的下降。实验发现生物油中的苯酚和热解气中CO的实际产率均显著下降。
(3)催化剂/纤维素质量比明显影响气液相产物组成。催化剂比例的上升会带来生物油中苯酚富集度的迅速上升。但过高的比例则会导致苯酚实际产率的下降。同时,催化剂比例上升还会带来CO体积产率的线性增加,但CO体积分数的最佳值出现在质量比为1∶1时。
(4)热解温度对热解产物品质影响最为明显。热解温度上升带来生物油中苯酚相对含量的迅速增长和热解气中CO和H2体积产量的快速增加,但苯酚峰面积仅在450℃时取得最大值。
(5)最佳热解产物出现在热解温度450℃,催化剂比例1∶1时。此时,生物油中酚类物质占可检测有机组分的62.31%,其中苯酚为45.37%,标定后的产率为1.78%(质量)。热解气中CO体积分数为69.21%(体 积),质 量 产 率 为169.95 ml/g,热 值 为12.93 MJ/m3。
