铁基催化剂光催化还原CO2研究进展
2021-10-31党永强李博妮李可可张建兰冯香钰张亚婷
党永强,李博妮,李可可,张建兰,冯香钰,张亚婷,2
(1西安科技大学化学与化工学院,陕西西安 710054;2自然资源部煤炭资源勘查与综合利用重点实验室,陕西西安 710021)
引 言
目前,化石燃料等不可再生能源在全球能源供应中占比较高,但其使用导致了大气中二氧化碳浓度上升,加剧了环境问题[1-2],如全球变暖、酸雨和海平面上升等现象均与二氧化碳浓度上升有关[3]。因此,开发高效环保的二氧化碳捕集、存储或转化技术以降低CO2排放并将其有效利用成为当前环境和能源的一个主要研究方向。其中,将二氧化碳转化为甲烷、甲醇等有价值的碳氢燃料,既能降低大气中二氧化碳的浓度,又能缓解能源危机[4-5],是最具吸引力的可持续发展途径之一。
在过去的几十年里,已经报道了几种有效的将二氧化碳转化为碳氢燃料的方法,包括光催化[6-7]、电催化[8]、光电化学法[9]和热化学法[10]等。其中,光催化技术是一种能直接利用太阳能将其转化为化学能的绿色技术,于1982年由Lehn等[11]率先利用该技术转化CO2,成为CO2转化的一条新途径。光催化技术因具有节能和无污染的特性引起了科研人员的广泛关注[12-14]。在光催化反应中,光催化剂的选择至关重要,在过去几年,用于光催化还原CO2的光催化剂研究发展迅猛。已报道的光催化剂材料有半导体材料、钙钛矿材料、金属配合物、生物酶和金属-有机骨架(metal-organic frameworks,MOFs)等多种类型[15-18]。尽管如此,实现大规模光催化还原二氧化碳仍然任重道远,其中开发高效、廉价、易于工业化利用的催化剂是加快光催化应用进程的关键。本文从各类铁基光催化剂出发,概述了半导体和金属配合物光催化剂光催化还原CO2的机理,并介绍了近年来几种铁基催化剂在光催化还原CO2方面的研究进展。
1 光催化还原CO2机理
根据光催化剂种类的不同,还原CO2的机理也有所不同,对于金属化合物来说,主要有半导体和配合物两类。半导体光催化剂还原CO2的基本原理如图1所示。当催化剂被能量等于或大于禁带宽度的光照射时,价带(VB)的电子被激发到导带(CB),随后电子迁移到催化剂的表面和吸附的CO2发生反应,在VB中留下带正电的空穴。为了发生氧化反应,VB电位必须比所需氧化电位更正,而为了发生还原反应,CB电位必须比所需还原电位更负[14,20]。理想情况下,光生电子迁移到催化剂表面,然后与表面吸附的CO2反应[20-21]。但当催化剂材料的带隙过窄或催化剂表面的活性位点太少时,跃迁到导带的电子会因和价带的空穴发生复合而无法迁移到催化剂表面发生还原反应。为了让尽可能多的电子参与到还原反应中去,降低光催化剂的载流子复合速率非常关键,解决方案通常有以下两种:(1)加入电子给体(还原剂),既可以清除空穴,又能提供氢气[22-23];(2)选择两种或两种以上催化剂构建异质结(图2),利用不同半导体之间的能级差别,使电荷有效分离,抑制电子-空穴的复合和扩展光致激发波长范围[24-25]。

图1 半导体光催化剂上光催化CO2转化的可能机理[19]Fig.1 Schematic illustration of probable mechanism of photocatalytic CO2 conversion over a semiconducting photocatalyst[19]

图2 不同异质结上光生载流子的转移路径Fig.2 Transfer paths of photogenerated carriers on different heterojunctions
金属配合物光催化还原CO的反应机理与半导2体材料不同,在大多数情况下,转化通过还原猝灭途径进行,涉及三个主要阶段(图3):首先,光催化剂(PC)经光照射后,通过金属到配体之间的电荷转移(MLCT)产生相应的激发态(PC*);随后,激发态的催化剂(PC*)从还原剂处获取电子,生成还原态的配合物(PC-1);最终,还原态的配合物被重新氧化成PC,同时,CO2被还原成CO、CH4等[26]。

图3 金属配合物在CO2光催化转化中还原淬灭的示意性机理Fig.3 Schematic description of reductive quenching pathway of metal complexes in photocatalytic conversion of CO2
在光催化反应中,CO2转化过程中的多个质子和电子转移步骤必须协同完成,还原过程可能涉及不同质子和电子数的转移过程,见表1[27]。

表1 在25℃、101.325 kPa、pH 7的水溶液中CO2还原的标准电势Table 1 Standard potentials of CO2 reduction to various products in aqueous solutions at 25℃,101.325 kPa and pH 7
2 光催化还原CO2的铁基催化剂
结合两类光催化反应机理,提升光催化剂的光催化效率主要需要提高光吸收范围和催化反应效率。过渡金属元素能够将催化剂的光谱响应从紫外扩展到可见光区域,拓宽光吸收的范围。其中,铁的化合物价层电子轨道的多变能够诱导电子能带结构调制[17],有利于提高光催化还原CO2的效率。同时,铁是地壳中含量最多的过渡金属元素,原料丰富,价格低廉,也具有很好的催化效率,在合成氨、乙苯催化脱氢、工业脱硫等领域得到了大规模应用。因此,用铁替代贵金属如Au、Ag、Pt等,开发高效、低毒、易制备的催化剂有利于实现光催化还原CO2的大规模应用[18]。近年来发展的铁基光催化剂主要包括铁氧化物半导体、铁配合物、铁基MOFs、铁氧化物钙钛矿和铁掺杂半导体催化剂等[23,28-30],本文对这些铁基催化剂的结构特点、催化选择性及催化活性进行了比较,并对它们光催化还原CO2的研究前景进行了展望。
2.1 铁氧化物半导体催化剂
氧化物半导体光催化剂是目前研究和应用最广泛的光催化剂,其中,过渡金属氧化物(TMO)在CO2光催化还原中通常表现出对指定产物有特定路径的能力。氧化铁类材料光吸收范围广,且自然资源十分丰富[31-33]。其中,赤铁矿(α-Fe2O3)是一种在环境条件下具有热力学稳定性的氧化铁,具有低成本、无毒、良好的耐腐蚀性和出色的环境相容性等优点,在催化领域具有广泛的应用前景,但单独用作光催化剂活性较弱,需要与其他半导体材料复合提高光催化性能[34]。Wang等[35]通过湿化学方法和水热法制备的g-C3N4/α-Fe2O3纳米复合材料,利用g-C3N4良好的导电性,提高了载流子的分离效率。15CN-F(15% g-C3N4)对CO和CH4的光催化活性分别为15.8μmol/(g·h)和3.1μmol/(g·h);水热法合成的FCN(质量比为40∶60)还原CO2制CH3OH的速率为5.63μmol/(g·h),是 纯g-C3N4[1.94μmol/(g·h)]的2.9倍[36]。这一方面说明不同方法制备的催化剂结构存在较大差异,导致生成的产物和选择性等方面具有多样性。另一方面,光催化活性的提高归因于α-Fe2O3和g-C3N4之间的相互作用。基于Fe2O3和InVO4匹配的能带,Anurag等[37]合成了InVO4/Fe2O3Z型异质结复合材料,又将其沉积在由壳聚糖功能化的rGO上面,利用rGO良好的导电性,进一步提高了催化剂的载流子分离效率,增强了光还原CO2生成甲醇的能力,其生产甲醇的最大产率可达16.9 mmol/g(图4)。Zhao等[38]通过功能离子预吸附辅助法制备了氧化铁修饰ZSM-5分子筛,实现了CO2的高效光催化还原。在该体系中,铁的电子态起着重要的作用,Fe2+能与CO2▪-作用形成(Fe-CO2)+的中间产物,进一步生成CO。而不同FeⅡ/FeⅢ在ZSM-5上的协同作用和对能带结构的控制,为CO2吸附/活化和C—C偶联提供了良好的带隙和活性中心。此外,表面FeOx低聚物通过促进中间体C—C偶联和抑制CO的竞争性生成,提高了醛的选择性。FZ3(3% FeOx)光催化还原CO2生成CO和CH3CHO产率最高,分别为10.01μmol/(g·h)和3.80μmol/(g·h)(选择性为43.1%)。

图4 空白反应、rGO、InVO4/Fe2O3、InVO4、rGO/InVO4/Fe2O3上CO2转化成甲醇的产率[37]Fig.4 Conversion of CO2 to methanol over time using blank reaction,rGO,InVO4/Fe2O3,InVO4 and rGO/InVO4/Fe2O3[37]
将氧化铁与其他金属氧化物制成铁酸盐形式的复合氧化物,可以通过改变双金属离子的组合构型,从而使催化剂具备不同的光催化性能[39]。与ZnO和Fe2O3相比,铁酸锌(ZnFe2O4)具有较窄的禁带(1.90 eV),导带(CB)位于1.5 eV,光化学稳定性好且价格低廉,是一种很有前途的光催化剂[40-41]。Xiao等[42]采用一锅溶剂热法制备了超细ZnFe2O4纳米粒子光催化剂,在可见光照射下显示出有效的光催化CO2还原活性,CH3CHO和CH3CH2OH的产量分别为57.8μmol/(g·h)和13.7μmol/(g·h)。为了进一步提高ZnFe2O4的光催化活性,Tahir[43]采用简单的水热法制备了ZnFe2O4微球与Ag/TiO2纳米棒(NRs)偶联的Z型异质结复合催化剂,复合材料比ZnFe2O4/TiO2的NRs高1.49倍。这归因于ZnFe2O4调整了TiO2-NRs能带结构,为CO2还原提供更多的负还原电位,从而显著提高了光催化活性。除此之外,铁酸盐的形貌也会影响其光催化性能。例如,何小刚等[39]利用溶剂热法合成了棒状的铁酸镍(NiFe2O4)和铁酸铜(CuFe2O4),CuFe2O4的光催化活性高于NiFe2O4。用水热法合成的片状CuFe2O4,用Au纳米颗粒修饰后,催化还原CO2制CO的产率为537.6μl/(g·h),可能是因为Au颗粒在Fe、Cu双金属离子表面形成了类似突触的天线结构,三种金属原子之间产生了协同催化的作用,且片状的CuFe2O4拥有更大的比表面积,单位面积吸附的CO2分子更多,大大提升了光催化效率,同时提高了产物的选择性。
与TiO2等氧化物相比,铁氧化物催化剂具有资源丰富、可见光吸收范围广等优点,但也存在单独作催化剂光催化活性弱的缺点。制备不同结构(包括空心、核壳、多孔等)的铁氧化物材料、构筑复合材料异质结都是改善其光学性能和提高载流子分离传输效率的可行路径;另外,还应对其光催化的反应机理进行深入探究,为铁氧化物催化剂的优化提供有效指导。
2.2 铁配合物催化剂
金属配合物光催化CO2还原大多是在均相体系中进行,通过吸光基团吸光和一系列质子和电子转移来实现CO2还原。相对于非均相催化剂而言,均相催化剂具有确定的空间结构,有利于结构设计和优化,也有利于研究催化机理、建立构效关系[44-46]。近年来,基于卟啉(P)、酞菁(Pc)、咔咯(Cor)、环戊二烯酮和四联吡啶等的铁配合物在光催化CO2还原中表现出优异的催化性能[47-49]。1997年,铁卟啉首次用于CO2光还原,Grodkowski等[50]在N,N-二甲基甲酰胺(DMF)/三乙胺(TEA)溶液中,于λ=360 nm处进行光激发,CO转化数(TONCO)为70。之后,他们也尝试用铁酞菁(FePc)、铁咔咯(FeCor)来还原CO2,但和铁卟啉相比,催化效率相差甚远,只有它的30%~45%。通过改变金属配合物中心的金属原子、与不同的有机配体结合或对配体进行修饰,均能在一定程度上提高产物的转化数和目标产物的选择性。Robert等在铁配合物光催化还原CO2方面做了大量的研究,主要通过对铁卟啉配体上的苯环进行修饰来提高光催化性能(图5)。他们以Fe-p-TMA(三甲氨基官能化的铁卟啉)为光催化剂,在乙腈/水(体积比为3∶8)溶剂中加入四氟乙烯(TFE),成功将CO2还原为CH4和H2,且对CH4具有良好的选择性(81%)[51];在此基础上,又尝试用FeTPP-p-TMA(三甲氨基官能化的铁苯基卟啉)在乙腈溶液中光催化还原CO2,分别用TEA和BIH作还原剂,但TONCO分别只有33和63[52-53];除此之外,他们还用FeTPP-o-OH(羟基官能化的铁苯基卟啉)作催化剂,该光催化系统将TONCO提高到140[54]。

图5 Fe-p-TMA、FeTPP-p-TMA和FeTPP-o-OH的结构Fig.5 The structure of Fe-p-TMA,FeTPP-p-TMA and FeTPP-o-OH
CO(羰基)和四联吡啶由于能够稳定过渡金属的低氧化态,并能与多种金属离子配位,使配合物更具功能性,常用作金属配合物光催化还原CO2的配体。Alsabeh等[55]用十二羰基三铁([Fe3(CO)12])光催化还原CO2,CO和H2的转化数分别为36与32,接近1∶1;加入联吡啶配体(bpy)后,CO和H2的转化数都有所提高,分别达到42和47;为了进一步提高光催化活性,他们引入环戊二烯酮,合成了更加稳定的环戊二烯酮三羰基铁配合物,光照1 h后,TONCO约为600,初始周转频率(TOF)高达22.2 min-1[56]。还有研究报道了一种基于环戊二烯酮铁配合物的高选择性光催化体系用于将CO2还原为CO,发现TONCO可达487,选择性高达99%,ΦCO=13.3%[57]。Guo等[58]以四联吡啶铁配合物为催化剂将CO2光催化还原至CO。在MeCN/TEOA(体积比为4∶1)溶液中,对CO的选择性高达92%;而Cometto等[59]用四联吡啶铁配合物作催化剂和介孔石墨化氮化碳(mpg-C3N4)组成的光催化系统进行高效选择性CO2-CO还原,用TEOA作为电子给体,选择性高达97%。
由于像铁卟啉这样的分子催化剂在长时间的紫外线照射下会发生光降解[44],因此,铁配合物的光催化体系中通常需要引入光敏剂,光敏剂能够降低可见光区域所需的吸收能,从而提高光还原效率[60]。Robert等[53]在他们的光催化体系中分别添加了铱基光敏剂、9-氰基蒽(9-CNA)和purpurin(红紫素)(结构见图6)等,结果表明,光敏剂能明显提高对光的吸收,使得光催化活性有不同程度的提升。Guo等[58]在光催化系统中分别添加红紫素和Ir(bpy)2+3作光敏剂后,光催化性能大大提升,TONCO分别提升到1365和3844;但这些光敏剂大多基于贵金属Re、Ru、Ir等,昂贵的成本限制了大规模应用。Lian等[61]用带负电荷的胶体CuInS2/ZnS量子点作为敏化剂,与带正电荷的FeTMA静电组装,发现静电结合的量子点卟啉体系比类似的不带电荷的体系具有更高的催化活性。利用该催化剂体系,在可见光(λ=450 nm)下30 h内,CO2可高效地转化为CO,TONCO为450,选择性高达99%。

图6 光敏剂的结构:三[2-苯基吡啶-C2,N]铱(Ⅲ)、9-氰基蒽和红紫素Fig.6 Structures of the tris(2-phenylpyridine)iridium,9-anthrracenecarbonitrile and purpurin
均相催化剂包括铁金属配合物能与反应物更有效地接触,但是大多需要在使用还原剂和有机溶剂的情况下才表现出光催化还原CO2活性,而且大多数催化剂反应活性和稳定性仍然不够理想。通过对催化机理的深入理解和揭示,设计合成催化活性高、稳定性高、反应条件更温和环保的铁基分子催化剂是进一步努力的方向。近几年铁配合物催化剂在光催化还原CO2方面的应用见表2。

表2 近几年铁配合物催化剂在光催化还原CO2方面的应用Table 2 Application of iron complex catalyst in photocatalytic reduction of CO2 in recent years
2.3 铁基MOFs催化剂
金属-有机骨架材料(MOFs)是由多齿有机连接体相互连接的金属团簇构成的一类三维晶体多孔杂化材料,具有高度有序的结构、超高的比表面积及孔径可调等诸多优点[62-63]。MOFs用于光催化还原CO2时,其光吸收能力可以通过对金属离子和有机连接物的修饰来调节,从而实现对太阳能的高效利用;MOFs的有机连接物和不饱和金属离子都具有高催化活性和CO2吸附量,因此活性中心CO2浓度高,有利于光催化反应;除此之外,孔结构使MOFs能够结合客体光活性材料,对光催化CO2还原具有协同作用[64-65]。这些对于开发提高CO2还原性能的催化剂至关重要。
铁基MOFs由于存在大量的铁氧簇,能够显著提升反应的催化效率[66],这一点由Wang等[67]的工作得到证实。他们研究了三种铁基MOFs[MIL-101(Fe),MIL-53(Fe),MIL-88B(Fe)]在可见光照射下催化CO2还原生成甲酸的活性。其中,氨基化后的MIL-101(Fe)在光照射8 h内产生的甲酸为178 μmol。因为氨基化后的MIL-101(Fe)具有不饱和位点,不仅可以增加对CO2的吸附量,还能使金属和配体被可见光同时激发,产生双重激发路径(图7):在可见光激发下,通过将O2簇中的电子转移到FeO簇中的Fe3+,Fe3+因此被还原成Fe2+;第二条途径是通过激发NH2官能团,电子从受激发的有机接头转移到金属中心生成Fe2+,而Fe2+能够有效还原CO2。基于此,Dao等[68]采用无溶剂[69]的方式制备了上述三种氨基化铁基MOFs,与常规的气-液-固反应路线相比,气-固界面法不但对环境友好,还能增加催化剂与反应气体之间的接触,且有利于CO2的原位吸附。结果表明,NH2-MIL-101(Fe)具有最高的光催化活性,光催化还原CO2产生CO的速率可达17.52μmol/(g·h)。

图7 氨基功能化铁基MOFs上的双重激发途径[67]Fig.7 Dual excitation pathways over amino-functionalized Fe-based MOFs[67]
通过选择合适的光活性材料将其与MOFs结合,利用它们之间的协同作用可以得到具有特定功能的MOFs光催化材料。Wu等[70]通过顺序沉积路线将MAPbI3QDs封装在PCN-221(Fex)的孔中构建了一系列复合光催化剂MAPbI3@PCN-221(Fex)(x=0~1),封装后不仅没有改变它们的晶体结构,还能提高稳定性和光吸收能力。同时,封装后的量子点中的光生电子可以快速转移到MOFs的Fe催化位点,稳态发光光谱还表明了在光激发后从卟啉到铁催化位点的三重电子转移的出现,有效提高了光催化活性。Dao等[71]构 建 了NH2-MIL-101(Fe)/g-C3N4(MCN-X)无溶剂光催化体系。其中,MCN-3(3% g-C3N4)表现出优异的CO2光催化还原活性和选择性,CO2转化生成CO的产率比原始的g-C3N4提高了6.9倍。该体系中,MCN-3的高孔隙率和NH2-MIL-101(Fe)中NH2的存在,增强了可见光吸收和CO2的吸附;同时,通过杂化g-C3N4,调节g-C3N4与NH2-MIL-101(Fe)之间的接触界面,可以提高g-C3N4与NH2-MIL-101(Fe)之间光生载流子的转移率。
MOFs的内部可以设计为具有开放的金属位、功能化的有机配体与其他结构单元相互作用的金属催化剂。Wang等[72]通过先合成铟卟啉框架,然后利用卟啉稳定单个铁、钴位点,并改变Fe3+和Co2+的量,设计合成了一系列铁和钴配位的铟基三维框架,实现了可见光驱动的CO2到CO的高效转化。由于卟啉环既能支持金属中心作为催化活性中心,又能吸收可见光以实现高性能的CO2转化,在24 h内可以获得3469μmol/g的高CO产率和高CO选择性(99.5%)。通过研究金属电子构型对金属-碳相互作用的影响,与钴类似物和铟MOFs相比,铁中心更能接受光激发MOF中的电子以完成CO2还原,并且该性能大大提高(图8)。
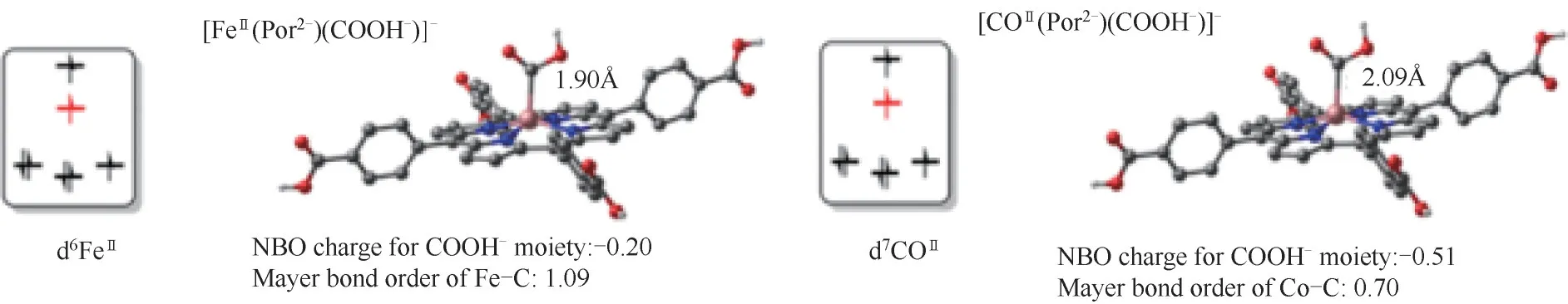
图8 [FeⅡ(Por2-)(COOH-)]-和[CoⅡ(Por2-)(COOH-)]-中金属中心的电子构型对金属-碳相互作用的影响[72]Fig.8 Influence of the electron configurations of the metal centers on the metal-carbon interactions in[FeⅡ(Por2-)(COOH-)]-and[CoⅡ(Por2-)(COOH-)]-[72]
铁基MOFs不仅可以简单地作为载体,将MOFs的光催化特性与其结构中的Fe催化位点的催化性能结合,也可以在光照条件下实现一些复杂的转化过程。但MOFs用于光催化还原CO2存在耐酸、耐碱、热稳定性较差的问题。另外,对MOFs光催化性能的研究主要集中在几类MOFs中,如MIL-101(Fe)和MIL-125(Ti)等。目前已有很多种MOFs被报道,拓展MOFs基光催化材料的种类将为开发高效的MOFs光催化材料带来更多的可能性。
2.4 铁氧化物钙钛矿催化剂
钙钛矿型(ABO3)复合氧化物是一种具有独特的电子和晶体结构及光催化活性的新型无机非金属材料,一般为立方体或八面体形状。其中,A位离子通常是稀土或者碱土具有较大离子半径的金属元素,B位一般为离子半径较小的元素,如Mn、Co、Fe等。当A位、B位离子被其他离子部分取代(掺杂)时,其钙钛矿结构保持不变。掺杂会使得钙钛矿本身完整的晶型产生缺陷和畸变,无序性增大,体系能量升高,形成掺杂能级,有利于光的吸收和光生电子-空穴对的分离[73]。然而,纯钙钛矿材料的光催化能力对稳定的分子如CO2的转化较弱。为了克服这一限制并提高光活性,将钙钛矿材料与其他光活性材料耦合可能是开发新型高活性可见光光催化剂的一条有前景的途径[74]。
BiFeO3(BFO)是由Fe2O3和Bi2O3组成的金属氧化物复合材料,具有较好的光化学稳定性和低成本的优点[75]。李鑫等[76]用溶胶-凝胶法制备了碳纳米管/BiFeO3复合材料,光催化还原CO2制甲醇的累积产量在4~6 h内最高可达1000μmol/g。除了碳纳米管能引导电子的转移外,主要是因为BiFeO3具有较窄的带隙,Bi3+电子构型较Fe3+不稳定,易失去1个电子变为Bi4+,且Bi-O结合能小于Fe-O结合能,从而在催化剂晶体中或表面形成氧空位,提高了光催化效率。Karamian等[77]通过水热法合成了不同摩尔比的BiFeO3-ZnO复合材料,该催化剂的光催化转化率最高可达到21%。其可见光催化活性的增强归因于p-n异质结的协同效应和BiFeO3钙钛矿结构对可见 光 的敏感性。当p型BFO和n型ZnO形成p-n结时,由于相反粒子之间相互吸引的静电力,在界面处产生载流子浓度梯度,BFO中的激发态电子上升到较高的能级,有利于电子向CO2的转移;同时,在两种光催化剂的界面处,能带发生弯曲,形成一个由ZnO侧向BFO方向的内电场,迫使电子和空穴朝相反的方向流动,抑制了电子-空穴对的复合。
Kumar等[78]制 备 了 一 系 列ABR(Ag2CrO4/Ag/BiFeO3@RGO)复合材料并研究了它们在可见光下还原CO2的活性。ABR-11(含11%RGO)能够在8 h内选择性地生成180μmol/g的CH4(在碱活化下为260μmol/g),约为BiFeO3的60倍。ABR系列的优异性能归功于多个因素:(1)金属Ag和RGO除了通过Ag的表面等离子体共振效应产生载流子外,还能缩短迁移距离、增加载流子的寿命;(2)Ag2CrO4带隙较低、光学吸收系数高且具有独特的电子结构[79];(3)通过添加NaOH增加了CO2的溶解度,且形成的碳酸盐是弱碱性介质,有利于形成羟基自由基,导致电子-空穴的有效分离,从而实现更高的还原能力[80]。
铁酸镧(LaFeO3)也是一种典型的具有钙钛矿结构的稀土复合金属氧化物,具有稳定的晶体结构,独特的电磁、催化特性。Raziq等[81]用TiO2和氨基功能化的碳纳米球(AC)耦合氮掺杂多孔钙钛矿材料LaFeO3(N-LFO)成功合成了一种高效、廉价的光催化剂。其良好的光催化性能得益于三个方面:通过引入孔结构增加了材料的比表面积;N的掺杂可使可见光吸收延长;耦合TiO2促进了载流子的迁移和分离。光催化活性如图9所示。
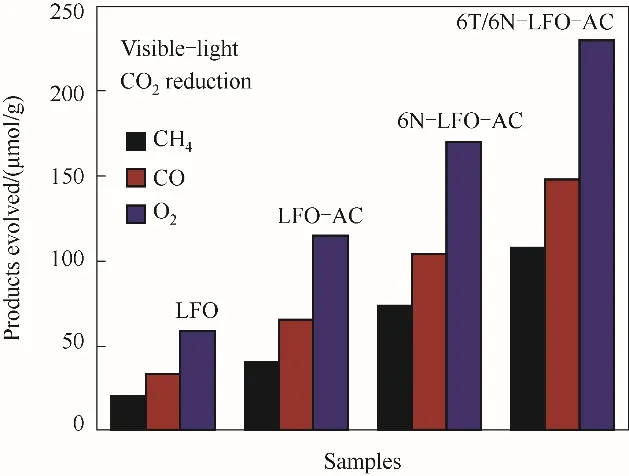
图9 LaFeO3及其复合材料在光催化二氧化碳转化过程中的产物量[81]Fig.9 Product amounts of LaFeO3 and its composites during the photocatalytic CO2 conversion[81]
由于优异的光电性能和独特的电子结构,越来越多的氧化物钙钛矿材料被应用到光催化领域。但也伴随着稳定性差、催化效率低等问题,在载流子传输和界面复合方面仍然有很大的研究空间,在这方面的研究将有助于实现对氧化物钙钛矿催化潜能的进一步开发和对其性能的有效利用。
2.5 铁掺杂半导体催化剂
1990年Ileperuma等[82]最先发现在半导体中掺杂不同价态的金属离子后,半导体的催化性质被改变。从化学观点看,金属离子掺杂可能在半导体晶格中引入了缺陷位置或改变其结晶度,从而影响电子-空穴对的复合。Fe3+由于其半填充电子构型而被广泛用于半导体光催化剂掺杂。
TiO2是目前应用最广泛的光催化剂,具有光催化活性较高、耐腐蚀能力强、稳定、无毒、价格相对较低等优点。但它存在可见光利用率低(由于宽带隙)、光生电子-空穴的快速复合等缺点[83-84]。因为Fe3+(0.065 nm)与Ti4+(0.068 nm)的离子半径接近,可以比较容易地掺杂到二氧化钛晶格中,促进电子转移,从而提高光催化活性。在TiO2中进行Fe掺杂时,制备方法、掺杂方式、掺杂浓度及后处理等多种因素均会影响TiO2的光催化活性。如Xu等[85]以MIL-101(Fe)为模板和铁离子源,采用一步水热法成功制备了Fe3+掺杂的空心TiO2八面体,TiO2的形成和MIL-101(Fe)的蚀刻在F-的驱动下同时发生。所获得的Fe-TiO2-500八面体表现出优异的光催化活性,在可见光照射下反应12 h后,CH4的产率约为7.73μmol/g。Chen等[86]采用溶胶-凝胶法制备了Fe3+掺杂的TiO2气凝胶。相比水热法,用溶胶-凝胶法制备的Fe-TiO2,TiO2的前体水解前就掺入Fe3+,水解过程中Fe3+能够较好地分布到TiO2粒子中,实现分子水平上的均匀掺杂。与纯TiO2气凝胶相比,掺杂的气凝胶具有较窄的带隙,可见光吸收增强;能抑制光生电子-空穴对的复合,延长了激发电子的寿命,甲醇产率明显提高。Khalilzadeh等[87]通过原位溶胶-凝胶法将Fe、N共掺杂的TiO2固定在介孔SBA-15上以提高CO2的光还原性能。Fe和N原子进入TiO2晶格,导致TiO2结构中产生Ti3+和氧空位,提高了光催化活性。此外,铁可以作为电子阱,减少电子-空穴对的复合。共掺杂后,CH4和CH3OH的最大产率分别可达到38.37μmol/(g·h)和1.7μmol/(g·h)。
以二氧化铈(CeO2)为代表的稀土氧化物由于特殊的4f轨道结构,表现出良好的催化活性。Wang等[17]采用纳米铸造法制备了Fe掺杂CeO2催化剂,光催化还原CO2生成CO和CH4的产率分别为12.38 μmol/(g·h)和2.88μmol/(g·h)。因为Fe掺入CeO2后,出现了新的掺杂能级,使得CeO2带隙缩小;且铁离子d电子与CeO2导带或价带之间的电子转移跃迁引起了Fe-CeO2吸收边的红移,改善了氧化铈的光学性质。此外,Fe3+可以大大增强氧化铈表面的化学吸附氧,这些氧很容易捕获电子并产生具有优异还原能力的表面氧自由基,从而促进光催化反应的进行。
铁掺杂不仅可以改变半导体材料的结晶度,制造缺陷空位,抑制电子-空穴对的复合,还能改变半导体的能带,提高对可见光的吸收。但在如何精确调控掺杂浓度、状态、分布以及相关表征技术方面还需进一步探索。表3总结了近几年报道的铁基催化剂,包括光催化剂的组成、产物及产率。
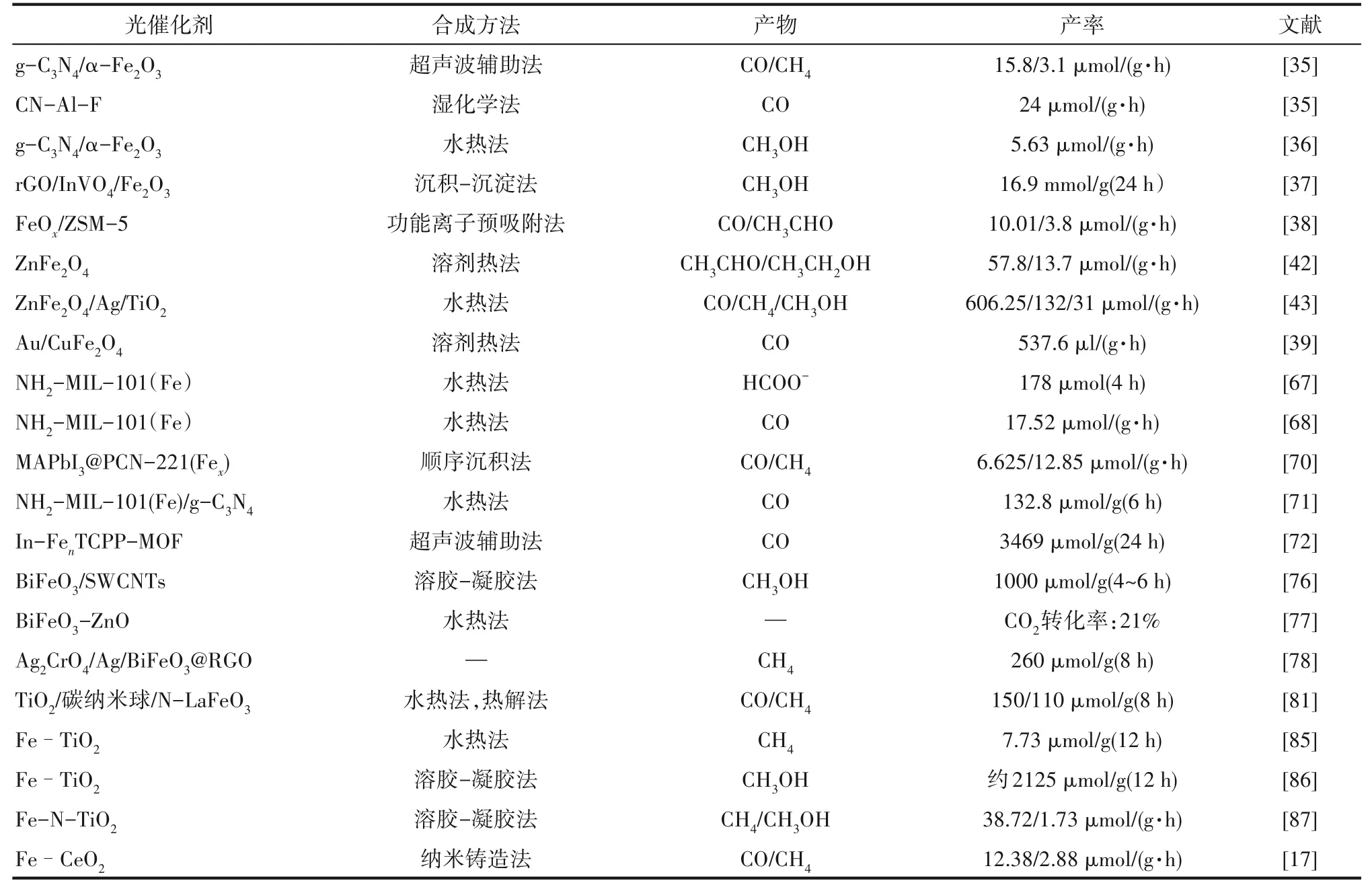
表3 近几年铁基催化剂在光催化还原CO2方面的应用Table 3 Application of iron-based catalysts in photocatalytic reduction of CO2 in recent years
3 结论与展望
光催化CO2转化技术对于保护环境、促进可持续发展具有重要意义,开发高效、廉价、易制备的光催化剂有助于实现大规模光催化转化CO2。目前已经开发了多种新型光催化剂,并在催化剂组成、结构、活性、产物选择性、光催化还原机理等方面进行了大量研究;但是,现阶段各类光催化剂(包括铁基催化剂)在工业化光催化还原CO2方面仍然任务艰巨,主要表现在:(1)CO2的转化率较低,产量大多为μmol/(g·h)级别;(2)牺牲剂或还原剂的使用提高了成本,降低了环境友好度;(3)光催化的表面还原机理研究尚浅,难以有效指导光催化剂的设计;(4)对还原产物选择性的研究较少,且主要集中在C1产物,少有C2及更具实用价值的有机物。
基于光催化还原CO2机理,提高催化效率可以考虑从以下几个方向进行:(1)提高光吸收效率方面,通过调控材料的组成、结构、形貌等调节材料的能带结构,或者引入可以高效吸收可见光及近红外光的光敏剂以拓宽半导体或金属配合物的光吸收范围;(2)设计合成新型光催化材料或多元复合体系,构建异质结,促进载流子的分离及向半导体表面传输,减少电子与空穴的再复合;(3)深入研究催化剂与CO2的反应机理,通过调节催化剂表面状态如暴露晶面、活性位点等加快表面催化反应效率,调控还原产物的种类。总之,设计开发新型催化剂、提高光催化还原CO2效率、实现大规模转化CO2的工作任重道远,需要不断探索与研究。
