橘子中维生素C稳定性的研究
2021-10-25何飞强王尚贤熊方永丁健桦
何飞强,王尚贤,熊方永,张 英,丁健桦
(东华理工大学 化学生物与材料科学学院,江西 南昌 330013)
维生素C(L-抗坏血酸,简称VC)是一种重要的营养物质,是维持机体正常生命活动所必需的一类小分子有机化合物,具有抗氧化、解毒、促进机体对钙、铁等人体必需元素的吸收作用,其主要的生理功能有促进胶原蛋白及结缔组织的合成、促进伤口愈合和增强机体免疫力、提高酶活性,预防癌症等(陈国峰等,2014;曾翔云,2005)。尽管VC对人体非常重要,但是人体缺乏古洛糖内酯氧化酶,不能自身合成VC,必须从天然食物、强化食品或药物中获取。但过多或过少摄入VC都不利于健康,严重时会引起病变等不良反应。如缺乏VC可引起坏血病;过量摄入VC会引起皮疹、结石、动脉硬化等疾病(陈莉,2012)。因此补充VC时应注意控制用量,根据国家卫生健康委员会发布的水溶性维生素摄入的卫生行业标准(中国营养学会,2018),成年人对VC的日平均需要量(EAR)为85 mg/d、推荐摄入量(RNI)为100 mg/d,可耐受最高摄入量(UL)为2 000 mg/d;而未成年人对VC的摄入标准低于成年人,但即使一岁儿童其EAR、RNI、UL分别不低于35 mg/d、40 mg/d、400 mg/d。因此,对日常食物或药物中VC含量进行测定,使人们了解和控制自身VC摄入量非常重要。
目前VC测定的方法一般有滴定法、碘量法、比色法、荧光法、紫外分光光度法等(赵平娟等,2017),这些方法具有试剂用量多、操作复杂等不足。高效液相色谱(HPLC)法则具有试剂用量相对较少、操作简单、省时省力,以及稳定快速、高效分离和运行自动化等优点(曹博等,2013;梁华正等,2012),已经广泛应用于食品、药品中维生素、有机酸、氨基酸等的检测(Shahdousti et al., 2018; Pullar et al., 2018)。近十几年来,HPLC法测定VC含量的方法也得到了充分的发展和完善。
由于VC在常态下不太稳定,易被氧化(李军明等,2009),易受温度、pH、光照等条件的影响(Ramesh et al., 2010),因此结合日常生活经验,较系统地研究了时间、温度、光照以及厨房调味料和茶水等介质对VC稳定性的影响。本研究利用HPLC分析橘子中VC的含量,取得了比较满意的结果。不但可为人们根据营养需求合理选择和科学搭配果蔬提供科学依据,也可为果蔬中VC的保存、提取以及利用等提供参考。
1 材料与方法
1.1 材料与试剂
橘子、食盐、食醋和食用碱等调味料及茶叶均购于当地超市。
草酸(分析纯)、 天津市大茂化学试剂厂;VC(分析纯) 购于国药集团化学试剂有限公司;实验所用水均为超纯水。
1.2 仪器与设备
高效液相色谱仪LC-15C (配有SPD-15C紫外-可见检测器和LC solution 15C色谱工作站,日本岛津公司);循环水式真空泵(SHZ-D(Ⅲ),巩义市予华仪器有限公司);数控超声波清洗器(KQ5200DB,昆山市超声仪器有限公司);电子分析天平(BSA224S,赛多利斯科学仪器(北京)有限公司)。
1.3 方法
1.3.1 溶液的配制
(1)草酸溶液的配制。称取1.000 0 g草酸固体,用纯水溶解、转移至1 000 mL容量瓶中定容,得到0.1%的草酸溶液。
(2)标准储备液的配制。快速准确称取0.250 0 g VC标准品于100 mL的烧杯中,用0.1% 的草酸溶解,转移至250 mL棕色容量瓶中,并用0.1%的草酸溶液定容,得到1.00 g/L标准储备液,避光贮存,现配现用。
1.3.2 橘子样品溶液的制备
准确称取橘子果肉20.0 g,迅速切碎置于研钵中研成匀浆后迅速移入100 mL烧杯,再用25 mL移液管分两次准确移取25.00 mL 0.1%的草酸溶液清洗研钵,并将清洗液转移至上述烧杯中,精密称重,再将其置于超声波清洗仪中超声15 min辅助提取。超声后再精密称重,用0.1%的草酸溶液补重。随后溶液用0.45 μm滤膜过滤得到目标溶液。用移液管准确移取续滤液10.00 mL于50 mL容量瓶,用0.1%的草酸溶液定容得到橘子样品溶液。将该样品溶液超声5 min,过0.45 μm滤脱,进行HPLC分析。
1.3.3 调味料和茶水等溶液的制备
分别称取0.10 g食盐、食用碱和蔗糖标准品,用纯水溶解并分别转移至25 mL容量瓶中,再用0.1%草酸溶液定容,配成食盐溶液、食用碱溶液和蔗糖溶液;称取5.0 g普通茶叶于250 mL的玻璃杯中用开水封闭浸泡4小时制成茶水,再将上述配好的溶液以及购买的食醋分别用0.45 μm滤膜过滤,过滤后超声7 min。
1.3.4 色谱条件
色谱柱:Accurasil-C18柱;检测器:SPD-15C紫外-可见检测器(岛津,250 mm×4.6 mm,5 μm);检测波长:255 nm;流动相:0.1%的草酸溶液;流速:1.0 mL/min;进样量:20 μL。
1.4 VC剩余率的计算

(1)
式中,A0为样品溶液中VC的起始含量;A为样品溶液在不同条件下所对应的VC含量。
2 结果与分析
2.1 VC的HPLC法测定
2.1.1 色谱条件的选择
根据相关文献(Klimczak et al., 2015; 王敬等,2014)同时结合VC的性质,色谱柱采用C18柱,选择0.1%的草酸作为流动相,其他条件分别为流速1.0 mL/min,进样量20.0 μL,检测波长255 nm。在该色谱条件下,浓度为1.00 mg/L的VC标准溶液的色谱图如图1所示。由图可见VC的峰形好且无VC的氧化物干扰峰,能满足VC分析的需求。
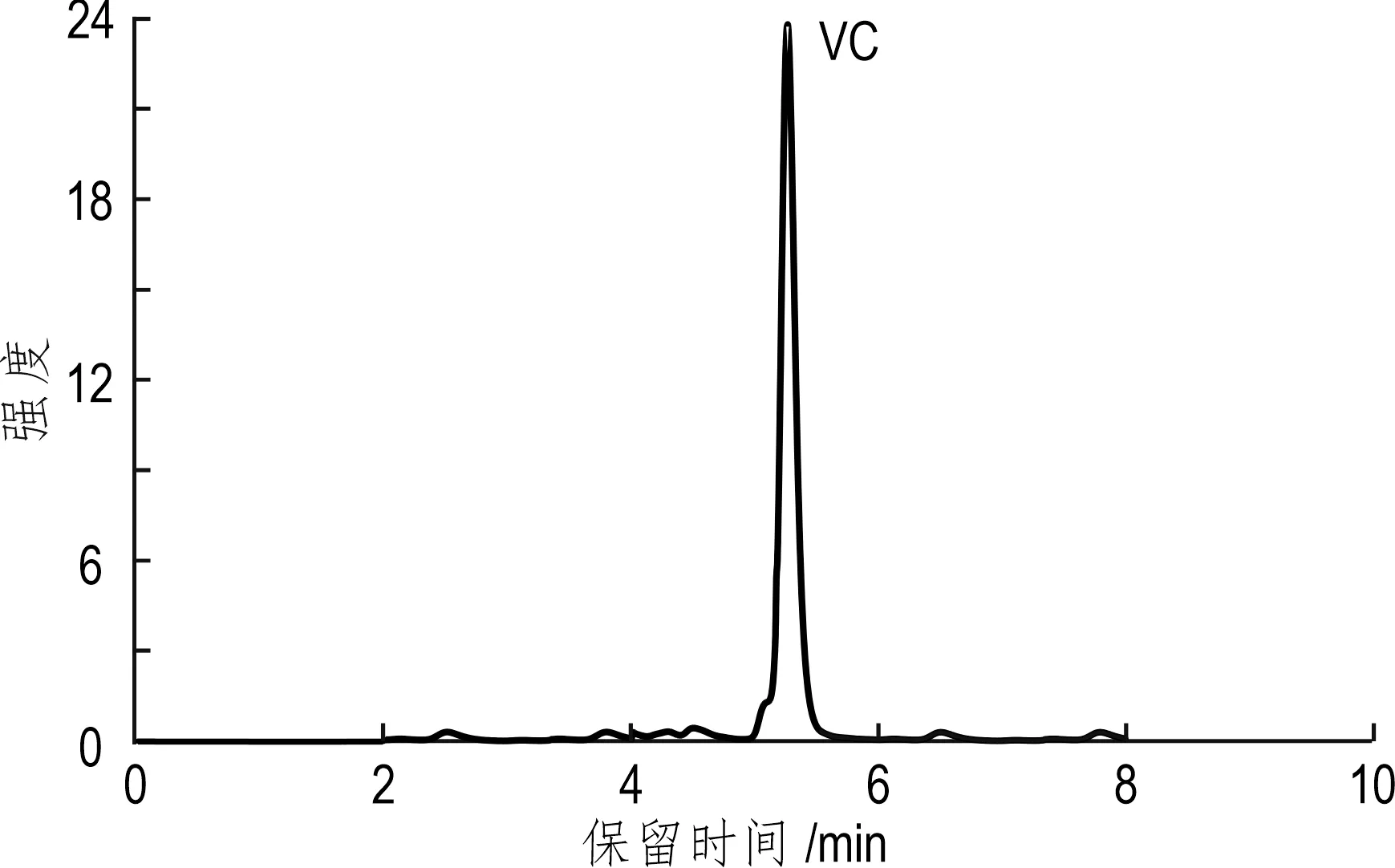
图1 VC标准色谱图Fig.1 Standard chromatogram of vitamin C
2.1.2 VC的线性精密度和检出限
用1.00 g/L的VC标准储备液稀释配制系列浓度的VC标准液,在所选色谱条件下进行HPLC检测。以VC峰面积对浓度绘制校准曲线,结果显示,在0.10~6.00 mg/L浓度范围内,VC标准溶液的线性回归方程为y=330 32x+3 233.3,相关系数R2为0.999 6,表明VC标准溶液在该浓度范围内线性良好。
将0.50 mg/L的VC标准溶液,在所选色谱条件下连续重复测定11次,得到VC检测精密度,再根据检出限计算公式LOD = 3σc/S(式中:σ为标准偏差,c为VC标准品浓度,S为相应信号强度的平均值),计算出VC的检出限(表1)。从表1可以看出本法检测VC具有重现性好、检出限低等优点。
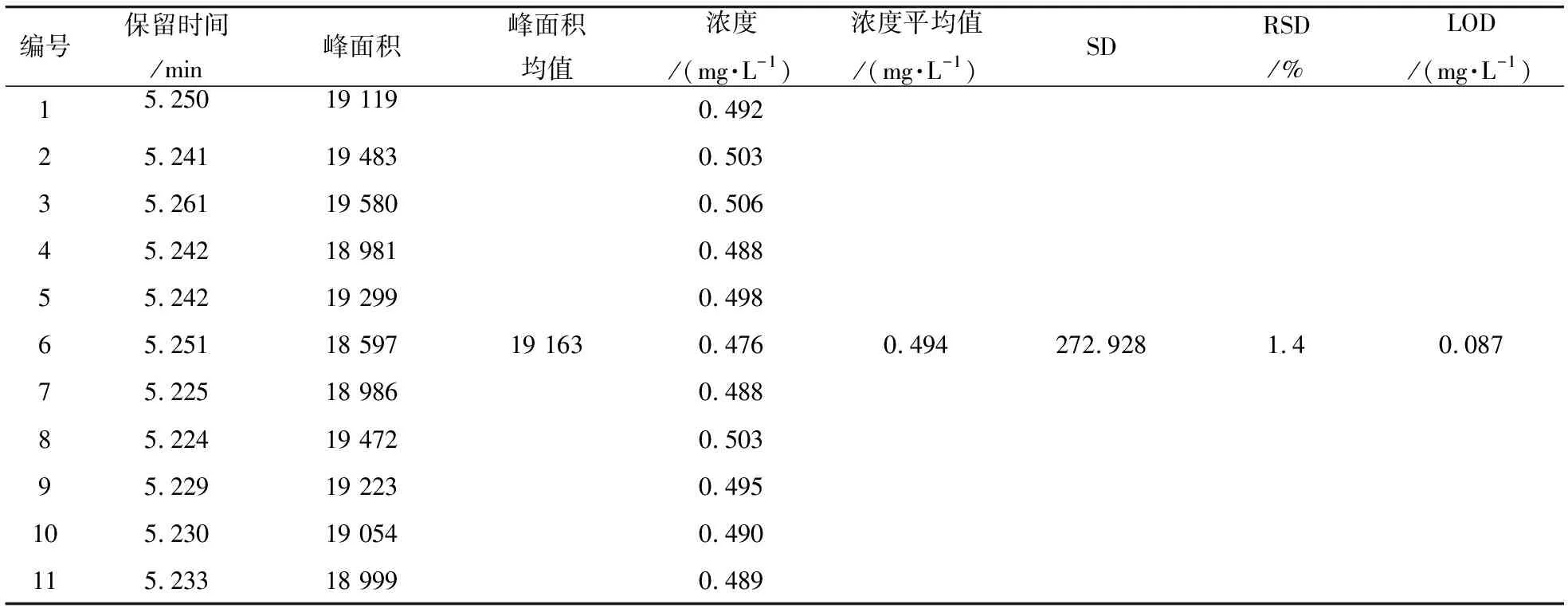
表1 VC检测的精密度和检出限Table 1 Precision and detection limits on the determination of vitamin C
2.1.3 样品测定和加标回收
将购买的同一批3个外表健康、颜色均匀的橘子分别标为1、2、3号样品,并按前述预处理的方法进行处理,然后进行HPLC检测,每个样品平行测定3次,结合标准曲线得到样品中VC浓度,再计算出每100 g该橘子所含VC的量(表2),并将此数据作为下文探究橘子样品中VC稳定性的起始值。

表2 橘子样品分析结果Table 2 Results of analysis on orange samples
在体积均为50 mL的1、2、3号样品中分别添加150 μg的VC标准品,超声处理5 min后,每个样品平行测3次,得到加标回收率(表3)。

表3 橘子样品的加标回收率Table 3 Recoveries of orange samples
2.2 VC稳定性的探究
2.2.1 时间、温度和光照对VC稳定性的影响
将1、2、3号橘子样品剥开后分别在室温光照、室温避光和低温避光3个条件下放置0 h (即刚剥开时的检测结果,表2)、6 h、18 h、24 h后按前述方法进行处理和测定,检测对应的VC含量,考察VC随时间、温度和光照的变化情况。将橘子样品的VC含量随放置时间的变化做折线图(图2)。
实验过程中发现,1号样品搁置24 h后局部出现腐烂情况,而2号和3号样品依旧完好,故推断除了低温有利于防腐外,VC的散失也会加剧食品的腐烂,这跟VC的抗氧化性是一致的。即VC可能具有防腐的功能。
由图2可知,随着时间的增加,3个样品VC含量均减少了(放置24 h后减少35%以上),但减少的程度各不相同。对比1、2号样品发现,光照会使VC加速分解;对比2、3号样品发现,低温能减缓VC的分解;对比1、2、3号样品发现,在避光和低温共存的条件下,VC分解最少。可见,为防止橘子中VC流失,应尽量将其保存至低温、避光环境中,且剥开后的橘子不应长期保存。

图2 橘子样品中VC含量随时间的变化图Fig.2 Changes in vitamin C quantity in orange samples over time
由图2可见,在0~24小时内,随着时间的延长,在各条件下VC含量均逐渐减少,且分解速率呈减缓的趋势。这可能是因为VC的分解大致包括两个过程(高晗等,2008):第一个过程为抗坏血酸(还原态)氧化生成脱氢抗坏血酸(氧化态)和脱氢抗坏血酸还原生成抗坏血酸的过程,这个过程是可逆的;第二个过程是抗坏血酸氧化生成脱氢抗坏血酸,而后直接进行不可逆分解的过程。因此,两个过程综合作用的结果是随时间延长,VC的分解逐渐达到平衡,分解速率会逐渐减缓,但是不存在VC不再分解的时间点。
假设橘子中VC以下列反应式降解:
nA→产物
(2)
根据VC降解的相关文献报道,VC的降解大部分呈现一级反应动力学模型。为此,本次研究进行相关验证,假设n=1。上式可简化为:
(3)
(4)
lnc=-kt+C1
(5)
式(2)至(5)中,r为VC的降解速率,mg/(100 g·h);c为VC在任意时刻t的浓度,mg/100 g;k为降解速率常数;C1为常数。
通过对lnc-t作图,发现不同条件下的 lnc-t呈线性关系,且线性相关性较高,R2均在 0.97以上,这表明此反应符合一级反应模型,验证了橘子中VC符合一级反应降解规律。
结合图3中方程,得到1号、2号和3号样品中VC分解的速率常数k分别为0.024 18 h-1、0.020 44 h-1、0.019 44 h-1,该值直接反映了反应速率的快慢,对确定反应历程、设计合理的反应器以及保存运输等提供了重要依据。
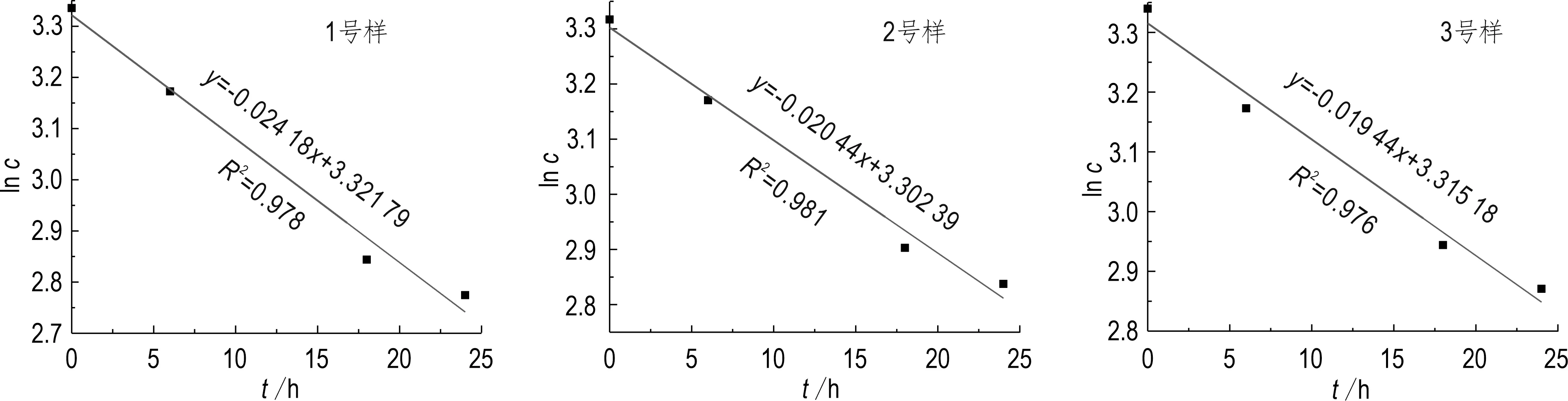
图3 lnc与t线性拟合图Fig.3 Plots of lnc to t
2.2.2 调味料和茶水等介质对VC稳定性的影响
为了更加贴近生活实际,探究了食盐、食醋、食用碱、蔗糖等生活中常用调味料以及饮用水、茶水等对VC的影响。将食盐、食用碱、蔗糖、茶水等按1.3.3的方法配成溶液。分别将同批购买的6个橘子(依次编号为4、5、6、7、8、9号)按1.3.2的方法提取后,各取10.0 mL样品初始溶液,依次加入6个50 mL的棕色容量瓶中。然后分别加入饮用水、食盐水、食醋、食用碱溶液、蔗糖溶液、茶水5 mL,再用0.1%的草酸溶液依次定容,配成4至9号样品溶液。将这6种溶液在室内环境(室温,自然光)下搁置0 h (即起始测得值)、2 h、4 h、6 h时,在1.3.4的色谱条件下分别检测VC含量,再根据1.4中剩余率的计算公式求出0 h、2 h、4 h、6 h所对应的剩余率(表4)。

表4 调味料和茶水等介质对VC 稳定性的影响Table 4 Effect of seasoning and tea water on the stability of VC
由表4可知,饮用水、食盐、食醋、食用碱、蔗糖和茶水等介质对VC的分解有不同程度的影响。其中VC在碱性介质(如食用碱)中最易分解,中性介质(如饮用水)中次之、酸性介质(如食醋)中分解最慢。与饮用水相比,食盐溶液对VC分解影响不大;茶水对VC的散失具有较弱的加速作用,这是因为茶水虽然含有茶碱、咖啡碱、生物碱和胆碱等弱碱物质,但是也含有茶多酚等弱酸性物质,在这些物质的综合作用下茶水显很弱的碱性;蔗糖溶液对VC分解具有很大加速作用,可能是由于蔗糖是一种还原糖,它会与VC氧化产生的脱氢抗坏血酸发生氧化还原反应而被大量消耗的缘故(邱紫云等,2015)。
3 结论
建立了橘子中VC的HPLC测定方法,经方法学考察表明,该方法具有检出限低、精密度高、稳定性好等优点,可为橘子中VC含量的检测提供科学的分析方法。利用该方法,对VC标准样品进行分析,结果表明,VC浓度在0.10~6.00 mg/L范围内具有良好的线性关系,其线性回归方程为y=33 032x+3 233.3,相关系数R2为0.999 6,RSD为1.424%,LOD为0.087 mg/L;市售橘子中VC的稳定性研究结果显示,VC在低温和避光条件下比较稳定,在碱性介质中易被破坏,在酸性介质中较为稳定,在盐溶液中影响不大,而蔗糖溶液对VC的分解具有很大的加速作用,VC的分解呈现一级反应动力学规律。
