基于生长发育评估和干预的儿童甲状腺B超筛查的横断面调查
2021-10-22王峥嵘郭佳运
李 阳 王峥嵘 郭佳运 张 勇 李 辉
以往认为,儿童多囊性甲状腺疾病(PCTD)少见,仅为个案报道[1-3]。PCTD的发生机制和临床意义至今未明,部分与甲状腺功能减退[1, 4]、甲状腺亢进[2, 5]和多囊肾病[6]等疾病同时存在,但儿童PCTD转归如何,是否与成年后其他甲状腺疾病的发生有关联,目前未知。有学者在成人甲状腺乳头状癌和低分化癌患者的甲状腺切除标本中观察到PCTD[7],但目前尚缺乏PCTD转变为恶性肿瘤的证据。成人中甲状腺结节和甲状腺癌的发生率逐年增加[8, 9],与儿童期PCTD等甲状腺异常是否有关联不清楚。目前超声检查是甲状腺疾病筛查与长期随诊的首选方法,有利于早期发现病变。近几年,本研究团队关注到体检儿童中甲状腺B超中PCTD检出率较高,复习文献发现,国外临床研究中儿童PCTD检出率也较高[10-13],且各年龄段均有分布。本研究基于首都儿科研究所附属儿童医院(我院)生长发育门诊对身高偏矮、身高生长速度减慢或青春期发育评估的儿童,经临床评估后需要采取药物干预前行B超安全性筛查的数据,了解儿童PCTD的发生率及超声特征,为进一步认识和研究PCTD提供参考。
1 方法
1.1 纳入标准 同时满足以下5项,①2017年5月19日至2020年11 月19日在我院保健科生长发育门诊首次就诊和随访的儿童;②主诉为身高偏矮或身高生长速度减慢或青春期发育评估;③甲状腺功能检查FT3、FT4正常,甲状腺球蛋白抗体(Tg-Ab)、甲状腺受体抗体(TR-Ab)和甲状腺过氧化酶抗体(TPO-Ab)检测阴性;④临床评估后需要采取药物(生长激素或者抑制剂)干预治疗前行B超安全性筛查;⑤甲状腺功能检测和B超检查时间相距1周内。
需要说明的是,以上纳入标准③~⑤也是我院生长发育门诊对身高偏矮、身高生长速度减慢或青春期发育评估的诊疗常规。
1.2 排除标准 通过问诊排除:①使用可能影响甲状腺功能的药物(碳酸锂、糖皮质激素和苯妥英等);②有甲状腺疾病家族史及其他器官囊肿家族史;③有颈部放射史;④有慢性疾病。
1.3 剔除标准 主诉因身高生长速度减慢而致身材矮小并伴有其他体征,如肘外翻、内眦赘皮等,遗传代谢性疾病行染色体和基因检测有阳性发现者。
1.4 甲状腺功能、抗体检查 采用雅培I 2000化学发光免疫分析仪测定甲状腺功能指标和甲状腺抗体。我院参考值范围如下,FT3:3.3~6.8 pmol·L-1,FT4:10.8~20.0 pmol·L-1,TSH:0.8~5.0 mIU·L-1,Tg-Ab:≤113 IU·mL-1,TR-Ab:≤1.22 IU·L-1,TPO-Ab:≤34 IU·mL-1。
1.5 甲状腺超声检查 使用Philips IU 22和GE LOGIQ E9彩色超声诊断仪,线阵探头频率分别为5~12 MHz和6~15 MHz。于我院超声科检查,患儿取仰卧位,头部后仰,医者去除其颈部装饰物,充分暴露颈前区,对于颈部较短或肥胖儿童在双肩及颈后部垫枕,呈头低颈高位。嘱平稳呼吸,勿吞咽,对甲状腺及周围组织进行全面扫查。
1.6 超声图像观察分析指标
1.6.1 甲状腺容积 单叶甲状腺容积[14]计算公式,V(mL)=0.479×长径(cm)×宽径(cm)×厚径(cm)。数据分析中的甲状腺容积为两侧叶容积之和,V(mL)=V左+V右。不同年龄甲状腺大小异常值参考文献[14]。超过参考值上限定义为甲状腺肿大。因仅有≥6岁儿童参考值,故<6岁儿童不分析容积大小。
1.6.2 甲状腺实质回声 均匀、不均匀和网格状回声。
1.6.3 甲状腺先天性畸形与异常 异位甲状腺,甲状腺舌骨囊肿,甲状腺结节(囊性、实性和囊实性)等,其中囊性结节也称为囊肿。
1.6.4 囊肿描述 ①囊肿位置:左叶、右叶、峡部;②数量:单发(1个)、2~3个、多发(≥4个);③囊肿大小:取最大囊肿的最大内径;④形态:规则(圆形、类圆形或椭圆形)、不规则;⑤点状强回声:有、无;⑥点状强回声伴彗星尾征:有、无。
1.7 多囊性甲状腺疾病(PCTD)判定标准 PCTD目前没有明确的诊断标准,根据既往文献[11]报道:①囊肿≥4个;②甲状腺自身抗体为阴性;③排除甲状腺实质网格状回声;④排除囊性结节之外的甲状腺先天性畸形与异常。
1.8 临床资料采集 对行B超筛查患儿的当天病历和超声检查纸质报告进行拍照留存,从留存病历中提取性别、年龄、身高、体重、家族史、既往特殊用药史、实验室检查结果,如FT3、FT4、TSH、Tg-Ab、TR-Ab和TPO-Ab、超声检查日期、超声描述诊断。以每1岁为年龄分1组。以HtSDS<-2为身材矮小,-2≤HtSDS≤+2为身材正常,HtSDS>+2为高身材; 以WtSDS<-2为低体重、-2≤WtSDS≤+2为正常体重,WtSDS>+2为体重过重。以B超提示PCTD为分组依据。需要说明的是,B超显示甲状腺实性结节、多发囊肿伴实性结节和囊肿数量<4个的患儿归为其他组。
1.9 统计学分析 采用Epidate 3.0进行数据录入和逻辑检错,用SPSS 22.0软件进行数据处理及统计分析。计量资料,符合正态分布的使用t检验或方差分析;不符合正态分布的采用独立样本非参数秩和检验。P<0.05为差异具有统计学意义。
2 结果
2.1 一般情况 符合本文纳入标准的病历596例;排除4例先天性甲状腺功能减退、4例甲状腺功能亢进、2例甲状腺弥漫性改变伴自身抗体升高、1例幼年特发性关节炎和1例白血病;剔除染色体异常(特纳综合征)10例和基因变异2例;572例进入本文分析,男童259例,女童313例;年龄3.0~17.0(9.5±2.73)岁,其中>15岁3例,故分析时将其归入14岁组。
表1显示,正常组364例,PCTD 组161例(28.2%),其他组47例(8.2%)。PCTD男童检出率为23.6%(61/259),女童检出率为31.9%(100/313)。≥7岁PCTD的检出率(>27.0%)明显上升,8~12岁尤其明显,PCTD检出率均>35%。
正常组3~5岁年龄段和PCTD组4~5岁年龄段均为身材矮小,PCTD组5岁年龄段低体重。身高标准差值在6岁和9岁年龄段,正常组较PCTD组差异有统计学意义;体重标准差值在5、9、11和14岁年龄段,正常组较PCTD组差异有统计学意义。需要说明的是,鉴于其他组甲状腺功能正常,B超有异常描述,异质性比较大,故不将其身高、体重标准差值与正常组和PCTD组比较。
2.2 PCTD超声影像特征
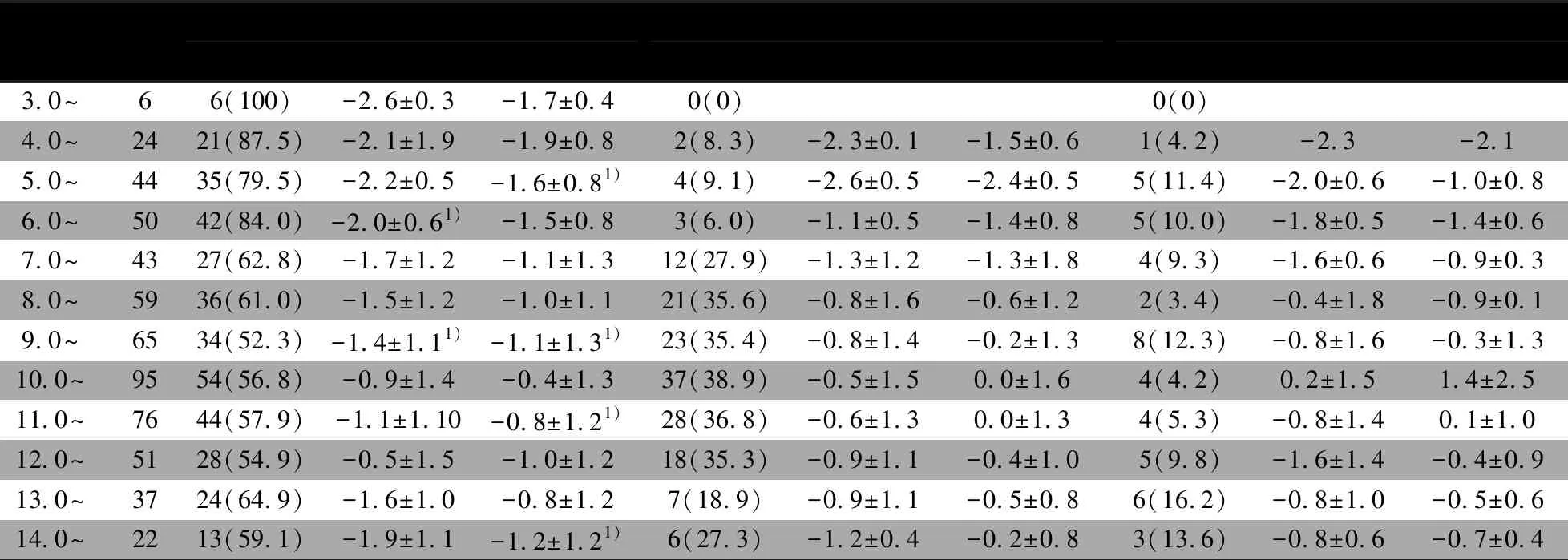
表1 不同年龄组儿童甲状腺超声PCTD的检出情况和体格水平比较
2.2.1 甲状腺大小 PCTD组6~14岁年龄段155例,甲状腺肿大11例(7.1%);正常组6~14岁年龄段302例,甲状腺肿大14例(4.6%)。
2.2.2 甲状腺实质回声 PCTD组3~14岁年龄段161例,实质回声均匀120例(74.5%),实质回声不均匀41例(25.5%),未见网格状回声;正常组3~14岁年龄段364例,实质回声均匀357例(98.1%),实质回声不均匀6例(1.6%),网格状回声1例(0.3%)。
2.2.3 PCTD组囊肿描述 ①囊肿均为规则边缘;②弥漫分布于双叶及峡部28例(17.4%),双叶113例(70.2%),右叶17例(10.5%),左叶3例(1.9%);③位于左叶的囊肿最大直径1.0~8.0(2.6±1.1)mm,3例≥5 mm;位于右叶的囊肿最大直径0.7~7.2(2.5±1.1)mm,4例≥5 mm。④囊肿内可见点状强回声伴彗星尾征138例(85.7%)。
2.3 TSH值 正常组14例和PCTD组9例TSH>5 mIU·L-1,处于亚临床甲状腺功能减退。
3 讨论
PCTD超声图像特征为多个散在分布于甲状腺内的小圆形、薄壁的囊性灶。既往儿童PCTD被认为是一种少见现象,多为偶然发现[1-3],有关儿童PCTD的发生率及相关研究在国内尚未见报道。本文纳入我院生长发育门诊3年间连续的572例身高偏矮、身高生长速度减慢或青春期发育评估的儿童,这些儿童FT3、FT4正常,Tg-Ab、TR-Ab和TPO-Ab检测阴性,为临床评估后需要采取药物干预治疗前行B超安全性筛查的儿童,正常组3~5岁年龄段和PCTD组4~5岁年龄段均为身材矮小,其他年龄段平均身高标准差值处于正常范围,总体体重标准差值在正常范围,但HtSDS和WtSDS均在-2~0水平,说明本研究人群从生长发育水平角度还可归类于正常儿童人群。
本文PCTD的检出率为28.1%,说明儿童PCTD已非少见现象,而是儿童期常见的甲状腺疾病。Tamar[11]对521名3~17岁儿童进行甲状腺超声检查,发现PCTD 112例,检出率为21.5%。就诊于加拿大三级儿童医院的儿童(因非甲状腺指征而接受甲状腺超声检查,年龄1d至17.5岁,男153名,女134名)中甲状腺超声异常的发生率为18.0%,其中PCTD和单发囊肿的检出率分别为8.7%(25/287)和3.5%(10/287)[10]。日本青森、山梨和长崎3个县(4 365名3~18岁幼儿园、小学和初中儿童进行甲状腺超声筛查)和福岛地区儿童(4~15岁, 1 214名根据病史、触诊和实验室检查排除患有甲状腺疾病,男330名,女884名)PCTD的发生率明显高于文献[10]和[11]的报道,42.5%~58.4%儿童被检查出有囊肿,大多数囊肿数量≥2个[12, 13]。此外,PCTD的检出率与性别、年龄有关。本研究中女童的PCTD检出率高于男童(31.9%vs23.6%),与既往文献报告结果一致[12]。7岁以后PCTD检出率明显升高,尤其是8~12岁开始青春期发育阶段,一方面说明PCTD是后天形成的,另一方面也提示PCTD可能与青春期发育有关。
PCTD检出率增高的原因可能与地区门诊患儿数量、年龄分布、患儿社会生态环境不同以及超声检查技术提高有关,也不排除存在致病风险因素(如碘摄入过多、电离辐射等)作用增强的影响[12, 13]。囊肿过于细小时,也会受超声设备声像图清晰度影响,囊腔可不显示,仅表现为稀疏的点状强回声,超声易诊断为“砂粒样”钙化[15]。
尽管不同研究的PCTD发生率不同,但达成的共识是PCTD儿童的囊肿直径以<5 mm为主[3, 10, 13]。PCTD可能是结节退化形成的包含有浆液或胶质的囊性无回声影,彗星尾征可能与囊腔中胶质的存在有关,是良性囊肿的标志,敏感度和特异度均为100%[16]。本研究85.7% PCTD囊肿中可见彗星尾征。此外,PCTD超声表现多样,囊肿的分布可为散在性或弥漫性,可双叶同时存在或局限在单侧叶。PCTD儿童甲状腺肿大发生率(7.1%)较正常组高(4.6%)。有学者认为多发的囊肿替代了甲状腺原本的滤泡细胞,导致滤泡细胞数量减少[7]。由于正常滤泡细胞数量减少,即使在碘充足的情况下,甲状腺激素的分泌可能并不能满足生理需求,甲状腺激素相对缺乏,TSH分泌增多,导致滤泡上皮细胞内胶质堆积,甲状腺轻度增大。此外,Henjum等[17]的研究显示,儿童甲状腺容积与碘摄入量呈正相关。因此高碘饮食、PCTD和甲状腺肿大三者之间的关系值得进一步研究。
有关PCTD的转归和预后,有学者认为成人PCTD与甲状腺功能减退有关[7, 18],但这个结论并未得到大样本的临床研究证实。本研究结果显示,仅正常组13例(3.5%)和PCTD组9例(5.6%)TSH>5 mIU·L-1,处于亚临床甲状腺功能减退。成人中PCTD的发生率为0.74%(28/3 783)[19],据此推测PCTD可能随儿童生长发育进程自行消失,至青春期结束后,甲状腺激素需要量减少,甲状腺亦可能恢复正常。但对健康体检或者其他原因发现的小样本PCTD儿童进行的随访研究显示,2~4年内多数儿童未见超声图像和甲状腺功能的改变[3, 5, 10],仅有1名儿童在发现PCTD的16个月后诊断为甲状腺功能亢进[2],并未发现甲状腺恶性变。进行随访观察的研究文献中,个别(1~2名)儿童囊肿消失[3, 5, 10],2名儿童在随访时被确认首次检查时将血管中的伪影误认为是结节/囊肿[5]。提示在超声检查时需要仔细甄别。PCTD可能属于良性病变,短期内变化不明显,少有发生甲状腺功能异常,但其远期变化目前尚不清楚,因此需要对已经发现有PCTD的儿童进行随诊。
综上,PCTD已非少见疾病,检出率为28.1%,7岁以后儿童的检出率明显升高,女童检出率高于男童,但无特异性临床症状。PCTD儿童的囊肿多位于双叶,囊肿大小多<5 mm,囊内可见点状强回声,伴彗星尾征。
