多孔聚(丙烯酰胺-co-丙烯酸)微球的制备及对亚甲基蓝的吸附性能
2021-10-21刘建安张利雄
刘建安,张利雄
(南京工业大学 化工学院 材料化学工程国家重点实验室,江苏 南京 211800)
随着现代印染工业的快速发展,印染废水排放导致的环境问题越来越严重[1-2]。亚甲基蓝(MB)是偶氮类染料的一种,广泛应用于皮革、纺织品、纸张和衣物等[3-5]。其制作工艺简单、染色牢固、适用性广,是印染废水中具有代表性的阳离子污染物之一[6]。目前,对含有MB废水的处理方法主要有吸附法[7-8]、离子交换法[9]、化学沉淀法[10]、微生物降解法[11]、光催化降解法[12]和膜分离法等[13]。其中吸附法由于其经济性和高效率、不产生有害物质等优点,被认为是较适合的处理方法[14]。常用于吸附MB的材料有壳聚糖[15]、活性炭[16]、金属-有机框架[17-18]和丙烯酸基水凝胶[19-20]等,对MB的最大吸附量分别为169、225、239 mg/g和1.193 g/g。丙烯酸基水凝胶材料对MB的吸附量最高。
朱俊芳等[21]通过酸解法制备纳米纤维素,再利用自由基聚合法将甲基丙烯酸接枝到纳米纤维素上,得到含有多孔[22]结构的水凝胶,此材料对MB的最大吸附量为1.250 g/g。Fosso-Kankeu等[23]使用口香糖和丙烯酸(AA)接枝共聚合成了口香糖和丙烯酸基接枝共聚合物,该材料对MB的最大吸附量为909.09 mg/g。Thakur等[24]在交联剂、引发剂和TiO2纳米颗粒的存在下,将AA接枝共聚到海藻酸钠上来制备水凝胶,此材料对MB的最大吸附量为2.257 g/g。Yao等[25]以丙烯酰胺(AM)为单体、PEG-4000为造孔剂,采用聚合致分相方法制备多孔聚丙稀酰胺(PAM)微球,再通过在Fe2+/Fe3+溶液里浸渍和在碱性溶液中进行后处理,制得了多孔磁性PAM微球,微球对MB的最大吸附量为1.990 g/g。水凝胶材料对MB的高吸附能力,得益于水凝胶的三维交联网络结构上带有电荷,通过静电相互作用能吸附带相反电荷的离子和有机染料。水凝胶中的羧基在吸附MB阳离子染料的过程中发挥了重要作用,上述前3种水凝胶材料通过引入羧基制备复合带特定功能基团材料,而多孔磁性PAM微球则是通过碱液处理后酰胺基团分解生成大量羧基,使其对MB具有较高的吸附能力。
本研究以羧基更丰富的AA和AM为单体、PEG-4000为造孔剂,采用聚合致分相方法制备多孔聚(丙稀酰胺-co-丙稀酸)(p(AM-co-AA)微球)(简称PPMS),随后将微球浸渍在NaOH溶液中进行改性,考察了单体中AA质量分数对微球孔结构和对MB吸附能力的影响。进一步探究吸附温度、MB初始浓度及pH等因素与吸附量的关系,通过Langmuir方程对PPMS吸附MB的结果进行拟合,PPMS对MB的最大吸附量高于不加AA时制得的多孔PAM微球对MB的吸附量。
1 实验
1.1 药品与试剂
丙烯酰胺(AM)、丙烯酸(AA)、过硫酸钾、N,N′-亚甲基双丙烯酰胺(MBAM)、脱水山梨糖醇脂肪酸酯(Span 80)、NaOH,分析纯,国药集团化学试剂有限公司;聚乙二醇(PEG-4000),分析纯,阿拉丁工业公司;液体石蜡,分析纯,上海凌峰化学试剂有限公司;亚甲基蓝(MB),分析纯,上海三爱思化学试剂公司;无水乙醇,分析纯,无锡市亚盛化工有限公司;去离子水,自制。
1.2 PPMS的制备
取不同质量比的AM和AA(单体总质量分数为10%)、PEG-4000质量分数为10%、过硫酸钾和MBAM质量分数分别为0.6%的水溶液作为分散相,并将含有质量分数为5%span的液体石蜡作为连续相。分别注入同轴微流体装置的两个入口,分散相通过针头(Φ0.11 mm)插入已浸入水浴的聚四氟乙烯(PTFE)管(Φ0.56 mm×650 mm)中,结果见图1。分散相和连续相的流速分别为0.4和4 mL/h,单分散的液滴通过连续相的剪切力形成,液滴流入加热到96 ℃的PTFE管中以引发AM和AA聚合,停留时间约为80 s。流出物收集在装有乙醇的烧杯中,过滤并用乙醇洗涤3次后,在70 ℃烘箱干燥1 h;干燥后取0.1 g试样分散在100 ℃的NaOH溶液(20 mL、0.5 mol/L)中处理2 h;最后,用蒸馏水和乙醇洗涤3次碱处理后的微球。
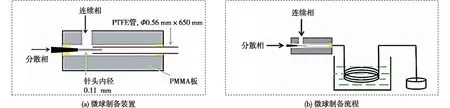
图1 PPMS的制备过程[25]Fig.1 Preparation process diagram of PPMS[25]
1.3 PPMS吸附实验
1.3.1 PPMS微球吸附性能测定
通过控制单因素变量法,考察不同合成条件制备的PPMS和外部环境对MB吸附性能影响。吸附性能实验的变量范围分别为:单体中AA质量分数为0~40%、MB溶液pH(3~9)和吸附温度(25~50) ℃。
准确称量PPMS 5 mg分别浸入100 mL质量浓度为100 mg/L的MB溶液中,120 r/min下振荡吸附24 h。吸附结束后取上清液稀释定容,采用可见分光光度计,检测664 nm处溶液的吸光度,计算PPMS的吸附量。
1.3.2 PPMS的吸附等温线
准确称量5 mg PPMS分别浸入100 mL不同质量浓度梯度(50~400) mg/L的MB溶液,调节溶液的温度和pH,120 r/min下振荡吸附。吸附结束后,采用1.3.1节步骤计算微球对MB的吸附量。
1.3.3 PPMS的吸附动力学
将5 mg PPMS浸入100 mL质量浓度为100 mg/L的MB溶液中,调节溶液的温度和pH,120 r/min下振荡吸附(5~720) min。吸附结束后,采用1.3.1节步骤计算微球对MB的吸附量。
通过下列等式计算PPMS平衡吸附量。
qe=(ρ0-ρe)V/m
(1)
qt=(ρ0-ρt)V/m
(2)
式中:ρ0、ρt、ρe分别为MB的初始质量浓度、吸附时间为t时及吸附达平衡时的质量浓度,mg/L;qt和qe分别为t时的吸附量和达到平衡时的吸附量,mg/g;V为溶液的体积,L;m为吸附实验中所用的吸附剂的质量,g。
1.4 材料表征
采用扫描电子显微镜(SEM,S-4800型,日本Hitachi公司)观测PPMS的形貌;采用红外光谱仪(FT-IR, Nicolet 6700型,美国Thermo Fisher Scientific公司)检测试样的特征峰;采用紫外分光光度计(UV, Lambda 35型,美国PE公司)测定MB溶液664 nm处的吸光度。
2 结果与讨论
2.1 PPMS的表征结果
图2为不同AA质量分数制备的PPMS和微球表面结构的扫描电镜照片。由图2可以看出,当不加入AA时,微球表面具有孔结构,随着AA质量分数增加,微球的表面变得致密,将小球切开,内部也是致密的。这是因为当AM开始聚合时,含有PEG的水溶液会从AM聚合形成了初级PAM网络中分离出来,这是微球具有孔结构的原因[26]。当AA质量分数增大,由于PEG对PAA没有分相作用,所以孔结构会减少。在Yao等[25]的研究基础上,以AA和AM共聚制备了PPMS,从扫描电镜照片可以观察到两者的孔结构相似。

图2 单体中不同AA用量下制备得到的PPMS电镜图片Fig.2 Electron micrograph of PPMS prepared under different AA dosages in the monomer


图3 PPMS(a)、碱液处理后的多孔PAM微球(b)和多孔PAM(c)的红外光谱图Fig.3 Infrared spectra of PPMS (a), porous PAM microspheres treated with alkaline solution (b) and porous PAM (c)
2.2 PPMS对MB的吸附性能
2.2.1 单体中AA用量对MB吸附性能的影响
图4为不同AA质量分数合成的PPMS对MB的吸附量。由图4可知,试样对MB的吸附量随AA用量先增加后减小。AA质量分数为单体的20%时,PPMS对MB吸附量最高,达到1 814 mg/g。相比酰胺基团,PPMS上的羧基基团对MB具有更强的吸附作用。因此,随着合成体系中AA质量分数的增大,PPMS对MB的吸附量也逐渐增大。AA质量分数为单体的20%时,PPMS对MB的吸附量最大,此后再增大AA的质量分数,PPMS时MB的吸附量反而减小。这是因为随着AA质量分数的增加,PPMS中的孔结构变少,使得吸附量下降。

图4 AA质量分数对PPMS吸附MB的影响Fig.4 Effects of AA mass fraction on the adsorption of MB by PPMS
2.2.2 温度对吸附效果的影响
图5为不同溶液温度(25~50) ℃下PPMS对MB的吸附量结果。随吸附温度的升高,PPMS对MB吸附量呈下降趋势。从不同吸附温度下PPMS对MB吸附热力学参数可知,焓变ΔH小于0,说明PPMS对MB的吸附过程为放热反应,因此适当降低吸附温度可提高PPMS对MB的吸附效果。
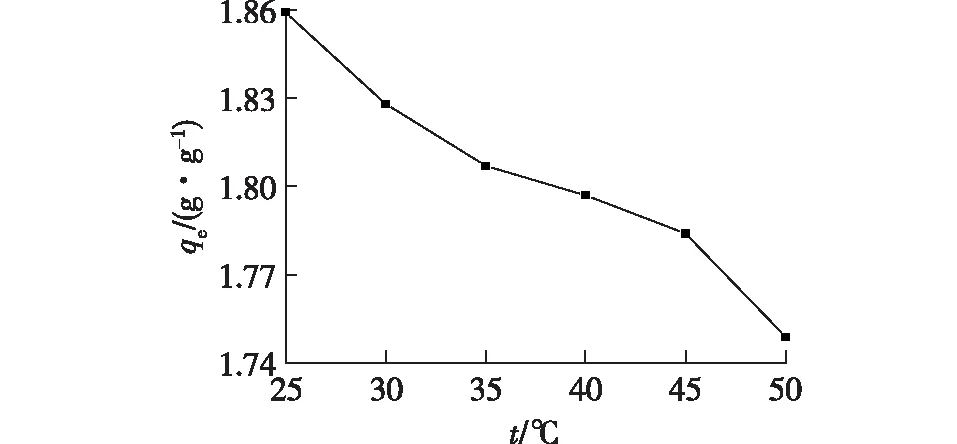
图5 溶液温度对PPMS吸附MB的影响Fig.5 Effects of solution temperature on the adsorption of MB by PPMS
2.2.3 pH对吸附效果的影响
PPMS对MB的吸附效果如图6所示。当溶液pH从3增大至5时,PPMS对MB的吸附量迅速从96 mg/g增大至1.83 g/g;当染料溶液pH大于5时,处于吸附高位,PPMS对MB的吸附量基本保持不变。pH为8时,吸附量最高,当染料溶液pH较低时,染料溶液中过多的H+使PPMS结构上的羧基被质子化,—COOH无法释放出负电荷,降低了—COOH与MB之间的静电作用;当MB溶液pH增大时,逐步发生去质子化过程,—COOH转化为与MB具有良好结合能力的—COO-。

图6 溶液pH对PPMS吸附MB的影响Fig.6 Effects of solution pH on the adsorption of MB by PPMS
2.2.4 PPMS的吸附等温线


图7 PPMS对MB的吸附等温线及对MB吸附数据进行Langmuir和Freundich的拟合曲线Fig.7 Adsorption isotherm of PPMS to MB and the fitting curve of Langmuir and Freundich on MB adsorption data

表1 Langmuir与Freundlich吸附等温线模型拟合常数
2.2.5 PPMS的吸附动力学


图8 PPMS吸附MB的吸附动力学Fig.8 Adsorption kinetics of MB by PPMS

表2 PPMS对初始质量浓度为100 mg/L MB的拟二阶动力学参数
2.2.6 PPMS吸附MB的机制研究
PPMS对MB溶液有很好的吸附效果。Thakur等[24]提出,MB在含有TiO2掺杂的丙烯酸基海藻酸钠水凝胶的吸附机制可能是由于阳离子染料与水凝胶上的羧酸根基团之间的静电吸引以及酰胺基团之间的氢键相互作用所致。因而电荷引力是PPMS强吸附作用的一个重要因素。在制备PPMS的过程中,PEG质量分数会对微球的孔道性质产生重要的影响,因此可推断微球的多孔性质是导致其高吸附量的另一重要原因。按照1.2节所述方法在不同PEG质量分数下制备了PPMS试样。选用上述PPMS试样吸附MB来说明微球的孔道性质对MB吸附过程中的重要作用。图9为不同PEG质量分数条件制备出的PPMS对MB的吸附量变化曲线。由图9可知,当不加PEG时,微球对MB的吸附量为1.145 g/g,随着PEG质量分数增加,微球对MB的吸附量呈递增趋势,在PEG质量分数为10%时,微球对MB的吸附量为1.814 g/g。由此可见,孔结构对微球的吸附同样有着重要的作用。

图9 不同PEG质量分数对PPMS吸附MB的影响Fig.9 Effects of different PEG mass fraction on the adsorption of MB by PPMS
2.2.7 PPMS的脱附再生性能
取5 mg PPMS于50 mL质量浓度为10 mg/L的MB溶液中,达到吸附平衡后。过滤得到吸附有MB的PPMS,将其置于10 mL pH为2的50%甲醇溶液中进行脱附,脱附完成后重复上述吸附实验,如此循环5次,再生性能如图10所示。相较于未使用的微球吸附剂,经再生的微球吸附剂的吸附效率出现微小的下降,此后其对于MB的去除率基本稳定,保持在96%。
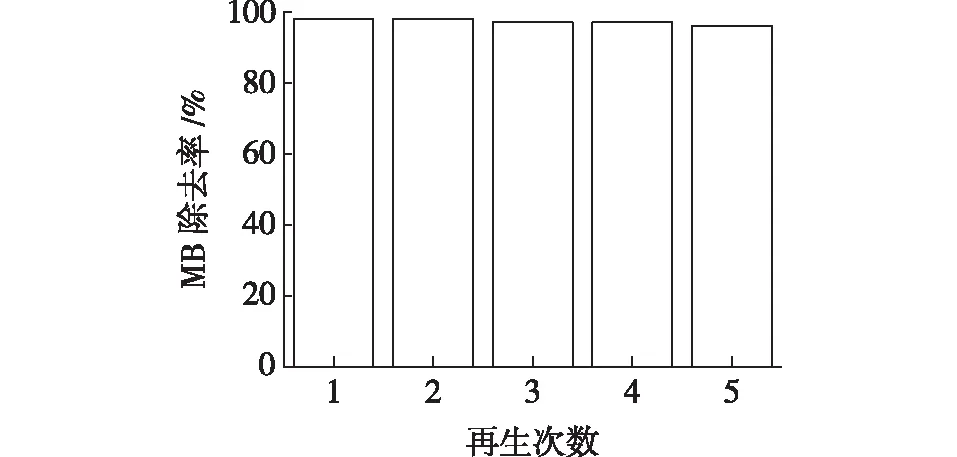
图10 经再生的PPMS循环使用次数对溶液中MB去除率的影响Fig.10 Effects of recycle times of regenerated PPMS on MB removal rate in solution
大多数吸附剂材料在去除MB后都缺乏与水分离的能力,而水凝胶在完成吸附过程后,通过简单的脱水即可与水分离,不需要通过如离心、沉降等其他方法与水分离。由2.2.3节可知,减小溶液的pH可降低丙烯酸基水凝胶材料对MB的吸附量。所以通过降低溶液的pH,可以提供更多的H+与已经吸附在水凝胶上的MB进行离子交换,可以促进脱附反应的进行,提高水凝胶的脱附效率。
3 结论
1)采用聚合致分相过程制备PPMS。研究了单体中AA用量对微球结构和对MB吸附的影响,随着AA用量的增加,微球的孔结构逐渐减少,当AA质量分数为单体的50%时,微球观察不到孔结构;当AA质量分数为单体的20%时,微球对MB吸附量最高。
2)用Langmuir吸附等温线模型很好地描述了微球的吸附过程,微球对MB的最大吸附量达到2.565 g/g,微球的吸附行为符合拟二阶动力学方程。
3)PPMS吸附后,在pH为2的50%甲醇溶液中,脱附后再吸附,再生的试样仍然保持高吸附能力,并且可以重复使用至少5个循环。
