乳清蛋白肽美拉德反应产物的优化制备及其抗氧化活性
2021-10-13蔡惠钿谢妍纯张逸
蔡惠钿,谢妍纯,张逸
(1.华南农业大学食品学院,广东 广州 510642;2.华农(潮州)食品研究院有限公司,广东 潮州 521000)
美拉德反应是氨基化合物与还原糖(羰基化合物)之间发生的非酶褐变反应,在该反应过程中无需任何催化剂,美拉德反应仅通过加热的方式就能自发进行[1-2]。随着反应的进行会产生一系列复杂的产物,如还原酮、类黑精、含氮、含硫等挥发性杂环化合物[3]。大量研究已经证实美拉德反应产物(Maillard reaction products,MRPs)中的反应初期产物具有较强的抗氧化活性,通常作为天然抗氧化剂加入到食品中,以提高食品的抗氧化活性[4]。蛋白质在水解酶作用下会产生抗氧化肽,抗氧化肽也可以与还原糖发生美拉德反应,所得产物的抗氧化活性显著增强[5]。近年来,研究表明MRPs能有效提高天然蛋白质、肽及氨基酸的抗氧化活性,同时具有天然抗氧化剂高效、低毒和无污染的优点[6]。林巍等[7]研究糖对紫花芸豆肽美拉德反应产物的抗氧化活性的影响,研究发现美拉德反应产物的抗氧化活性显著高于紫花芸豆肽。Vhangani等[8]研究水性核糖-赖氨酸和果糖-赖氨酸体系,发现水性核糖和果糖与赖氨酸发生美拉德反应所得产物的抗氧化活性均显著高于赖氨酸。Huang等[9]探究了葡萄糖-甘氨酸、葡萄糖-二甘氨酸和葡萄糖-三甘氨酸3种体系发生美拉德反应产物的抗氧化活性,结果发现MRPs对ABTS+自由基和DPPH自由基清除率以及铁还原力显著高于3种氨基酸,同时葡萄糖-二甘氨酸体系所得的MRPs抗氧化活性最强。闫芳等[10]研究了壳聚糖与赖氨酸发生美拉德反应,测定MRPs、壳聚糖和赖氨酸的抗氧化活性,研究发现MRPs抗氧化活性显著高于壳聚糖和赖氨酸,结果表明美拉德反应能显著提高物质的抗氧化活性。王文琼等[11]研究发现乳清蛋白与葡萄糖、乳糖、木糖、麦芽糖和果糖5种糖的复合产物都能有效清除DPPH自由基,同时具有较高的还原能力。张曦等[12]研究发现乳清蛋白-木糖发生美拉德反应,其产物包裹在核桃仁上能有效抑制核桃仁酸价的升高,但单独使用乳清蛋白膜对核桃仁酸价升高无显著的抑制作用。
目前,国内外研究主要集中在美拉德乳清蛋白复合物的制备及抗氧化活性等方面,而对于采用乳清蛋白水解物进行美拉德反应,研究乳清蛋白水解物与还原糖发生美拉德反应制备其产物及其抗氧化活性的报道较少。前期研究发现乳清蛋白在碱性蛋白水解酶的作用下,所得的水解物具有较强的抗氧化活性。以此为依据,本研究以乳清蛋白碱性蛋白酶水解物为原料与葡萄糖发生美拉德反应,制备乳清蛋白肽美拉德反应产物(whey protein peptides Maillard reaction products,WPP-MRPs),探究其制备工艺,同时探究不同浓度WPP-MRPs对ABTS+自由基和羟基自由基清除能力,为WPP-MRPs作为天然抗氧化剂在功能性食品中的应用提供依据。
1 材料与方法
1.1 材料与试剂
乳清蛋白:南京帕尔斯生物科技有限公司;碱性蛋白酶(200 000 U/g,分子质量约为27 300 D):上海金穗生物科技有限公司;ABTS:美国Sigma公司;铁氰化钾(分析纯)、三氯乙酸(分析纯)、氯化铁(分析纯):上海金锦乐实业有限公司;乙醇(分析纯):湖北威德利化学科技有限公司;水杨酸(分析纯)、过氧化氢(分析纯):上海源叶生物科技有限公司;过硫酸钾(分析纯)、乙酸钠(分析纯):温州市金海化学品市场有限公司;磷酸盐缓冲液(分析纯):上海盛思生化科技有限公司。
1.2 仪器与设备
U-T6紫外可见分光光度计:上海元析仪器有限公司;ZA120.4电子天平:上海赞维衡器有限公司;HHW420电热恒温水浴锅:济南欧莱博科学仪器有限公司;XD-52AA旋转蒸发仪:上海贤德实验仪器有限公司;KH20R-Ⅱ台式高速冷冻离心机:湖南凯达科学仪器有限公司;FD-2D-80压盖挂瓶型真空冷冻干燥机:上海继谱电子科技有限公司。
1.3 方法
1.3.1 WPP-MRPs的制备
参考Peng等[13]的方法,并稍作调整。准确称取2.0 g乳清蛋白,配制成质量浓度为5%的乳清蛋白溶液,将其在95℃恒温水浴锅中,保持5 min,随后加入质量浓度1 mol/L的NaOH溶液,将溶液pH值调至8.5,然后按照酶与底物1∶50(体积比)的比例加入碱性蛋白酶(200 000 U/g),在55℃恒温水浴锅中振荡水解,在水解过程中不断向溶液中加入质量浓度1 mol/L的NaOH溶液,使溶液pH值保持在8.5,持续水解3 h,最后煮沸5 min,使碱性蛋白酶失活。待水解结束后,向其中加入一定比例的还原糖,保持一定的温度,并不断搅拌,反应一段时间后,立即用冰水混合物迅速将其进行降温,终止反应,所得的样品置于离心机中,离心15 min,除去沉淀,将得到的上清液进行减压浓缩,最后置于真空冷冻干燥机中冻干,获得WPP-MRPs。
1.3.2 还原糖种类的筛选
选择葡萄糖、果糖、乳糖作为还原糖原料,分别加入到质量浓度为5%的乳清蛋白水解液中,确保3种糖的质量浓度为5%,溶液初始pH值为8.5,分别取10 mL的溶液于25 mL具塞玻璃管中,在80℃的恒温水浴中反应 0、1、2、3、4、5 h,取样后立即放入冰水浴中冷却,最终获得WPP-MRPs,在4℃冰箱中保存,用于测定其抗氧化活性(以还原力为考察指标),确定最佳的还原糖种类。
1.3.3 单因素试验
将WPP-MRPs作为研究对象,考察葡萄糖浓度、反应温度、反应时间和pH值对WPP-MRPs的抗氧化活性(以还原力为考察指标)的影响。在预试验的基础上,设定葡萄糖浓度5%、6%、7%、8%、9%5个水平;反应温度 50、60、70、80、90 ℃ 5 个水平;反应时间 1、2、3、4、5 h 5 个水平;pH 7.0、7.5、8.0、8.5、9.0 5 个水平。每组试验重复3次。
1.3.4 响应面法试验
在单因素试验的基础上,以葡萄糖浓度(X1)、反应温度(X2)、反应时间(X3)和 pH 值(X4)为自变量,以还原力(Y)为响应值。根据Box-Behnken试验设计,优化出制备WPP-MRPs的工艺。因素与水平设计如表1所示。

表1 试验设计因素与水平Table 1 Coded and actual value of factors and levels
采用响应面法(response surface methods,RSM)得到的二次回归模型,其模型如下。

式中:b0为截距回归系数;bi为线性回归系数;bii为二次效应回归系数;bij为交互项回归系数;Xi、Xj为自变量。
1.3.5 遗传算法设计
依据单因素试验结果,选取葡萄糖浓度、反应温度、反应时间和pH值4个因素为决策变量,如式(2)所示。



遗传算法优化的约束条件:选择各因素水平的上下限,WPP-MRPs的还原力最优的约束条件如式(5)所示。

1.3.6 WPP-MRPs的超滤分级纯化
利用中空纤维超滤膜将1.3.1中制备的WPP-MRPs混合物上清液(最优制备工艺下)进行超滤分级。当温度在20℃和压力在0.1 MPa条件下,将WPP-MRPs先后通过5 kDa和0.8 kDa的超滤膜进行截流分段,将分子量<0.8 kDa、0.8 kDa<分子量<5 kDa、分子量>5 kDa分别记为组分Ⅰ、组分Ⅱ和组分Ⅲ,将得到的3种组分首先利用旋转蒸发浓缩,然后利用真空冷冻干燥机将其冻干,备用。
1.3.7 抗氧化活性的测定
1.3.7.1 还原力的测定
参照Canabady-Rochelle等[14]的方法并略作改动。分别将WPP-MRPs和组分Ⅰ、Ⅱ、Ⅲ分别配制成质量浓度为 10、20、30、40、50、60、70 mg/mL 的样品溶液,分别从中取出0.5 mL置于20 mL具塞玻璃管中,然后分别加入2.5 mL磷酸盐缓冲液(0.2 mol/L)和2.5 mL铁氰化钾(1%)溶液,充分混合,将其置于50℃恒温水浴锅中保持20 min后,立即用冰水浴将其冷却,随后加入2.5 mL三氯乙酸(10%)溶液,然后以7 000 r/min离心15 min,取2.5 mL上清液,再加入2.5 mL蒸馏水和0.5 mL氯化铁(0.1%)溶液,充分混合,静置10 min,最后在700 nm波长处测定样品的吸光度。
1.3.7.2 ABTS+自由基清除能力的测定
参照Huang等[15]的方法并略作改动。分别将WPPMRPs和组分Ⅰ、Ⅱ、Ⅲ分别配制成质量浓度为10、20、30、40、50、60、70 mg/mL 的样品溶液。将质量浓度为7.0 mmol/L ABTS溶液与终浓度为2.45 mmol/L的过硫酸钾充分混合,在25℃条件下,避光静置12 h。利用pH值为4.5的乙酸钠溶液稀释至波长734 nm处的吸光度为0.7±0.02。取3 mL溶液与20 μL样品溶液混合,静置6 min,在波长734 nm处测定每个样品的吸光度,以不加样品液为对照,依据式(6)计算ABTS+自由基清除率。
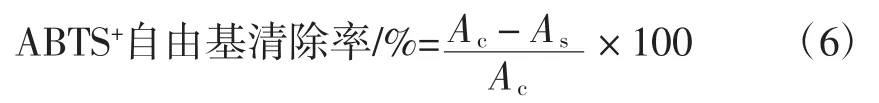
式中:Ac为对照品的吸光度;As为样品的吸光度。
1.3.7.3 羟基自由基清除能力的测定
参照Li等[16]的方法并略作改动。分别将WPP-MRPs和组分Ⅰ、Ⅱ、Ⅲ分别配制成质量浓度为10、20、30、40、50、60、70 mg/mL的样品溶液。分别取1 mL不同浓度的样品溶液于20 mL具塞玻璃瓶中,依次加入1 mL质量浓度为7.0 mmol/L的FeSO4溶液和1 mL质量浓度为6.0 mmol/L的H2O2溶液,混合均匀,静置10 min,然后再加入1 mL质量浓度为6.0 mmol/L的水杨酸溶液,充分混合,静置30 min后,在波长510 nm处测定每个样品的吸光度。以乙醇溶液代替待测液作空白,测定吸光度,以不加样品液为对照,依据式(7)计算羟基自由基清除率。
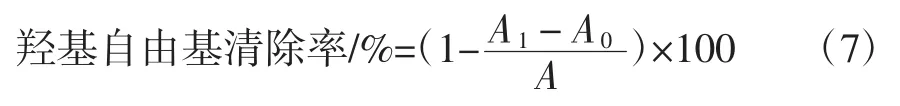
式中:A0为无水杨酸时样品液的吸光度;A1为对照品的吸光度;A为空白对照的吸光度。
1.4 数据处理
每组试验重复3次,结果用平均值±标准偏差;采用Statistics 8.0软件对试验数据进行显著性分析;采用Design-Expertver 8.0软件设计Box-Behnken组合试验;采用Matlab R2018b软件优化WPP-MRPs的制备工艺;采用Origin9.0软件进行作图。
2 结果与分析
2.1 还原糖种类的确定
还原法常用于判断物质是否具有抗氧化活性,其机理是待测物质如果能提供电子和质子氢,达到清除过量自由基的目的,从而表现出较好的抗氧化活性[17]。故本研究可利用该原理判断美拉德产物是否具有抗氧化活性,即还原能力越强,抗氧化活性越显著。本试验分别选取葡萄糖、乳糖、果糖与乳清蛋白肽进行美拉德反应,反应条件设定如下:反应温度80℃,还原糖浓度为7%,反应时间0~5 h,以WPP-MRPs还原力为指标,其结果如图1所示。
由图1可知,当反应时间在0~3 h内,随反应时间的延长,葡萄糖与乳清蛋白肽反应生成的WPP-MRPs的还原力显著增加(P<0.05),当反应时间超过3 h,随反应时间的延长WPP-MRPs还原力无显著变化(P>0.05)。当反应时间在0~5 h内,乳糖、果糖与乳清蛋白肽反应生成的WPP-MRPs的还原力随反应时间的延长而显著增加(P<0.05),呈时间依赖性。将葡萄糖、乳糖、果糖与乳清蛋白肽反应生成WPP-MRPs,对比产物的还原力,经对比发现,葡萄糖与乳清蛋白肽反应生成的WPP-MRPs的还原力显著高于乳糖、果糖与乳清蛋白肽反应生成WPP-MRPs。其原因是由于葡萄糖碳链较短,更易于蛋白质反应,从而改变蛋白质原有的生理特性[7]。Dong等[18]和Gu等[19]分别在研究葡萄糖与β-乳球蛋白和酷蛋白进行美拉德反应产物的还原能力也有类似的结果。

图1 还原糖种类对WPP-MRPs还原力的影响Fig.1 Effect of types of reducing sugar on reducing power of WPP-MRPs
2.2 单因素对WPP-MRPs还原力的影响
单因素对WPP-MRPs还原力的影响,其结果如图2所示。
由图2A可知,当葡萄糖浓度在5%~7%范围内,随葡萄糖浓度增加WPP-MRPs还原力显著增加(P<0.05)。其原因是随葡萄糖浓度增加,葡萄糖更易于乳清蛋白肽发生美拉德反应,生成WPP-MRPs还原力更强[20]。但当葡萄糖浓度超过7%时,继续增加葡萄糖浓度WPP-MRPs还原力无显著变化(P>0.05)。该研究结果与孙常雁等[21]探究乳清蛋白肽美拉德反应产物的抗氧化活性有相似的结果。综上,选择葡萄糖浓度范围为7%~9%进行后续的组合试验。


图2 不同试验因素对WPP-MRPs还原力的影响Fig.2 Effect of different experimental factors on the reductive power of WPP-MRPs
由图2B可知,当反应温度在50℃~80℃范围内,WPP-MRPs还原力随反应温度升高呈显著增加的趋势(P<0.05),反应温度在 80℃时,WPP-MRPs还原力取得最大值0.82±0.03。其原因是随反应温度的升高,促进美拉德反应,可在较短时间内生成更多的产物(还原酮和杂环化合物等),产物具有较强的抗氧化活性,进而提高WPP-MRPs还原力[10]。但当反应温度超过80℃时,WPP-MRPs还原力随反应温度升高而显著降低(P<0.05)。这归因于美拉德反应产物不稳定,在较高的温度下易分解,从而失去原有的抗氧化活性[22]。故反应温度选择70、80、90℃这3个水平进行后续组合试验。
由图2C可知,当反应时间在3 h内,随反应时间延长WPP-MRPs还原力显著增加(P<0.05),反应时间在3 h时,WPP-MRPs还原力取得最大值0.86±0.02。这是由于随反应时间延长,美拉德反应更加充分,美拉德反应中间产物经脱氢、缩合及分子重排最终形成类黑精以及挥发性的杂环化合物,从而使WPP-MRPs还原力显著增加[23]。但当反应时间超过3 h,继续延长反应时间,会导致产物分解,造成WPP-MRPs还原力降低。综上,反应时间选择2、3、4 h这3个水平进行后续组合试验。
由图2D可知,当pH值在7.0~8.5范围内,WPPMRPs还原力随pH值增加呈显著增加的趋势(P<0.05),pH值在8.5时,WPP-MRPs还原力取得最大值(0.87±0.04)。Lertittikul等[24]同样发现 pH 值低于 8.5时,随pH值增加美拉德反应越易进行,所得的产物抗氧化活性越强。当pH值过高,也不利于美拉德反应的进行,从而使得抗氧化活性降低。闫芳等[10]在探究壳寡糖-赖氨酸美拉德反应产物抗氧化特性时也有类似的结果。故pH值选择8.0、8.5、9.0这3个水平进行后续组合试验。
2.3 响应曲面法试验结果
2.3.1 模型建立与显著性检验
通过遗传算法优化WPP-MRPs制备工艺,所得的试验方案和结果见表2。

表2 响应曲面法试验设计及结果Table 2 Experimental design and results of response surface methodology

续表2 响应曲面法试验设计及结果Continue table 2 Experimental design and results of response surface methodology
以WPP-MRPs的还原力(Y)为响应值,对试验所得的数据进行多元回归拟合分析,得到WPP-MRPs的还原力对葡萄糖浓度(X1)、反应温度(X2)、反应时间(X3)和 pH 值(X4)的回归模型如式(8)所示。

对回归方程系数进行显著性检验,结果如表3所示。
由表3可知,数学模型决定系数R2=0.849 6,F=5.65,P<0.01,结果表明通过RSM建立的数学模型极显著。该模型失拟项P=0.086 4>0.05,表明模型失拟项不显著。通过以上数据分析表明通过RSM所建立的数学模型对试验数据拟合充分,可靠性较好。
利用F值大小可以判断试验因素对响应值的影响程度,F值越大,说明该因素对响应值的影响越显著。由表 3 知,F(X1)=15.50、F(X2)=5.90、F(X3)=0.21 和F(X4)=7.64,即各试验因素对 WPP-MRPs的还原力的影响顺序为葡萄糖浓度(X1)>pH值(X4)>反应温度(X2)>反应时间(X3),且葡萄糖浓度对 WPP-MRPs的还原力的影响达到极显著水平。

表3 WPP-MRPs制备工艺回归模型系数的显著性检验报告Table 3 Significance test report of regression model coefficients of WPP-MRPs preparation process
利用等高线图形来判断因素交互作用对响应值的影响程度是否显著。当等高线图形为椭圆时,代表因素交互作用显著影响响应值变化;当等高线图形为圆形时,代表因素交互作用对响应值变化无显著影响[25]。图3反映各试验因素交互作用对WPP-MRPs的还原力的影响。
由表3方差分析结果可知,X1X2、X1X3和X1X4的交互作用均对WPP-MRPs的还原力无显著影响(P>0.05),故在此不做分析。X2X3和X2X4的交互作用均能显著影响WPP-MRPs的还原力(P<0.05)。由图3A和3C可知,WPP-MRPs的还原力均存在极值点。图3B和3D的等高线图均呈椭圆型,表明X2X3和X2X4的交互作用显著影响WPP-MRPs的还原力。综上可知,对WPP-MRPs的还原力影响因素顺序为葡萄糖浓度(X1)>pH 值(X4)>反应温度(X2)>反应时间(X3),该结果也与方差分析的结果一致。
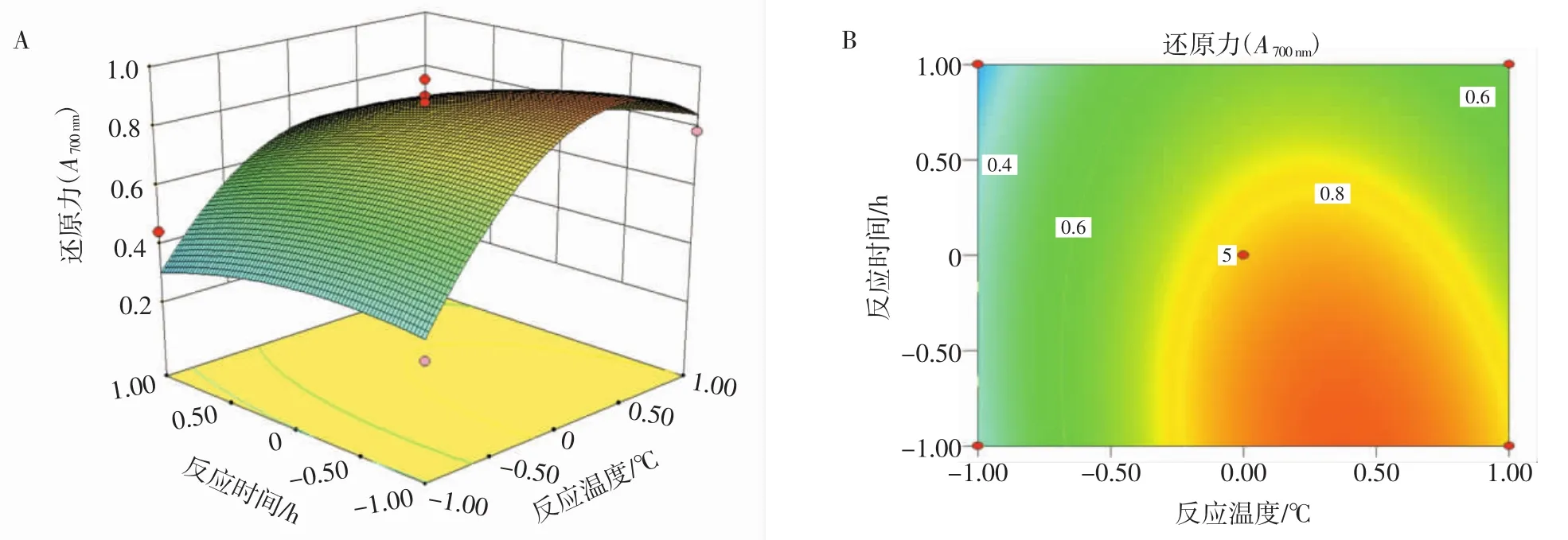

图3 各试验因素交互作用的响应面和等高线图Fig.3 Response surface and contour plots of interaction of experimental factors
2.3.2 WPP-MRPs制备的工艺参数优化
利用Matlab R2018b软件中的遗传算法优化工具箱进行分析优化,迭代128次,WPP-MRPs的还原力取得最大值,此时葡萄糖浓度(X1)、反应温度(X2)、反应时间(X3)和 pH 值(X4)水平编码分别为 0.296、1、1、1,即试验水平分别为8.296%、90℃、4 h和9.0,在此条件下,所得WPP-MRPs还原力理论值为0.97。遗传算法M文件运行结果如图4所示。
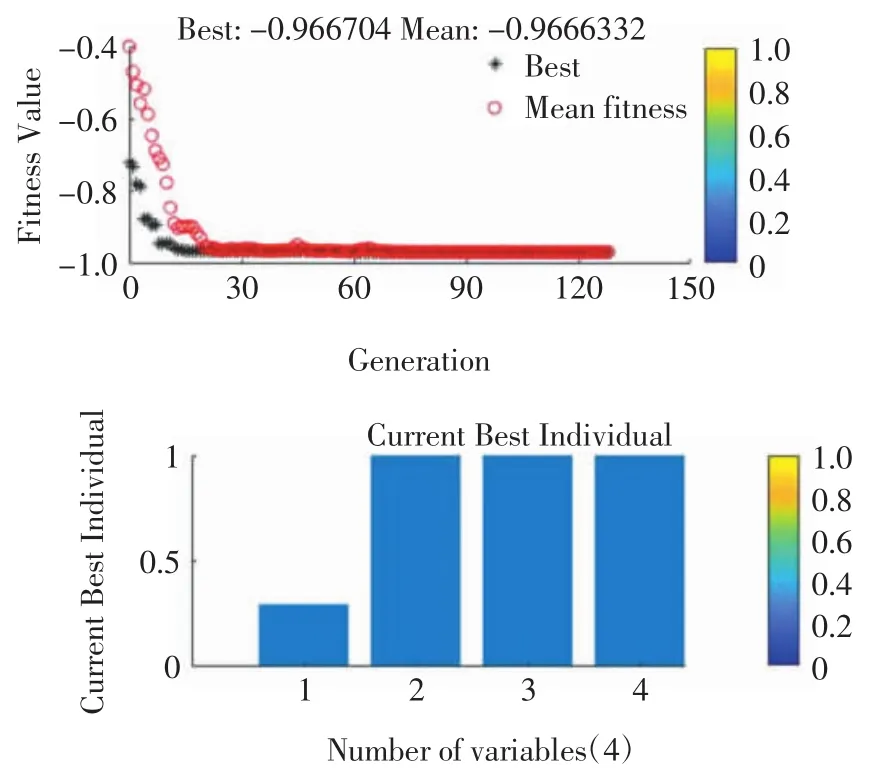
图4 遗传算法优化结果Fig.4 The results optimized by the genetic algorithm
2.3.3 试验验证
采用遗传算法优化WPP-MRPs的制备工艺参数为:葡萄糖浓度8.296%、反应温度90℃、反应时间4 h和pH9.0,WPP-MRPs的还原力的理论值0.97。为验证遗传算法的可靠性,结合实际情况,将上述工艺参数修正为葡萄糖浓度8.3%、反应温度90℃、反应时间4 h和pH9.0,在此条件下WPP-MRPs的还原力的试验值0.93±0.02,试验值和理论值的相对误差为4.36%。说明遗传算法可较好地模拟和预测WPP-MRPs的还原力,进一步证明采用遗传算法优化WPP-MRPs的制备工艺参数是可行的。
2.4 抗氧化结果
2.4.1 ABTS+自由基清除能力的结果分析
ABTS经过氧化剂氧化后生成性质稳定的蓝绿色ABTS+自由基,向ABTS+自由基加入抗氧化剂时,抗氧化剂与ABTS+自由基发生反应,会使蓝绿色褪色或消失[26]。抗氧化剂的抗氧化活性越强,提供电子的能力越强,ABTS+自由基清除能力越强。因此,通过测定反应液吸光度的变化,可以反映样品的抗氧化能力的强弱。WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ对ABTS+自由基清除能力结果如图5所示。
由图5可知,随WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ质量浓度的增加ABTS+自由基清除率显著增加(P<0.05),呈浓度依赖性。对数据进行回归分析可知WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ对ABTS+自由基清除率的IC50分别为(47.15 ±0.83)、(56.86 ±1.15)、(39.92 ±0.72)、(57.37 ±1.11)mg/mL。IC50越小,说明物质的抗氧化活性越强,对比WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ的IC50值可知,组分Ⅱ抗氧化活性最强,组分Ⅰ和组Ⅲ无显著差异。Nienaber等[27]研究发现美拉德反应产物中中低分子量的产物抗氧化活性最强。该结果与本试验结果一致。结果表明WPP-MRPs具有较强的抗氧化能力,可作为理想的抗氧化剂用于功能性食品中。

图5 WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ对ABTS+自由基清除能力的影响Fig.5 Effect of WPP-MRPs,components I,II and III on ABTS+radical scavenging capacity
2.4.2 羟基自由基清除能力的结果分析
羟基自由基属于活性较强的自由基,几乎可以与细胞内的所有有机物发生反应,造成DNA和细胞膜损伤、多糖解聚和不饱和脂肪酸发生过氧化、多种酶失活等变化,进而损伤细胞和机体的生理功能[28]。因此,羟基自由基的清除能力作为抗氧化活性评价中最主要的指标。WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ对羟基自由基清除能力结果如图6所示。

图6 WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ对羟基自由基清除能力的影响Fig.6 Effect of WPP-MRPs,components I,II and III on hydroxyl radical scavenging capacity
由图6可知,羟基自由基清除率随WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ质量浓度的增加而显著增加(P<0.05),且呈浓度依赖性。其原因是WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ中碳链上的氢原子能与羟基自由基发生反应生成水,而碳链上的碳原子具有电子可氧化羟基自由基使其分解,从而直接清除羟基自由基[20]。对数据进行回归分析可知WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ对羟基自由基清除率的 IC50分别为(44.28±0.95)、(53.72±1.04)、(37.64±0.54)、(58.59±1.36)mg/mL。对比 WPP-MRPs、组分Ⅰ、Ⅱ、Ⅲ的IC50值可知,四者对羟基自由基清除能力的顺序为组分Ⅱ>WPP-MRPs>组分Ⅰ>组分Ⅲ。该研究结果与孙常雁等[21]研究乳清蛋白肽美拉德产物的抗氧化性结果一致。进一步表明WPP-MRPs具有较强的抗氧化能力。
3 结论
本研究通过遗传算法优化WPP-MRPs制备工艺,得到最优工艺参数为:葡萄糖浓度8.3%、反应温度90℃、反应时间4 h和pH9.0,在此条件下WPP-MRPs的还原力为0.93±0.02。在最优工艺条件下制备的WPPMRPs对ABTS+自由基和羟基自由基清除率的IC50分别为(47.15±0.83)、(44.28±0.95)mg/mL。研究结果说明WPP-MRPs作为食品原料在功能性食品领域中应用具有广阔的市场前景。
