纳米氧化锌/葡萄皮红改性大豆分离蛋白膜的制备与性能研究
2021-10-12冉锐敏王璐瑶何宾宾何淑蹇吴钰楼余惠容陈赛艳冀俊杰
冉锐敏,王璐瑶,何宾宾,何淑蹇,徐 鸥,吴钰楼,余惠容,陈赛艳※,冀俊杰
(1.四川农业大学食品学院,雅安 625014;2.山东技师学院,济南 250200)
0 引 言
石油基包装材料因其在成本和可用性方面的优势而被广泛应用,但因其不可降解性对环境造成的污染、资源消耗也不可忽视。随着人们环保意识的增强及对食品安全的日益重视,人们迫切需要寻找塑料包装的代替品。大豆分离蛋白(Soybean Protein Isolate,SPI)作为三大生物基物质(多糖、蛋白质和脂类),具有来源广、无毒、价格低廉、生物相容性好、生物可降解性强以及成膜性能优良等特点[1],用于食品包装工业中,可以减少石油基包装材料引发的“白色污染”,同时提高农副产品的应用价值。相对于多糖和脂类而言,所制备的薄膜具有优异的氧气和油阻隔性[2-3],但是SPI富含氨基、羟基、羧基和硫醇基等亲水性基团,成膜后表面易吸水,导致包装内环境湿度高,被包装食品货架期缩短,且成膜的机械性能和热稳定性能较差[3-5],限制了其在食品工业中的应用,因此需要采取一定的手段来改善薄膜性能。
目前有学者对大豆分离蛋白膜进行改性研究,如通过添加硬脂酸来提高大豆分离蛋白膜的耐水性能[4],添加甘草渣提高大豆分离蛋白膜的机械性能[2],添加京尼平提高大豆分离蛋白膜耐水和机械性能[6],但改性多集中在大豆分离蛋白膜的机械和耐水性能,对同时改善机械性、耐水性、耐热性和功能性的研究较少。纳米氧化锌(ZnO NPs,ZnO Nanoparticles)作为一种高功能精细无机产品,具有无毒,比表面积大及较强的防紫外线、抗菌性能和热稳定性[7-8],添加到聚合物中能改善薄膜的机械性、耐水性和耐热性[9],同时赋予薄膜抑菌活性,且 ZnO NPs被美国食品和药物管理局(21 CFR182.8991)视为安全材料,在人体内可消化降解[10],因此在食品包装行业颇具吸引力。但纳米氧化锌的高能性、不饱和性、不稳定性易导致薄膜表面粗糙[11],影响表观性能,消费者不易接受,故需要加入一定的辅助剂,促进ZnO NPs在SPI膜基质中融合。甘油作为常用的辅助剂,可通过增加膜成分的流动性促进其融合,但过量的甘油易导致薄膜机械强度较差[1,3,12],因此亟需新的辅助剂来改善其性能。葡萄皮作为葡萄工业尚未充分利用的废弃物,含大量葡萄皮红色素(Grape-Skin Red,GSR),作为天然花色苷类色素,具有典型的C6-C3-C6碳骨架结构,含苯甲酰环和含氧六元杂环,且含氧六元杂环上带有阳离子,具有2-苯基-苯并吡喃阳离子的典型结构[13],能在一定程度上提高 SPI膜的机械强度,同时具有提高薄膜结构均一性和表面光滑性的作用[14-16],且葡萄皮红具有极强的抗氧化活性,可增加薄膜的功能特性[17]。故本研究选用葡萄皮红作为辅助剂,赋予薄膜较好的物理化学性能,同时为提高葡萄皮废弃物利用率提供新思路。
本研究以大豆分离蛋白为成膜基材,添加纳米氧化锌和葡萄皮红改善大豆分离蛋白膜的微观结构、机械性能、阻隔性能、热稳定性和抗菌性能,以期提高复合膜的综合包装性能,为后期应用提供数据参考和科学指导。
1 材料与方法
1.1 材料与试剂
大豆分离蛋白,食品级:哈尔滨高科技大豆食品有限公司;亚硫酸钠、甘油、氢氧化钠,分析纯:成都市科隆化学品有限公司;纳米氧化锌(平均粒径20 nm):北京德科岛金科技有限公司;葡萄皮红,食品级:济南鲁源生物科技有限公司。
1.2 仪器与设备
FJ200-SH数显恒速高速分散均质机(上海垒固仪器有限公司);HD-B609B-S智能电子拉力试验机(海达国际仪器有限公司);Nicolet 6700傅里叶变换红外光谱仪(赛默飞世尔科技公司);JSM-7500F扫描电子显微镜(中国富瑞宝国际有限公司);Rise-2006型He-Ne激光粒度分析仪(济南润之科技有限公司);DSC差示扫描量热仪(耐驰科学仪器商贸上海有限公司)。
1.3 复合膜的制备
根据前期的试验基础和文献[18],葡萄皮红、ZnO NPs和大豆分离蛋白以1∶2∶25的质量比制备复合膜。在含7 g大豆分离蛋白的水溶液中(80 mL)加入3 g的增塑剂甘油,在温度为(25±1)℃,转速为1 000 r/min条件下磁力搅拌 20 min。待系统混合均匀后在 80 ℃下水浴 30 min,冷却至(25±1)℃,制得SPI与甘油的混合液,将混合液在9 000 r/min转速下均质10 min,再于真空度为-0.095 MPa下脱气 2 h,加入 0.01 g还原剂亚硫酸钠(Na2SO3),蒸馏水定容到100 mL,制得SPI成膜液。复合膜的制备工艺流程如图1所示。
在80 mL蒸馏水中加入0.56 g ZnO NPs,360 W超声1 h,加入 7 g大豆分离蛋白粉和 3 g甘油,在温度为(25±1) ℃,转速为1 000 r/min条件下磁力搅拌20 min。待系统混合均匀后在 80 ℃下水浴 30 min,冷却至(25±1) ℃,制得SPI与ZnO NPs/甘油的混合液,将混合液在 9 000 r/min转速下均质 10 min,再于真空度为-0.095 MPa下脱气2 h,加入0.01 g Na2SO3,蒸馏水定容到100 mL,制得SPI/ZnO NPs成膜液。
在上述SPI/ZnO NPs/甘油混合液中加入0.28 g葡萄皮红色素。在9 000 r/min转速下均质10 min,再于真空度为-0.095 MPa下脱气2 h,加入0.01 g Na2SO3,蒸馏水定容到100 mL,制得SPI/ZnO NPs/GSR成膜液。
用1 mol/L的氢氧化钠将SPI成膜液、SPI/ZnO NPs成膜液、SPI/ZnO NPs/GSR成膜液pH值调节至10±0.5,取90 mL成膜液流延至有机玻璃板上,在40~50 ℃下干燥 10~12 h,揭膜,置于温度为(25±1)℃、相对湿度为55%±1%的环境中回湿24 h,待测。
1.4 复合膜性能表征与测定
微观结构测定:将样品裁成20 mm×20 mm的试样,在60 ℃干燥24 h,用液氮将复合膜冷冻断裂,真空溅射喷金,通过扫描电子显微镜(SEM,Scanning Electron Microscopy)观察复合膜的横截面(放大500倍)及表面(放大3 000倍),加速电压为5~15 kV[19]。
傅里叶变换红外光谱测定:将复合膜在60 ℃干燥24 h,使用傅里叶变换衰减全反射红外光谱(ATR-FTIR,Total Reflectance Fourier Transform Infrared Spectroscopy)测定干燥后复合膜的红外光谱,扫描范围650~4 000 cm-1,光谱分辨率4 cm-1,扫描次数 32次[20]。
厚度测定:参照《GB/T 6672—2001》[21]方法测定复合膜的厚度。
机械性能测定:参照《GB/T 1040.3—2006》[22]的方法测试复合膜的抗拉伸强度(TS,Tensile Strength)和断裂伸长率(EB,Elongation at Break)。
水蒸气透过系数测定:参照《GB/T 30412—2013》[23]的方法测试复合膜的水蒸气透过系数(WVP,Water Vapor Permeability)。
含水率测定:根据董宇豪等[24]的方法,将膜裁剪成20 mm×20 mm,称量(W1,g)后放入105 ℃的烘箱烘干24 h,取出后称量(W2,g)。每种类型的膜测量3次,使用以下公式计算复合膜的含水率(MC,Moisture Content)
差示扫描量热法(DSC,Dynamic Stability Control)测定:根据许安等[25]的方法做少量修改。在氮气环境下,以10 ℃/min的速率从20 ℃升温至250 ℃,并记录相关数据。
粒径大小及Zeta电位测定:将膜液用去离子水稀释100倍,使用激光粒度分析仪以 90°的固定散射角和(25±0.1)℃的温度测定复合膜液的粒径及Zeta电位[26]。
抑菌性能测定:采用抑菌圈法,测定复合膜的抑菌活性(金黄色葡萄球菌和大肠杆菌)。
1.5 数据统计与分析
采用Microsoft Excel和SPSS 26.0进行基本数据处理,采用Origin 2017软件制图和拟合数据。
2 结果与分析
2.1 复合膜的傅里叶变换红外光谱分析
复合膜的红外光谱如图2所示。对于大豆分离蛋白膜,1 038 cm-1是C-O的伸缩振动峰[27],1 234 cm-1是C-N和N-H的伸缩振动峰[6],1 538、1 624 cm-1分别是N-H(酰胺II)的弯曲振动和 C=O(酰胺I)的伸缩振动峰[4],2 875、2 930 cm-1处的峰是聚合物基质中C-H键的拉伸振动峰,在3 100~3 500 cm-1处有一个宽的吸收带,这归因于O-H拉伸振动和 N-H弯曲振动[2],随着纳米氧化锌和葡萄皮红的添加,3 272、1 538 cm-1处的波峰向低波数偏移,这是由于大豆分离蛋白与纳米氧化锌及葡萄皮红之间所产生的氢键作用[28]。而3 272 cm-1处的峰值强度降低,这是因为大豆分离蛋白在碱性条件下所产生的阴离子与葡萄皮红花色苷的阳离子产生偶极-偶极相互作用,致使大豆分离蛋白O-H拉伸振动减弱[29]。以上结果表明,纳米氧化锌和葡萄皮红已成功分散在大豆分离蛋白膜中,并通过氢键和静电吸附与大豆分离蛋白分子发生相互作用。
2.2 复合膜的厚度和机械性能分析
薄膜厚度主要受成膜面积、膜液浓度、膜液溶质中分子结构及成膜过程中的相互作用影响[30]。本研究中成膜面积是恒定的,复合膜的厚度在125.67~157.33μm范围内,SPI/ZnO NPs膜最厚(157.33μm)。葡萄皮红的添加促进了ZnO纳米颗粒在SPI基质中的融合,膜均匀性提高,如表1所示,SPI膜厚度(125.67μm)相对于SPI/ZnO NPs/GSR膜降低(135.00μm)。薄膜的机械性能受成膜组分的性质和化学结构以及分子之间内聚力的影响,复合膜的机械性能如表1所示。SPI膜的拉伸强度(TS,Tensile strength)为1.37 MPa,断裂伸长率(EAB ,Elongation At Break)为135.89%,拉伸强度低于已报道的SPI膜[2,4],这归因于成膜组分性质的差异。本研究SPI溶液具有较低的粒径(352.03 nm),比王艳红等[31]的研究低了60%左右(SPI溶液粒径:890 nm),粒径较小时,在成膜过程中 SPI易产生黏连,影响致密网络结构的形成,膜抗应变力降低。当加入ZnO NPS,拉伸强度显著增加至2.74 MPa(P<0.05),这与Wu等[32]的研究结果相似,在其研究中纳米粒子可作为聚合物基质中的机械增强剂,限制聚合物的柔韧性和分段迁移性,提高薄膜的刚性,相对于SPI膜(TS:1.68 MPa,EAB:133.6%),SPI/ZnO NPs复合膜 TS和EAB分别增加至2.24 MPa和171.7%。在本研究中,ZnO NPS与SPI之间的氢键以及带正电的葡萄皮红分子与带负电的大豆分离蛋白分子之间的静电作用减少了聚合物链之间的自由体积,并形成了高密度和低渗透性的聚合物网络[33],使得 SPI/ZnO NPs/GSR膜呈现更高的TS(3.28 MPa),相对于SPI膜上升了139%。SPI/ZnO NPs/GSR膜的EAB(113.29%)优于其他含葡萄皮红的膜,如塔拉胶/纳米纤维素晶体/葡萄皮红膜(54.80%)[34],ĸ-卡拉胶/葡萄皮红膜(19.65%)[35],这归因于GSR与SPI/ZnO NPs膜基质良好的相容性,在研发具有一定延展性包装膜时极具潜力。
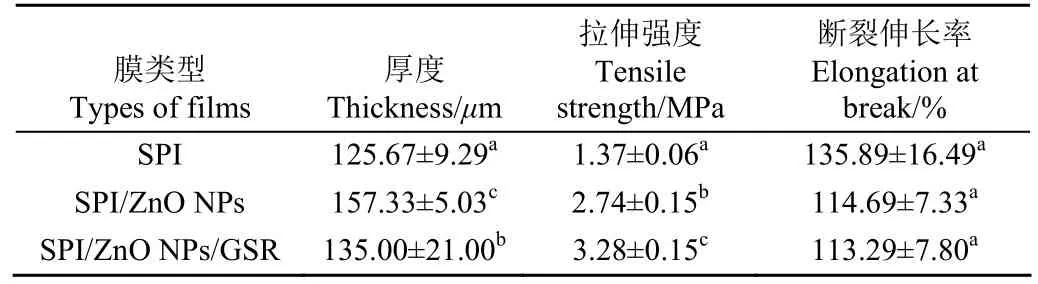
表1 复合膜的厚度和机械性能Table 1 Thickness and mechanical properties of composite films
2.3 复合膜的耐水性能分析
复合膜的耐水性能如表2所示。添加ZnO NPs后,SPI膜的含水率从34.41%降低至28.91%,SPI与ZnO NPs之间相互作用增强,限制了蛋白质分子与水分子间的相互作用,从而降低了膜的吸水能力[33],添加 GSR后,复合膜的含水率降至25.37%,相对于SPI膜降低了26%,这与Jancikova等[36],Qin等[37]研究花青素类薄膜时的结果相反。这可能是由于GSR和SPI的强相互作用抵消了GSR亲水性的影响,低含水率对薄膜在生产、储存和加工过程中保持膜的完整性是有利的,且此时耐热性能较佳。同样的原理也适用于水蒸气透过系数(WVP,Water Vapor Permeability),生物聚合物之间相互作用所形成的致密空间网络结构,导致水蒸气分子穿过复合膜的路径更加曲折[38],WVP降低。由表2可知,SPI膜的WVP为5.57×10-12(g·cm)/(cm2·s·Pa),加入 ZnO NPs,纳米颗粒易渗入聚合物网络中的一些孔隙,阻碍水蒸气分子的渗透[39],导致水蒸气透过率降低。GSR的添加虽使复合膜WVP值上升,但相对于SPI膜,WVP值下降了15%左右,在研发SPI基保鲜包装膜时展现出极大的优势和潜力。
2.4 复合膜的扫描电镜分析
利用扫描电镜观察复合膜的微观结构。由图3可知,SPI膜具有光滑、均匀的表面和横截面结构,表明大豆分离蛋白成膜性良好。加入ZnO NPs后,复合膜内部出现少量颗粒和团聚的现象,但无裂痕,这可能是由ZnO NPs粒子表面的高能性、不饱和性、不稳定性引起[11]。Wu等[32]在制备SPI/ZnO NPs/肉桂醛复合膜时,发现了相似的趋势,ZnO NPs在SPI膜基质中随机分散,复合膜呈现粗糙的表面结构。但是与SPI/ZnO NPs膜相比,SPI/ZnO NPs/GSR膜的白色颗粒明显减少,说明葡萄皮红的存在可促进ZnO纳米颗粒在SPI基质中的融合,提高薄膜的均匀性和致密性,同时改善薄膜的机械性能和阻隔性能,这与表1和表2中的结果一致,均匀、致密的微观结构有利于提高消费者的接受力,便于后期在食品包装中的应用。

表2 复合膜的含水量和水蒸气透过率Table 2 Moisture content and water vapor permeability of composite films
2.5 复合膜的热重分析
由于包装材料在食品的生产、储存和加工过程中经常被加热,因此薄膜的热性能是影响其应用的重要因素。本研究通过差式扫描量热法(DSC)分析了复合膜的热稳定性,结果如图4所示。SPI膜在194 ℃处出现吸热峰,SPI膜发生熔融;相对于SPI膜,SPI/ZnO NPs复合膜显示出更高的熔点(215 ℃),这是因为ZnO NPs自身较高的热稳定性和ZnO NPs与SPI分子间的相互作用导致的较低聚合物链运动,使其热量渗透到内部结构的速率较低,故SPI/ZnO NPs膜的耐热性更佳[40],同时SPI与ZnO NPs/SPI复合膜的之间的相互作用(氢键)也可以提高复合膜的热稳定性。SPI/ZnO NPs/GSR膜出现两个熔融峰,第一个峰在160 ℃左右,可能是葡萄皮红的分解,第二个在231 ℃,此时膜内的聚合物网络结构发生熔融。熔点相对于SPI膜上升了19%。复合膜稳定性与含水量呈相反趋势(表2),这与Saitta等[41]的研究结果一致,水可作为增塑剂,促进大豆分离蛋白链的流动,影响蛋白质的结构和稳定性,含水率越低,热稳定性越好。
2.6 复合膜粒径及Zeta电位分析
在pH值10时,测定复合膜液的粒径和Zeta电位,结果表3所示。所有膜液的PDI值较小(<0.3),溶液中粒子分布均匀。SPI膜液的粒径为352.03 nm,添加ZnO NPs后,粒径降低。加入葡萄皮红后,膜液粒径并无显著变化,说明葡萄皮红与SPI/ZnO NPs具有良好的相容性,如图3所示。
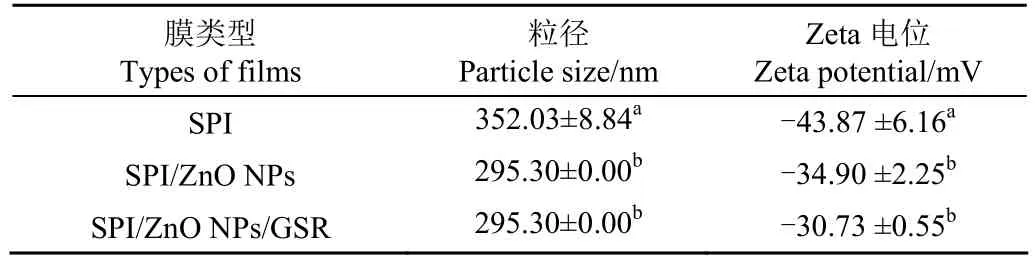
表3 复合膜的粒径和Zeta电位Table 3 Particle size and Zeta potential of composite films
SPI膜的Zeta电位值为-43.87 mV,复合膜的电位值在-30.73~-34.90 mV范围内。成膜溶液的负电荷是由聚合物基质引起的,随着ZnO NPs和葡萄皮红的添加,电荷值(绝对值)降低,说明ZnO NPs和葡萄皮红已成功掺入大豆分离蛋白膜的网络结构中,ZnO NPs、葡萄皮红通过交联作用固定在蛋白质分子内部或吸附在表面,使蛋白质二级、三级结构发生变化,从而改变 SPI的电荷分布情况[42]。一般来说,Zeta电位绝对值在30以上,成膜溶液的稳定性好[43]。
2.7 抑菌效果分析
采用抑菌圈法测定复合膜的抑菌效果,通过抑菌圈直径大小反映复合膜的抑菌性能。由图5可知,SPI膜对大肠杆菌和金黄色葡萄球菌均无抑菌活性,加入ZnO NPs后,对两种目标细菌均表现出抑菌活性,抑菌圈直径显著增加(P<0.05),且该膜对金黄色葡萄球菌的抑制作用强于对大肠杆菌,这与 Shahvalizadeh等[9]的研究结果一致。ZnO NPs与SPI基质融合之后,薄膜基质中释放的Zn2+能有效抑制细菌生长,而且纳米氧化锌颗粒表面能产生过氧化氢,具有强氧化作用,能影响细菌代谢[44]。通常,革兰氏阳性菌(金黄色葡萄球菌)相对于革兰氏阴性菌(大肠杆菌)会多一层脂蛋白层和脂多糖层,一定程度上限制其与抑菌物质的结合,所以复合膜对黄色葡萄球菌的抑制作用更强。加入葡萄皮红后,抑菌效果更显著(P<0.05),这得益于葡萄皮红中的花色苷含有能破坏蛋白质二级结构的游离酚羟基,当花色苷与活性蛋白质分子作用后,破坏细胞膜,引起细胞质缩水和解体,干扰细胞的正常代谢作用,赋予复合膜一定的抑菌效果[45]。以上结果表明,ZnO NPs/GSR作为活性物质加入食品包装膜中,具有作为抑菌膜的应用潜力,能同时抑制大肠杆菌和金黄色葡萄球菌的生长。
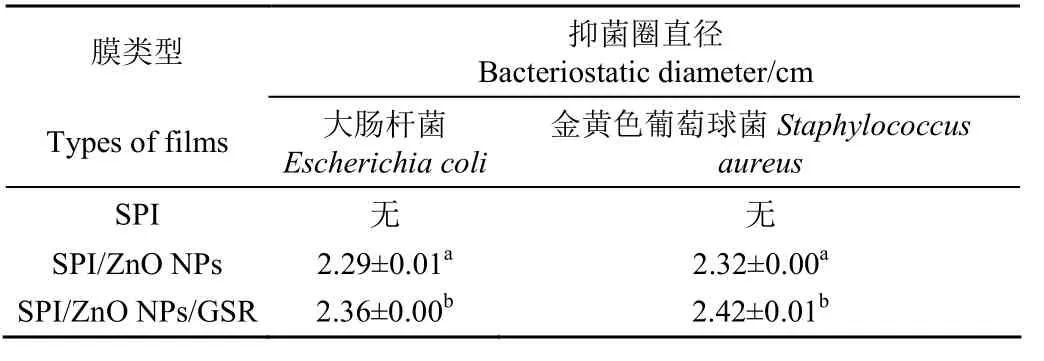
表4 复合膜的抑菌圈直径Table 4 Bacteriostatic diameter of composite films
3 结 论
1)ZnO NPs和葡萄皮红与SPI膜基质通过氢键和静电相互作用交联,改善了大豆分离蛋白膜的综合包装性能,扩大了其应用范围。
2)相比较于SPI膜,SPI/ZnO NPs/GSR膜具有增强的机械、热稳定和耐水性能,拉伸强度上升了139%,熔点上升了19%,含水率降低了 26%,水蒸气透过系数降低了15%。
3)葡萄皮红的加入促进了ZnO NPs在SPI膜基质中的融合,复合膜呈现出更致密、均匀的微观结构。
4)ZnO NPs和葡萄皮红赋予复合膜优异的抑菌活性,能有效抑制大肠杆菌和金黄色葡萄球菌的生长,抑菌圈直径随着活性成分的添加呈上升趋势,在活性包装中显示出巨大的应用潜力。
