血浆治疗儿童原发性肾病综合征重度水肿的临床疗效
2021-09-28赵成广傅桐侯玲王秀丽杜悦
赵成广,傅桐,侯玲,王秀丽,杜悦
(中国医科大学附属盛京医院小儿肾脏风湿免疫内科,沈阳 110004)
儿童原发性肾病综合征(primary nephrotic syndrome,PNS)是儿童时期常见的肾小球疾病之一,部分患儿在PNS初发或复发时可出现重度水肿,表现为胸腔积液、腹腔积液、外阴严重水肿等,影响患儿正常活动,降低睡眠质量,可引起消化功能紊乱、呼吸困难、肺部感染等,处理不当可危及生命[1]。因此,对PNS患儿重度水肿需采取及时有效的治疗以减轻水肿、改善肾脏功能。目前,对PNS重度水肿患儿通常在给予输注人血白蛋白、血浆及其他提升胶体渗透压的药物(如低分子右旋糖酐[2])等治疗后,利用呋塞米利尿,重症者可采取单纯超滤脱水,以缓解重度水肿。但在PNS重度水肿患儿的治疗中,关于白蛋白、低分子右旋糖酐、血浆这3种可以提升胶体渗透压的物质是否有差别,目前尚无报道,且哪种物质对PNS重度水肿患儿的治疗更为合适(即疗效良好、不良反应相对小)亦无确切结论。本研究回顾性分析了近3年中国医科大学附属盛京医院小儿肾脏风湿免疫内科病房收治的PNS重度水肿患儿的临床资料,比较了血浆、低分子右旋糖酐和白蛋白治疗前后的各项指标,探讨哪种治疗更有利于减轻水肿、缓解病情。
1 材料与方法
1.1 一般资料
本研究为单中心回顾性临床对照研究,选择2017年1月至2019年12月在中国医科大学附属盛京医院小儿肾脏风湿免疫内科病房住院的符合临床诊断标准的PNS重度水肿患儿。排除既往诊断慢性肾脏病(包括透析、肾移植)的患儿。
共纳入PNS重度水肿患儿60例,按治疗方法不同,分为低分子右旋糖酐治疗组(n=15)、白蛋白治疗组(n=20)、血浆治疗组(n=25)。在60例患儿中,PNS重度水肿并发急性肾损伤(acute kidney injury,AKI)35例,其中,白蛋白治疗组15例,血浆治疗组20例。在白蛋白治疗组20例患儿中,PNS重度水肿应用白蛋白后并发AKI 12例,在给予呋塞米及糖皮质激素等治疗基础上,单纯输注血浆治疗患儿5例,血浆联合甘露醇治疗患儿7例。治疗前各组患儿性别、年龄、体质量、尿蛋白定量、血白蛋白、24 h尿量、血肌酐(serum creatinine,Scr)均无统计学差异,具有可比性。
1.2 临床诊断标准
PNS诊断标准[3]:(1)大量蛋白尿,即24 h尿蛋白定量≥50 mg/kg,或晨尿蛋白/肌酐≥2.0,1周内3次晨尿蛋白定性(+++)~(++++);(2)低蛋白血症(血清白蛋白<25 g/L);(3)不同程度的水肿;(4)高脂血症(血清胆固醇> 5.7 mmol/L)。其中,(1)和(2)为诊断必需项,并排除继发因素所致的肾病综合征。
AKI诊断标准[4]:48 h内Scr升高≥26.5 μmol/L,或较原Scr值增长≥50%和(或)尿量<0.5 mL/(kg·h)达6 h。
重度水肿:在原发病基础上,出现全身严重水肿,伴有胸腔积液、腹腔积液、外阴严重水肿。
1.3 治疗方法
3组患儿在提高胶体渗透压治疗的基础上,均加用利尿剂(呋塞米1 mg/kg,1次/12 h,静脉注射),糖皮质激素(醋酸泼尼松1.5~2 mg·kg-1·d-1,3次/d,口服),同时口服补钙、维生素D。所有患儿均给予对症处理,保持水电解质平衡。
低分子右旋糖酐治疗组:低分子右旋糖酐5~10 mL·kg-1·d-1,缓慢持续静脉滴注,直至水肿明显消退。白蛋白治疗组:人血白蛋白10 g/d,隔日1次,静脉输注,共2次。血浆治疗组:滤白病毒灭活冰冻血浆5~10 mL·kg-1·d-1,隔日1次,静脉输注,共2次;7例PNS重度水肿应用白蛋白后并发AKI患儿给予血浆联合甘露醇治疗,20%甘露醇2.5~3 mL·kg-1·d-1,1次/d,静脉注射,连续3~5 d。
1.4 观察指标
观察各组治疗第3、7、10天后的尿量、体质量变化,记录治疗第7天的Scr变化。
1.5 统计学分析
采用SPSS 13.0软件进行统计分析。计量资料采用表示,用t检验进行比较。计数资料采用χ2检验比较。P< 0.05为差异有统计学意义。
2 结果
2.1 3组PNS重度水肿患儿疗效的比较
如表1所示,治疗前3组患儿性别、年龄、体质量、24 h尿量、尿蛋白定量、血白蛋白、Scr比较无统计学差异。
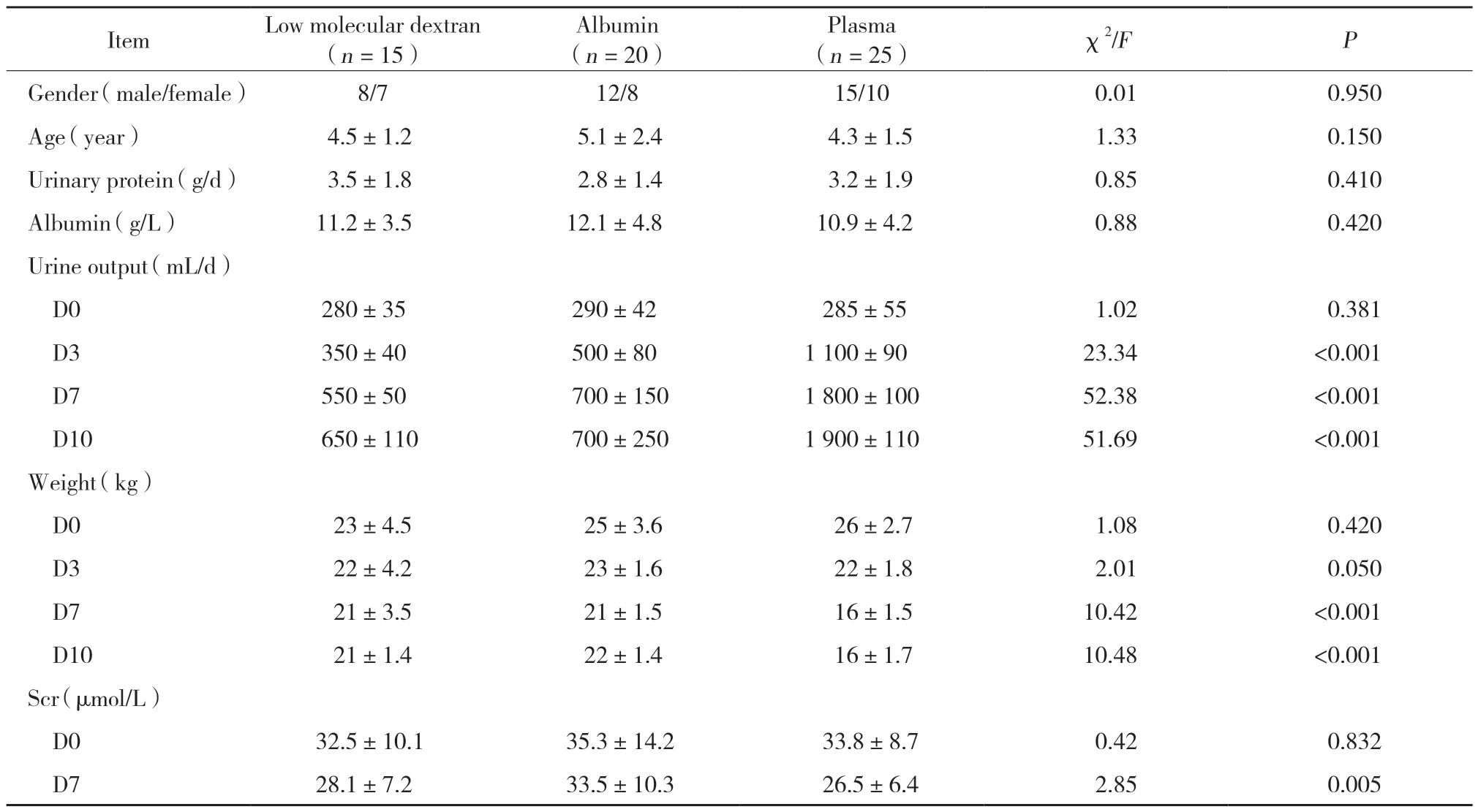
表1 60例PNS重度水肿患儿应用低分子右粒糖酐、白蛋白、血浆治疗效果的比较Tab.1 Comparison of therapeutic effects for low molecular dextran,albumin and plasma in 60 children with severe edema of PNS
治疗后3组患儿的尿量均较治疗前增多,体质量及Scr均较前降低。血浆治疗组患儿的尿量在血浆治疗第3、7和10天明显多于其他2组,体质量在血浆治疗第7和10天较其他2组明显下降,差异有统计学意义(均P< 0.001)。肾功能改善方面,血浆治疗组患儿Scr在治疗第7天较其他2组降低更为显著(P=0.005),提示疗效优于其他2组。因此,血浆治疗组患儿较其他2组在治疗后尿量增加、体质量及Scr降低明显,提示血浆治疗在减轻水肿、改善肾功能方面优于白蛋白和低分子右旋糖酐。
2.2 PNS重度水肿并发AKI患儿应用白蛋白与血浆治疗效果的比较
60例PNS重度水肿患儿中,有35例并发AKI。如表2所示,白蛋白治疗组和血浆治疗组PNS重度水肿并发AKI患儿的发病情况与性别、年龄无关,且治疗前体质量、24 h尿量、尿蛋白定量、血白蛋白及Scr方面无明显差异。在治疗后,2组患儿均尿量增多,体质量及Scr降低。与白蛋白治疗组相比,血浆治疗组患儿的尿量在血浆治疗第3、7、10天增多更明显(P< 0.001),体质量在血浆治疗第7、10天下降更明显(P< 0.005),Scr在血浆治疗第7天亦有大幅度降低(P< 0.001)。提示对于PNS重度水肿并发AKI患儿,血浆治疗效果明显优于白蛋白治疗。
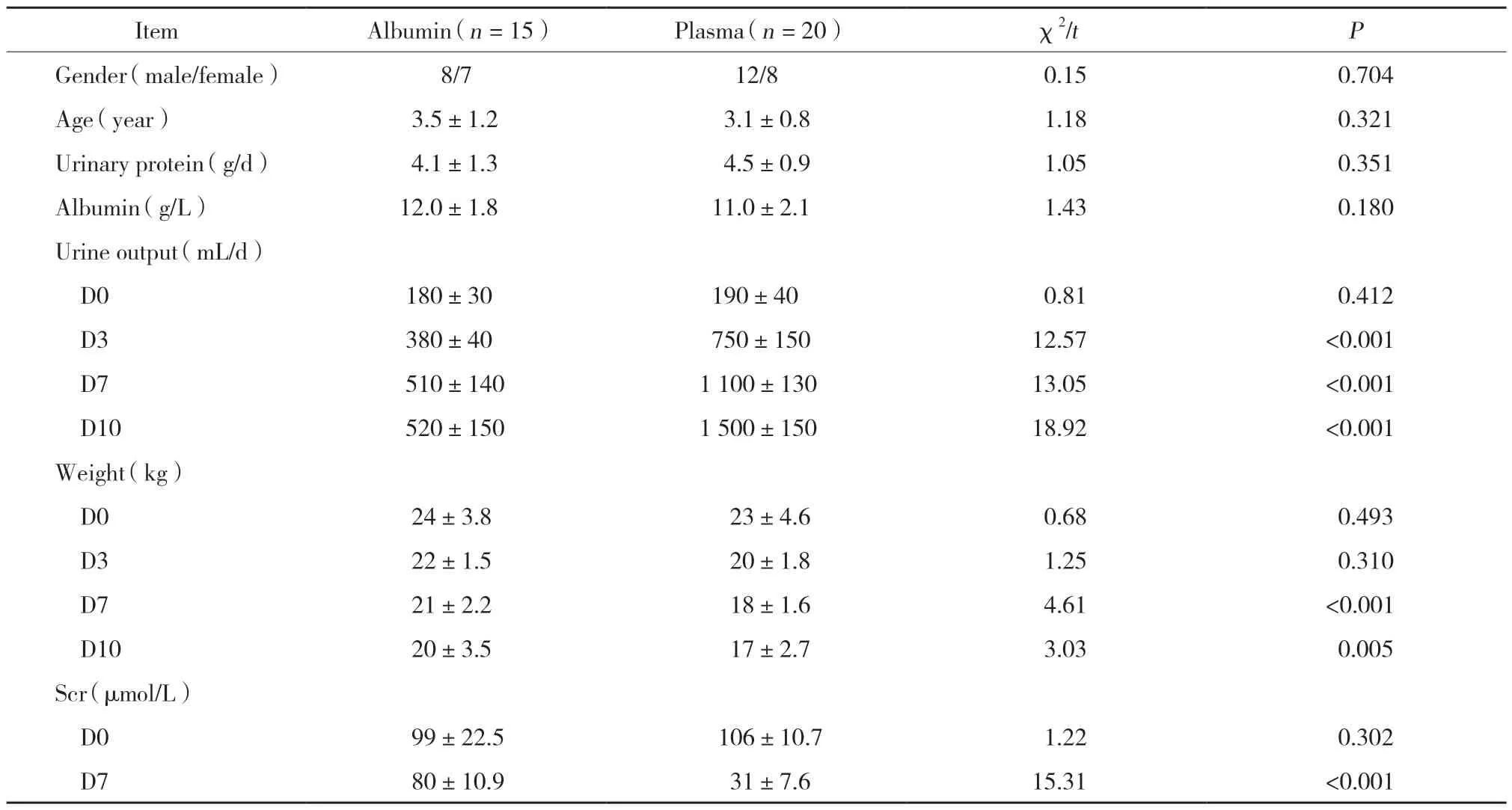
表2 35例PNS重度水肿并发AKI患儿应用白蛋白、血浆治疗效果的比较Tab.2 Comparison of therapeutic effects for albumin and plasma in 35 children with severe edema of PNS complicated with AKI
2.3 血浆和甘露醇治疗PNS重度水肿应用白蛋白后并发AKI患儿疗效的比较
本研究中,共有20例PNS重度水肿患儿应用白蛋白治疗,其中12例在静脉输注白蛋白后出现Scr升高,尿量减少(符合AKI诊断标准)。对此12例患儿在呋塞米及糖皮质激素等治疗基础上,分别再给予血浆治疗或血浆联合甘露醇治疗。如表3所示,与单纯输注血浆相比,血浆联合甘露醇治疗在用药第5、10天的尿量明显增加(P< 0.005),体质量在治疗第5天后明显下降(P< 0.05),Scr在治疗第7天明显降低(P< 0.05);然而在治疗第10天后,单纯输注血浆患儿与血浆联合甘露醇治疗患儿的尿量无统计学差异。由此推测,部分PNS重度水肿应用白蛋白后并发AKI患儿中可能存在滤过屏障尚未完全修复、白蛋白浓度过高等,导致大量蛋白由肾小球滤出进入肾小管,从而引起肾小管阻塞水肿、尿量减少,继而引起Scr升高。在应用血浆联合甘露醇治疗后,肾小管水肿消退,尿液因管腔通畅而大量排出,肾功能改善,水肿消退。
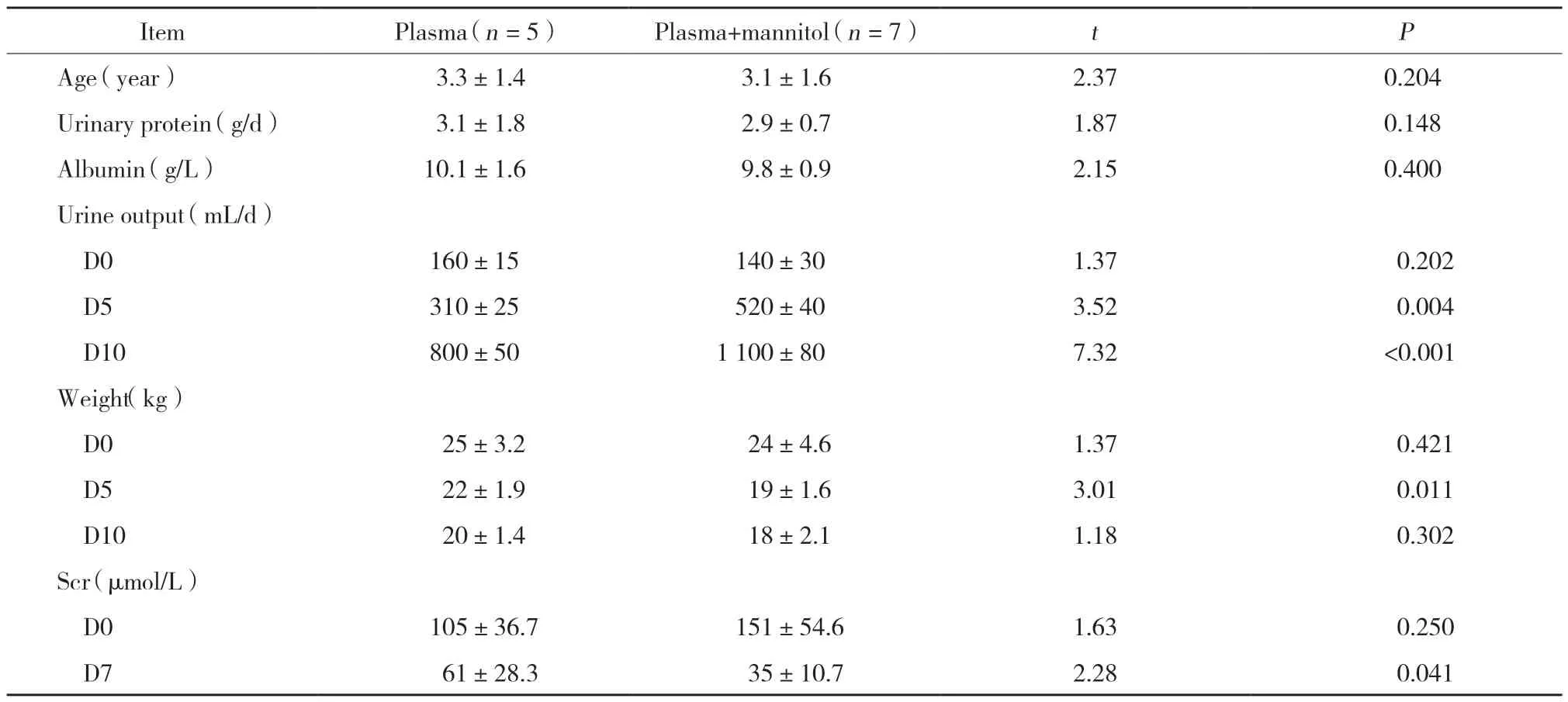
表3 12例肾病综合征重度水肿应用白蛋白后并发AKI患儿应用血浆和甘露醇治疗效果的比较Tab.3 Comparison of plasma and mannitol in the treatment of 12 children with severe edema of PNS complicated with AKI after albumin administration
3 讨论
重度水肿是儿童PNS的一个重要临床表现,AKI是儿童PNS较为严重的并发症之一。国内文献[5]报道,成人PNS基础上AKI的发病率为2.1%~9.9%。国外有文献[6]报道,儿童PNS 并发AKI的发病率达50.9%。有研究[7]表明,儿童原发性肾脏综合征并发AKI的发病率为13.8%,与国内成人相似。PNS 并发 AKI 的机制目前尚不完全明确,可能与潜在的血容量不足、急性肾小管坏死、蛋白管型阻塞、肾间质水肿、持续肾小血管收缩或肾小球滤过面积减少等因素有关[8]。持续水肿时间长、尿量减少明显、胃肠道症状、发热感染、曾输注白蛋白都是AKI的相关危险因素,在临床中应予以重视[7]。动态监测并及时发现肾功能的变化,早期发现并治疗AKI,对疾病预后具有很大影响。在某些基层医院,当发现患儿白蛋白明显降低时,医生为急于减轻患儿的水肿表现,反复输注白蛋白,引起大量蛋白从肾小球丢失,堵塞肾小管,导致肾小管间质水肿而引发AKI。因此,PNS患儿若无严重的水肿表现,应尽可能减少输注白蛋白频次,以防止AKI的发生。
目前,治疗儿童PNS重度水肿的方法包括输注人血白蛋白、血浆和低分子右旋糖酐等血浆代用品。低分子右旋糖酐是一类合成的高分子葡萄糖聚合物,作为血浆代用品,具有改善微循环、提高渗透压、抗血栓和扩充血容量的作用,因其可提高胶体渗透压,可用于治疗儿童PNS。人血白蛋白作为血浆提取物,亦可提高血浆胶体渗透压,促使组织间隙中的水分回流到血管中[9],但研究发现白蛋白会因短期内尿蛋白排泄增加导致蛋白负荷性肾病,甚至引发激素反应迟缓。输注白蛋白对正常肾小球屏障并无损伤,但对于已有肾小球滤过屏障损伤的PNS患儿,白蛋白可引起肾小球滤过膜孔结构进一步损伤以及肾小管严重水肿阻塞,甚至发生AKI[5]。血浆是全血在保存期内或过期5 d以内经自然沉降或离心后分离出的血液成分,获得后立即于-30 ℃冰冻后即为普通冰冻血浆。该制品内几乎含有正常人血浆的全部成分,包括白蛋白、丙种球蛋白、各种凝血因子等,可提升胶体渗透压,改善凝血状态。现有研究[10-11]证明,静脉滴注低分子右旋糖酐+呋塞米和静脉滴注白蛋白+呋塞米在治疗PNS严重水肿时均能够取得良好的利尿消肿效果,但有关血浆对PNS重度水肿患儿的疗效及与其他治疗方法的优劣比较尚无报道。血浆输注疗法适用于PNS,也可能由于正常人群血浆不含有损伤滤过屏障的成分,且存在有利于修复滤过屏障和损伤水肿的肾小管的成分,更利于肾脏功能的恢复。血浆是否有可能帮助缩短重度水肿患儿激素治疗后的尿蛋白缓解时间并减少住院时间,尚有待于进一步研究。
本研究回顾性分析了近3年我科收治的PNS重度水肿患儿的临床资料,结果显示,血浆在治疗儿童PNS重度水肿的疗效及预后方面明显优于白蛋白和低分子右旋糖酐,血浆输注对PNS重度水肿并发AKI患儿的疗效显著优于白蛋白治疗。本研究还发现,对于PNS重度水肿应用白蛋白后并发AKI的患儿,在呋塞米及糖皮质激素等治疗基础上,血浆输注后应用甘露醇更有利于水肿消退和肾功能改善,对缓解病情可发挥更快、更显著作用。总之,PNS患儿无论重度水肿或并发AKI,间断输注血浆的疗效均明显优于白蛋白和低分子右旋糖酐。即使由于输注白蛋白后诱发PNS患儿出现AKI表现,输注血浆仍能有效缓解症状,同时联合应用小剂量甘露醇会使疗效更为显著,尿量在联合治疗2~3 d后可明显增加,随之水肿消退、肾功能改善。因此,在临床工作中,对于PNS重度水肿患儿,在发生AKI及低分子右旋糖酐疗效不佳时,建议首选输注血浆联合小剂量甘露醇治疗。
本研究属于单中心回顾性临床研究,仍有诸多不足之处,存在病例数偏少、未观察记录尿蛋白消退时间、未对不同病理类型PNS患儿进行分组等问题。期待将来能出现更多中心、更多病例、更细致的临床或病理分组的前瞻性临床研究,以期为PNS重度水肿患儿制定更为完备的治疗方案。
