CHB患儿干扰素α1b长期给药后血清β2-微球蛋白浓度的影响因素分析
2021-09-26柴燕涛王福川姜棋予毕京峰
柴燕涛 王福川 侯 俊 贾 凡 刘 佳 姜棋予 张 敏 毕京峰▲
1.中国人民解放军总医院第五医学中心感染病医学部,北京 100039;2.中国人民解放军总医院第五医学中心肝病医学部,北京 100039;3.中国人民解放军总医院第五医学中心临床检验中心,北京 100039;4.中国人民解放军总医院第五医学中心临床输血科,北京 100039
慢性乙型肝炎(chronic hepatitis B,CHB)是影响我国人民健康的一个重大疾病[1]。截至2018 年4 月,我国慢性乙型病毒性肝炎(viral hepatitis type B,HBV)感染者9300 万人,慢性肝炎患者高达2000 万人[2-3],其中1~4岁、5~14岁和15~29岁人群乙型肝炎表面抗原(hepatitis B surface antigen,HBsAg)流行率分别为0.32%、0.94%和4.38%[4]。乙型肝炎E 抗原(hepatitis Be antigens,HBeAg)阳性孕妇为7.00%~11.00%,HBeAg阴性孕妇为0%~1.00%[5-6],新生儿及1岁以下婴幼儿的HBV 感染慢性化风险为90.00%[7]。干扰素-α(interferon-α,IFN-α)已被我国批准用于儿童患者的治疗[8],由于β2 微球蛋白的体内浓度-时间曲线与IFN的体内药-时曲线有相似的趋势,是公认的药效学指标[9-12]。然而,在连续给药,尤其儿童患者在长期给药后,疗程、年龄、性别等因素是否影响β2-微球蛋白的血清浓度尚不明确,客观上可能影响其能否作为药效学指标应用于儿童长期给药药代/药效学联合研究的效果。本研究已获中国人民解放军总医院第五医学中心(以下简称“我院”)医学伦理委员会的批准。
1 资料与方法
1.1 一般资料
收集2017 年12 月至2019 年9 月于我院就诊的108例接受IFN α1b 治疗的门诊及住院CHB患者的血清样本,该样本参考欧洲“2013 ESPGHAN 儿童时期慢性乙型肝炎的诊治指南”[13],符合CHB 临床诊断及IFN 治疗指征。纳入标准:①年龄1~16岁,男女不限;②基线血清丙氨酸氨基转移酶(aminotransferase,ALT)为正常值上限2~10 倍;③HBV DNA≥2.00×103IU/ml;④患者及家属签署知情同意书。排除标准:①合并其他病毒性肝炎或艾滋病;②合并重要系统、器官等的重大疾病;③合并智力异常、痴呆、精神病;④研究医生认为不适宜参与本研究;⑤接受过其他抗病毒药物治疗。
1.2 临床资料的采集与管理
①血液样本采集:所有样本均来自儿童进行生化检测时的剩余样本,台式高速冷冻离心机(Thermo 公司,Micro 21R)900 g,15 min 分离血清,置-70℃冰箱中保存待测。②制订儿童慢性乙型肝炎临床信息采集表,包括基本信息:联系方式、姓名、性别、年龄、民族、身高、体重、体重指数(body mass index,BMI)、生活习惯(吸烟、饮酒)、病史、临床诊断、病毒基因分型,详细记录血样采集前给药时间、血样采集时间、给药剂量。
1.3 β2-微球蛋白检测方法
①样品准备:完全融化后,混匀,900 g,10 min 后吸取上清,用样本稀释液稀释5000 倍,使稀释后的样本光密度(optical density,OD)值落在标准曲线对应的OD 值范围内,如果OD 值未在此范围内,再对稀释倍数进行相应调整。②试剂配制及操作方法:按照试剂盒[Human Beta-2 Microglobulin(B2M)SimpleStep ELISA Kit,货号:ab181423]说明书进行标准品工作液、Antibody Cocktail、洗液的配置,其中标准品工作液浓度由高到低分别为2000.00、1000.00、500.00、250.00、125.00、63.00、31.25 pg/ml。在板中按顺序加入50.00 μl稀释后样本、标准品工作液(均做2 个复孔)后,加入50.00 μl Antibody Cocktail,平板摇床(LE PARD 公司,Leopard V)室温400 r/min 反应1 h,洗板机(BioTek 公司,ELX50)洗板3 次,最后1 次用纸拍干。再加入100.00 μl TMB Develpoment Solution,平板摇床400 r/min 避光反应15 min 后,加入100.00 μl Stop Solution 平板摇床400 r/min 混匀1 min(注意避光),微孔板检测仪(BioTek 公司,Synergy H4)450 nm处读取OD 值。③结果分析:根据标准品工作液的浓度及各浓度对应的OD 值绘制标准曲线,然后用Origin软件对标准曲线进行曲线拟合,所有数据r2均>0.90。将OD 值带入到曲线拟合的公式中,换算出各个样本的浓度,乘以稀释倍数即为样本的最终浓度。
1.4 样本量的确定依据
本研究拟应用多重线性回归分析相关影响因素。根据临床经验,预计纳入BMI、疗程、年龄、给药时间、HBV 基因型、给药剂量、性别等7 个自变量。考虑到多重线性回归分析要求样本量应为自变量个数的10~20 倍,拟纳入至少100例样本。
1.5 统计学方法
所有数据存储于Epidata 数据库。所有统计分析过程均基于SAS 9.4 完成。正态分布计量资料以均数±标准差()表示,采用t 检验。偏态分布计量资料以中位数和四分位数[M(P25,P75)]表示,采用Wilcoxon 秩和检验。计数资料以例数或百分比表示。采用Spearman 相关分析β2 微球蛋白与年龄、疗程、给药时间及BMI的关系。多重线性回归分析β2 微球蛋白的相关影响因素。以P <0.05 为差异有统计学意义。
2 结果
2.1 患者临床信息基本情况
本研究共采集了108例患儿的血液样本,年龄1~16岁,中位年龄为5(4,7)岁;男性患儿64例(59.26%),女性患儿44例(40.74%);全部为汉族;均无烟、酒史,均无其他疾病病史。中位BMI 为15.85(14.85,16.65)kg/m2;中位疗程为338(167,715)d;给药时间(采样时间与采样前最后1 次用药的间隔时间)为1123(842,2349)min;给药剂量≤40.00 μg 共47例(43.52%),>40.00 μg 共61例(56.48%);HBV 基因型中B型有20例(18.52%),C型有81例(75.00%),6例患者基因型缺失,1例为非B 非C型,故未纳入分析。
2.2 β2 微球蛋白与年龄、疗程、给药时间及BMI的相关性分析
β2 微球蛋白与年龄、疗程、给药时间及BMI 无相关性(P >0.05)。见图1。

图1 β2 微球蛋白与年龄、疗程、给药时间及BMI的相关性分析
2.3 不同性别、HBV 基因型、给药剂量β2 微球蛋白的比较
不同性别、HBV 基因型、给药剂量β2 微球蛋白,差异无统计学意义(P >0.05)。见表1。
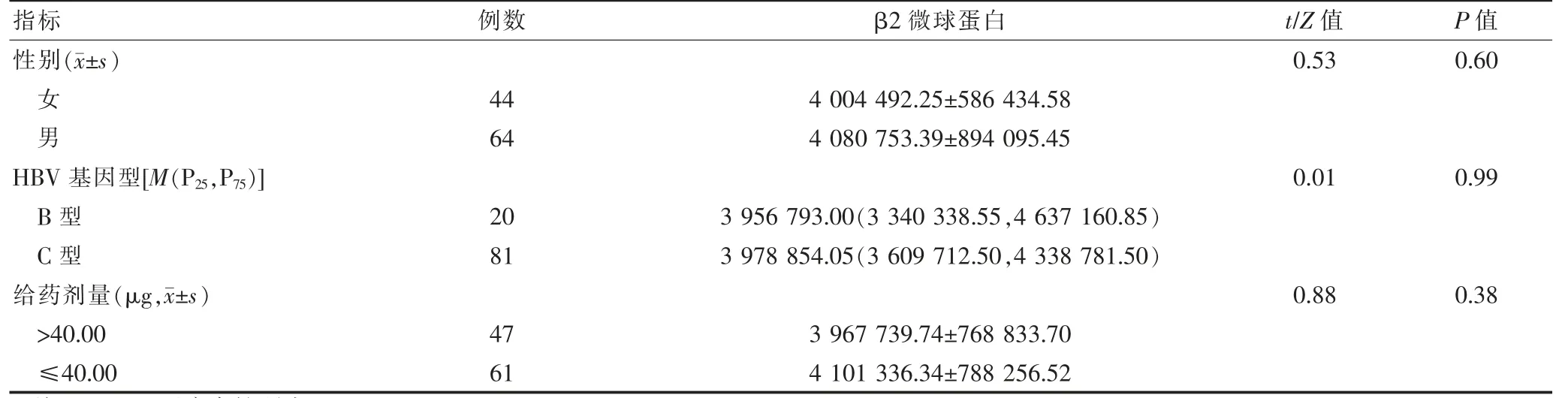
表1 不同性别、HBV 基因型、给药剂量β2 微球蛋白的比较
2.4 血清β2 微球蛋白浓度影响因素的多因素分析
将血清β2 微球蛋白浓度作为因变量,性别(女=1,男=2)、给药剂量(≤40.00 μg=1,>40.00 μg=2)、HBV基因型(C型=1,B型=2)、年龄、给药时间、疗程、BMI作为自变量引入模型以α=0.1 为检验水准。给药剂量、年龄、给药时间、疗程是影响血清β2 微球蛋白浓度的相关因素(P <0.05),其中血清β2 微球蛋白浓度伴随给药剂量的升高而升高,伴随年龄、给药时间及疗程的增大而降低。见表2。
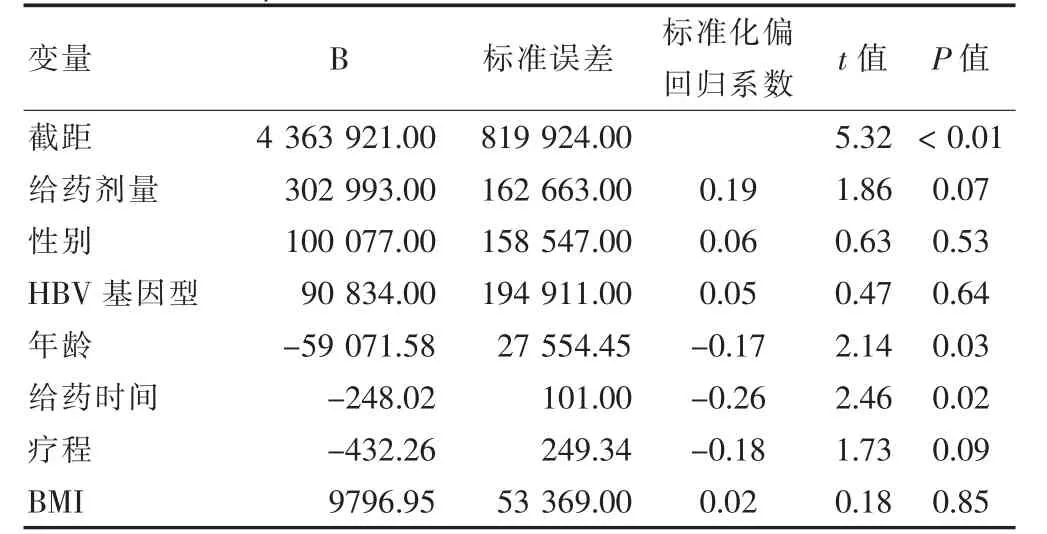
表2 血清β2 微球蛋白浓度影响因素的多重线性回归分析
3 讨论
β2-微球蛋白是由99 个氨基酸构成的多肽,是由淋巴细胞、血小板、多形核白细胞产生的一种小分子球蛋白[14-16],是细胞中完整组织相容性抗原分子的一部分[17]。正常条件下,血中含量极微,生成量较恒定[18-19],其主要生理作用为参与识别异己物质和提供杀伤细胞受体的作用[18]。由于分子量小,且不与血浆蛋白结合,故可自由通过肾小球,但原尿中的β2-微球蛋白约99.90%在近端肾小管被重吸收并降解,仅有微量约0.10%随尿液排出体外[20],因此,β2-微球蛋白常作为肾损伤的标志物用于临床肾损伤检测[21-23]。
近年来,β2-微球蛋白常作为INF的药效学标志物[12,24]用于INF的药代/药效学研究,通常被解释为INF 结合β2-微球蛋白表面受体后触发的复杂细胞内反应的结果,刺激了患者体内抗病毒蛋白的合成[24-25]。多项研究显示,在单次给药后,β2 微球蛋白的体内浓度-时间曲线与INF的体内药-时曲线有相似的趋势[12,21],但缺乏连续给药后,β2-微球蛋白影响因素的相关证据,客观上可能影响其能否作为药效学指标应用于长期给药的药代/药效联合研究的效果。
本研究基于108例1~16岁应用IFN α1b 治疗的CHB患儿,发现给药剂量、年龄、给药时间、疗程对血清β2-微球蛋白浓度均有显著的影响。其中,伴随给药剂量的升高,血清β2 微球蛋白浓度呈升高趋势,而伴随年龄、给药时间及疗程的增大,血清β2 微球蛋白浓度呈降低趋势。本研究提示,血清β2-微球蛋白的浓度不仅仅与给药剂量有关,给药时间、疗程及年龄也对血清β2 微球蛋白浓度具有一定的影响。
该研究存在的主要问题是,受伦理学的影响,只能应用住院儿童患者早上抽取的生化检测的剩余样本进行分析,导致多数患者的给药时间,即采样时间与采样前最后一次用药的间隔时间较长,一般大于12 h,属于间断数据,在“给药时间”这一指标的分析中可能存在一定的误差,寄希望于在未来的研究中进一步证实。
