环脂肽生物合成的研究进展
2021-09-24侯正杰孙慧中白松陈新月曹春阳程景胜
侯正杰,孙慧中,白松,陈新月,曹春阳,程景胜
(教育部合成生物学前沿科学中心,系统生物学教育部重点实验室,天津大学化工学院,天津 300350)
脂肽是一类重要的由氨基酸衍生的低分子量生物表面活性剂和抗菌肽,主要通过非核糖体肽和聚酮杂合途径生物合成[1]。其结构中既含有亲水性的氨基酸,又有疏水性脂肪酸链,其两亲性质对其抗菌活性至关重要[2]。其中,氨基酸肽链连接成环或与部分脂肪酸链连接成环形成环脂肽。细菌环脂肽是由微生物产生的次级代谢产物,具有表面活性剂性质,并且针对不同细菌、真菌等病原体具有广谱的抑菌活性[3]。环脂肽在生物防治、微生物采油、临床治疗、环境治理等方面具有多种应用[4]。常见的环脂肽有表面活性素(surfactin)、丰原素(fengycin)、多黏菌素(polymyxin)、达托霉素(daptomycin)、伊枯草菌素(iturin)等。近年来,包括多黏菌素和达托霉素在内的几种环脂肽类抗生素已经获得FDA 批准用于治疗多重耐药性超级细菌感染[5]。多黏菌素对许多耐药细菌的治疗具有有效性,多黏菌素B和E 被认为是对抗耐药细菌的“最后一道防线”,世界卫生组织将多黏菌素重新列为“至关重要的药物”用于临床治疗。但已有研究发现多黏菌素耐受基因,在全球引起高度关注[6-7]。同时,环脂肽类抗生素在生产和使用过程中面临着一些问题:多种同系物存在导致发酵产品品质难控,多种结构复杂的类似物难预测、形成不同的生物活性,不同制造商和发酵过程的稳定性差异性大[8]。而且环脂肽产物组分的不统一,对临床使用造成困扰,影响药代动力学、药效学和毒性动力学成效等[9-10]。新型环脂肽分子可能成为一类新的抗菌剂[11]。面对越来越多耐药病菌的出现,急需寻找新的抗生素,更好地理解抗菌肽的合成、修饰和作用机制将重启它的商业开发。
1 脂肽合成的微生物底盘
1.1 主要的细菌脂肽和来源
产脂肽的微生物分支,包括芽孢杆菌属(Bacillus)、类芽孢杆菌属(Paenibacillus)、乳酸杆菌属(Lactobacillus)、链霉菌属(Streptomyces)、假单胞菌属(Pseudomonas)、沙雷菌属(Serratia)和伯克菌属(Burkholderia)等。很多脂肽不仅能降低表面张力,而且具有显著的生物活性[12-13],以玫瑰孢链霉菌(Streptomyces roseosporus)中的达托霉素和多黏芽孢杆菌(Paenibacillus polymyxa)中的多黏菌素B 为代表[14-15]。脂肽一般由亲水性的寡肽和疏水性的脂肪酸链组成,根据结构特点又可细分为环状阳离子脂肽、环状非阳离子脂肽、线性阳离子脂肽。主要的细菌脂肽如图1 所示。其中,环脂肽构成了结构多样的天然产物家族,主要由链霉菌[16]、芽孢杆菌[17]和假单胞菌属[18]细菌生物合成。环脂肽的大部分生物活性归因于其两亲特性,可作为理想的生物表面活性剂。因此,许多环脂肽对于菌群运动和生物膜的形成至关重要[19]。其表面活性剂性质被广泛应用于石油开采、环境治理等方面。在结构上,环脂肽由一个寡肽和一个肽连接的N 末端脂肪酸组成。线性或分支的脂肪酰尾巴长度(通常为C6~C18)和氧化程度可以不同[20]。寡肽(最多25 个氨基酸)的C 末端与寡肽侧链或脂质部分中存在的羟基、酚或氨基官能团形成内酯或内酰胺,从而形成大小各异的肽环(通常为4~16 个氨基酸)[3]。通过非核糖体肽合成酶(NRPS)生物合成的环脂肽,寡肽中可以存在非蛋白质(如D-构型或β-氨基酸)和修饰的氨基酸(如4-氯苏氨酸)[21]。除了具有生物表面活性剂的性质,环脂肽还表现出有效和具有选择性的抗细菌、真菌和细胞毒性的作用。由Cubist 公司开发的达托霉素是为数不多的新批准用于治疗革兰氏阳性细菌感染的抗生素之一[12]。另外,某些芽孢杆菌菌株可以被用做作物保护中的生物防治剂,产生的环脂肽可以提高植物的整体适应性[17]。
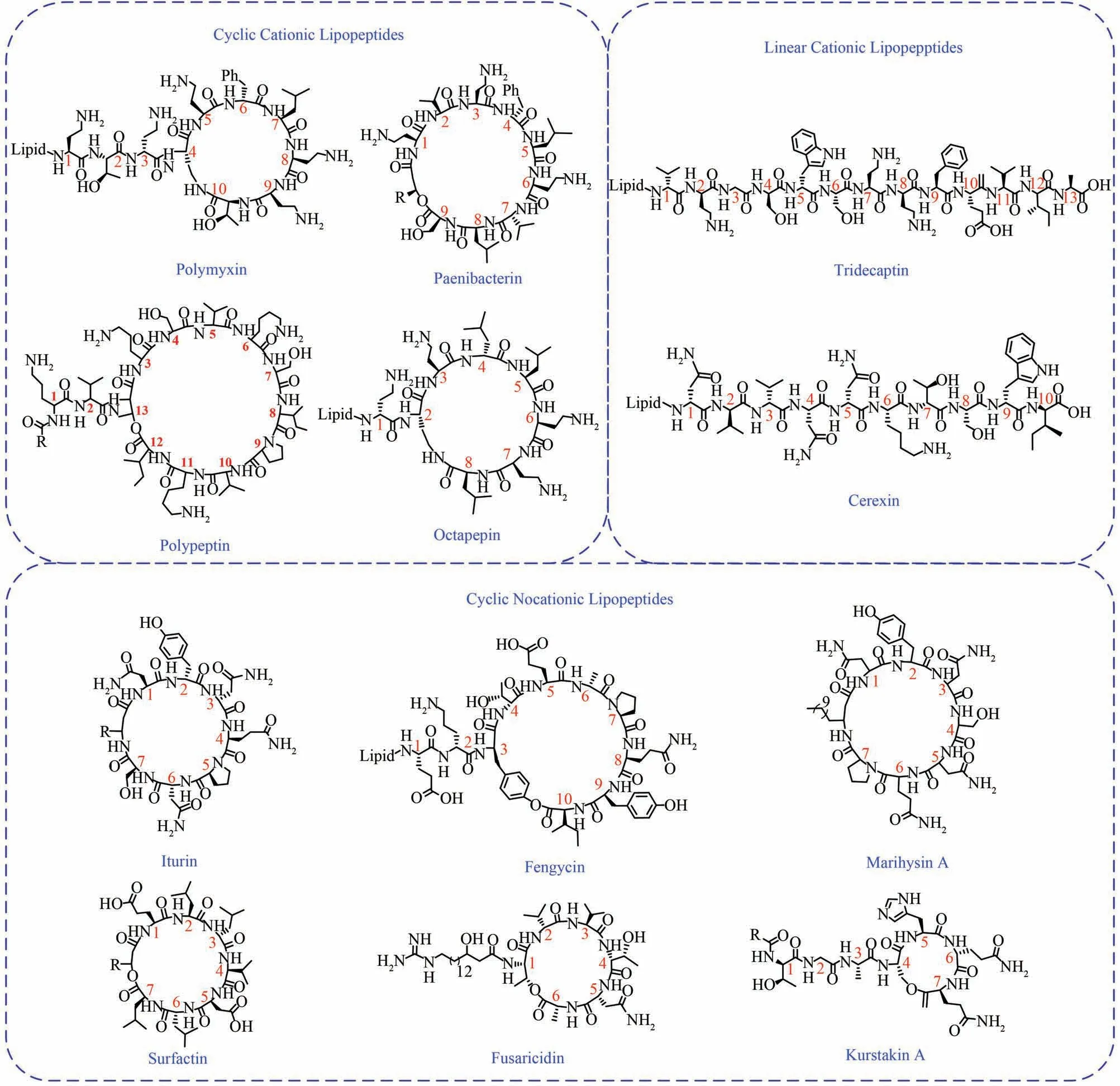
图1 部分常见的脂肽类型Fig.1 Some common types of lipopeptide
近年来,海洋和沿海环境已成为发掘和获得非核糖体肽的重要来源。Martínez-Núñez等[2]通过转录组分析发现海岸沉积物中高表达NRPS的生物菌群Proteobacteria和Firmicutes,并预测和鉴定了NRPS 结构域基因序列。Zhang 等[22]通过同源建模、生物信息学分析和分子对接的方法确定了海洋Bacillus atrophaeusC89 非核糖体肽合成酶合成Bacillamide C过程中两个腺苷酰化结构域的底物特异性。天然产物生物合成的蛋白质组学策略如次生代谢蛋白质组学(PrISM)[23]、正交活性位点识别系统(OASIS)[24]等应用,以及基于活性NRPS蛋白质谱(ABPP)探针的开发,促进了NRPS 基因簇的鉴定和结构域的功能分析[25]。
1.2 天然产物底盘菌株开发现状
天然产物底盘菌株构建的常见方法包括基因组精简与优化、各类调控因子的改造(转录调控因子,包括全局调控因子、途径专一性调控因子等)和强化前体物供应[26]。其中基因组精简和优化是最主要和直接的方法。通过删除同类非目标天然产物竞争途径中的长基因簇,以及删除基于脂肽合成模块化代谢工程中无用的代谢途径,可以有针对性地提高目标脂肽的合成效率和质量,提高底盘的生产性能。
天然产物底盘菌株需要从生长周期、转化效率、菌株形态、遗传稳定性、次级代谢谱、能量和还原力、异源蛋白合成能力、次级代谢产物表达能力等方面进行系统评估[27]。常见的脂肽合成底盘宿主包括链霉菌、伯克菌、芽孢杆菌等。这些菌株可以提供生物合成的前体分子,并且对各自的表面活性终产物表现出足够的耐受性。而且,由于系统发育的关系,它们在鸟嘌呤-胞嘧啶含量和密码子使用方面具有一系列生产菌株的遗传相容性[28-29]。随着基因测序技术的快速发展和各种基因发掘方法的建立和应用,很多天然产物包括环脂肽类物质合成基因簇被鉴定出来。但这些基因簇在天然宿主中绝大部分都是沉默的,无法实现产物的最终合成,或者可合成的天然产物产量极低,提取困难,无法实现工业化生产。运用合成生物学的方法建立高效合成脂肽类天然产物的底盘菌株,不但可以改善菌株的遗传稳定性,提高异源表达,而且可以通过应用强度和功能已知且可控的启动子、终止子、转录调控开关等各种元件对目标产物的合成基因进行调控。重构天然产物的合成途径和基于前体物合成的代谢网络可以实现新型天然产物的开发。
链霉菌是最大的天然产物来源菌。Komatsu等[30]通过简化阿维链霉菌基因组,构建了通用模式底盘菌株Streptomyces avermitilisSUKA17,对包括NPRS 类化合物Holomycin 在内的20 种不同类型的次级代谢合成基因簇进行了异源表达。Liu等[31]删除了Streptomycessp.FR-008 三个内源性聚酮合酶(PKS)基因簇,构建出一个相对干净的无聚酮合成竞争的底盘宿主,为异源表达天然产物合成基因簇提供了平台。Tan 等[32]通过转录调控策略在Streptomycessp.SCSIO 02999 中原位激活了TPM A 的生物合成基因簇,敲除两个负调控基因(totR3/totR5)和超表达一个正调控基因(totR1),实现了主产物TPM A 的合成和一个磺酸化的新产物TPM C 的分离鉴定。为提高工程菌的遗传稳定性,将TPM A 在模式菌株S.lividansTK64 中进行异源表达,结合基因调控策略,TPM A 产量提高约6倍。此外,一些海洋生产菌株属于放线菌进化枝,链霉菌作为最有价值的代表,适用于作为一些海洋生物表面活性剂生产的宿主系统,尤其是对NRPS衍生的化合物[33-34]。
伯克菌是仅次于链霉菌的天然产物来源的第二大类细菌。Wang 等[35]建立了伯克菌DSM 7092 基因组无痕修饰的方法,实现了对大片段基因簇的敲除,为改造伯克菌为通用底盘菌株提供了基础。此外,Zhi等[36]通过基因组学和转录组学发现解淀粉芽孢杆菌MT45拥有同类解淀粉芽孢杆菌中更小的基因组和显著富集的表面活性素(Surfactin)合成途径,包括中心碳代谢和脂肪酸生物合成。Wu等[37]通过强化Bacillus subtilis168细胞内支链脂肪酸合成路径提高前体物脂肪酸的供应,使表面活性素产量提高了20.8 倍。Hühner 等[38]建立酿酒酵母NRPS基因表达系统进行α-酮羧酸二聚体生物合成,为酵母底盘菌株的构建提供了借鉴。
2 脂肽合成的模块结构域特点
非核糖体肽与核糖体肽不同,复杂的蛋白结构不受特异性氨基酸序列限制,具有大量潜在而且灵活的结构多样性。在非核糖体肽生物合成中,氨基酸通过腺苷酰化(A)结构域进行腺苷酰化,该结构域包含特异性识别元件以选择正确的掺入基团[39],该基团装载到肽基载体蛋白(PCP)上,通过缩合(C)结构域催化的酰胺化反应进入肽支架。其他步骤可通过差向异构化(E)和甲基化(甲基化酶,MT)结构域催化的PCP 结合中间体反应来进行。C 结构域的一个常见变体是环化(Cy)结构域,将半胱氨酸、丝氨酸或苏氨酸等掺入中间体并将其环化为噻唑啉和唑啉。氧化(Ox)结构域可将这些杂环分别转化为噻唑和唑。在经典NRPS中,遵循共线性规则,不同亚基选择性地以非严格共价的方式相互作用形成最终完整的脂肽合成生产线(图2)。NRPS亚基间的非共价相互作用是由专门的N 端和C 端对接结构域(DD)介导的。研究证明DDs 中氨基酸交换不仅会导致体外蛋白质亲和力的变化,而且会导致体内不同肽的产生[40]。

图2 用于脂肽合成的非核糖体肽合成酶(NRPS)催化合成脂肽的典型过程Fig.2 Typical processes catalyzed by non-ribosomal peptide synthetase(NRPS)used for lipopeptide synthesis
脂肪酸链的装配和氨基酸的延伸是非核糖体肽合成过程中的重要环节。非核糖体肽合成酶每个模块激活并修饰一个特定的氨基酸(aa),然后通过下一个模块激活并修饰的aa 对其进行延长,从而生成长度取决于所用模块数量的肽。典型的NRPS 延伸模块由1 个用于激活特定氨基酸的腺苷化(A)结构域,1 个用于形成肽键的缩合(C)结构域和1 个巯基化(T)结构域组成。脂肽合成在宿主菌中,通过辅助元件促进氨基酸修饰、分子伴侣功能、产物输出和宿主抗性[12]。7 种类型的结合元件按如下顺序连接组装:长链脂肪酸到L-氨基酸,L-氨基酸到L-氨基酸,L-氨基酸到D-氨基酸,D-氨基酸到L-氨基酸,L-氨基酸到手性氨基酸(如甘氨酸、肌氨酸),手性氨基酸到L-氨基酸,手性氨基酸到D-氨基酸[41]。每一个氨基酸结合元件由两个功能性模块组成,每个模块至少包括3 个酶结构域,通过内蛋白连接(-)或间蛋白连接肽(:)依次连接(比如CAT-CAT、CAT-CATE、CATE-CAT、CATE:CAT)。连接脂肪酸到氨基酸的元件由脂肪酰连接酶(AL)和酰基载体蛋白(ACP)和一个NRPS 模块组成(例如AL:ACP:CAT 或者AL-ACP:CAT)。自然界进化出3 种类型的C 结构域,分别连接脂肪酸到L-氨基酸、L-氨基酸到L-氨基酸、D-氨基酸到L-氨基酸;同时也进化出3 种T 结构域(或PCP肽基载体蛋白),与上游的AC 结构域和下游的C结构域、与下游的E 和C 结构域、与下游的TE 结构域相互作用[12]。A 结构域类型有多种,决定何种氨基酸将要被绑定、激活和参与到氨基酸的偶联过程中。
非核糖体肽合成酶的结构多样性和各结构域的作用机制,决定了脂肽合成过程中多种同系物的产生。例如多黏菌素和镰刀菌素,首先从多黏菌的菌株中分离出来[42]。其中的多黏菌素是由环状七肽和被N 末端脂肪酸酰化的三肽侧链组成的家族,包括多黏菌素A、B、D、E 和M[43]。研究表明,多黏菌素B1的药代动力学与商用购买的多黏菌素B混合物存在显著差异,单一纯组分的药理学活性并不能推广到商业使用的混合物[44]。不同品牌的多黏菌素虽有类似的组成,但抗菌活性存在差异[45]。药代动力学发现尽管脂肽中只有一个氨基酸差异,多黏菌素A和B与血浆结合能力低于多黏菌素B1、B2,体内清除能力和在肾脏的积累差异明显,因此对目前可用于临床的脂肽商品的组成成分需要更严格的控制和标准化[46]。Roberts等[47]发现N 末端只有一个碳差异的多黏菌素B1和E1对细胞的体外凋亡作用有显著差异,与商业多黏菌素产品相比,单独的脂肽组分具有更多的体内抗微生物活性。
NRPS 进化过程主要包括4 个种类:复制和协同进化;通过复制和重组产生的结构域N 末端添加;和其他生物合成基因簇(BGCs)进行结构域的交换;不同氨基酸特异性结合位点的快速突变以及多个过程的组合进化[48]。天然产物生物合成的遗传基础揭示了遗传改变引起化学结构多样性的重要作用。基于NRPS 进化过程,对NRPS 生产线中的结构域进行非理性改造,重构生物合成途径的遗传成分可以有效改变脂肽的产品特性和同系物的组分,以及产生“非天然”的天然产物。天然产物类似物可以通过改变不同的合成阶段产生,如前体物导向的生物合成、工程化改造合成过程中涉及的巨酶、模块组装后的修饰等。通过对达托霉素和A54145 NRPS 生产线的改造产生了超过120 种非天然衍生物[12]。通过重组来自不同菌株(Photorhabdus,XenorhabdusandBacillus)NRPS亚基产生了10多种新型脂肽[49]。
3 脂肽合成和调控研究进展
传统脂肽类似物化学合成的方法,严重限制了脂肽合成的整体效率,抗菌活性显著降低,且脂肽结构的多变性不适合化学合成。同时化学合成的过程存在产量少、污染大、成本高等问题[50-51]。脂肽合成结构域的一个或多个改变可以改变氨基酸的种类与数目,同时脂肪酸酰化酶以及缩合结构域对脂肽脂肪酸的特异性具有调控作用(表1)。脂肽合成过程的顺利完成会受到多个代谢途径和代谢过程的影响和调控(图3)。

图3 脂肽合成的主要代谢途径Fig.3 Main metabolic pathways for lipid peptide synthesis

表1 脂肽合成域改造调控相关研究Tab.1 Studies on regulation and modification of lipopeptide synthesis domain
3.1 脂肽合成的代谢工程改造
脂肽类天然产物是目前生物制剂研究的热点[71],但是长期以来,成本高、产率低一直是制约脂肽类物质微生物合成的难题[72],利用基因工程技术和代谢工程方法构建高效合成脂肽类物质的工业菌株具有十分迫切的需求。不同于初级代谢产物的合成,脂肽类天然产物作为一种重要的次级代谢产物,其代谢网络更为复杂,往往需要多种初级代谢产物如各种氨基酸、脂肪酸及其衍生物的参与,其合成受到多种途径特异性因子和复杂的全局调控因子调控。而且大多数脂肽合成基因簇是沉默的或者表达效率低,无法高效启动制约着产物的合成。通过优化前体代谢、提高脂肽合成基因簇表达、阻断脂肽合成竞争途径、各类调控因子的改造可以有效提高脂肽产品的合成。
研究最多也最为成熟的是表面活性素的合成。Wu 等[37]在模式菌株Bacillus subtilis168 中整合了完整的表面活性素合成酶基因簇sfp,实现表面活性素从无到有的积累;删除与生物膜形成相关的基因和非核糖体多肽合成酶/多酮合成酶途径来减少竞争,表面活性素产量提高3.3 倍;过表达细菌自我抗性相关蛋白,表面活性素产量提高8.5 倍;强化前体支链脂肪酸的合成途径,表面活性素产量提高20.3 倍;强化srfA表达,使乙酰辅酶A 节点处的代谢流从细胞生长转移到表面活性素生物合成,表面活性素产量进一步得到提升。Wang 等[73]通过过表达B.subtilisTS1726 中生物素羧化酶Ⅱ基因yngH增强脂肪酸的供应,表面活性素产量较对照提升43%,达到13.37 g/L。此外,Dang等[74]通过过表达多效性调节因子DegQ,使伊枯草菌素(iturin A)的产量提高11.8倍。Xu等[75]利用强启动子PbacA控制iturin A合成酶基因簇,iturin A产量提升132.15%,敲除iturin A合成酶操纵子负调节基因abrB,iturin A产量进一步提升19.8%,结合培养条件优化,产量最终达到(2013.43±32.86)mg/L。Huang 等[76]突变失活负调节基因wblA,达托霉素(daptomycin)产量提高51%。利用代谢工程策略有效提高了脂肽产品的产量。但是基于前体物导向和调控因子导向的改造方法,仍无法解决产物中多组分同系物共存或高价值组分比例低的问题,往往导致发酵过程和产品批次的不稳定,制约着脂肽类化合物产品品质的提升。因此,对脂肽多组分同系物的调控也格外重要。
3.2 肽链氨基酸对脂肽同系物组分调控
NRPS 调控产生新肽产物的研究涉及:①通过激活替代底物的A结构域的替换;②A结构域的底物结合口袋的改变;③CA 结构域作为不可分割的整体替换(图3)[77]。A 结构域的取代可以改变NRPS 模块对氨基酸底物的选择性,可以成功提高所需结构类似物的浓度。Uguru 等[78]对CDA 合成酶中的天冬氨酸A 结构域定向突变导致产生含有天冬酰胺的十二氢萘的肽和一种特殊的线性六肽中间体。Schauwecker 等[52]通过将N-甲基缬氨酸活化结构域取代缬氨酸活化结构域,导致催化非甲基化和N-甲基化酰基二肽的合成。Kim 等[62]第1 次用基因工程的方法对多黏菌素合成酶进行改造,通过在多黏菌素A 编码基因的基础上替换多肽链上的A 结构域,合成了多黏菌素E、B、P。Kries等[60]通过替换A 结构域的结合口袋部分,将编码不同特异性的亚结构域移植到对Phe特异性的GrsA 模块中,得到了不同的蛋白。通过交换具有不同氨基酸特异性的外源A 结构域可能导致生产不是后续生物合成步骤的中间体,另外,A结构域操纵策略可能受到对受体底物显示特异性的上游C 结构域的限制[79]。Ackerley 等[80]在pvdD的第1 个模块中的结构域替换实验发现还有可能的原因是取代结构域的来源不同,或是结构域的取代损坏了上下游的结构,C结构域也可能表现出一定程度的供体位点特异性。尽管对A 结构域进行替换、突变、删除、插入等基因操作可以有效改变脂肽中氨基酸的种类和数量,肽残基数量的减少或增加是产生脂肽结构多样性的替代方法,但是这些操作可能会导致产物的产量减小和活性降低。
除了对氨基酸具有特异性的A结构域外,有些脂肽NRPS模块中还有特殊的结构域影响脂肽的结构。Duerfahrt 等[54]利用Cy 结构域代替C 结构域,产生新型杂环二肽。使用重组TE 结构域来催化脂肽区域特异性环化是产生具有改进性质的新化合物的有力方法。de Ferra 等[81]通过将C 末端TE 结构域移位到内部结构域来修饰SrfA,从而导致产生新的线性表面活性素类似物。Schwarzer等[69]发现异源NRPS 的TE 结构域可以选择性地控制肽链的环化与终止,产生结构多样性。
3.3 多结构域对脂肽同系物组分调控
通过进行多个结构域的替换,或通过引入腺苷化(A)和硫醇化(PCP)结构域的融合或者腺苷化(A),肽基载体蛋白(T)和缩合结构域(C)的融合,可使多肽中氨基酸重新排列[63]。Mootz 等[70]将目标模块与tyrocidine 合成酶的前两个模块以及硫酯酶结构域融合,获得预测的新型三肽。Duerfahrt 等[82]通过融合包含腺苷化(A),肽基载体蛋白(T)和缩合结构域(C)的Asp 和Phe 激活模块,实现了6 种不同的Asp-Phe 合成酶的转录。因此,应该优选在PCP和C结构域之间选择NRPS 模块的融合体,以使CA 连接完整。通过用分枝杆菌素和黏噻唑菌醇的MbtB 和MtaD 模块取代支化环状噻唑啉NRPSs 中BacA 的第2 个模块[54],将整个D-羟基苯基甘氨酸模块插入模块4和5 之间的巴林霉素中导致生成八肽产物[83]。这些研究主要集中在保持CA 或CAT结构域完整的交换,同时仅在域间连接区域进行域融合。通过使用基因缺失、基因交换、双重和三维交换,整个模块交换和多模块交换的组合产生了足够数量的新型脂肽抗生素。但是,在多数情况下仅表现出发酵过程中最丰富的脂肽成分,新型脂肽以及衍生物占比很低。为了实现商业规模的脂肽生产,运用合成生物学策略,通过工程化生物合成途径,有望快速提高单一组分脂肽产量和产品质量。
3.4 脂肪酸侧链对脂肽同系物组分调控
脂肪酸链以不同的方式整合进入脂肽,包括酰基辅酶A 连接酶和ACP 编码基因的存在,以及独特的N 末端C 结构域共价连接到第1 个氨基酸的载体蛋白质结合[84]。单独的酰基转移酶是脂肽的脂肪酰基掺入脂肽所必需的,但在一些脂肽基因簇以及基因簇附近未发现负责将N 末端脂肪酰基连接与脂肽酯化作用的脂肪酸连接酶[85–87]。脂肽基因簇的第1 个C 结构域(starter C)可能介导脂肪酰基和第1个氨基酸的连接,在钙依赖性抗生素(CDA)基因簇中starter C 结构域表现出在其供体位点对酰基载体蛋白(ACP)的高特异性,在受体位点对CP 的松弛特异性,但是对附着的底物具有高选择性[88]。达托霉素是一种环脂肽类抗生素,对革兰氏阳性菌具有优良抗菌活性。达托霉素和A54145 具有将长链脂肪酸与第1 个氨基酸偶联的特殊CAT 起始模块,酰基连接酶(AL)和酰基载体蛋白(ACP)参与A21978C 和A54145 生物合成过程中脂肪酸的活化和偶联。在玫瑰孢链霉菌合成达托霉素的过程中,A21978C 基因簇中DptE和DptF涉及将长链脂肪酸与氨基酸的偶联进而引发A21978C 的生物合成[89]。starter C 结构域之间的异质性,反映了不同脂肪酸的物理调节或与对接和转移活化的酰基硫代酯构建脂肽的特定载体蛋白的相互作用[90]。所以,C 结构域中的底物选择性可能是脂肽合成酶控制和进行有效工程化改造的另一个障碍。通过在脂肽合成途径之间交换N 末端C 结构域,或者将它们添加到不被酰化的产物NRPS 中,将使脂肪酰基的N 末端改造成为可能。脂肪酸侧链供给的调节是对脂肽同系物组分调控策略之一。
目前新型脂肽的合成包括了脂肪酸侧链改变下形成的新型脂肽,如N-甲基化和脂肪酸偶联合成的具有高效抗菌活性和高蛋白水解稳定性的新型蜂毒抗菌肽anoplin 类似物[91]。突变lpdV基因改变了枯草芽孢杆菌对脂肪酸链的选择性,更倾向于合成表面活性素C14[92]。突变起始缩合结构域的活性位点改变了脂肪酸链的特异性,进而合成A54145的同系物[93-94]。
3.5 外源添加对脂肽同系物组分调控的影响
脂肽的前体脂肪酸除了生物合成外还可以通过初级代谢来提供,所产生的代谢物的种类根据生长培养基的组成和培养条件而变化,所涉及酶的底物特异性的变化导致最终产品性质的改变[85]。脂肽侧链的分布在一定程度上可以通过加入特定的脂肪酸或氨基酸来调节[95]。脂肽同系物的酰基可以通过脂肪酸补充来改变,在发酵过程中A54145 环脂肽可以产生大量的同系物,但它们的比例可以通过添加氨基酸(L-Val、L-Ile 或L-Glu)来调节,而加入各种中链脂肪酸(如己酸、辛酸或壬酸)会产生新的酰基衍生物[96]。Ding 等[97]研究发现,添加肉豆蔻酸、十五烷酸、棕榈酸、十七烷酸、十八酸和壬酸等外源烷酸可以促进脂肽的产生,增强解淀粉芽孢杆菌Pc3 脂肽粗提物的抗真菌活性,利用奇数碳链长的烷酸可进一步提高解淀粉芽孢杆菌Pc3 中iturin A C15的合成量。外源添加调控脂肽合成相关研究见表2。

表2 外源添加调控脂肽合成相关研究Tab.2 Studies on regulation of lipopeptide synthesis by exogenous addition
外源添加氨基酸对脂肽的产量有直接影响。Zhou 等[98]研究发现在培养基中添加L-Leu 后表面活性素产量显著增加,而添加D-Leu后表面活性素产量急剧下降,结果表明L-Leu作为前体或底物参与了表面活性素的合成,而D-Leu可能是竞争性抑制剂抑制了表面活性素的合成。添加L-Asn、L-Pro和L-Ser的复合氨基酸可提高iturin A 的产量,且外源添加的L-Ser 浓度与iturin A 产量呈正相关,说明L-Ser 是iturin A 生物合成途径中的限速化合物[99]。L-Ile 的加入极大提高了多黏菌素B1 的比例,而L-Glu 和L-Gly 存在时多黏菌素D1和D2含量显著增加[100]。通过补充氨基酸(L-Ala、L-Arg、L-His、L-Cys、L-Asn、L-Gln、L-Ser 和L-Thr)会以浓度依赖性方式刺激多黏菌素D1和D2的产生,而低浓度(0.5 mmol/L)的L-Lyr有利于多黏菌素D的合成,多种多黏菌素D 类似物显著低于多黏菌素D1和D2[87]。这些研究表明,氨基酸添加对多黏菌素等环脂肽同系物组分的调控至关重要。
Bartal 等[101]研究表明使用葡萄糖以外的碳源对表面活性素产量也会产生影响,而且在某些情况下表现出选择性。添加麦芽糖、纤维二糖和蔗糖分别对1 个(C16)、2 个(C13、C16)和4 个(C13、C14、C17、C18)组有显著的负面影响,甘露醇和乙醇的使用分别增加了C15和C15-C16组的相对量,但也使某些组的合成减少。此外,发酵培养基中添加不同的金属离子可以通过促进细胞生长、影响氮利用和其他可能的未知机制来显著影响脂肽的产量[102]。Lin 等[103]通过添加亚铁离子提高了解淀粉芽孢杆菌产iturin A 的能力。Cooper等[104]研究发现锰和铁盐的加入可以提高表面活性素的产量。Bartal 等[101]研究表明金属离子的使用对表面活性素的影响较大,并且发现了第5 位含有AME5 的表面活性素同系物。其检测结果还表明金属离子促进了更长脂肪酸链的脂肽化合物产生,产物中有2/3 是C16、C17或C18的表面活性素同系物。
4 几种常见环脂肽的合成调控
4.1 多黏菌素
多黏菌素(polymyxin)是由多黏类芽孢杆菌(Paenibacillus polymyxa)产生的一组多肽类抗生素。对大多数革兰氏阴性菌有抑制作用。多黏菌素的肽链由10 个氨基酸组成,结构上为线性三肽连接环状七肽,不同位点氨基酸种类和构型的差异形成了不同的多黏菌素同系物。多黏菌素氨基酸序列为:L-Dab-L-Thr-3-L-Dab-L-Dab-6-7-LDab-L-Dab-L-Thr。其中前3 位的氨基酸呈线形连接,后7 位的氨基酸呈环形。第3、6、7 位氨基酸的不同决定了其同系物的种类(表3)。对多黏菌素NRPS 的部分结构域进行改造,可以达到改变产物中多黏菌素同系物比例的目的(图4)。Yuan 等[109]通过替换P.polymyxaCJX518 中多黏菌素合成酶基因簇pmxA中的A 结构域和pmxE中的C 结构域,获得了B1 组分提高,Ile-P-B1 和B3组分降低的重组菌株。Kim 等[62]通过将P.polymyxaE681 中第7 位L-Thr 特异性的A 结构域替换为来自P.polymyxaATCC 21 830 中L-Leu 特异性的A 结构域,第6 位D-Leu 特异性的A 结构域替换为来自P.polymyxaF4 的D-Phe 特异性的A结构域,在B.subtilisBSK4dA 中表达并成功合成了polymyxin B 和E。

图4 多黏菌素合成的NRPS结构域改造Fig.4 Modification of NRPS domain of polymyxin synthesis

表3 多黏菌素同系物化学结构Tab.3 Chemical structure of polymyxin homologues
4.2 表面活性素
表面活性素的肽链包含7 个氨基酸,序列为L-Glu-L-Leu-D-Leu-L-Val-L-Asp-D-Leu-L-Leu,首位的L-Glu 和第7 位的L-Leu 连接形成七肽环[110]。表面活性素肽环的第2、3、4、6、7位氨基酸为疏水性氨基酸,第1、5 位为亲水性氨基酸。与多黏菌素不同,表面活性素的肽环比较稳定,由肽环氨基酸改变形成的表面活性素同系物较少。表面活性素肽环的化学结构见表4。Stachelhaus 等[65]通过同源重组靶向替换了B.subtilissrfA 操纵子中的氨基酸激活结构域。Schneider 等[111]在B.subtilis中通过体内重组的方式将亮氨酸激活模块替换为鸟氨酸激活模块,将鸟氨酸直接结合在肽环第2 位,形成了实质性的肽环构象变化。Eppelmann 等[67]通过比较和同源建模分析了NRPSs 的底物选择性编码序列,而后对表面活性素合成酶的srfA 序列进行定点突变,合理地改变了NRPS 模块的底物特异性。Jiang 等[112]敲除了B.subtilisBP2-L1 中 的SrfA-A-Leu、SrfA-B-Asp 和SrfA-B-Leu 模块,其中敲除了第6 位Leu 的表面活性素变体表现出更显著的抗真菌活性。
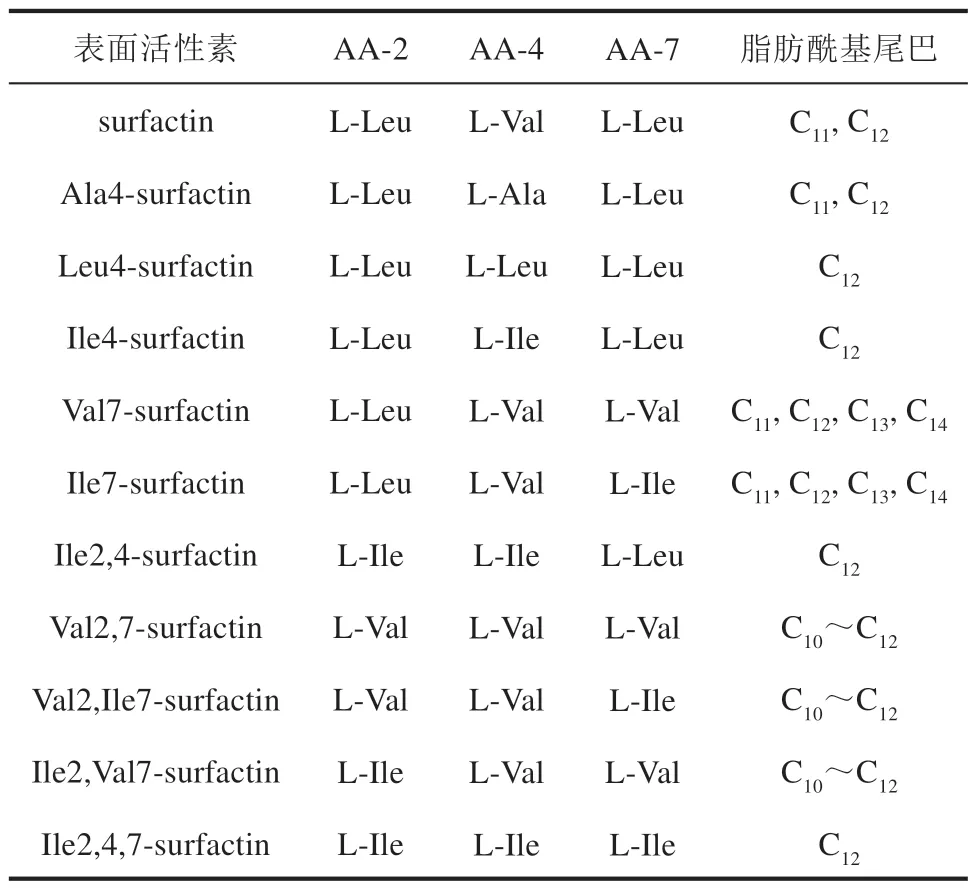
表4 表面活性素同系物化学结构Tab.4 Chemical structure of surfactin homologues
4.3 丰原素
丰原素的肽环结构类似于多黏菌素,由线性二肽连接环状八肽而成。第3 位和第10 位氨基酸之间以内酯键成环[113]。丰原素肽链氨基酸序列为L-Glu-D-Orn-3-4-L-Glu-6-L-Pro-L-Gln-9-10。根据已有的报道,第3、4、6、9、10 位的氨基酸决定了丰原素的不同构型。fengycin A 和fengycins B 是最常见的两种亚型,它们的氨基酸序列为L-Glu-D-Orn-D-Tyr-D-Thr-L-Glu-6-L-Pro-LGln-L-Thr-L-Ile。区别在于第6 位的氨基酸,fengycin A 是 D-Ala,fengycin B 是 D-Val。fengycin C 是fengycins 家族的一个新亚型,由一个七肽链和脂肪酸链相连而成。其氨基酸序列为:L-Glu-D-Orn-D-Tyr-D-Thr-L-Glu-D-Val-L-Pro-L-Gln-D-Thr-L-Ile。fengycin C 在第9 位的氨基酸与fengycin B 不同,在第6 位和第9 位的氨基酸与fengycin A 不 同[114]。fengycin S 分离自B.amyloliquefaciens,与fengycin B 相比,该亚型在第4 位 是D-Ser,而不是D-allo-Thr[115]。丰原素同系物见表5。

表5 丰原素同系物化学结构Tab.5 Chemical structure of fengycin homologues
plipastain 是fengycin 的一类重要同系物,其氨基酸序列为L-Glu-D-Orn-L-Tyr-D-allo-Thr-L-Glu-D-Ala/Val-L-Pro-L-Gln-D-Tyr-L-Ile[116]。plipastain 同样包含几种不同的同构型,plipastain A 和plipastain B 在第6 位氨基酸分别为 D-Ala 和 D-Val[117]。Ma 等[118]从B.amyloliquefaciensSH-B74 的发酵液中分离鉴定出plipastain A1,其氨基酸序列为L-Glu-D-Orn-L-Tyr-L-Glu-D-Ala-L-Pro-L-Gln-D-Tyr-L-Ile。Gao 等[116]通过单个结构域缺失策略来设计plipastain 的生物合成途径,生成了新型的线性五肽、六肽的plipastain 衍生物。将plipastain 合成酶的TE 结构域前移到上一个模块的T 域位置,从而合成预测的线性肽链plipastain 衍生同系物,同时揭示了plipastain TE 结构域在NRPS 合成酶系中的区域选择性[119]。
4.4 达托霉素
达托霉素是钙依赖性环状脂肽类抗生素A21978C 组分中的一种,最初从玫瑰孢链霉菌(S.roseosporus)的发酵液中分离出来,对多种革兰氏阳性菌均显示出优异的活性,但对革兰氏阴性菌则无活性。达托霉素和脂肽A21978C 组的所有其他成分是通过相同的模块化非核糖体合成酶系统合成的,并包含相同的肽部分。它们之间唯一不同的结构部分是N 末端连接的脂肪酰基残基。常见肽段包含13 个氨基酸,其中6 个非蛋白质氨基酸:D-Asn2,鸟氨酸(Orn6),D-Ala8,D-Ser11,(2S,3R)-谷氨酸甲酯(MeGlu12)和犬尿氨酸(Kyn13)。C 末端的10 个氨基酸形成一个大环核心,该核心在Thr4的侧链与C 末端Kyn13的α-COOH 之间包含一个闭环酯键。N 末端三肽从环突出,并带有可变的脂肪酰基残基,该残基与Trp1相连[120]。脂肪酰基残基的性质会影响抗菌活性和毒性,其衍生物的挖掘也主要通过改变不同的脂肪酸侧链来进行,而氨基酸的改变往往导致活性和产量的下降[121]。发酵过程中通过外源添加不同的脂肪酸或脂肪酸酯可以被反异构十一烷酰、反式十二烷酰、反异构十三烷酰等基团替代,得到新的达托霉素型衍生物[122]。达托霉素同系物见表6。

表6 达托霉素及其同系物Tab.6 Schematic diagram of daptomycin and its homologues
4.5 伊枯草菌素
伊枯草菌素是一种主要由芽孢杆菌产生的抗生素环脂肽,具有溶血和抗真菌的特性。伊枯草菌素的肽链包含7 个氨基酸,经典的氨基酸序列为 L-Asn-D-Tyr-D-Asn-L-Gln-L-Pro-D-Asn-L-Ser,其中第5 位和第7 位氨基酸可变性较强[123]。伊枯草菌素包含众多的同系物,包括iturin A、iturin C、iturin D、bacillomycin D、bacillomycin F、mycosubtilin。目前虽然对伊枯草菌素模块与结构域间的作用已经研究清楚,但对于修饰改造其肽链氨基酸生成新型同系物的研究还比较少,因此在未来的研究中可尝试针对性的研究。伊枯草菌素同系物见表7。

表7 伊枯草素同系物化学结构Tab.7 Chemical structure of iturin homologues
脂肽家族成员众多,除了上述5 种环脂肽外,对其他脂肽结构域的改造也有许多研究,既包括常见的结构域替换、删除,也有对其进行点突变和模块融合的研究。通过对氨基酸激活模块以及脂肪酸整合模块进行修饰和再造,可以得到一些活性或产量提高的产物、有用组分增大的同系混合物以及新型脂肽等。
5 混菌对脂肽生物合成的影响
目前,人工混菌研究已从混菌组成的生态关系向提升混菌合成功能产品的效率方向发展。针对脂肽生物活性物同系物组分多、功能可控性差、产量低问题,进行人工微生物混菌系统的构建,可以解决前体物质水平与脂肽同系物复杂性之间的关系,同时可能提高多细胞体系的代谢功能和效率,实现纯培养微生物无法完成的任务。在群体效应等细菌群体行为调控机制中,链霉菌可接受其他细菌产生的小分子信号物质,以及在环境胁迫等多重压力下可自发激活次级代谢产物合成基因簇的表达[124]。Steptomyces endusS-522 和Tsukamurella pulmonisTP-B0596的共培养,可诱导产生新的抗生素alchivemycin A[125]。将环境中产生表面活性素的地衣芽孢杆菌和假单胞菌菌种与生物膜形成菌株(铜绿假单胞菌和无病李斯特菌)混合发酵可以促进表面活性素产量的提升[126]。Woźniak‑Karczewska 等[127]发现不同菌群间的群体效应和混菌培养影响生物表面活性素同系物的形成。混菌体系的丰富性也赋予其更强的生物防治、石油降解等能力。B.amyloliquefaciensACCC11060和T.asperellumGDFS1009 共培养,使抗菌脂肽对真菌B.cinerea抑制能力的显著提升[128]。B.subtilisSPB1 和A.radioresistens RI7 菌株混合培养时,可将柴油降解率提高到55.4%[129]。人工构建脂肽合成的生态系统(多细胞体系)将扩大脂肽类物质的生产和应用潜能。
6 合成生物学用于脂肽合成的研究
合成生物学是一门综合的学科,以传统生物学获得的知识和材料为基础,利用系统生物学的手段对其加以定量的解析,在工程学和计算机的指导下设计新的生物系统或对原有生物系统进行深度改造。由于NRPSs 多模块多酶的复杂性,导致来自非核糖体肽合成酶的新次生代谢产物的组合生物合成一直处于缓慢发展。环脂肽类天然产物含有多种组分,其组成和结构影响整体生物活性[130]。运用合成生物学策略对非核糖体肽合成酶异源表达实现环二肽的生物合成[131],由3 个非核糖体肽合成酶(OctA、OctB、OctC)合成的脂肽(octapeptin,八肽菌素)能有效抗革兰氏阴性耐药菌[9]。对NRPS合成操纵子的生物信息学分析可以较为直观地分析不同脂肽同系物合成序列的差异,将组合生物合成技术与序列比对、同源建模等方法结合起来,定向地对NRPS 合成酶进行改造,从而达到精准合成预测产物的目的。
随着基因组装技术的发展,更加灵活和精准的方法应用于脂肽合成中模块结构域的改造,距离人工设计脂肽肽链构型生物精准合成的目标也日益趋近。Yan 等[49]基于type IIS 限制性内切酶酶切克隆的方法创造了通过质粒高效组装NRPS 生产线的方法,可以轻松实现对各功能结构域的替换,促进了新型生物合成基因簇的开发和药物发掘。因此,运用合成生物学策略合成NRPSs的标准化元件和模块生产新结构脂肽,结合微生物基因组挖掘将扩大NRPS源天然产物药物范围和提升新药的发现速度,利用合成生物学在工程化的酿酒酵母中设计完成多细胞真菌复杂的生物合成,将加快非核糖体肽抗生素理性工程化合成。此外,利用合成生物学思想设计与构建基于前体物导向和脂肽合成模块的不同功能分工的人工细胞,通过群体机制反馈指导不同分工细胞内模块的集成原则,提高菌群协作和性能也将促进生物合成脂肽类活性物质的开发。
7 总结与展望
环脂肽作为抗生素、生物表面活性剂等,在生物防治、药物开发、环境修复和疾病治疗等方面广泛应用,具有迫切的市场需求和广阔的发展前景。特别是脂肽类抗生素因其临床耐药菌株的出现概率极低、可生物降解、多生物活性(抗菌、抗肿瘤、抗病毒等)、无交叉耐药性等特点,在抑菌药物中引起广泛关注,预计未来10 年批准用于临床的脂肽类抗生素的数量将会不断增加[20]。同时,脂肽的生物合成还存在产量低、多种同系物共存以及产品和菌株特性造成的发酵过程难控等问题,限制脂肽类抗生素的工业化和商品化生产。本文综述了环脂肽生物合成的研究进展,为进一步研究和开发脂肽类的应用提供依据。
目前,利用微生物生产脂肽类天然产物还存在一些困难,其中包括:①很多生产菌不能被培养,或是不能进行基因改造;②具有功能的潜在的生物合成基因簇(BGCs)需要进行克隆,或是通过合适的外源宿主进行表达和基因工程改造;③由于复杂的细菌以及分子量庞大的BGCs基因,进行克隆、途径改造和构建重组文库时存在困难;④在外源宿主中产量低,可能是由于转录效率低、蛋白质不正确折叠等原因。通过对野生菌株的实验室驯化,利用和开发先进的基因编辑工具,构建合适的外源宿主等方法可以加快脂肽类天然产物的开发,强化其生物合成过程,解决基因表达和产物合成中的一些难点问题。DNA测序技术的迭代发展为菌株基因组的解析和基因簇蛋白功能的分析创造了有利的条件,以合成生物学中“设计”“构建”“系统”“标准化”的工程化思想为指导构建脂肽合成的人工细胞是今后研究脂肽物质生物合成的重要方向。
环脂肽多组分同系物严重限制它们的应用,特别是在生物医药领域的应用。就脂肽同系物组分人工调控而言,无论是不同功能结构域与同系物组分的相关性,还是前体供给与脂肽同系物组分和功能间的关系,有关获取脂肽单一组分的调节机制尚不清楚,特别是人工微生物混菌系统来调控脂肽同系物组分的研究尚未见报道,因此,进行底盘优越的人工合成体系的研究势在必行。建立脂肽多组分同系物生物合成的人工调控策略,获得可控的单一组分脂肽,提高其抗菌活性、降低脂肽同系物组分的生物毒性,具有重要理论意义和实际价值。因此,在今后的研究工作中,有必要开展脂肽同系物单一组分生物合成人工调控的分子机制研究,为寻求脂肽同系物单一组分可控、高效合成的人工混菌系统工程改造和构建提供理论依据。为扩大环脂肽的应用领域,利用合成生物学技术开展原料高效利用、复杂底物响应机制和代谢途径优化研究,寻找廉价底物用于环脂肽的合成,将是降低环脂肽生产成本的重要途径之一。此外,脂肽类物质在反应器放大培养过程中还存在泡沫多、发酵过程稳定性差等问题,对发酵设备、发酵工艺和过程调控都具有较高的要求,通过设计和运用新型消泡生物反应器可以有效强化脂肽产品的发酵过程和提高过程的稳定性。随着合成生物技术的迅速发展和运用,结合传统的代谢工程和发酵工程手段的延伸,应用于脂肽类天然产物的微生物合成也有望实现产品“质”和“量”的提升。
致谢:谨以此文致敬Daniel I.C.Wang 教授在基因工程及生化工程等领域的开创性贡献。
