彩色多普勒超声引导下局部加压联合凝血酶注射治疗假性动脉瘤3例
2021-09-24郝艳红刘逸凡张炎晶刘静静杨光照
郝艳红,刘逸凡,张炎晶,刘静静,陈 武,杨光照
近年来,随着血管内微创技术的发展以及围术期高效抗凝药物的应用,医源性假性动脉瘤成为临床中较为常见的并发症。如果对假性动脉瘤不进行及时有效的诊治,有可能发生动脉瘤的破裂、血栓栓塞,以及由此引发的临床相关肿胀、压迫等严重后果。既往临床多采取手术方式治疗假性动脉瘤,但这些方法创伤大、临床并发症多,因此,微创技术逐渐应用于假性动脉瘤的治疗。目前临床中对假性动脉瘤的各种腔内微创治疗方法已经获得了许多成功治疗的经验[1-2],本研究旨在探讨超声引导下瘤口经探头加压并经皮凝血酶注射对医源性假性动脉瘤治疗的有效性和安全性。
1 资料与方法
1.1 临床资料 选取2018年5月—2019年5月在我院心血管内科因急性冠状动脉疾病行经外周动脉径路选择性冠状动脉造影和冠状动脉介入术后假性动脉瘤病人3例,均为女性,年龄40~76岁,平均61岁。假性动脉瘤位于穿刺动脉穿刺点附近,患肢肿胀、疼痛及皮肤瘀斑,局部伴有搏动性肿块,听诊可闻及吹风样血管杂音。3例中1例为股总动脉旁假性动脉瘤,2例为肱动脉旁假性动脉瘤。瘤体大小(4.3×1.8) cm~(5.1×3.1) cm;瘤口直径0.28~0.65 cm,瘤口区域入瘤流速118~372 cm/s,出瘤流速70~156 cm/s。2例瘤体内血栓形成,1例肱动脉旁假性动脉瘤为多腔假性动脉瘤,多个囊腔间可见瘘口相连,近端瘤口处可见典型的来回型血流频谱,距离越远瘤口处入瘤血流速度越低,最表浅瘤腔内仅可见经瘘口的出瘤血流信号,流速较低。 详见图1~图3。

图1 肱动脉旁假性动脉瘤(可见肱动脉血流经瘤口进入假性动脉瘤瘤腔内)

图2 复杂假性动脉瘤(可见多个瘤腔,瘤腔之间有瘤口相通,瘤腔内可见来回型血流)
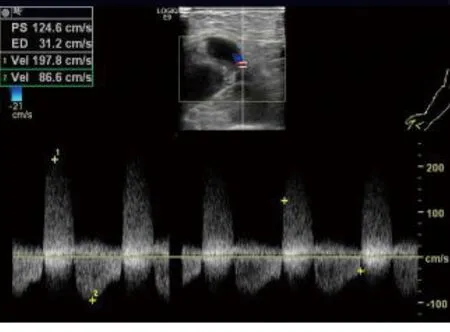
图3 假性动脉瘤(瘤口处血流频谱)
1.2 仪器与方法 使用GE Logiq E9彩色多普勒超声诊断仪,探头频率7~10 MHz,5 mL注射器,凝血酶采用湖南一格制药有限公司生产的凝血酶冻干粉(每支500 U),操作前以0.9%氯化钠注射液稀释成200 U/mL[3]备用。病人平卧位,充分暴露受检肢体,观察假性动脉瘤体表投影区附近皮肤表面有无破损或感染,观察瘤体大小、形态、数目,必要时行超声造影检查除外局部动静脉瘘。治疗操作前充分与病人沟通,选取载瘤动脉长轴并同时显示瘤口和瘤体最大切面,通过彩色多普勒超声观察瘤体内血流方向及测量瘤口处流速。探头于瘤口处垂直皮肤表面加压,通过彩色多普勒超声观察瘤口处血流能否被阻断及病人承受能力[4]。选择好穿刺路径、床边备肾上腺素等急救药品后,用2%利多卡因对穿刺路径局部浸润麻醉,采用平面外进针法,探头用上述方法垂直皮肤表面加压至尽量压闭瘤口而载瘤动脉血流动力学不发生明显变化时,将穿刺针头刺入瘤体顶端流入道处并远离瘤口;1例多瘤腔瘤体选择穿刺对象为第1个瘤腔,另2例病人瘤体内可见周边血栓形成,穿刺时应避开血栓区域,以免造成无效注射。超声引导穿刺到位后快速注入凝血酶1 mL,二维超声观察到瘤腔内即刻形成的线样纤维素高回声,在瘤腔内短暂旋转后凝聚成高回声血栓团,超声观察瘤腔内完全形成血栓时注射终止。注射凝血酶过程中密切关注病人患肢皮肤反应,预防过敏反应发生。待瘤体内血栓稳定后切换至彩色多普勒模式观察瘤腔内有无残留血流存在,同时检测载瘤动脉远端(腕部或踝部)血流频谱参数。治疗后用弹力绷带持续轻微加压6 h并卧床休息,24 h后复查患肢血管超声。
2 结 果
本组3例假性动脉瘤超声引导下瘤口加压经皮穿刺凝血酶注射1 mL后瘤腔均栓塞成功,瘤体内及瘤口部位血流信号消失,多腔瘤体经治疗第1个瘤腔后远端瘤腔内也形成完全栓塞,3例治疗时间均在2 min以内。1例肱动脉旁假性动脉瘤病人因载瘤动脉近心端血流频谱呈低阻力改变,操作前超声造影证实无动静脉瘘形成。所有病人治疗后24 h复查瘤体及瘤口处未见血流信号显示(见图4)。3例病人操作中均未发生凝血酶过敏反应,未发生载瘤动脉远端动脉急性栓塞等并发症,治疗后未见复发、感染等。所有病人治疗后随访1~3个月,均未见复发。

图4 凝血酶注射治疗后24 h复查彩色多普勒血流显像
3 讨 论
医源性假性动脉瘤是血管损伤的并发症,随着介入微创技术的广泛开展,各种大口径管、鞘的运用及围术期抗凝药物的使用和穿刺人员技术水平的差异,使医源性假性动脉瘤的发生率明显增加,成为临床上最常见的并发症[5]。假性动脉瘤的形成是指动脉壁部分破裂后,血液外溢在血管破口周围形成血肿,血肿被周围纤维组织包裹形成囊壁,因动脉搏动的持续冲击力,使血管破口与血肿相通形成搏动性血肿。与真性动脉瘤不同,假性动脉瘤不具备动脉血管的外膜、中层弹力纤维和内膜三层结构。有研究认为,假性动脉瘤一般不能自愈,可出现压迫、栓塞或自行破裂、急性动脉系统栓塞或出血后果严重,因此,早期确诊并采取适当的治疗措施显得尤为重要[6]。
针对假性动脉瘤的微创治疗临床已经有多种尝试,如植入腔内移植物、弹簧圈栓塞、腔内球囊封闭裂口联合经皮假性动脉瘤腔内凝血酶注射、腔内球囊压迫止血等多种微创手段,但上述方法仍存在相对创伤大、病人经济负担重等弊端[7]。蓝春勇等[8]超声实时监测下通过徒手揉压法压迫瘤口对假性动脉瘤进行修复,取得满意疗效,但对肿胀肢体的揉压时间至少需要10 min,部分病人因肢体肿胀不能耐受外力压迫引起的疼痛而导致修复失败。本研究采用超声引导下瘤口处压迫经皮穿刺凝血酶注射治疗假性动脉瘤,明显缩短了治疗时间,病人易于耐受。多数学者采用平面内进针法[9],平面内进针法可以清晰显示瘤体表面及浅层的软组织结构,可以实现安全精准的进针路径同时保证对病人的损伤达到最低。经皮腔内注射凝血酶是近年来假性动脉瘤治疗方面的新进展,但凝血酶为牛血或猪血中提取的凝血酶原经激活而获得的局部止血药物,可引发过敏反应、动脉远端血栓形成等并发症[10],因此,在临床的广泛使用受到一定的限制。本组3例病人治疗过程中虽无一例发生过敏反应,但治疗前仍然需要使用必要的抗过敏药物。
本组3例病人均为经外周动脉冠状动脉造影术后1~3 d出现穿刺动脉所在肢体肿胀,2例病人有明显局部搏动性肿块,听诊有杂音;1例肱动脉旁假性动脉瘤病人主要表现为肢体肿胀、皮肤瘀斑,早期未闻及杂音,3 d后肿胀减轻但听诊可闻及杂音,可触及搏动性包块。考虑本例病人假性动脉瘤瘤体形态为多腔豆荚样,且瘤体表面有较厚的上肢肌肉组织覆盖,加之局部肿胀病人触痛明显,导致体征不明显未引起临床重视,仅在怀疑血栓行常规上肢血管超声检查时发现瘤体存在。3例病人均在超声明确诊断假性动脉瘤后第2天实施超声引导下的凝血酶注射治疗。超声引导下经平面外进针,与传统的X线片引导下微创介入技术相比较,不仅能实时显示针尖位置,而且能更全面地观察到目标区域周围的组织结构及其与穿刺针的关系,有利于防止损伤其他组织结构,同时使穿刺路径最短,对病人损伤最小[11]。
1例肱动脉旁假性动脉瘤注射凝血酶时超声显示瘤腔内凝血酶入血后即刻形成血栓纤维条索,同时极微量血栓纤维经瘘口进入肱动脉远段,瘤腔内血栓形成迅速,并封闭瘘口,未见血栓纤维继续进入血管远段。操作过程中密切观察病人上肢反应,治疗后彩色多普勒血流显像显示瘤腔内未见血流信号显示,上肢动脉远段检查见血流充盈好,血流频谱形态正常,呈三相波形。治疗后24 h复查彩色多普勒血流显像,患肢水肿程度减轻,动脉血流充盈好,血流频谱形态正常,呈三相波形,且病人自述无明显不适。多项研究强调凝血酶注射治疗有可能引起远端肢体动脉内血栓形成,但本研究3例病人无一例出现远端动脉血栓,推测穿刺针位置选择在假性动脉瘤血流流入道且经瘤口进入远端动脉管腔内的血栓纤维素数量极微小,正常人体血液中存在凝血-纤溶平衡体系,以及病人围术期抗凝药物的应用使远端动脉栓塞不易发生。同时瘤口处适当加压,有利于阻断载瘤动脉与瘤体之间的通道,实现瘤腔内封闭环境加快血栓形成。对于较复杂瘤腔,比如瘤颈位置较深不易在瘤颈处加压的病例,改良加压法可以实现同样的瘤口处加压的效果[12]。姚佐懿等[13]认为,复杂假性动脉瘤首选在远端瘤腔的底部,认为靠近载瘤动脉的瘤腔穿刺困难,同时注射凝血酶速度宜慢,本研究中1例为多腔复杂假性动脉瘤,载瘤动脉为肱动脉,凝血酶注射近载瘤动脉瘤腔后中远端瘤腔内也迅速形成血栓。因此,复杂假性动脉瘤近端瘤腔较易穿刺时可以其作为首选穿刺瘤腔。凝血酶注射速度应适度[14-15],速度过慢易导致针尖周围血栓封堵,导致无效注射。
本研究假性动脉瘤凝血酶注射治疗结果显示,超声引导下瘤口局部加压联合凝血酶注射治疗在假性动脉瘤修复中具有经济、安全、有效的优势。但是本研究病例数少,超声引导下凝血酶注射治疗假性动脉瘤可能的并发症理论上依旧不可避免,还需加大样本量进一步研究。血管内微创技术的开展在超声引导下进行可精准、安全地施行血管穿刺技术,有助于进一步降低假性动脉瘤的发生率,但这一观点尚需进一步研究证实。
