慢阻肺首次急性加重后5年死亡的危险因素分析
2021-09-24侯会娜
侯会娜
慢阻肺是一种严重影响人类健康的常见呼吸道疾病,到2020年,慢阻肺的社会和经济负担将上升至第五位,成为全球第三大死亡原因[1]。关于慢阻肺的一项大型调查包括七个地区和20245名成年人,结果显示在中国40岁以上的人群中,慢阻肺的患病率高达8.2%[2]。平均每位慢阻肺患者每年有0.5~3.5次急性加重,是患者死亡的主要原因[3]。一项流行病学研究,在中国慢性阻塞性肺疾病急性加重(Acute exacerbation of chronic obstructive pulmonary disease,AECOPD)患者每年的住院费用为11 598元[4]。特别是对于住院期间死亡的患者,其高昂费用与生命支持治疗有关[5]。AECOPD增加了社会负担,并且对患者的生活质量、肺功能和疾病进展产生负面影响,本文主要分析影响AECOPD预后的危险因素,识别潜在的死亡风险因素有助于改善患者的治疗方案,延长生存时间。
资料与方法
一、 研究对象
回顾性分析2012年1月至2015年6月在我院呼吸内科诊断为慢阻肺急性加重的患者523例,男363例,女160例,年龄(67.4±12.5)岁。纳入标准:①患者的诊断标准符合《慢性阻塞性肺疾病诊治指南(2013年修订版)》[6];②第一次因急性加重入院治疗。排除标准:①合并肺结核、哮喘等肺部疾病;②严重肝肾功能障碍者;③合并血液系统性疾病;④合并其他感染性疾病;⑤失访患者。本研究经过医院伦理委员会批准,患者知情并签署知情同意书。
二、 资料收集
收集患者的一般临床资料,主要包括:年龄、性别、是否吸烟、病程、住院天数、体重指数和呼吸支持情况。生化检测指标,主要包括:中性粒细胞比例,红细胞、白细胞和血小板计数,血红蛋白和白蛋白浓度、谷丙转氨酶、谷草转氨酶、血清肌酐、抑胱素c、尿素氮、纤溶酶原、国际标准化比值、D-二聚体和痰细菌/真菌培养。血气分析检测指标,主要包括:PH值、PaO2、PaCO2、PaO2/FiO2。合并症主要包括:高血压、糖尿病、缺血性心脏病、心力衰竭、肺源性心脏病、肺动脉高压、肺炎、肺栓塞、支气管扩张、肺癌和脑血管病。完成随访时间为2020年6月,以患者死亡或随访时间结束为随访终点,主要记录患者随访结束时的生存状况、死亡时间和死因。
三、 统计分析
应用SPSS21.0软件行统计分析,计数资料组间比较采用卡方检验,符合正态分布的计量资料组间比较采用独立样本t检验,非正态分布的计量资料以M(P25~P75)表示,组间比较采用秩和检验,Kaplan-Meier法计算生存率,应用log-rank法检验,Cox多因素回归分析影响患者5年存活率的危险因素,以P<0.05为差异有统计学意义。
结 果
一、 患者基本的临床资料
两组患者在性别、病程、吸烟、住院天数、体重指数和呼吸支持之间差异无统计学意义(P>0.05),死亡组年龄大于存活组,组间差异有统计学意义(P<0.05)(见表1)。
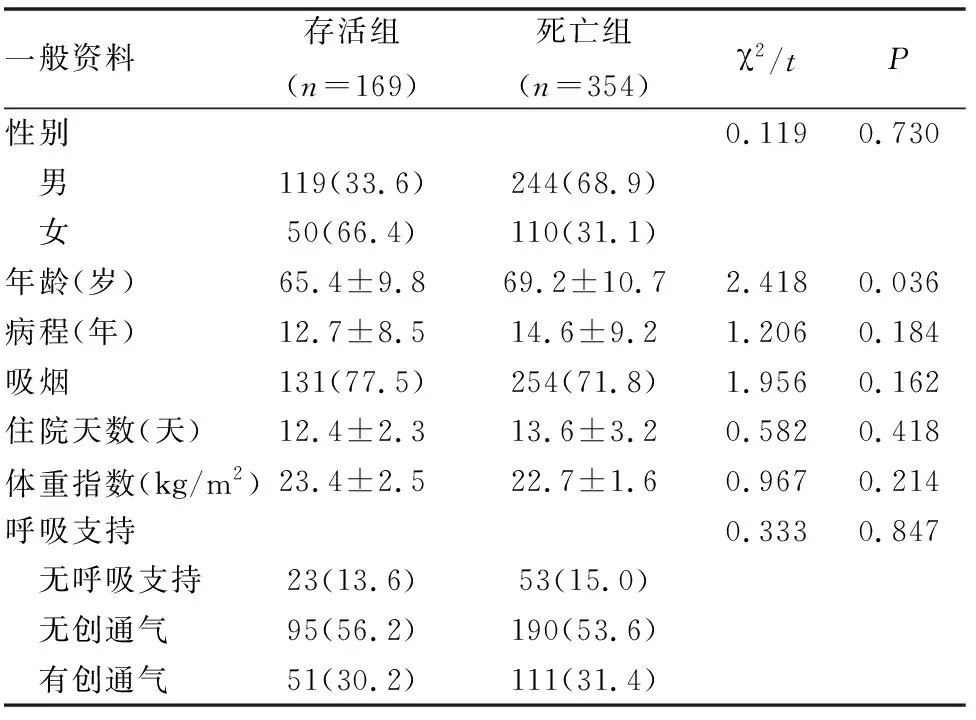
表1 两组患者一般临床资料比较
二、 两组患者生化检测指标的比较
死亡组中性粒细胞比例、白细胞计数、血清肌酐高于存活组,血红蛋白浓度和白蛋白浓度低于存活组,痰细菌培养阳性和痰真菌培养阳性患者比例高于存活组,其他指标之间差异无统计学意义(见表2)。
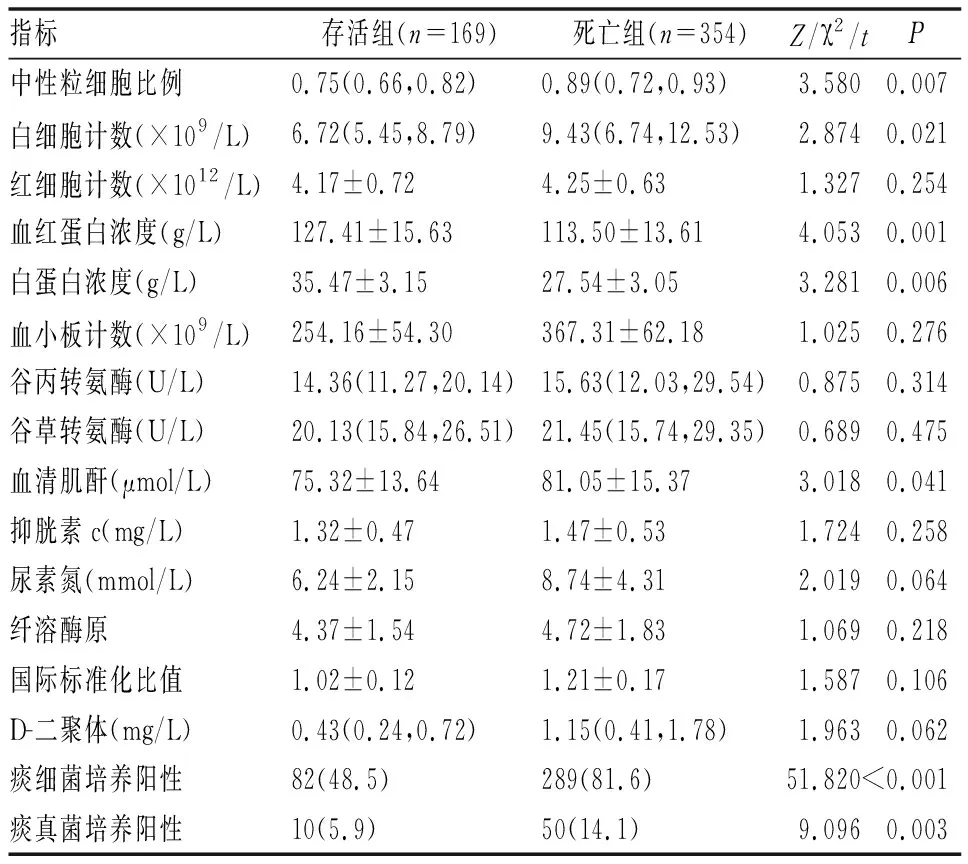
表2 两组患者实验室检测指标的比较
三、 两组患者血气分析比较
两组患者的PH值、PaO2、乳酸浓度和PaO2/FiO2之间无统计学差异,死亡组PaCO2高于存活组(P<0.001)(见表3)。

表3 两组患者血气分析比较
四、2组患者合并症的比较
死亡组患者伴随脑缺血心脏病、心力衰竭、肺源性心脏病、肺炎、肺癌和脑血管病的比例高于存活组,其他合并症之间差异无统计学意义(见表4)。
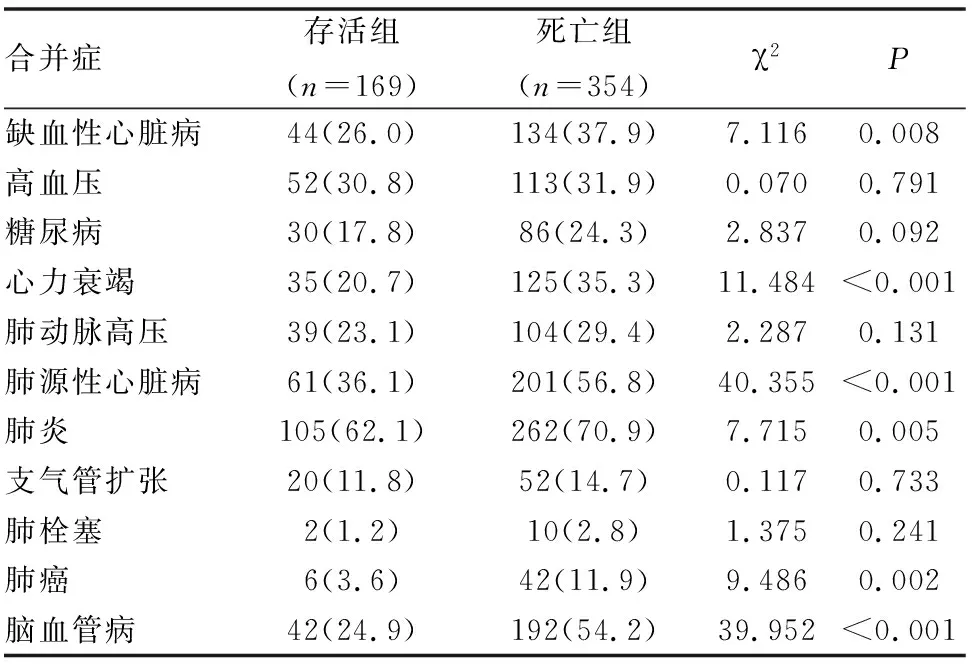
表4 两组患者合并症的比较
五、 Cox多因素回归分析影响慢阻肺疾病急性加重后5年死亡的危险因素
将表1-4中的因素行Kaplan-Meier法计算生存率,并用log-rank法检验,结果显示年龄(<60岁vs.>60岁)、中性粒细胞比例(<0.7vs.>0.7)、白细胞计数(<10×109/Lvs.>10×109/L)、血红蛋白浓度(<110g/Lvs.>110g/L)、白蛋白浓度(<35g/Lvs.>35g/L)、血肌酐(<70μmol/Lvs.>70μmol/L)、D-二聚体(<0.5mg/Lvs.>0.5mg/L)、痰细菌培养(阳性vs.阴性)、痰真菌培养(阳性vs.阴性)、PaCO2(<40 mmHgvs.>40 mmHg)、缺血性心脏病(有vs.无)、糖尿病(有vs.无)、肺癌(有vs.无)、脑血管病(有vs.无)间慢阻肺疾病急性加重后5年死亡率均有统计学差异。将以上因素带入Cox多因素回归模型中,结果显示年龄、白蛋白浓度、痰细菌培养阳性、心力衰竭和肺癌为慢阻肺患者首次急性加重后死亡的危险因素(见表5)。
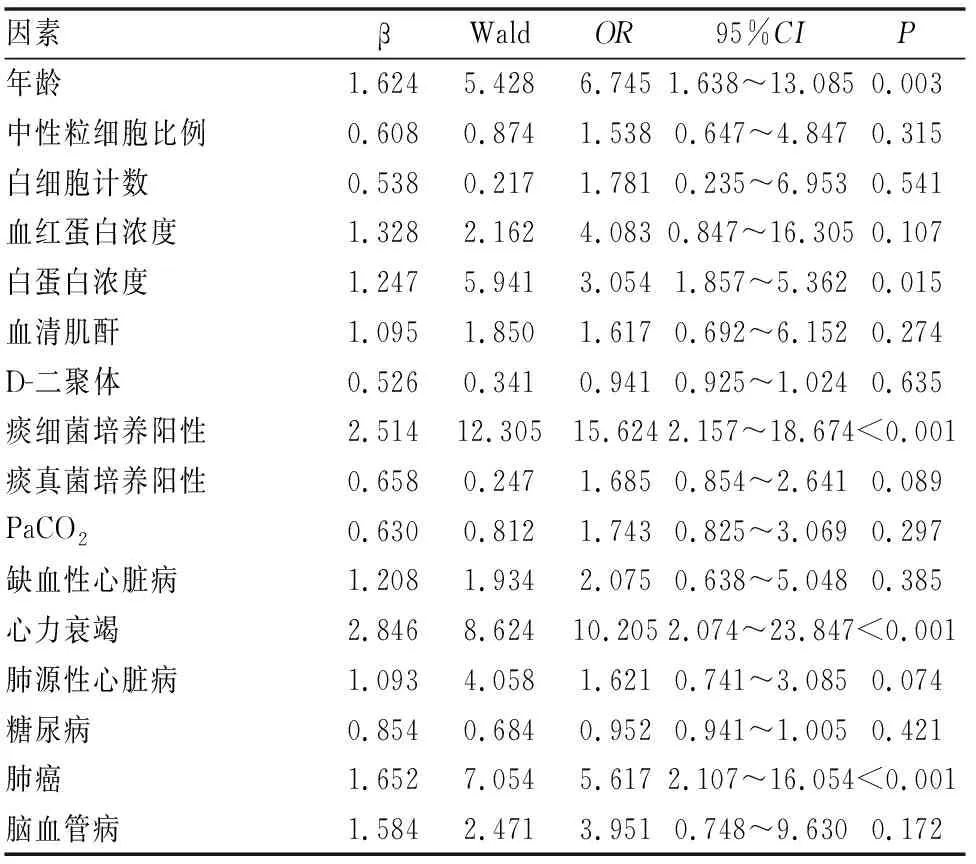
表5 Cox多因素回归分析
讨 论
AECOPD与呼吸道症状的急性恶化相关,严重影响慢阻肺的预后。AECOPD会进一步增加疾病加重的频率、降低健康状况、加速肺功能下降和增加死亡率,给患者带来巨大的经济负担[3]。考虑到AECOPD在COPD患者的预后中的重要作用,因此加重期间早期和准确的个体死亡风险评估,对临床管理和优化分配医疗资源至关重要。寻找AECOPD入院后具有临床意义的死亡率预测指标,具有重要的临床价值[7]。一项纳入757例慢阻肺患者住院后1年和5年病死率分别为26.2%和64.3%[8]。本研究共纳入543例AECOPD患者,随访5年后354例患者死亡,病死率为65.2%,与García-Sanz等研究结果相似。而Chung等[9]报告,AECOPD住院后接受无创机械通气治疗的5年死亡率为74%,另外一项研究[10]显示在ICU接受治疗的AECOPD患者5年死亡率为76%。本研究患者的5年死亡率略低于以上两项研究,可能与患者病情严重程度不同相关。
本研究中,AECOPD患者死亡与年龄相关。Piquet等[11]研究显示,≥60岁的AECOPD与<60岁的患者相比,死亡风险增加2.99倍,年龄≥60岁是AECOPD患者死亡的危险因素。另有一项研究[12]表明年龄对AECOPD患者的近期和远期死亡率均有影响,年龄较大患者的死亡率明显增加,以上两项研究结果均与本研究结果相似。细菌或病毒感染是诱发AECOPD的常见原因,中国进行的一项多中心研究表明,884例AECOPD患者痰液细菌阳性率为37.4%[13-14]。在本研究中痰培养细菌阳性为AECOPD患者死亡的危险因素。慢阻肺可增加肺癌的发生,由其是长期吸烟的患者,肺癌发生的风险更高,同时肺癌也是慢阻肺死亡的常见危险因素[15]。慢阻肺因肺癌死亡的患者比例从4%~33%不等,可能与纳入的人群特征差异较大相关[16]。在本研究中,死亡组患者合并肺癌的患者占11.9%,在预后的分析中肺癌为AECOPD患者死亡的危险因素,合并肺癌的死亡风险增加4.617倍。慢阻肺患者也常合并心血管疾病,本研究中心力衰竭为AECOPD患者死亡的危险因素,可能与患者使用受体激动剂导致心脏性猝死或不稳定心绞痛相关。血清白蛋白是判断营养状况的一项常见指标,在许多危重症预后判断中也发挥一定作用[17]。AECOPD患者体内蛋白处于急速消耗的状态,血清白蛋白水平降低对AECOPD患者死亡评估具有一定的临床价值。
综上所述,本研究结果显示,年龄、白蛋白浓度、痰细菌培养阳性、心力衰竭和肺癌为慢阻肺患者首次急性加重后死亡的危险因素。本研究为回顾性分析,部分AECOPD患者住院时未完善肺功能的检查,对于患者的治疗用药情况未统计分析,对本研究的结果均有一定的影响,故在后续的工作中还需开展前瞻性研究,做更详细的实验设计,对本研究结果加以验证。
