糖类抗原125在预测肝细胞癌微血管浸润及预后中的应用价值探讨
2021-09-22胡方彬何小华
胡方彬,何小华
(四川省资阳市人民医院,四川 资阳 641300)
原发性肝癌是最常见的恶性肿瘤之一,其发病率在全球范围内仅次于肺癌,占癌症发生率的第二位[1]。而全球约一半的肝癌患者来自我国,每年约35万人死于肝癌,为我国居民的健康带来严重威胁[2]。作为原发性肝癌中发病率率最高的病理类型,肝细胞癌(HCC)具有恶性程度高,多浸润性生长等特点,在临床中,HCC患者多见癌细胞侵犯动静脉及胆管,手术切除率低,且术后极易复发和转移,严重影响HCC患者生存率。研究发现[3],微血管浸润(MVI)作为判断肿瘤侵袭性的重要指标,是肝癌发生转移的起始环节。因此,在术前对HCC患者是否发生MVI做出准确诊断,对于患者治疗方案的选择及预后均会产生积极的作用。术后标本的病理学检查是确定MVI的金标准,目前随着医疗学技术的发展,虽然通过多种医学影像技术在一定程度上能对MVI进行术前诊断,但由于其灵敏度及成本等因素的制约难以推广。寻找一种对HCC患者术前是否发生MVI进行诊断且易于检测的标志物具有重要的临床价值。血清糖类抗原125(CA125)是癌症最重要的肿瘤标志物之一。研究发现,CA125在直肠癌[4]、口腔癌[5]、胰腺癌[6]等多种肿瘤中异常表达,其在肿瘤的诊断、预后预测和疗效评估中发挥重要作用。本研究探讨术前CA125对HCC患者并发MVI的预测价值,为临床的诊断提供参考。
1 方法
1.1 一般资料2014年7月至2019年7月我院接受外科手术治疗的HCC患者186例,纳入标准:①年龄18~80岁;②病理诊断为原发性HCC;③肿瘤单发,肝功能储备正常,且肿瘤直径≤5 cm;④根据Child-pugh肝功能分级标准,为A、B、C级;⑤均为同一组医师在全麻下行肝癌切除手术,符合RO标准。排除标准:①癌细胞侵犯门脉主干、总胆管及其一级分支,肝静脉主干,或已发生肝外转移;②采集数据节点之前进行新辅助治疗或辅助治疗;③合并其他恶性肿瘤;④临床资料显示伴有严重心血管疾病。其中男114例,女72例;年龄38~80岁[(56.42±10.43)岁];按照国际抗癌联盟TNM分期标准第8版[7]:Ⅰ~Ⅱ期110例,Ⅲ~Ⅳ期76例;组织分化程度:低分化99例;中分化54例,高分化33例。患者及家属均知情同意并积极配合,本研究已经我院伦理委员会审批通过。
1.2 分组MVI诊断标准:根据中华人民共和国国家卫生和计划生育委员会《原发性肝癌诊疗规范(2017年版)》中的相关标准[8],术前影像学图像无血管内癌栓征象,术后病理大体标本未见血管侵犯迹象,仅显微镜下于内皮细胞衬覆的血管腔内见到癌细胞巢团(≥50个癌细胞),其中主要是含有包膜内血管的门静脉分支。根据术后标本病理诊断是否并发MVI将患者分为MVI组(n=72)和非MVI组(n=114)。
1.3 检测方法在本院电子病历系统中选择患者接近手术日期3~7天的清晨血常规及血液生化指标进行分析;所有患者血液生化指标包括空腹血糖(FPG)、总三酰甘油(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)、糖化血红蛋白(HBA1c)、丙氨酸氨基转肽酶(ALT)、天冬氨酸氨基转肽酶(AST)、血肌酐(Scr)、超敏C反应蛋白(hsCRP)、尿素氮(BUN)通过本院全自动生化分析仪(Beckman Coulter AU-680)检测,甲胎蛋白(AFP)检测采用比浊法血小板计数;血小板计数(PLT)、白细胞计数(WBC)、中性粒细胞计数(NEUT),淋巴细胞计数(LY)采用流式细胞仪(迈瑞6900)进行计数,所有样本排除感染因素。采用雅培Ci162000全自动生化免疫测定系统检测血清CA125、异常凝血酶原(PIVKA-II)水平,试剂盒购自上海雅培生物科技有限公司,所有检测检测均严格按照仪器使用说明操作。
1.4 随访经门诊、复查、再住院、电话等方式对所有入选患者进行2年随访。术后每3个月来院行肝功能、肝脏超声、肝脏增强CT、MRI检查和AFP等检查,根据临床及影像学检查,判断是否肝内复发或肝外转移,并记录无事件生存时间,其定义为术后至再次确诊复发、肿瘤相关性死亡或随访结束的时间。
1.5 统计学方法采用SPSS 20.0软件分析数据。计数资料以百分比表示,组间比较采用χ2检验;诊断价值分析采用受试者工作特征曲线(ROC);危险因素分析采用Logistic多因素回归分析,根据CA125的临界值对患者进行危险分组,采用Kaplan-Meier生存分析法比较不同分组患者的无事件发生率。P<0.05为差异有统计学意义。
2 结果
2.1 MVI组和非MVI组临床资料比较两组ALT、AST、AFP、HsCRP、PIVKA-II、CA125、WBC、NEUT、LY、TNM分期、分化程度、肿瘤直径比较,差异有统计学意义(P<0.05),其他临床指标比较,差异无统计学意义(P>0.05),见表1。
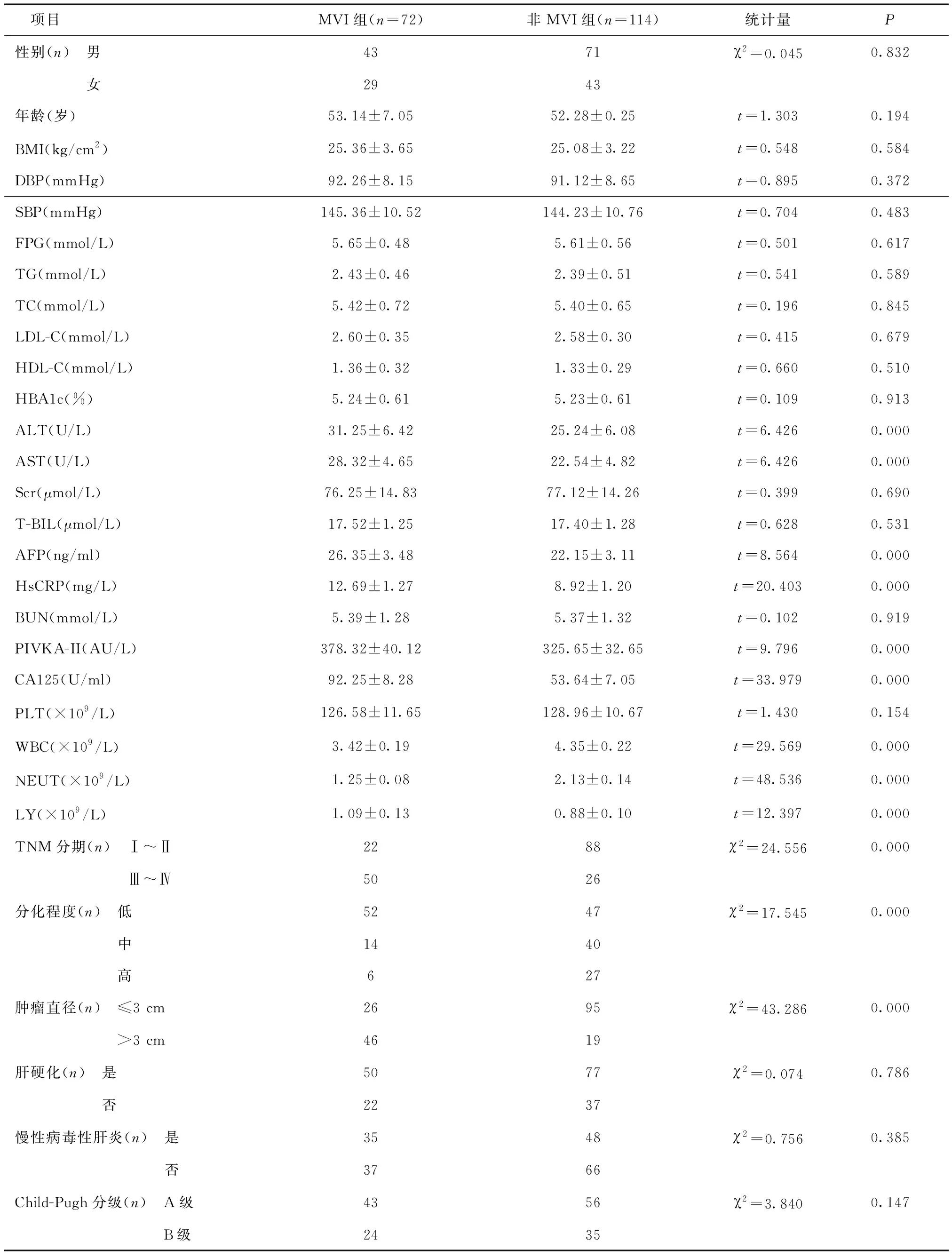
表1 MVI组和非MVI组临床资料比较
2.2 HCC患者并发MVI的危险因素分析ALT、AFP、PIVKA-II、CA125、WBC、TNM分期、组织分化程度、肿瘤最大直径是HCC患者发生MVI的独立危险因素(P<0.05),见表2。

表2 HCC患者并发MVI的危险因素分析
2.3 各危险因素对HCC患者并发MVI的预测价值分析ALT、AFP、PIVKA-II、CA125、WBC、TNM分期、分化程度、肿瘤最大直径诊断MVI的截断值分别为28.22 U/L、26.32 ng/ml、361.23 AU/L、79.629 U/ml、4.02×109/L、Ⅲ期、低分化程度、2.86 cm,曲线下面积分别为0.726、0.698、0.716、0.884、0.821、0.801、0.782、0.632,其中CA125敏感度为95.46%,特异度为75.18%,诊断价值最大,见表3。

表3 ROC曲线分析多指标对MVI的预测价值
2.4 不同CA125水平患者各危险因素比较根据CA125预测MVI的最佳临界值将患者分成CA125≤79.62 U/ml组(n=77)和CA125>79.62 U/ml组(n=109)。CA125≤79.62 U/ml组AFP、PIVKA-II水平及肿瘤最大直径小于CA125>79.62 U/ml组,WBC水平、TNM低分期和高分化程度占比大于CA125>79.62 U/ml组,见表4。

表4 不同CA125水平患者各危险因素比较
2.5 不同CA125水平患者预后分析CA125≤79.62 U/ml组中位无事件生存时间为9.56个月,CA125>79.62 U/ml组为7.05个月,两组生存曲线经时序检验,差异有统计学意义(P<0.05)。
3 讨论
HCC具有特殊的临床病理特点及生物学行为,HCC常伴有血管浸润及肝内转移。研究发现[9],MVI与肝内病灶转移密切相关,且多项研究指出,MVI是影响原发性肝癌患者生存和复发的独立危险因素,所以MVI目前作为HCC侵袭性及恶性程度的重要标志。随着对肿瘤侵袭的分子机制相关研究的深入,越来越多的研究表明,肿瘤的发生、发展与机体的免疫反应系统密切相关[10]。免疫反应下降可提高肿瘤细胞增殖能力,通过降低DNA损伤的突变的预防能力,抑制了癌细胞的凋亡,对于提高肿瘤细胞的侵袭能力具有重要意义。
CA125首先在上皮性卵巢癌患者被发现,随着研究的深入,近年来研究发现,CA125在食管癌、肺癌、子宫癌等多种癌症中差异表达[11~13],并且其被证实在肝癌转移或者存在腹水患者的血清中CA125呈高表达状态。有研究发现,CA125可参与肿瘤上皮间质转化(EMT),而EMT是肿瘤细胞增殖和转移发生的重要机制之一[14]。此外,有研究表明[15],CA125可通过与肿瘤血管内皮细胞相互作用,促进血管的生长。此外还有研究发现[16],CA125水平对于肝癌放化疗水平不敏感,相比与低水平CA125患者,CA125水平升高患者更容易发生癌细胞转移。鉴于CA125与肿瘤预后的密切关系及MVI在肿瘤复发中的作用,本研究提出利用CA125预测肝癌患者MVI发生的可能性。采用ROC曲线分析CA125对HCC患者发生MVI的诊断价值,结果显示曲线下面积为0.884,截断值为79.62 U/ml,诊断价值较高;分析发现CA125是影响MVI发生的独立危险因素,说明CA125与MVI密切相关,可以作为预测HCC发生MVI的指标。CA125在一定程度上反映机体在对抗肿瘤细胞生长的一种平衡状态。虽然目前HCC并发MVI患者CA125升高的机制尚不清楚,推测可能为肝癌的进展伴随着多种信号通路的改变,其中CA125可使癌细胞能够获得移动的能力和抵抗凋亡的能力,所以当CA125升高时,HCC患者发生MVI的可能性更高。
本研究显示,AFP、肿瘤最大直径、TNM分期及组织分化程度均是HCC患者合并MVI的独立危险因素。AFP是一种肿瘤血清标志物,由肝细胞合成,肝癌患者AFP水平明显升高,而研究表明,AFP在促进肿瘤血管生成中发挥重要作用,其水平的升高表明肿瘤呈高侵袭性。研究显示[17],在肺癌中直径越小、TNM分期越低及分化程度越高,肿瘤边界越清晰,肿瘤合并MVI及卫星灶越少。本研究中,不同CA125分组间肿瘤直径、TNM分期及肿瘤分化程度患者比例差异有统计学意义,再次说明了CA125与MVI有关。据报道[18],CA125比值越低的肺癌患者术后的总体生存率及复发率较差。本研究结果显示,CA125组复发率明显高于CA125组。其原因可能在于,MVI是肝癌术后复发的主要影响因素,而是否合并MVI及其进展又与转移、侵袭能力有关。
综上所述,术前CA125是HCC患者发生MVI的独立危险因素,对于合并MVI具有较高预测价值,外科医生根据患者术前CA125对患者进行分组,将有利于最佳治疗方案的选择。同时术前CA125对HCC患者预后生存具有良好的预测作用。
