右美托咪啶与艾司洛尔治疗急性A 型主动脉夹层的临床效果研究
2021-09-22张松涛
肖 扬,赵 威,张松涛,尹 文
(空军军医大学第一附属医院急诊科,陕西 西安 710032)
主动脉夹层(aortic dissection,AD)是心血管急症中最为凶险的一种疾病[1]。近年来其发病率呈逐年上升趋势,是由各种原因导致的主动脉内膜、中膜撕裂,主动脉内膜与中膜分离,血液流入使主动脉腔被分隔为真腔和假腔,导致血管屏障功能损伤,极易发生破裂,是一种致死率极高的动脉血管疾病。其中最为关键的致死因素为高血压和心率过快[2],控制血压和心率稳定是主动脉夹层围手术期非常重要的治疗措施[3]。主动脉夹层好发于有高血压病史的患者,发病后因主动脉内膜剥脱产生剧烈样疼痛,机体处于高应激状态,血压、心率急剧升高,导致夹层破裂,致死风险极大。有研究表明,在急性A 型主动脉夹层发病前48 h 不能及时有效进行临床干预,每小时死亡率增加1%~2%,发病1 周病死率超过70%[4]。及时的控制血压和心率能减轻血流对动脉血管壁的冲击,降低主动脉的剪应力,避免主动脉夹层进一步撕裂导致破裂死亡风险。艾司洛尔注射液是超短效的选择性β1-受体阻滞剂,在心肌主要竞争儿茶酚胺结合位点,从而减慢静息和运动心率,降低血压,降低心肌耗氧量,还可避免因血压降低引起的反射性心率增快,提高动脉壁性能[5]。右美托咪定为高选择α2肾上腺素能受体激动剂,起效快,通过抑制中枢系统去甲肾上腺素神经元兴奋,降低儿茶酚胺释放,起到抗交感活动作用,进而降低交感兴奋性。右美托咪定还可通过脑干蓝斑核处受体产生镇静效果,并能作用于脊髓神经突触受体,抑制刺激向大脑中枢传导,从而产生镇痛效果及心肌保护作用[6]。本研究观察右美托咪啶联合艾司洛尔在主动脉夹层患者早期的治疗效果,以期为降低主动脉夹层患者术前死亡率,创造手术机会提供解决方案,现报道如下。
1 资料与方法
1.1 一般资料 收集空军军医大学第一附属医院急诊科2019 年1 月-2020 年12 月收治的急性A 型主动脉夹层患者共120 例。根据是否使用右美托咪定治疗,分为右美托咪定组(Dex 组)57 例,非右美托咪定组(Non-Dex 组)63 例。Dex 组和Non-Dex 组年龄、性别、基础疾病(高血压、动脉粥样硬化)、纽约心脏病协会(NYHA)心功能分级、入院时平均动脉压(mean arterial pressure,MAP)情况比较,差异无统计学意义(P<0.05),具有可比性,见表1。
表1 两组一般资料比较()

表1 两组一般资料比较()
1.2 纳入与排除标准 纳入标准:①急性A 型主动脉夹层患者均由胸、腹主动脉CTA 检查确诊;②年龄25~75 岁;③突发胸痛、背部疼痛或者腹痛,病程不超过24 h,伴有高血压、心率快。排除标准:①合并严重心、脑、肾等重要器官衰竭;②入院时病程超过24 h 或者慢性夹层,低血压或严重器官灌注不良;③正在口服降压药物和或抗心律失常药物;④于外院转诊过程中已应用降压、控制心率药物;⑤合并急性心肌梗死、肺栓塞、脑血管意外、低血压、恶性心率失常、脏器功能不全等患者及入院后4 h 内死亡患者。
1.3 治疗方法 入院后两组均常规内科治疗,包括心电监护,绝对卧床休息等,选择静脉药物控制血压、心率、镇痛、镇静等。根据《主动脉疾病的诊断和治疗指南》将心率(HR)控制至60~80 次/min,降低左室收缩力及张力,收缩压(SBP)100~120 mmHg 为达标范围,HR<60 次和或SBP<90 mmHg 时减量或停药。Non-Dex 组给予艾司洛尔(齐鲁制药有限公司,国药准字H19991059,规格:10 ml∶100 mg)500 mg 原液,以0.2 mg/(kg·min)泵入,根据心率、血压调节泵入速度;Dex 组在此基础上静脉联合右美托咪啶(扬子江药业集团有限公司,国药准字H20183220,规格2 ml∶0.2 mg)0.5 μg/(kg·min)微量泵持续静脉泵入[7]。
1.4 观察指标 比较患者入院时(T0)、用药后1 h(T1)、用药后2 h(T2)、用药后4 h(T4)、用药后6 h(T6)HR 和MAP,两组患者HR 和MAP 达标时间及心率达标率,两组患者术前及术后2 周死亡率。
1.5 统计学方法 采用SPSS 19.0 软件对数据进行处理分析,计量资料以()表示,比较采用t检验,计数资料采用(n)或(%)表示,采用χ2检验,比较采用单因素方差分析,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组治疗前后不同时间段MAP 和HR 比较Dex 组T1、T2、T4、T6时HR、MAP 均低于T0,差异有统计学意义(P<0.05);Non-Dex 组T2、T4、T6时HR、MAP 均低于T0,差异有统计学意义(P<0.05);Non-Dex 组T0与T1时HR 比较,差异无统计学意义(P>0.05);Dex 组T6时的MAP 和HR 达标率高于Non-Dex 组,MAR、HR 平均达标时间短于Non-Dex 组,差异有统计学意义(P<0.05),见表2、表3。
表2 两组不同时间点MAP、HR 比较()

表2 两组不同时间点MAP、HR 比较()
注:与同组T0 比较,*P<0.05;与对照组比较,#P<0.05
表3 两组MAP、HR 早期达标率(,%)
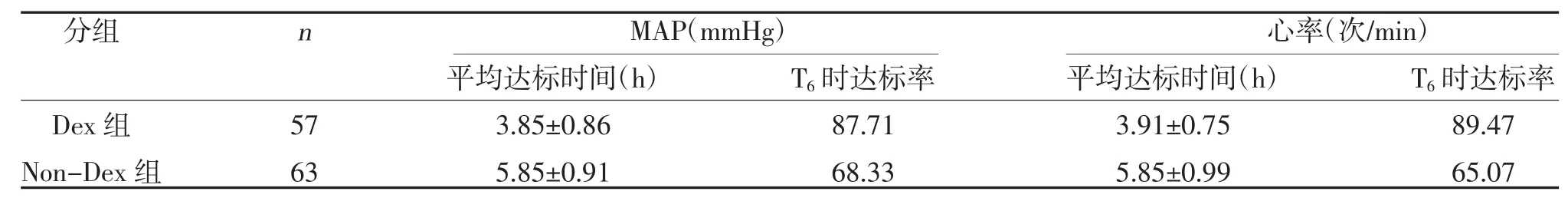
表3 两组MAP、HR 早期达标率(,%)
2.2 两组围手术期死亡率 Dex 组术前及总死亡率低于Non-Dex 组,差异有统计学意义(P<0.05);Dex 组术后2 周死亡率低于Non-Dex 组,但差异无统计学意义(P>0.05),见表4。

表4 两组手术前后死亡率比较[n(%)]
3 讨论
目前主动脉夹层死亡率仍居高不下,而Stanford A 型夹层发病30 天死亡率高达71%[8],其中术前死亡率接近50%。在患者有机会接受手术前的积极干预是降低主动脉夹层患者死亡率重要环节,其中术前血压和心率的控制至关重要。β-受体阻滞剂是心脏手术围手术期的传统用药,有减少心肌缺血和心律不齐发作的作用[11,12]。右美托咪啶目前在许多心脏大手术患者及重症患者中也有应用,通过降低心肌缺血的发生率和肌钙蛋白的血清水平,为高危患者提供心脏保护[13]。但单独使用右美托咪啶在控制心脏手术患者心率中并没有明显作用[14],只是能降低心率波动幅度。
本研究中Dex 组T1、T2、T4、T6时HR、MAP 均低于T0(P<0.05);Non-Dex 组T2、T4、T6时HR、MAP 均低于T0(P<0.05);Non-Dex 组T0与T1时HR 比较,差异无统计学意义(P>0.05);Dex 组T6时的MAP和HR 达标率高于Non-Dex 组,MAR、HR 平均达标时间短于Non-Dex 组(P<0.05),表明右美托咪啶联合艾司洛尔在控制患者心率方面相较于MAP 更有优势。
研究显示[9,10],主动脉夹层患者在转运途中大概花费4.3 h,到达后到手术前仍需要4.3 h 左右,而本研究显示右美托咪啶联合艾司洛尔达到控制MAP 时间为(3.85±0.86)h、控制心率时间为(3.91±0.75)h,均能够在4 h 左右,控制较好,为Stanford A 型夹层术前治疗提供了相对有效的解决方案。由于院前患者心率、血压情况较难收集,本研究未纳入院前死亡患者。本研究中Dex 组术前及总死亡率低于Non-Dex 组(P<0.05);Dex 组术后2 周死亡率低于Non-Dex 组,但差异无统计学意义(P>0.05),表明应用右美托咪啶术前死亡率及围手术期总死亡率较未使用右美托咪啶降低,可能与应用右美托咪啶后能较快的使MAP、心率达标有关。此外,也有研究表明右美托咪啶在围手术期的镇静作用及抑制主动脉夹层患者炎症反应的发生也发挥积极作用[15,16],可能解释右美托咪啶降低主动脉夹层患者围手术期死亡率的原因。
综上所述,主动脉夹层患者的术前干预及非手术治疗研究极为重要,明确有效控制血压和心率在主动脉夹层患者的治疗具有重要意义。右美托咪啶联合艾司洛尔可更加有效地控制急性主动脉夹层患者血压、心率,缩短血压、心率达标所需时间,并降低主动脉夹层患者围手术期死亡率。
