人类免疫缺陷病毒相关神经系统疾病研究进展
2021-09-18代飞飞王佳伟
代飞飞 王佳伟
人类免疫缺陷病毒(HIV)感染导致的获得性免疫缺陷综合征(AIDS),又称为艾滋病。全世界约有38×103万例HIV感染患者[1],相关并发症病死率高。尽管目前尚无法治愈HIV感染,但自1996年开始应用联合抗逆转录病毒疗法(cART)后,已将其从致死性疾病转变为慢性进展且可控状态[2]。这一时期HIV相关神经系统疾病的流行病学发生较大变化,发病率降低、生存率提高,疾病谱也有一定变化。目前较常见的是HIV相关神经综合征,包括原发感染、机会性感染、免疫重建炎症综合征(IRIS)、抗逆转录病毒药物相关神经毒性作用等。随着HIV感染患者预期生存期的延长,其老龄化相关疾病逐渐突显,如HIV相关神经认知障碍(HAND)、HIV相关脑血管病、HIV相关周围神经病等。本文拟综述常见HIV相关神经系统疾病研究进展,以期提高临床医师对上述疾病的认识。
一、HIV相关神经综合征
1.原发感染HIV的主要致病型为HIV-1型,目前认为其侵入中枢神经系统的机制是通过单核细胞或受感染的T淋巴细胞自血液迁移至中枢神经系统,称为特洛伊木马理论;此外,促炎性因子和病毒蛋白等可以改变血-脑屏障通透性,病毒蛋白也可以直接作用于神经元和少突胶质细胞,加重神经细胞损伤和死亡,而巨噬细胞激活则可使促炎性因子、神经毒素、活性氧和活性氮水平增加[3]。HIV感染分为3个阶段,即急性期、慢性感染期和艾滋病期。急性期,血液中HIV载量较高,导致CD4+T细胞数目骤然下降,常见临床症状是头痛、淋巴结肿大、咽炎和皮疹;慢性感染期,CD4+T细胞数目恢复至正常水平,血液中HIV载量明显下降,虽然HIV仍持续感染且仍复制,但宿主并无临床症状,称为无症状阶段;艾滋病期,血液中HIV载量升高,CD4+T细胞数目<200个/μl,易出现机会性感染和恶性肿瘤。HIV原发感染相关神经系统疾病是在免疫介导的基础上发生的,通常发生于急性期或艾滋病期,主要为HIV相关神经认知障碍、远端对称性多发性神经病等。目前临床常见的HIV原发感染相关神经系统疾病参见表1[4]。治疗上多推荐糖皮质激素或免疫抑制剂治疗[5]。
2.机会性感染由于HIV感染患者免疫系统功能低下,易发生机会性感染。自cART疗法应用于临床以来,机会性感染发生率自1996-1997年的13.1/1000人 年 降 至2006-2007年 的1/1000人 年[6]。尽管HIV机会性感染发生率明显降低,但包括隐球菌性脑膜炎、脑弓形虫病和结核性脑膜炎等在内的中枢神经系统机会性感染仍是HIV感染发病率和病死率较高的主要原因。相对于急性期和慢性感染期,艾滋病期血液中HIV载量升高,CD4+T细胞数目<200个/μl,更易出现机会性感染。机会性感染通常可以检测到明确的病原体,若病原体检出困难,如结核性脑(膜)炎,则脑脊液白细胞计数增加、蛋白定量升高、葡萄糖和氯化物水平降低、结核分枝杆菌及利福平快速耐药检测(Xpert MTB/RIF)阳性均有助于诊断。机会性感染的治疗通常是在维持cART治疗的同时,针对相关病原体进行治疗[5]。目前临床常见的机会性感染相关神经系统疾病参见表2[4]。不同病原体对神经细胞的易感程度不同,称为细胞嗜性,例如,弓形虫可以感染所有神经细胞,JC病毒主要感染星形胶质细胞和少突胶质细胞,巨细胞病毒感染神经胶质细胞、神经元和血管内皮细胞,结核分枝杆菌感染巨噬细胞,EB病毒感染B淋巴细胞,隐球菌感染脑膜和脑脊液。对于HIV感染患者而言,机会性感染的易感性在很大程度上取决于T淋巴细胞介导的免疫抑制程度,因此,cART疗法恢复细胞免疫是预防中枢神经系统机会性感染的关键,保持CD4+T细胞数目>200个/μl并维持病毒抑制作用,是预防HIV感染患者发生中枢神经系统机会性感染的最佳策略[7]。

表2 HIV机会性感染相关神经系统疾病[4]Table 2.HIV-related opportunistic infections[4]
3.免疫重建炎症综合征尽管抗逆转录病毒疗法(ART)有效,但仍有部分患者可能出现临床症状突然恶化,这是由于机体对抗原(机会性感染引起的死亡或垂死的病原体,或者持续感染的病原体,或者自身抗原)的免疫反应恢复所致,称为免疫重建炎症综合征[8]。通常发生于ART治疗开始后,表现为系统或受累器官出现严重炎症反应,即头痛、发热、意识混乱、乏力、颈部疼痛、癫发作、视力下降等[9]。有文献报道1例HIV感染合并隐球菌性脑膜炎患者,予抗真菌治疗后,脑脊液白细胞计数减少、生化指标改善、隐球菌数量减少,但病情突然恶化,表现为剧烈头痛、颅内压升高,并伴有神经功能缺损[10]。除全身受累外,免疫重建炎症综合征还影响特定器官,取决于病原体,免疫重建炎症综合征相关神经系统症状及可能的病原体参见表3[8]。最常见的病原体是结核分枝杆菌、真菌和疱疹病毒。致病机制为抗原负荷、cART治疗开始后病原体特异性免疫反应恢复程度和宿主遗传易感性。高浓度的病原微生物可能是触发因素,针对病原体的特异性免疫重建则是主要致病因素。cART治疗开始后,血液中HIV RNA水平下降,CD4+T细胞数目增加,此时较高的抗原浓度使免疫系统高度激活并释放促炎性因子和趋化因子,诱导细胞死亡,从而导致免疫重建炎症综合征[11]。其诊断参考2004年French等[12]的标准:(1)ART疗法开始后,由未知的机会性感染导致的突发临床症状恶化或出现新症状。(2a)同时出现HIV-1 RNA水平降低1个Log10。或者(2b)符合以下2~3项标准,CD4+T细胞数目增加;针对相关病原体的特异性免疫反应增强;ART治疗的同时未予特定的抗菌药物治疗,症状自行缓解。(3)排除导致临床症状恶化的其他病因。其中,临床症状恶化或出现新症状是原发感染所致还是免疫重建炎症综合征所致,需定期监测CD4+T细胞数目和HIV载量[9],影像学检查[13]亦可资鉴别。目前尚无明确的治疗指南,通常建议持续ART治疗的基础上予非甾体抗炎药和皮质类固醇激素控制症状。HIV感染合并隐球菌性脑膜炎的患者发生免疫重建炎症综合征时,临床表现为头痛加重、颅内压升高、白细胞计数减少、蛋白定量降低,应用糖皮质激素后,头痛缓解,2周后颅内压明显下降[10]。但应注意的是,不同形式的免疫重建炎症综合征患者服用皮质类固醇激素可能诱发其他潜在感染。

表3 免疫重建炎症综合征相关神经系统症状及可能的病原体[8]Table 3.Clinical manifestations and possible etiology of IRIS[8]
4.抗逆转录病毒药物相关神经毒性作用目前治疗艾滋病的主要抗逆转录病毒药物为核苷类逆转录酶抑制剂(NRTIs)、非核苷类逆转录酶抑制剂(NNRTIs)、蛋白酶 抑制剂(PIs)、整合 酶抑制剂(INSTIs)等。抗逆转录病毒药物可能导致沿神经轴的一系列不良反应,致使治疗方案改变或终止治疗。核苷类逆转录酶抑制剂如齐多夫定等,可引起线粒体肌病或精神症状[14]。非核苷类逆转录酶抑制剂的中枢神经系统不良反应发生率最高,文献报道其>50%[15],主要表现为失眠、神志不清、梦魇以及包括焦虑和抑郁在内的神经精神症状,如依法韦仑常引起神经精神症状,可能与血-脑屏障完整性破坏和脑组织促炎性因子水平升高相关。体外研究显示,蛋白酶抑制剂的中枢神经系统不良反应最小,但仍有神经毒性风险[16],如利托那韦等常引起口周和周围神经感觉异常,或者脂质代谢改变致脑血管病风险增加。整合酶抑制剂主要用于三线治疗,如雷特格韦等的不良反应为睡眠障碍、情绪改变等,可能是由于应激反应激活,但其不良反应发生率较低,较少发生因不良反应而停药的情况[17]。
二、老龄化相关神经系统并发症
1.HIV相关神经认知障碍 既往曾称为HI V脑病和艾滋病相关痴呆,2007年由美国国家心理健康研究所(NIMH)和美国国立神经病学与卒中研究所(NINDS)统一为HIV相关神经认知障碍,也称为Frascati标准,包括HIV相关无症状性神经认知障碍、HIV相关轻度神经认知障碍和HIV相关痴呆(表4)[18]。然而最新文献报道,该标准的假阳性率超过20%[19],受教育程度和社会经济因素等均可影响认知功能测验结果。尽管无症状性神经认知障碍并无临床症状,但认知功能测验结果欠佳并不总反映HIV对大脑的直接影响。因此,有学者提出HIV相关神经认知障碍诊断标准的新框架,并与Frascati标准进行比较(表5)[19]。目前,HIV相关疾病发病率业已下降,但HIV相关神经认知障碍发病率较其他HIV相关疾病下降幅度小,且随感染后时间的推移而有所升高,达20%~50%[20]。HIV相关神经认知障碍发病隐匿,进展缓慢,如果感染HIV后4周发病,应警惕其他病因。疾病早期表现为注意力、记忆力和执行功能障碍,随着疾病进展,逐渐出现精神运动迟缓,伴抑郁及其他情感障碍,如易怒等,最终进展为完全痴呆、卧床、大小便失禁。HIV相关神经认知障碍是临床诊断,目前尚无特效辅助诊断方法,神经心理学测验、影像学检查、生化检查(脑脊液)和电生理学检查[脑电图、体感诱发电位(SEP)]等有助于诊断。HIV相关神经认知障碍是病毒和宿主因素共同控制的多维、复杂免疫性病理生理学过程,初次感染过程中,HIV即通过受感染的淋巴细胞和单核细胞或者通过跨膜迁移进入脑实质[3]。目前已发现特定基因型,如涉及CC趋化因子配体2(CCL2)、肿瘤坏死因子-α(TNF-α)和CC趋化因子受体5(CCR5)的Delta-32缺失易导致HIV相关神经认知障碍[21]。此外,还有多种导致HIV相关神经认知障碍的危险因素,如受教育程度低、严重免疫抑制、高龄、TNF-α水平高、CD4+T细胞数目少[21]。美国卫生与公共服务部(HHS)建议,未开始cART治疗的HIV相关神经认知障碍患者应立即开始治疗;已接受cART治疗的患者,如果血浆病毒仍复制,需调整cART药物种类以抑制病毒复制,如果血浆病毒复制抑制,需行腰椎穿刺脑脊液病毒载量测定,有可能存在脑脊液病毒逃逸现象,即血浆病毒载量长期抑制而脑脊液可检测到病毒复制现象,考虑中枢神经系统活性药物,但其疗效尚未确定[22]。
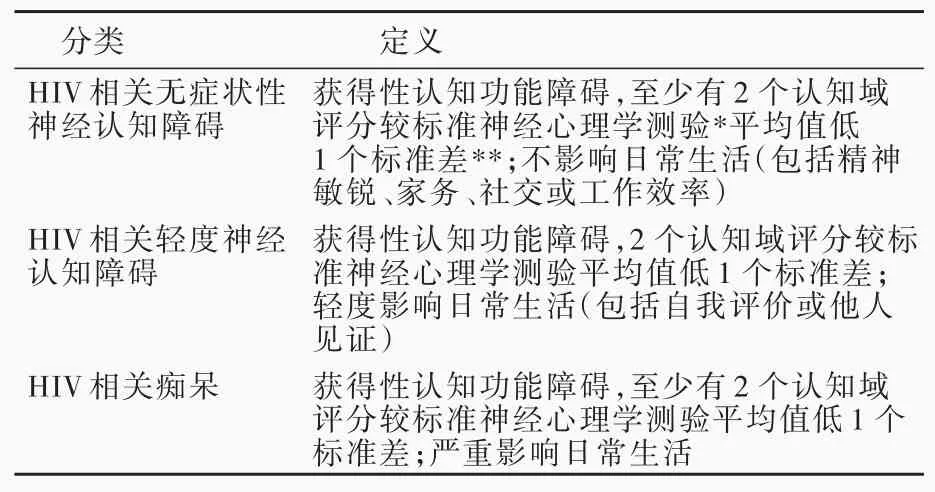
表4 HIV相关神经认知障碍的分类[18]Table 4.HIV-associated neurocognitive disorders[18]
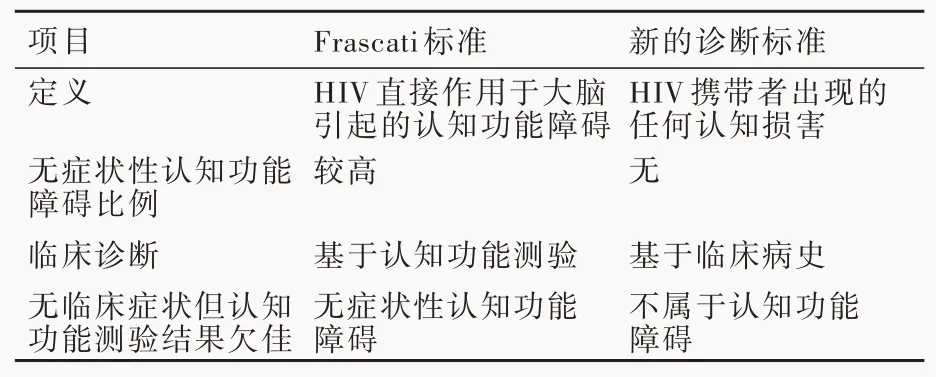
表5 Frascati标准与新诊断标准框架的主要不同点[19]Table 5.Summary of key differences between Frascati criteria and new framework[19]
2.HIV相关脑血管病尽管cART疗法延长了HIV感染患者的预期生存期,但老龄化相关疾病发病率显著增加。有文献报道,脑血管病住院病例数减少,但HIV感染患者因脑血管病住院的病例数却急剧增加[23],即使控制传统脑血管危险因素(如高血压、高脂血症、糖尿病、吸烟等),HIV感染患者的脑血管病风险仍增加[24]。传统脑血管病危险因素如高血压、糖尿病、高脂血症、吸烟等在HIV感染患者脑血管病事件中的作用可能比HIV相关危险因素(如病毒载量)更重要[25]。其他病因,如HIV相关慢性炎症导致的早期动脉粥样硬化、凝血功能障碍、动脉狭窄,机会性感染导致的动脉内膜炎及血栓形成,抗逆转录病毒药物如蛋白酶抑制剂导致的血脂异常、脂肪营养不良和代谢综合征[26]等均为HIV感染患者发生脑血管病的因素。由此可见,与正常人群相比,HIV感染患者发生脑血管病的风险增加,且随年龄的增长其患病率持续上升,由于临床异质性,HIV相关脑血管病的误诊率较高,故其发病率实际上可能被低估。
3.HIV相关周围神经病随着HIV感染患者预期生存期的延长,HIV相关周围神经病日益显现,文献报道高达50%的HIV感染患者受其影响[22]。研究显示,年龄增长是HIV感染患者罹患周围神经病的危险因素[27-28]。有两项研究分别评估HIV感染患者症状性和无症状性周围神经病的进展风险,发现年龄增长是其进展的危险因素[27-28]。HIV相关周围神经病的最常见临床表现为远端感觉性多发神经病,占2/3,其次为单发性神经病(占1/5)、急性炎性脱髓鞘性多发性神经根神经病(占1/10)、慢性炎性脱髓鞘性多发性神经根神经病(占1/20)等。神经组织活检显示其典型病理改变为轴突变性而非脱髓鞘[29]。临床主要表现为出汗减少、麻木、疼痛、无力、肌肉抽搐等,其中,疼痛在中至重度周围神经病患者中更为常见,夜晚严重,行走和触摸可加剧疼痛,还可出现止痛步态[30]。典型体征为音叉振动觉异常(低频刺激最严重),关节位置觉和腱反射减弱或消失[26,31]。HIV相关周围神经病的发生与线粒体功能障碍有关。神经元胞体中的线粒体沿轴突向下运输以支持远端区域,与远端周围神经受累最常见的临床表现相一致。神经元对能量的需求很高,线粒体参与ATP的产生并调控氧化应激反应,氧化应激增加是周围神经病发展的危险因素[32]。HIV相关周围神经病的治疗目标主要是减轻疼痛,其次是改善生活质量。加巴喷丁、拉莫三嗪、乙酰基肉碱、大麻和辣椒素贴片对神经病理性疼痛的治疗有效。一项多中心前瞻性随机对照临床试验显示,与安慰剂相比,加巴喷丁可以有效改善疼痛和睡眠质量[33]。皮质类固醇激素或血浆置换疗法可以有效控制急性和慢性炎性脱髓鞘性多发性神经根神经病症状,有氧运动和催眠可以改善HIV相关周围神经病患者生活质量[29]。
综上所述,HIV相关神经系统疾病将继续导致严重的病残和病死,严重影响HIV感染患者生活质量。越来越多的证据表明,中枢神经系统在HIV感染的持久性中发挥至关重要的作用,了解HIV相关神经系统疾病的研究进展,有助于临床医师早期识别、及时诊断与治疗。
利益冲突无
