磁流体改性制备磁性肉骨生物炭及其对Cd2+的吸附特性
2021-09-15乔洪涛李海龙赵保卫张先庭贺瑞青
乔洪涛,李海龙,赵保卫,张先庭,贺瑞青,杨 刚
(1. 忻州师范学院化学系,忻州 034000;2. 兰州交通大学环境与市政工程学院,兰州 730070)
0 引 言
生物炭是生物质在完全/部分缺氧条件下低温(<700 ℃)热解制备而成的一类多孔炭质固体材料[1-2],对重金属等污染物具有较好的吸附去除效果[3-5]。由于生物炭粒径小且密度低,其吸附后的分离与再利用成为亟待解决的主要问题之一[6-7]。在生物炭中引入磁性介质(Fe[8]、Fe2O3[9]或Fe3O4[10])形成磁性生物炭,不仅能够提升生物炭对重金属的吸附能力,亦能够借助外加磁场试现高效分离[6,11]。磁性生物炭的制备方法主要包括前驱体混合热解法、化学共沉淀法及球磨法等[11-12]。其中,前驱体混合热解法和化学共沉淀法的主要缺点为难以控制所负载的铁氧化物的种类和粒径[13-16];而球磨法易使材料的晶体结构遭到破坏[17]。磁流体(磁性液体,Magnetic fluid)是由表面活性剂包覆的磁性介质(Fe3O4,直径约为10 nm)分散于基液(水或煤油等)中形成兼具流动性和磁性的胶体溶液[18-20],表面活性剂包覆提供短距离的空间位阻和颗粒间的静电斥力,防止纳米颗粒团聚,使其能够长时间稳定存在[19],在生物医药、环境治理及选矿等领域具有广泛的应用[20],而应用磁流体制备磁性生物炭的研究却鲜见报道。
生物炭对重金属的吸附/固定机理主要包括物理吸附、沉淀、表面含氧官能团络合、离子交换、静电吸附等[21-23]。通过不同机制吸附的重金属具有不同的环境意义[24-25]。通过物理吸附和离子交换机制吸附的重金属在环境中很容易释放,对植物和人类可构成直接威胁[24];通过表面含氧官能团络合吸附的重金属则不易释放[25-26];而通过沉淀吸附的重金属释放风险取决其沉淀类型,在乙酸钠/乙酸中溶解的部分可构成潜在威胁,不能溶解的则认为对植物和人类不构成直接威胁[25]。因此,搞清重金属在生物炭上的存在形态对评价生物炭的应用具有重要意义。
鉴于此,本研究以非正常死亡的鲤鱼为生物质原料,在600 ℃条件下制备肉骨生物炭(CBC,Carp meat bone Biochar),采用磁流体对其改性制得磁性肉骨生物炭(MCBC,Magnetic Carp meat bone Biochar),分析了磁流体改性对CBC理化性质的影响;以Cd2+为重金属污染物代表,探究了MCBC对Cd2+的吸附机理;通过顺序提取试验分析了Cd2+在MCBC上的存在形态,以期为MCBC在Cd2+污染修复过程中的应用提供一定的理论依据。
1 材料与方法
1.1 磁性肉骨生物炭的制备
1.1.1 肉骨生物炭的制备
非正常死亡的鲤鱼采自山西省忻州市某渔场,将鲤鱼切块冲洗后自然风干;粉碎过筛(0.83 mm)得鲤鱼肉骨粉,将肉骨粉装入刚玉坩埚中压试,在管式炉中600 ℃下缺氧热解7 h (N2氛围,升温速率15 ℃/min),冷却至室温后取出粉碎过0.25 mm筛,用环己烷溶液和乙醇洗去残留在生物炭表面的生物油,在80 ℃条件下烘干制得肉骨生物炭,标记为CBC。
1.1.2 磁性肉骨生物炭的制备
磁流体:将FeCl3·6HO2(1.35 g)与40 mL乙二醇混合溶解,加入1 g聚乙二醇(PEG-4000)和3.6 g NaAc进行磁力搅拌30 min后置于反应釜中200 ℃下反应12 h,冷却至室温后取出抽滤,并用无水乙醇清洗2~3次,将滤饼置于60 ℃条件下干燥6 h制得磁流体。
磁性肉骨生物炭:将1 g磁流体与4 g肉骨生物炭置于50 mL的去离子水中,在室温下下振荡8 h(转速为150 r/min)后抽滤,并用去离子水清洗至滤液成无色透明,将滤饼在60 ℃条件下烘干6 h,制得磁性肉骨生物炭,标记为MCBC。
1.2 生物炭的表征
采用元素分析仪(Elementar,德国)测定C、H、N、O、S含量;采用扫描电镜观测(JEOL JSM-7800F,日本)观测样品表面形貌和元素组成;采用物理吸附仪(Micromeritics ASAP2020C,美国)测定样品的比表面与孔径分布;采用X射线衍射仪(浩元DX-2700BH,中国)分析样品晶型;表面官能团采用傅里叶变换红外光谱仪(Bruker TENSOR27,德国)进行表征;采用Zeta电位分析仪测定(Hobriba sz-100,日本)样品表面电荷情况;采用X射线光电子能谱仪(Thermo Fisher Scientific ESCALAB 250Xi,美国)表征样品表面化学特性;采用振动样品磁强计(LakeShore 7404,美国)表征样品的磁滞回线。
1.3 吸附试验
将20 mL的Cd2+溶液(含有0.01 mol/L的NaNO3作为背景电解质)和0.0200 g的吸附剂加入系列50 mL锥形瓶中,在一定温度吸附温度下振荡(转速为150 r/min)吸附一定时间后过0.45μm滤膜,用火焰原子吸收分光光度计(岛津 AA-6300F,日本)测定滤液中Cd2+浓度。动力学试验:Cd2+初始浓度分别为50和100 mg/L,吸附时间和吸附温度分别为5~240 min和25 ℃;等温吸附试验:Cd2+初始浓度为30~250 mg/L,吸附时间为240 min,吸附温度分别为5、25和45 ℃。每组试验在相同条件下做三个平行。
1.4 顺序提取试验
将0.0200 g的MCBC和20 mL 100 mg/L的Cd2+溶液(含有0.01 mol/L的NaNO3作为背景电解质)加入系列50 mL锥形瓶中,在25 ℃条件下振荡吸附240 min后过0.45 μm滤膜,用火焰原子吸收分光光度计测定滤液中Cd2+浓度,收集吸附有Cd2+的CMBC(标记为CMBC+Cd)。顺序提取试验步骤参照参考文献[24-25]实施。
1.5 数据处理
吸附剂对Cd2+的平衡吸附量qe和去除率η按公式(1)和(2)计算采用准一级动力学方程(3)、准二级动力学方程(4)、Elovich方程(5)、颗粒内扩散方程(6)和D-C(Diffusion-Chemisorption)方程(7)进行动力学拟合
采用Langnuir方程(8)、Freundlich方程(9)和Temkin方程(10)进行等温吸附拟合
分离因子RL可根据公式(11)计算
式(1)~(11)中,qe和qt分别为Cd2+的平衡吸附量和吸附时间为t(min)时刻时的吸附量,mg/g;co和ce分别为Cd2+的初始浓度和吸附平衡时浓度,mg/L;V为溶液的体积,L;m为吸附剂的质量,g;k1(min-1)、k2(g/(mg·min))、kd(g/(mg·min))、kDC(g/(mg·min))、α(mg/(g·min))和β(g/mg)分别为准一级动力学、准二级动力学、Elovich、颗粒内扩散和D-C方程的常数;b为液膜层厚度的常数;KL(L/mg)、KF(L1/n·mg1-1/n/g)和KT(L/mg)为Langmuir、Freundlich和Temkin模型参数;n为Freundlic常数;A为Temkin模型参数;qm为最大饱和吸附量,mg/g。
2 结果与讨论
2.1 CBC和MCBC的理化性质
CBC和MCBC的基本理化性质见表1。MCBC中C、N、H、S含量相较于CBC均出现显著降低,O元素含量增大;MCBC中H/C原子比升高,说明CBC在磁化后碳化程度降低,O/C和(O+N)/C分别从0.24和0.38增大为0.35和0.48,说明MCBC较CBC具有更多的极性含氧官能团,具有更好的亲水性[26];能够表征生物炭稳定性的C/N值在磁化后增大,说明MCBC具有更高的环境稳定性[26]。Zeta电位表征结果表明,CBC和MCBC表面均带负电,且磁化后MCBC表面的带电量显著增加,说明MCBC可能通过静电引力的作用吸附重金属阳离子。

表1 CBC和MCBC的理化性质Table 1 Physico-chemical characteristics of Carp meat bone Biochar (CBC) and Magnetic Carp meat bone Biochar (MCBC)
CBC磁化后表面负载的铁氧化合物使其BET比表面积从47.6增大到71.7 m2/g,外表面积从22.9增大到60.8 m2/g,总孔体积从0.06增大至0.17 cm3/g;微孔面积和微孔体积均呈现出减小趋势,说明铁氧化物堵塞了部分CBC孔隙使其微孔数量减少。图1a为CBC和MCBC的N2吸附-脱附图,其均符合IUPAC中的第IV类,在相对压力为0.44~0.98区域内出现H3型滞后环,表明CBC和MCBC主要以介孔为主[27]。从图1a中的插图可知,CBC的孔径主要分布在3.24~4.48 nm和4.48~37.78 nm之间,且前者的数量明显多于后者;磁化后孔径主要分布在2.05~4.33 nm和4.33~37.80 nm之间,且2.05~4.33 nm的孔径明显减小,而4.33~37.80 nm的孔 径明显增多;进而使平均孔径从7.44增大到9.77 nm。
图1 b为CBC的SEM图像,CBC表面凹凸不平,存在不同大小的孔径和鱼骨在热解过程中产生的裂痕;图 1c为磁化后SEM图像,生物炭颗粒表面被铁氧化物小球覆盖,且未出现团聚现象。图1d为CBC和MCBC的磁滞回线,CBC的磁化曲线基本为一条直线(饱和磁化率为0.013 emu/g),基本不具有磁性;而MCBC的饱和磁化率为26.74 emu/g,在外磁场强度为0时,其剩余磁化强度和矫顽力均为零,说MCBC在室温下具有显著的超顺磁特性,图1d中的插图进一步说明MCBC具有较好的磁分离能力。
FTIR表征结果如图1e所示。CBC和MCBC的峰基本相同,2 010、1 030、561和419 cm-1附近的峰对应PO43-的特征吸收峰[28],1 454和875 cm-1附近为CO32-的特征吸收峰[28],1 414、1 590、1 651和3 400 cm-1附近为C-H、C=O、C=C和-OH/-NH的特征吸收峰[28];MCBC在596 cm-1附近出现了新的Fe-O特征吸收峰[29]。图1f为样品的XRD图谱,CBC主要以羟基磷石灰(HAP)、碳酸钙和氯化钾的晶体为主[26,28],亦含有类石墨结构,而MCBC在30.1°、35.5°、43.1°、53.5°、57.0°、62.6°和74.1°处出现了与Fe3O4晶体中(220)、(311)、(400)、(422)、(511)、(440)和(533)晶面对应的特征衍射峰[30-31],表明在生物炭表面已成功负载铁氧化物Fe3O4。
为了比较CBC和MCBC对Cd2+的吸附能力,使0.02 g的CBC和MCBC分别与20 mL 100 mg/L Cd2+溶液(0.01 mg/L NaNO3作为背景电解质)在室温下振荡吸附24 h,之后计算了CBC和MCBC对Cd2+的去除率,结果表明CBC和MCBC对Cd2+的去除率分别为21.5%和55.9%。说明磁化不仅能够试现生物炭的高效快速分离,亦能够使其对Cd2+的吸附效率提升160%;主要是因为:1)基于MCBC表面铁氧化合物提供的负电荷,其Zeta电位(-47.6 mV)显著降低于CBC(-21. mV),使带正电的Cd2+通过静电引力作用在MCBC表面的吸附量增大;2)MCBC在磁化后的比表面积显著增大,比表面能增加,Cd2+的吸附点位增加;3)MCBC表面铁氧化合物的含氧官能团能够提高重金属离子的络合和离子交换吸附能力[16]。该结果明显高于已报道的磁性小麦秸秆生物炭(117%)[32-33]和磁性玉米秸秆生物炭(81%)[26],可能与磁性生物炭表面负载的铁氧化物含量有关,相较于磁性小麦秸秆生物炭(8.43 emu/g)和磁性玉米秸秆生物炭(9.37 emu/g),MCBC具有更大的饱和磁化率(26.74 emu/g)说明MCBC表面铁氧化物含量较高。因此,接下来本研究将重点探讨MCBC对Cd2+的吸附过程及其机理。
2.2 MCBC对Cd2+的吸附动力学
MCBC对Cd2+的吸附动力学结果如图2a所示。Cd2+初始浓度为50、100 mg/L的吸附过程均经历了3个阶段,包括前25 min的快速吸附、30-90/60 min缓慢吸附和最终的表观平衡吸附,快速和缓慢吸附阶段对Cd2+的去除率分别为66.4%/42.5%和16.7%/13.4%;随着Cd2+初始浓度从50增大至100 mg/L时,MCBC对Cd2+的吸附平衡时间从180 min缩短至90 min,这主要是因为Cd2+初始浓度增大,致使吸附质在吸附剂表面的浓度梯度增大,传质驱动力增大,加快了传质速率,缩短吸附平衡时间。
采用准一级动力学、准二级动力学、Elovich、颗粒内扩散和D-C方程对动力学数据进行拟合分析,拟合参数见表2。相较于准一级动力学模型,准二级动力学能较好的拟合吸附过程(R2>0.99),且准二级动力学方程拟合得到的吸附量qcal(43.7/57.5 mg/g)相比于准一级动力学方程拟合得到的吸附量qcal(18.7/52.1 mg/g)更接近试验所得qexp(42.6/56.3 mg/g),说明该吸附过程主要受化学吸附控制。Elovich方程常被用来描述吸附质在固体表面的化学吸附动力学过程,其拟合的R2均大于0.99,证试MCBC对Cd2+的吸附主要为化学吸附。颗粒内扩散方程拟合结果如图2b所示。由图2b可知,MCBC对Cd2+的吸附是一个连续的三阶段过程,包括快速的液膜扩散、缓慢的粒子内扩散和最终的吸附/解吸平衡,分段拟合的相关性系数均R2均大于0.99,且kd1均大于kd2,说明吸附过程的速率控制步骤为内扩散机制,拟合的曲线并未通过坐标原点,表明内扩散并非唯一的速率控制机制,亦存在离子交换、沉淀等化学反应的影响。D-C方程常用来描述重金属离子在非均质介质上的吸附[34],其拟合的R2大于0.98,且拟合得到的qcal与试验所得qexp较为接近,表明D-C方程能够描述MCBC对Cd2+的吸附过程,进一步证试了Cd2+在非均匀介质MCBC上的吸附受扩散和化学吸附两种机制共同作用。
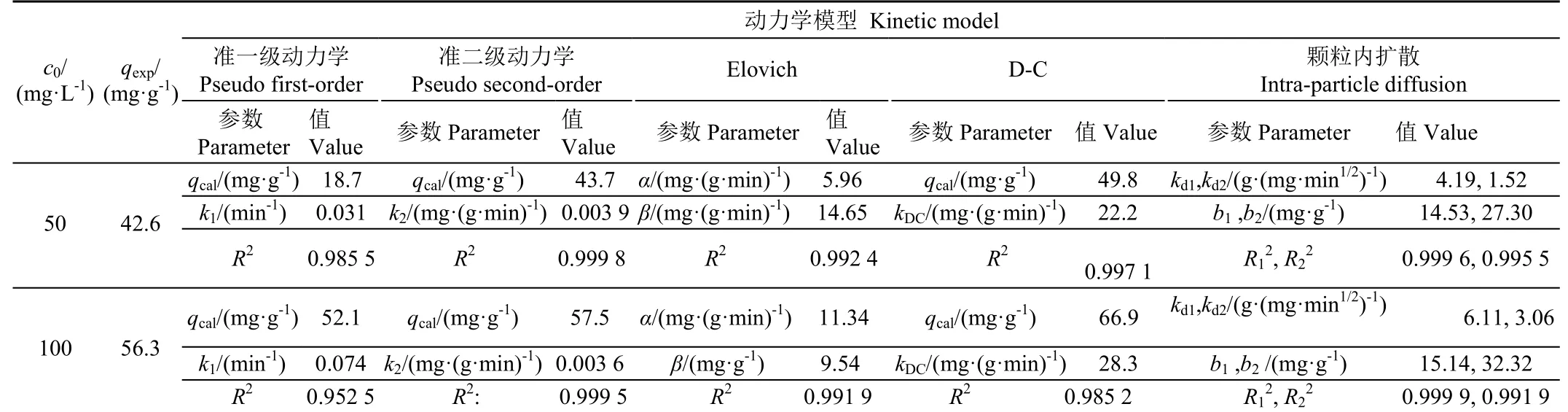
表2 MCBC对Cd2+的吸附动力学模型拟合参数Table 2 Adsorption kinetic model fitting parameters for Cd2+ adsorption on MCBC
2.3 MCBC对Cd2+的等温吸附
不同温度下MCBC对Cd2+的等温吸附结果如图3a所示。由图3a可知,当Cd2+的平衡浓度小于25 mg/L时,吸附量急剧增大,当Cd2+的平衡浓度大于25 mg/L时,吸附量增加趋势变缓。此外,MCBC对Cd2+的吸附量亦随着吸附温度的升高而增大;但当Cd2+平衡浓度小于2.8 mg/L时,随着吸附温度从278 K升高至318 K,吸附量仅从27.1增大到29.2 mg/g,说明温度对低平衡浓度时的吸附量影响较小。为进一步探究MCBC对Cd2+的等温吸附过程,采用Langnuir、Freundlich和Temkin方程对等温吸附数据进行拟合,拟合曲线如图3a所示,拟合参数见表3。

表3 MCBC对Cd2+的等温吸附模型拟合参数Table 3 Isotherm fitting parameters for Cd2+ adsorption on MCBC
Langnuir、Freundlich和Temkin方程均能较好的拟合MCBC对Cd2+的等温吸附过程,R2均大于0.95,但Freundlich的拟合效果最好,表明该吸附是多层吸附;此外,KF可表示Cd2+的浓度对吸附容量的影响程度,随着吸附温度的升高,KF从21.2增大至30.3 L1/n·mg1-1/n/g,说明升温更有利于吸附的发生;1/n在0.1~1之间时,表明MCBC易于吸附Cd2+。Temkin方程说明该吸附过程是化学吸附主导,与动力学结果一致。Langnuir方程中,KL的值随着温度升高而增大,说明吸附亲和力随着温度升高而越大,说明升温有利于吸附;基于Langnuir方程的饱和吸附量为74.6~96.2 mg/g,显著大于近来报道的碱和磁复合改性小麦秸秆生物炭(23.4 mg/g)[32]、磁性稻壳生物炭(23.3~30.3 mg/g)[33]、磁性玉米秸秆生物炭(43.5 mg/g)[26]、磁性松林生物炭(14.7~19.5 mg/g)[35]、高锰酸钾改性磁性生物炭(77.1 mg/g)[36]。
通过分离因子RL亦可进一步说明MCBC对Cd2+的吸附性能。由图3b可知,不同吸附温度下的RL值在0.038 5~0.322 6范围内(介于0~1),表明MCBC对Cd2+为有利吸附[32],且RL值随着吸附温度和co的增大而减小,说明吸附温度和Cd2+浓度越高吸附越有利[32]。
2.4 MCBC对Cd2+的吸附机理
本研究通过金属离子(Na+、Ca2+、K+和Mg2+)的净释放量探究了离子交换在Cd2+吸附过程的作用。金属离子的净释放量是通过MCBC(0.020 0 g)在背景电解质溶液(0.01 M NaNO3)中与在Cd2+溶液(100 mg/L,0.01 M NaNO3)中释放量的差值计算而得,结果如图4所示。Na+、Ca2+、K+和Mg2+的净释放量分别为0.118、0.740、0.083和0.033 meq/g,金属离子总的净释放量为0.974 meq/g,占Cd2+总吸附量(以离子交换容量计算为1.001 meq/g)的97.3%,说明离子交换在Cd2+的吸附过程中具有重要作用。Ca2+的净释放量显著大于其他3种金属离子,这可能与生物炭中存在大量的羟基磷石灰[HAP,CaI4CaII6(PO4)6(OH)2]有关,在HAP中CaI和CaII分别表示稳定的Ca和可交换的Ca[28],在吸附过程中,Cd2+与大量的CaII发生离子交换作用,进而使Ca2+的净释放量占金属离子总的净释放量76.0%。
MCBC+Cd的红外表征结果表明(图1e),Cd2+吸附前后,PO43-的特征吸收峰从419 cm-1变化到475 cm-1处,CO32-的特征吸收峰从1 454和875 cm-1附近变化到1 459和742 cm-1附近,这可能是由于PO43-和CO32-参于了Cd2+的吸附过程形成CdCO3和Cd3(PO4)2;3 400 cm-1附近的-OH在吸附后变为3 386 cm-1附近说明-OH可能通过络合作用参与了Cd2+的吸附。此外,MCBC+Cd的XRD表征结果(图1f)表明在MCBC+Cd中出现了新的晶体结构,包括CdCO3、Cd3(PO4)2和Cd3P2[26,30];在34.2°附近为CdFe2O4的特征衍射峰(标准卡片00-002-0975),CdFe2O4的形成是由于Cd2+作为Fe的内替代物吸附到Fe2O3的结构中[37],导致MCBC+Cd的XRD图谱中Fe3O4的特征衍射峰减弱/消失,该结论与Tan等[37]的研究结果一致。
由图5可知,MCBC中O1s经拟合后可分为C-O(532.98 eV)、C=O(531.13 eV)和Fe-O(530.03 eV),吸附Cd2+后出现Cd-O(530.13 eV)拟合峰,C-O和C=O的结合能分别位于533.18 eV和532.38 eV[38],且相对含量发生显著变化,说明Cd2+成功吸附在MCBC上,且含氧官能团参与了吸附过程;Fe-O的结合能位于531.33 eV;进一步对MCBC中Fe2p拟合,Fe2p3/2(710.28-715.63 eV)和Fe2p1/2(724.83-733.43 eV)说明MCBC中含有以FexOy、FeOOH和Fe(OH)x形式存在的Fe3+和Fe2+[31],吸附Cd2+后Fe2p和Fe-O的结合能均发生明显的变化,说明Cd和Fe之间发生了配位反应,这与XRD的表征结果一致,Khan等[31]同样也证试了Cd和Fe之间的作用。因此,MCBC对Cd2+的吸附机理主要包括离子交换、沉淀、含氧官能团络合,亦包括物理吸附和静电引力(详见2.1)。
2.5 Cd2+在MCBC上的赋存形态分析
通过顺序提取试验测定了Cd2+在MCBC+Cd上的形态,结果见表4。Cd2+在顺序提取试验过程中的回收率为81.6%,该回收率与Shen等[24-25]和Fristak等[39]的研究结果(78.4%~104.4%)接近。Cd2+在生物炭上的吸附主要以可交换态为主,占总吸附量的48.4%(22.20 mg/g);以物理吸附为主的水提态含量最小,占总吸附量的0.3%(0.13 mg/g),该结论与吸附动力学和等温吸附的结论“MCBC对Cd2+的吸附机理主要以化学吸附为主”的结果一致;水提态和可交换态的Cd2+在环境中最易释放,环境风险最大。酸可提取态的比例为29.5%(13.53 mg/g),该部分Cd2+的主要吸附机理包括静电引力和能够在NaOAc/HOAc溶液中溶解的沉淀,具有潜在环境风险,但在短期内可能是稳定的,但如长期暴露在环境中,可能会随着境变化而再次释放,造成一定的环境风险[24-25,39];稳定态Cd2+占总吸附量的21.8%(10.08 mg/g),这部分Cd2+主要通过含氧官能团络合和形成在NaOAc/HOAc溶液中不溶的沉淀物[24-25,39]。因此,Cd2+在MCBC+Cd上的主要存在形态为可交换态和酸可提取态。

表4 Cd2+在MCBC+Cd上各形态的含量及其占比Table 4 The content and proportion of each form of Cd2+ on MCBC+Cd
3 结 论
1)磁流体改性不仅能够使CBC表面较为均匀的负载Fe3O4,亦能够增大生物炭的比表面积、总孔体积、平均孔径和表面带电量,使生物炭对Cd2+的吸附效率提高160%。
2)MCBC对Cd2+的吸附过程符合准二级动力学、D-C、Freundlich和Temkin吸附模型,吸附过程为多机制的共同作用,主要以化学吸附为主;基于Langnuir方程的饱和吸附量为74.6~96.2 mg/g。
3)MCBC吸附Cd2+的主要机理为离子交换、沉淀、静电吸附和含氧官能团络合;Cd2+在MCBC+Cd上的存在形态包括:可交换态(48.4%)、酸可提取态(29.5%)、稳定态(21.8%)和水提态(0.3%)。
