基于Nafion-聚苋菜红-石墨烯纳米复合膜修饰玻碳电极的一氧化氮生物医学传感
2021-09-11朱春楠郑冬云
吴 颖, 杨 宁, 金 剑, 朱春楠, 郑冬云*
(1.武汉市第一医院,湖北武汉 430074;2.中南民族大学生物医学工程学院,湖北武汉 430074;3.中南民族大学脑认知国家民委重点实验室,湖北武汉 430074;4.医学信息分析及肿瘤诊疗湖北省重点实验室,湖北武汉 430074)
作为一种神经递质和血管舒张因子,一氧化氮(Nitric Oxide,NO)广泛存在于人体各组织器官中,在神经信息传递、心肺功能维持、脏器血流调节、内分泌调节、机体防御免疫功能发挥以及细胞凋亡调节等诸多方面都起着举足轻重的作用。一些疾病的发生,通常都与体内NO的浓度异常有关,如动脉粥样硬化[1]、哮喘[2]、肠炎[3]、肿瘤[4]等。因此,实现对生物样品中NO含量的准确检测,具有重要的生物医学意义和临床价值。现已提出的NO检测方法有很多种,包括电子自旋共振光谱法[5]、化学发光法[6]、荧光法[7]及生物医学传感法[8]等。其中,生物医学传感法因具有灵敏度高、操作简便、检测快速等优点而备受关注。近年来,NO生物医学传感器的研究主要集中于新型NO敏感功能材料的制备及其应用[9]。
石墨烯(Graphene,GR),是一种拥有二维原子共轭结构的新型碳纳米材料,具有大比表面积、高机械强度、优良的导电和导热性能,在生物医学传感领域应用广泛,已有报道将其应用于多巴胺[10]、同型半胱氨酸[11]、抗坏血酸[12]、5-羟色胺[13]等的电化学生物传感。将石墨烯应用于NO生物医学传感方面的研究也已见报道,如Yoon等于近年研发了一种基于氨基功能化MoS2纳米颗粒-氧化石墨烯-肌红蛋白修饰金电极的NO电流型生物传感器[14],该传感器具有较低的检出限,但操作较复杂。因此,继续探索石墨烯在NO生物医学传感方面的应用依然非常必要。
苋菜红(Amaranth Red,AR)是一种水溶性偶氮合成染料,作为食品着色剂在饮料和食品工业中应用广泛,在增加产品外观和吸引力方面表现突出[15]。但过量食用苋菜红会严重影响机体健康[16 - 18],因此,目前关于苋菜红的研究,大多集中于其在食品中含量的简单高效测定[19],而将其制备成聚合物薄膜并用作电极修饰材料的工作却鲜见报道。Chandra等最早提出了聚苋菜红薄膜在电化学传感领域的应用[20],该课题组首次制得了聚苋菜红薄膜,并基于该薄膜修饰铅笔芯电极,研发出了一种性能良好的多巴胺电化学传感器,该传感器可在尿酸共存的条件下,实现对多巴胺的选择性检测。聚苋菜红薄膜在该工作中所展现的显著电催化性能预示了其在生物医学传感领域的良好应用前景。
本文中制备了一种新型NO敏感功能薄膜,薄膜由Nafion-聚苋菜红(PAR)-氧化石墨烯(GO)共同组成,并借助于简单可控的滴涂成膜法和电化学聚合法将其固定于玻碳电极表面,构建了一种性能良好的NO电化学传感器。对NO在传感界面上的电化学反应机理进行了探讨,并对传感器的各项性能进行了考察。
1 实验部分
1.1 仪器与试剂
电化学实验在CHI660D电化学工作站(上海辰华仪器公司)上完成,采用三电极系统:以玻碳电极(GCE)或修饰的GCE作为工作电极,饱和甘汞电极(SCE)作为参比电极,铂丝电极作为对电极。电极及CHI120电极抛光材料购自上海辰华仪器有限公司。扫描电子显微镜表征借助于场发射电镜-SU8010完成。
苋菜红用pH=7.0的0.1 mol/L磷酸盐缓冲溶液(PBS)配制成浓度为5.0×10-6mol/L的储备液,置于4 ℃的冰箱内备用。氧化石墨烯(GO)水分散液购自江苏先丰纳米材料科技有限公司,质量浓度为2 mg/mL。尿酸、多巴胺、抗坏血酸和L-精氨酸(L-Arg)均购自上海如吉生物科技发展有限公司。1%Nafion溶液由5%Nafion溶液(武汉集思仪器设备有限公司)用超纯水稀释而得。超纯NO气体以及N2购自武汉纽瑞德特种气体有限公司。Na2HPO4、NaH2PO4、KCl均购自国药集团化学试剂有限公司。所有的化学试剂都为分析纯,未经任何纯化而直接使用。实验用水均为超纯水。
小鼠神经母瘤细胞由中南民族大学生物医学工程学院生物实验室提供。
1.2 NO饱和溶液的制备
NO饱和溶液的配制:首先采用排水集气法将超纯NO气体收集于250 mL的棕色试剂瓶中,收集满后,用橡胶塞塞紧瓶口并蜡封,然后用注射器注入10 mL已通N2除O2的超纯水并充分摇匀,于室温下静置过夜,即得NO饱和溶液,浓度为1.8 mmol/L[21]。超纯NO气体的收集在通风橱中进行。
NO标准溶液的制备:采用微量注射器吸取一定体积的NO饱和溶液,然后用通N2除O2的超纯水稀释得到一系列不同浓度的标准溶液。NO标准溶液需现配现用,且避光保存于密闭容器中。
1.3 电极的制备
氧化石墨烯修饰玻碳电极(GO/GCE)的制备:(1)首先将直径为3.0 mm的GCE在粒径为50 nm的Al2O3浆液中抛光,然后依次用体积比为1∶1的HNO3、无水乙醇及超纯水各超声清洗2 min,使电极表面呈镜面并待其自然晾干;(2)滴涂5 μL 1 mg/mL的GO分散液于GCE表面,自然晾干制得GO/GCE。
聚苋菜红修饰玻碳电极(PAR/GCE)的制备:GCE的抛光清洗步骤如前所述,将抛光清洗好的GCE置于5.0×10-6mol/L的苋菜红溶液(pH=7.0)中,在-0.2~1.6 V的电位范围内,以100 mV/s的扫描速率环扫15圈,超纯水冲洗后晾干,即制得PAR/GCE。
纳米复合膜(Nafion/PAR/GO/GCE)修饰电极的制备:(1)将GO/GCE置于5.0×10-6mol/L的苋菜红溶液(pH=7.0)中,在-0.2~1.6 V的电位范围内,以100 mV/s的扫描速率环扫15圈,超纯水冲洗后晾干,制得PAR/GO/GCE;(2)将PAR/GO/GCE置于0.05%Nafion水溶液中,在-1.6~1.6 V的电位范围内,以50 mV/s的扫描速率环扫10圈,超纯水冲洗后自然晾干,制得Nafion/PAR/GO/GCE,即NO电化学传感器。
2 结果与讨论
2.1 NO在不同电极上的电化学响应
为检验聚苋菜红-石墨烯纳米复合膜对NO的电催化性能,采用差分脉冲伏安法,以pH值为7.0的0.1 mol/L PBS为底液,研究了2.25×10-5mol/L的NO分别在裸GCE、GO/GCE、PAR/GCE、PAR/GO/GCE 4种电极上的电化学响应,结果如图1所示。从图1可以看出,NO在裸GCE上仅产生了一个峰形较钝的氧化峰,其峰电位为0.84 V,峰电流为1.1 μA(图1曲线a);在GO/GCE上,NO的电化学响应有所改善,具体表现为氧化峰电位负移至0.83 V,氧化峰电流增加至5.7 μA,但峰形依旧较钝(图1曲线b);在PAR/GCE上,NO的电化学响应改善更加明显,可观察到一个尖锐的氧化峰,峰电位负移至0.75 V,峰电流增加至6.4 μA(图1曲线c);相较于上述电极,NO在PAR/GO/CGE上的电化学响应最为明显,氧化峰电位最低(Ep=0.74 V),氧化峰电流最大(Ip=8.4 μA),如图1曲线d所示;而当底液中没有NO存在时,在PAR/GO/CGE上观察不到明显的电化学响应(图1曲线e)。这说明在图1中观察到的电化学响应是由NO的电化学氧化所产生,且聚苋菜红-石墨烯纳米复合膜对NO的电化学氧化具有明显的催化性能。
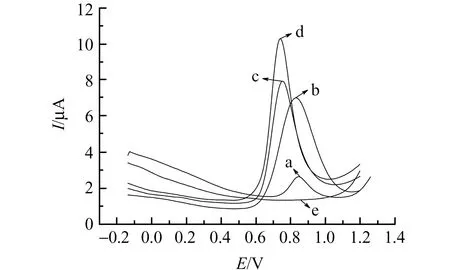
图1 裸GCE(a)、GO/GCE(b)、PAR/GCE(c)及PAR/GO/GCE(d和e)在含有(a,b,c和d)及不含有(e)2.25×10-5 mol/L NO的0.1 mol/L无氧PBS(pH=7.0)中的差分脉冲伏安图Fig.1 Differential pulse voltammogramms of bare GCE(a),GO/GCE(b),PAR/GCE(c),PAR/GO/GCE(d and e) in the presence(a,b,c and d) and absence(e) of 2.25×10-5 mol/L NO in 0.1 mol/L PBS(pH 7.0)
2.2 NO传感机理探讨
为进一步探讨Nafion/PAR/GO/GCE对NO的电催化氧化机理,对裸GCE、GO/GCE、PAR/GCE和PAR/GO/GCE进行了扫描电子显微镜(SEM)表征,结果如图2所示。裸GCE表面比较平滑(图2A);GO/GCE表面呈褶皱状薄膜结构(图2B);在PAR/GCE表面,可观察到一层有晶体颗粒构成的网格状薄膜(图2C);而PAR/GO/GCE的表面呈沟壑状,褶皱更加明显(图2D),这种结构有利于增加修饰电极的比表面积,从而提高NO在纳米复合膜表面的富集量,为传感器具有较高的灵敏度提供保障。

图2 裸GCE(A)、GO/GCE(B)、PAR/GCE(C)及PAR/GO/GCE(D)的扫描电镜(SEM)图Fig.2 SEM images of bare GCE(A),GO/GCE(B),PAR/GCE(C) and PAR/GO/GCE(D)
考察了裸GCE、GO/GCE、PAR/GO/GCE 3种不同修饰电极的交流阻抗谱,结果如图3所示。可以看出,裸GCE(a)的交流阻抗半径最大,其次是GO/GCE(b),而PAR/GO/GCE(c)交流阻抗半径最小。这说明PAR/GO/GCE的导电性能最好。良好的导电性能加快电子传递速率,从而缩短NO电化学传感器的响应时间。

图3 裸GCE(a)、GO/GCE(b)及PAR/GO/GCE(c)的电化学交流阻抗谱图Fig.3 Electrochemical impedance spectroscopy of bare GCE(a),GO/GCE(b) and PAR/GO/GCE(c)
通过考察扫描速率对NO在Nafion/PAR/GO/GCE上的氧化峰电流的影响,研究了NO的电化学氧化机理。在60~250 mV/s扫描范围内,随着扫描速率的增加,NO的氧化峰电流也随之增加(图4A)。扫描速率与氧化峰电流呈良好线性关系,其回归方程为:Ip=23.05+0.08v,R=0.99(图4B)。这说明NO在Nafion/PAR/GO/GCE上的电化学氧化反应是一个受吸附控制过程,并且为不可逆反应。NO氧化峰电位与扫描速率的自然对数呈线性相关:Ep=0.71+0.031lnv,R=0.98(图4C)。根据Laviron理论公式可以得出,NO在此传感器上的电化学氧化反应中的电子转移数为1.4≈1,即有一个电子参与了反应。

图4 (A)在不同扫速(由内向外:60~250 mV/s)下,于0.1 mol/L无氧PBS(pH=7.0)中,2.25×10-5 mol/L NO在Nafion/PAR/GO/GCE上的线性扫描伏安曲线;(B)NO的氧化峰电流与扫速之间的线性关系图;(C)NO氧化峰电位与扫速率的自然对数之间的线性关系图Fig.4 (A)Linear sweep voltammograms of Nafion/PAR/GO/GCE in 0.1 mol/L PBS(pH=7.0) containing 2.25×10-5 mol/L NO at different scan rates(from inner to outer:60 mV/s to 250 mV/s);(B)Relationship between the oxidation peak current of NO and the scan rate;(C)Relationship of the oxidation peak potential of NO with the natural logarithm of scan rate
2.3 复合膜修饰电极的性能及应用
2.3.1 线性范围的考察通过安培响应法,对Nafion/PAR/GO/GCE用于NO生物医学传感的线性范围进行了考察。将制备好的Nafion/PAR/GO/GCE置于pH=7.0的0.1 mol/L PBS中,采用安培响应法,设置工作电位为0.8 V,在200 s时,向底液中加入8 μL 1.0×10-5mol/L的NO标准溶液,随后每隔50 s加入不同浓度的NO溶液。不同浓度NO的安培响应情况如图5所示。当实验进行到500 s的时候,开始出现明显的电流阶梯,此时底液中NO的浓度为1.0×10-7mol/L;当实验进行到2 000 s时,电流阶梯基本结束,此时底液中NO的浓度为5.1×10-5mol/L。通过对图5中的实验数据进行处理可得,NO在传感器上的氧化峰电流与其浓度之间在1.0×10-7~5.1×10-4mol/L范围内呈现良好的线性关系。传感器的检出限(S/N=3)为1.8×10-8mol/L。


图6 在0.8 V的工作电位下以0.1 mol/L无氧PBS(pH=7.0)为底液,2.25×10-5 mol/L NO及同浓度的在传感器上的安培响应图Fig.6 Amperometric response of the sensor with successive injection of 2.25×10-5 mol/L NO,DA,UA,AA and in 0.1 mol/L deoxidized PBS solution(pH=7.0) under the work potential of 0.8 V
2.3.3 实际样品中NO的分析为探究Nafion/PAR/GO/GCE的实际应用能力,以小鼠神经母瘤细胞作为生物样品进行评价实验。将Nafion/PAR/GO/GCE置于pH=7.0的0.1 mol/L的无氧PBS中,并向其中加入一定量的小鼠神经母瘤细胞溶液。在200 s时,借助于微量注射器向底液中加入1 mL 0.1 mol/L的L-精氨酸(L-Arg)。另外做一组空白对照实验:将Nafion/PAR/GO/GCE置于没有添加小鼠神经母瘤细胞的pH=7.0的0.1 mol/L的无氧PBS中。在200 s时,借助于微量注射器向底液中加入1 mL 0.1 mol/L的L-Arg,监测信号,结果如图7所示。从图7中可以看出,向底液中加入L-Arg溶液时,两组实验均可观察到明显的电化学响应,该电化学响应对应于L-Arg 在传感器上的电化学氧化(图7a和图7b);加入L-Arg 大约125 s后,在图7a中观察到了一个明显的电流变化台阶信号,归属于L-Arg刺激小鼠神经母瘤细胞所释放的NO在传感器上发生了电化学氧化;而当底液中没有小鼠神经母瘤细胞时,观察不到该电流变化台阶信号(图7b),这是因为此溶液中没有NO的释放。实验结果表明,我们所研发的NO电化学传感器可成功应用于小鼠神经母瘤细胞所释放NO的实时监测,展现了其在生物医学领域可能具有良好的应用前景。
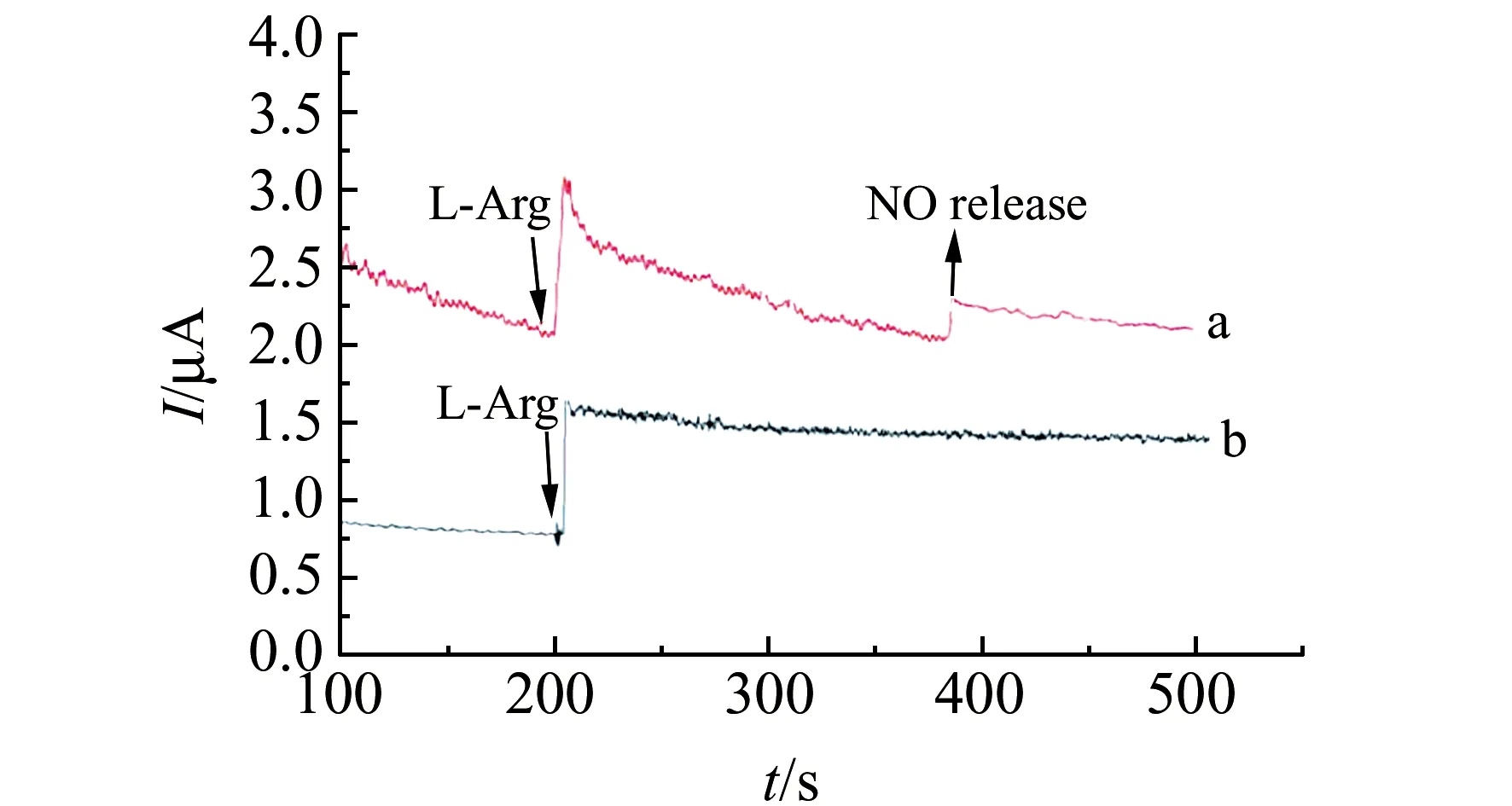
图7 以pH值为7.0,浓度为0.1 mol/L的PBS为底液,传感器分别在含小鼠神经母瘤细胞(a)和不含有小鼠神经母瘤细胞(b)的溶液中的安培响应Fig.7 Amperometric response of the sensor in 0.1 mol/L deoxidized PBS(pH=7.0) containing murine neuroblastoma cells(a) and without mouse neuroblastoma cells(b)
3 结论
本文通过简单可控的滴涂成膜法和电化学聚合法,将石墨烯和聚苋菜红纳米复合膜修饰到玻碳电极表面,制得一种新型的NO电化学传感器。借助于电子扫描显微镜和电化学交流阻抗技术对纳米复合膜进行了形貌和导电性表征,并结合电化学技术手段对传感器的性能进行了评价。结果表明我们所研发的NO电化学传感器具有灵敏度高,线性范围宽,响应灵敏等优点。此外,该传感器还可用于小鼠神经母瘤细胞释放NO的实时监测,展示了其在生物医学领域具有良好应用前景。
