胸腺嘧啶偶联羧基化磁性微球对水环境中汞的快速吸附与去除效果的研究
2021-09-10汪倩宋超刘照关裘丽萍吴伟胡庚东孟顺龙陈家长
汪倩,宋超,刘照关,裘丽萍,吴伟,胡庚东,孟顺龙,3,陈家长,3*
(1.中国水产科学研究院淡水渔业研究中心,江苏 无锡214081;2.农业农村部水产品质量安全环境因子风险评估实验室(无锡),江苏 无锡214081;3.农业农村部水产品质量安全控制重点实验室,北京 100141;4.苏州为度生物技术有限公司,江苏 苏州 215000)
近年来,中国经济高速发展的同时,能源、资源大量消耗,许多含汞的污染物质随着生态系统的自然运转进入水体,目前在某些地区的水体中仍可检测到较高浓度的汞[1-3]。由于汞的高毒性[4-5],在《地表水环境质量标准》(GB 3838—2002)[6]中,对其限量值做了严格规定,其中Ⅰ类和Ⅱ类水标准限制为0.05 μg/L,主要应用于农业用水的Ⅴ类地表水标准为1.00 μg/L;在《渔业水质标准》(GB 11607—1989)[7]中,对中国渔业水质中的汞含量做了明确的限制,不得超过0.50 μg/L。目前,有学者曾对环太湖流域及湖体本身的重金属污染进行了研究。徐泽新等[8]对太湖流域湖荡湿地的表层沉积物中汞的空间分布研究发现,汞在常州地区为轻度污染,在无锡、湖州、苏州及宜兴地区为偏中度污染。焦伟等[9]发现环太湖进出口河流的水体受到了不同程度的重金属污染。张小林等[10]和Wang等[11]通过对中国渤海海水进行污染调查,发现其受一定程度的汞污染。王乃姗等[12]发现河北衡水湖湿地表层水中总汞含量最高达0.57 μg/L,处于低生态风险区。张少庆等[13]研究葫芦岛市区不同的3条河流水体中汞的污染情况,发现五里河水中总汞浓度达10.45 μg/L,茨山河水中总汞浓度达11.04 μg/L,连山河区域由于降水冲刷带入河流造成的总汞浓度达17.32 μg/L。同时,也有许多学者[14-17]发现中国部分水库以及某些河流均受到了严重的汞污染。汞作为环境中一种生物毒性极强的持久性重金属污染物的办法,进入生物体后很难被排出,由于生物浓缩和生物放大效应,水体汞污染对人类健康造成了严重威胁。2013年,包括中国在内的87个国家和地区共同签署了《关于汞的水俣公约》[18],以寻求全球携手减少汞污染的办法,该公约在2017年8月16日生效,条例明令各国从2020年起,禁止生产及进出口含有水银的制品。因此,在水环境治理领域,对于水中汞污染的吸附去除技术研究越来越受到大家的关注。
有研究学者[19-22]提出的常被用来处理国内水污染中重金属吸附去除的方法主要包括植物修复技术以及基因工程等现代生物技术,而国外研究较多的主要是利用生物包括发酵工业的菌丝体废渣或海洋微生物对重金属的吸附作用,来治理重金属造成的污染。而在水体汞污染治理领域,Amde等[23]提出了运用改性后的纳米棒材料去除水体中游离的二价汞,在真实样品的应用去除过程中,对汞含量在 0.01 ~10.00 mg/L的水体样本有较好的去除效果。Shukla等[24]运用喷雾干燥法合成一种纳米二氧化硅-酿酒酵母生物杂交材料去除汞,在溶液pH 6.50和温度24.85 ℃时具有较好的吸附效果。张慧聪等[25]采用在NH3气氛下用氯等离子体改性生物炭进行除汞,其除汞效率达17.50%。有学者[26-29]运用葡萄蔗渣等废料进行汞吸附剂的研究,或者使用改性后的活性炭作为低成本吸附剂研究从水溶液中吸附汞,以及运用苏云金芽孢杆菌MC28作水处理过程中的吸附剂。现有汞污染治理研究的方法中,由于操作工艺复杂、处理过程中对环境要求高且处理效果还有待进一步提高等特点,不利于推广及运用,因此开发出高效、实用的汞分离检测新材料以解决水环境中汞污染问题,显得尤为重要。
针对目前国内外研究方法存在不足这一情况,本实验拟采用经羧基官能团修饰后的超顺磁磁性微球,通过化学键合或者物理吸附的方法将能与汞元素结合的胸腺嘧啶核苷酸作为抗体固载到磁性微球表面,从而特异性捕获水环境中存在的汞元素,运用磁性分离的方法实现水环境中汞的特异性吸附去除,达到操作简便且高效去除汞的目的,为中国水环境汞污染治理研究提供一种新思路。
1 材料与方法
1.1 仪器与试剂
Hydra AA系列全自动测汞仪(上海沃珑仪器有限公司);Agilent 7800 ICP-MS(美国安捷伦科技有限公司);Master-QUT水纯化系统(上海和泰仪器有限公司);超顺磁磁性微球(苏州为度生物技术有限公司);10.0 mg/L 混合标准储备液(美国安捷伦科技有限公司);100.0 mg/L 内标溶液(美国安捷伦科技有限公司);1.0 μg/L 质谱调谐液(美国安捷伦科技有限公司)。实验过程中所用各种酸及试剂均为优级纯;所有玻璃器皿均用5%硝酸浸泡过夜并用纯水冲洗干净备用;实验室用水均由超纯水机提供。
1.2 超顺磁磁性微球的羧基化
在70 ℃水体环境中加入表面活性剂与羧基基团活化剂,运用聚合反应,对磁性裸珠微球进行羧基修饰过程,即在磁性微球的表面引入羧基(—COOH)官能团,形成稳定羧基微球。
1.3 胸腺嘧啶偶联羧基化磁性微球
1.3.1 微球的清洗
使用前将微球混匀,取100 μL的微球到一个新的2 mL离心管中,然后加入200 μL 50 mmol/L MES(pH 6.0)混匀,离心去除上清液(离心转速为20 000 r/min,时间为20 min),最终将微球超声重悬于500 μL MES缓冲液中。
1.3.2 微球的活化
往离心管中分别加入使用50 mmol/L MES(pH 6.0)新鲜配制的20 μL NHS(50 mg/mL)和EDC(50 mg/mL)反应液,旋涡振荡混匀使微球充分悬浮,置于混合器上室温旋转孵育15 min。
1.3.3 微球与胸腺嘧啶的偶联
孵育结束后用500 μL MES缓冲液清洗2次,去除上清,往微球中加入500 μL胸腺嘧啶核苷酸,旋涡振荡混匀使微球均匀后室温孵育2~4 h。
1.3.4 微球上未结合表面基团的封闭
反应完成后离心去除上清液,然后往离心管中加入500 μL的封闭液(2% BSA,100 mmol/L乙醇胺溶液,pH 8.0)进行封闭,室温孵育2 h。
1.3.5 偶联完成后微球的清洗与保存
将偶联后的微球用1 mL封闭液进行洗涤,重复洗涤2次,然后将微球重新悬浮于500 μL PBS缓冲液(50 mmol/L PBS,pH 7.4)或Tris缓冲液(50 mmol/L Tris,pH 8.0)中,置于4 ℃保存。
1.4 胸腺嘧啶偶联羧基化磁性微球材料的表征
采用透射电子显微镜和扫描电子显微镜对本次实验制备的羧基微球偶联一定长度胸腺嘧啶的新型磁珠材料进行了表面微观结构的表征(图1和图2),通过观察其微观结构,不难发现新型磁珠材料具有良好的分散性,呈圆球状,形貌清晰。

图1 材料透射电镜图Fig.1 TEM image of the material
1.5 标准曲线的绘制
1.5.1 汞标准曲线的绘制
将10.0 mg/L汞单标储备液用2%硝酸稀释为100.0 μg/L 的标准中间液,由标准中间液稀释为标准曲线工作系列,浓度分别为0、0.1、0.5、1.0、2.0、5.0、10.0 μg/L,汞溶液均现配现用,将测汞仪的各项参数调试到最佳状态,待仪器稳定后,测定标准溶液实际浓度,每个样采集3次数据,取平均值,绘制标准曲线,相关系数R2达0.999(图3)。
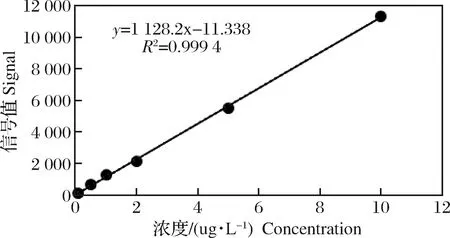
图3 汞标准曲线Fig.3 Mercury standard curve
1.5.2 混标标准曲线的绘制
将10.0 mg/L混标(Cr、Mn、Ni、Cu、Cd、Pb、As、Se和Ag)储备液用2%硝酸作溶剂稀释为100.0 μg/L的标准中间液,由标准中间液稀释为标准曲线工作系列,浓度分别为0、1.0、5.0、10.0、25.0和50.0 μg/L,运用ICP-MS仪器,编辑批处理方法,待仪器调谐稳定后,测定混标实际浓度,要求混标中各重金属元素的标准曲线对应的相关系数R2达0.999,对应的内标RSD小于5%。
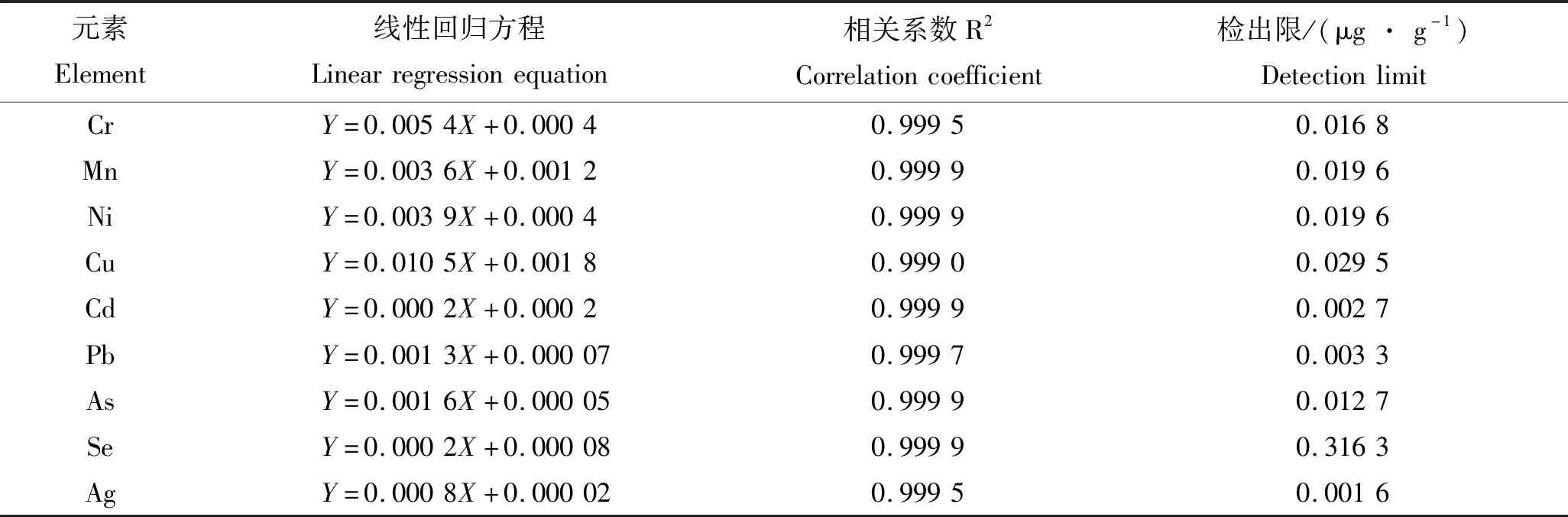
表1 回归方程与检出限Tab.1 Regression equation and detection limit
1.6 样品中汞的固定
由于汞的强吸附效应和不稳定性,给汞的测定带来一定困难,研究者[30-31]在对汞进行分析测验过程中,为了确保样品分析检测的准确性,会对采集的水样进行汞的固定,固定方法一般是采用2%硝酸或者低浓度的盐酸进行样品的酸化,以抑制汞的流失。
本实验为了进一步研究溶液pH及盛装样品的容器材质对汞挥发的影响,通过采用体积相同的塑料与玻璃两种材质的容器盛装由几种不同的溶剂作为介质配制的3种pH条件(酸性、中性及碱性)下浓度为10 μg/L的标准汞液250 mL,实验编号依次为A1、A2、B1、B2、C1、C2、D1、D2、E1、E2、F1和F2,各编号对应的溶剂、容器及具体的pH如表2所示,汞的初始母液浓度均为10 mg/L溶于2%硝酸,稀释方式均保持一致。运用测汞仪分别测定室温状态下静置时间为0、24及48 h的样品中汞浓度,比较不同介质中汞的挥发性强弱,优选出可以使汞稳定存在的介质环境,以利于后续准确分析磁珠材料对汞的吸附效果。
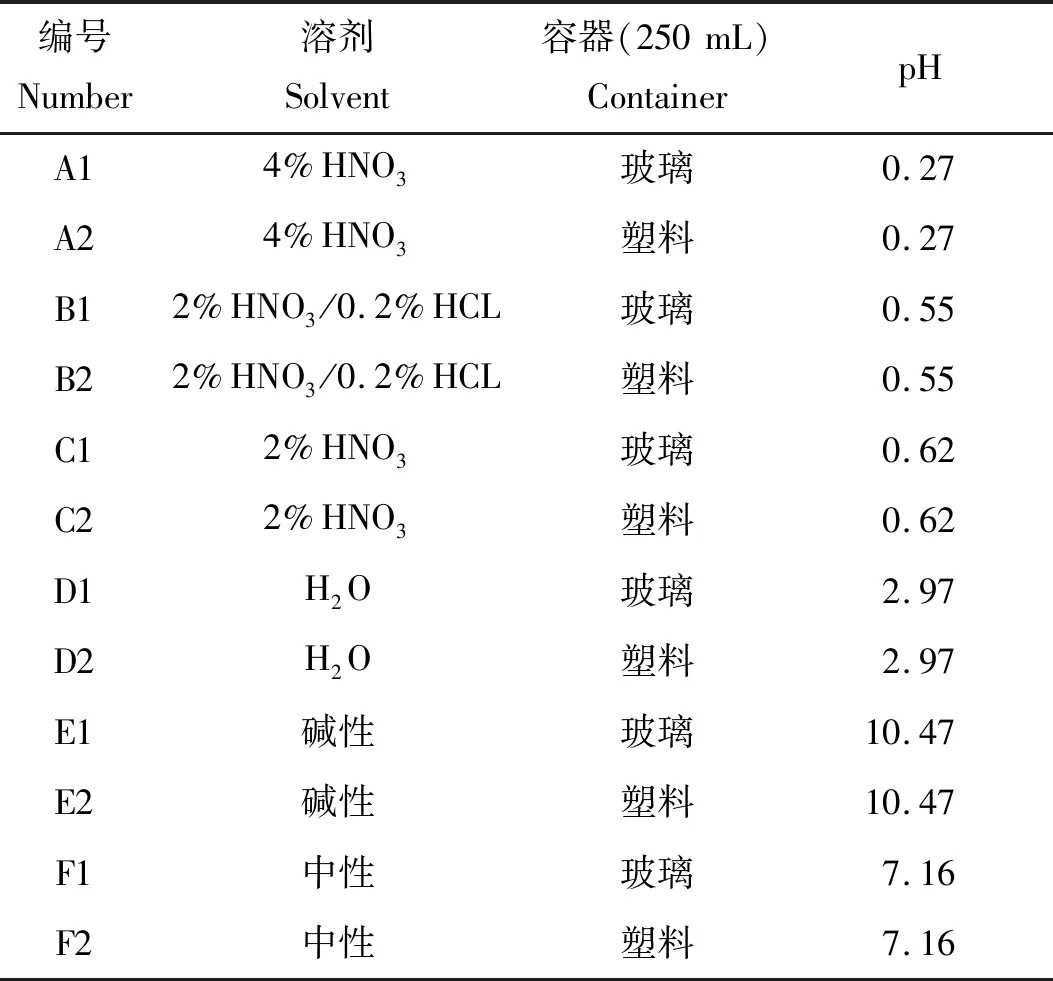
表2 各实验编号对应表Tab.2 Correspondence table for each experiment number
由图4可知,实验编号为D1、D2、E1、E2、F1和F2的样品中,溶液初始的汞浓度(即静置时间为0对应的浓度)与配制的理论浓度10 μg/L相差甚远,说明在碱性或中性环境中,用同一母液采用同样的稀释方式配制10 μg/L汞液时,汞挥发性较明显;同时也说明,用超纯水作为溶剂直接稀释母液,汞极易挥发。实验编号为A2、B1、B2、C1及C2的样品中,溶液初始的汞浓度测定值与配制的理论浓度10 μg/L相近,说明在酸性环境中,能较好地抑制汞的挥发,而盛装溶液的材质对汞挥发性影响不大,这与Takeuchi等[32]的研究结果相一致。因此,为便于操作以及节约成本,在后续实验过程中采用2%硝酸对样品溶液中汞进行固定,运用实验室现有的塑料容器盛装样品。
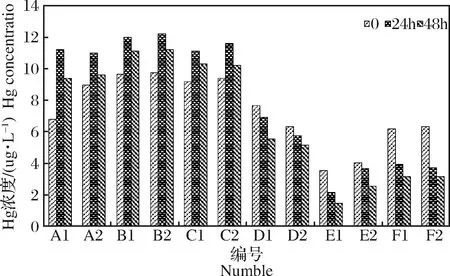
图4 汞挥发性实验结果对照图Fig.4 Comparison chart of mercury volatility experiment results
1.7 汞的测定与检测限
实验过程中,基于元素汞在室温,不加热条件下,即能挥发成汞蒸气并对波长253.7 mm的紫外光具有强烈的吸收作用,在一定浓度范围内汞浓度与吸收值成正比。将水样经某种处理后,加氯化亚锡,把水样中的汞离子还原成元素汞,用载气将汞蒸气带入吸收池内,用光电管检测吸收池内紫外线强弱变化,产生的光电信号经转换,放大及信号处理输出到数字显示表或记录仪上,从而实现对样品中汞含量的分析和测试。
由于实验水体中汞含量均较低,为保证实验结果的可靠性,通过逐级稀释法分析测试得出仪器检测限:0.050 μg/L,定量限:0.112 μg/L。
1.8 吸附和去除实验
在磁珠材料粒径优化实验中,运用2% HNO3作为溶剂配制10 μg/L汞液,取12个1.5 mL的塑料离心管,编号1~12,用移液枪依次取该汞液1 mL至编号后的12个塑料离心管中,投入由粒径依次为3、1及0.6 μm的裸珠合成的3种不同粒径新型磁珠10 μL进入含有汞液的不同编号的离心管中,然后摇匀,静置15 min,置于磁力架上15 min后,取上层清液进行上机测定汞浓度,比较不同粒径的磁珠对汞的吸附效果;在磁珠材料用量优化实验中,取12个1.5 mL的塑料离心管,编号依次为1~12,用移液枪依次取10 μg/L汞液1 mL至编号后的12个塑料离心管中,分别投入粒径为1 μm的磁珠2.5、5.0和7.0 μL至装好汞液的不同编号的离心管中,进行汞吸附实验,比较不同磁珠用量对汞的吸附效果;在优化汞浓度的实验中,运用2%硝酸作为溶剂分别配制3种不同浓度的汞液(1、5 和10 μg/L),分别取1 mL至塑料离心管中,依次投入粒径为1 μm的磁珠5 μL,进行汞的吸附实验;在汞特异性吸附实验中,运用汞单标和含有其他多种重金属元素的混标制备不同浓度的重金属全混合溶液,采用此磁珠材料对含有10种重金属元素的全混样进行吸附试验,实验过程中采用粒径为1 μm的磁珠,用量为5 μL/mL,其中汞的测定采用测汞仪,其他重金属元素的测定采用ICP-MS。
汞吸附实验示意图见图5和实验效果见图6所示。
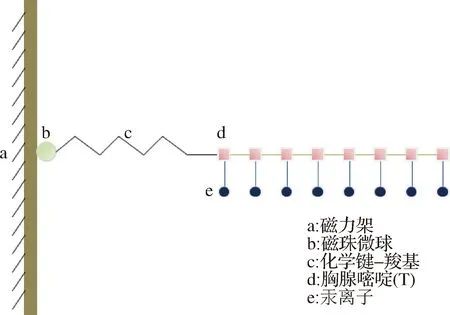
图5 吸附示意图Fig.5 Adsorption diagram

图6 吸附实验效果图Fig.6 Effect picture of adsorption experiment
1.8 去除率的计算
每组实验设计过程中,均保证了3个平行空白样品,取空白样品测定浓度的平均值为A,实验样品测定浓度的平均值为B,因此去除率的计算公式如下:
去除率(%)=(A-B)/A*100
式(1)
2 结果与讨论
2.1 粒径对去除效果的影响
由图7可知,不同粒径对汞吸附效果影响较大,磁珠粒径为3.0 μm和0.6 μm的新型材料对汞的吸附去除率达45%,而运用粒径为1.0 μm的磁珠,汞去除率可达93%,且对于汞浓度为10 μg/L溶液,在磁珠加量为10 μL处理1 mL该汞液的浓度配比条件下,进行汞吸附实验后,汞浓度可下降至0.6 μg/L,相较而言具有最好的吸附效果,因此选用粒径大小为1.0 μm的新型磁珠进行后续实验分析。

图7 不同粒径吸附效果图Fig.7 Adsorption effect chart of the material with different particle size
2.2 用量对去除效果的影响
由图8可知,对于1 mL汞初始浓度为10 μg/L的溶液,当磁珠用量为5.0与7.5 μL时,对汞均有较好的吸附效果,其中,磁珠用量为5.0 μL时,汞去除率可达96%,吸附实验后汞浓度为0.36 μg/L,磁珠用量加大至7.5 μL时,汞去除率变化不大,说明在用量为5.0 μL时,对溶液中汞的吸附已达到饱和状态,因此,从吸附效果以及节省材料的角度考虑,接下来的实验过程中处理10 μg/L的汞液,磁珠的用量浓度为5 μL/mL。

图8 不同磁珠用量对汞的吸附效果Fig.8 Adsorption effect for mercury with different dosage of magnetic beads
2.3 水体汞浓度对去除效果的影响
由图9可以发现,运用粒径大小为1.0 μm的磁珠在5.0 μL/mL加量的条件下进行汞吸附实验后,对于汞浓度5.0和10.0 μg/L的溶液,均有较好的吸附效果,汞去除率可达89.46%,而当溶液中汞浓度低至1.0 μg/L时,吸附效果明显降低,且当溶液中汞浓度达10.0 μg/L时,吸附效果更好,去除率更高。
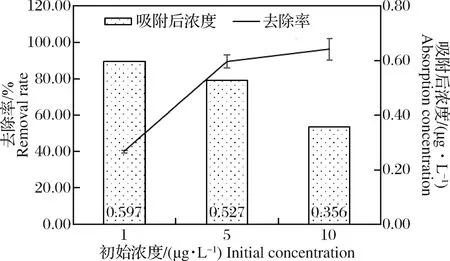
图9 不同汞浓度吸附效果图Fig.9 Adsorption effect chart of different mercury concentrations
2.4 对汞的特异性吸附
由表3可知,运用此材料对含有10种重金属元素的溶液进行去除实验后,在含有其他多种重金属元素干扰的情况下,对汞的吸附去除率可达96%,对全混样中铬、锰、镍、铜、镉、铅元素均没有明显的吸附去除效果,而对重金属银具有一定的吸附效果,去除率达66%,对砷、硒两种重金属元素均有较好的吸附去除效果,去除率均可达94%,说明此新型磁珠材料对水体环境中汞元素具有明显的特异性吸附作用,同时此材料对水溶液环境中砷、硒两种重金属元素也具有明显的特异性吸附效果。
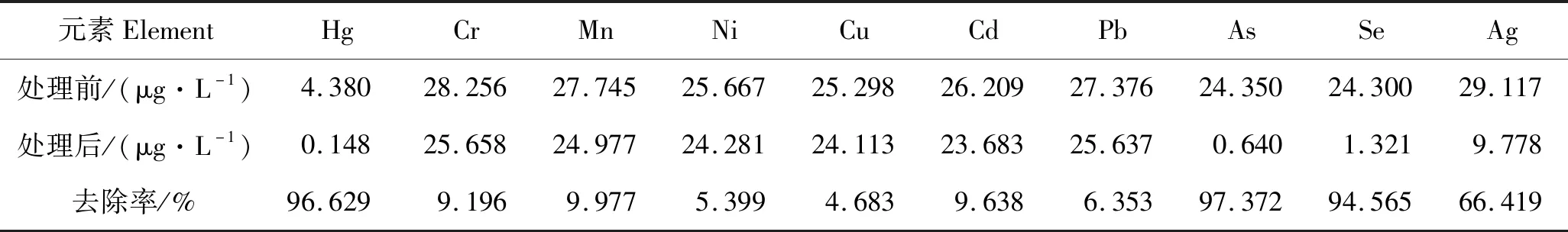
表3 材料对不同重金属元素的吸附效果对照表Tab.3 Comparison table of the adsorption effect of materials on different heavy metal elements
2.5 对重金属的特异性吸附
为了进一步研究此磁性材料对汞、砷、硒和银4种重金属材料的吸附机理,判断这4种重金属元素分别在磁珠的哪一部位进行吸附连接,实验过程中,分别采用经羧基微球偶联胸腺嘧啶后的磁珠材料、羧基微球和裸珠3种材料对同一个含有汞、砷、硒、银的全混样进行吸附试验,实验结果见表4所示。
由表4可以看出,本实验制备的经羧基微球偶联胸腺嘧啶后的磁珠材料对汞有较好的吸附效果,去除率达97%,而羧基微球和裸珠材料对汞没有明显的吸附效果,说明在汞的吸附过程中,汞元素主要通过与羧基微球上偶联的胸腺嘧啶稳定结合,由磁力架对此材料的吸附进而去除溶液中汞元素;羧基微球材料和磁珠材料对砷和硒元素均有较好的吸附效果,去除率可达91%,且这两种材料对砷和硒元素的去除效果相差不大,说明在砷和硒吸附过程中,砷、硒元素主要通过与羧基微球上的羧基稳定结合,由磁力架对此材料吸附进而去除溶液中砷、硒元素;裸珠和羧基微球材料对银元素均没有明显的吸附效果,而磁珠材料对银的去除率为44%,说明该材料对银有一定的吸附作用,且银元素主要通过与羧基微球上偶联的胸腺嘧啶结合才能实现银去除。
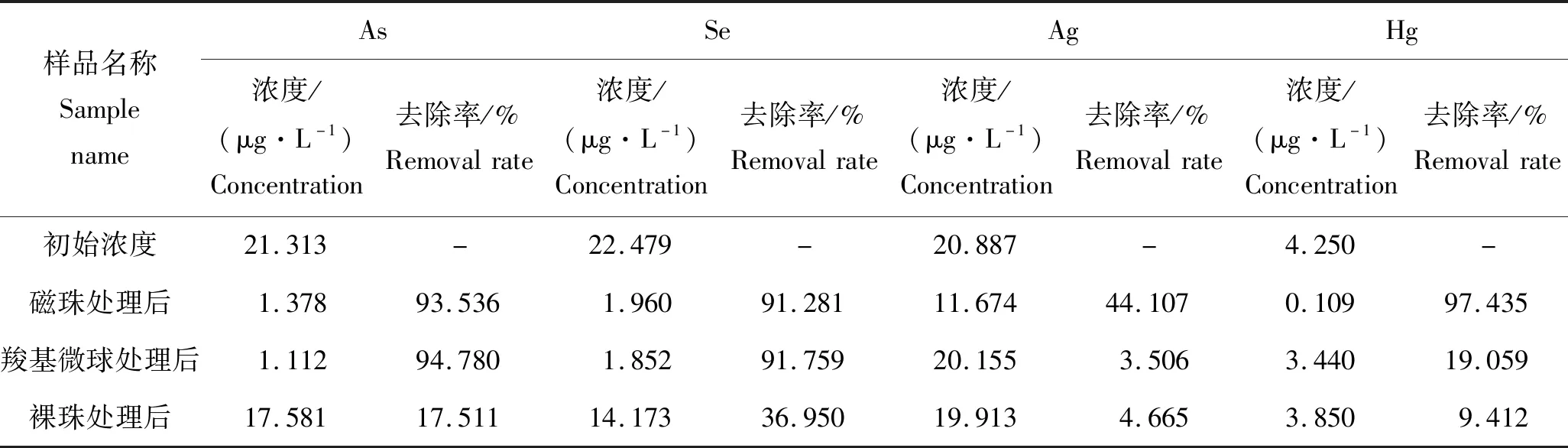
表4 不同材料对重金属的吸附效果影响Tab.4 The effects of different materials on the adsorption of heavy metals
3 结论
本实验制备了粒径大小分别为3.0、1.0和0.6 μm的3种磁性裸珠材料,通过在裸珠表面进行羧基修饰后偶联一定长度的胸腺嘧啶形成对溶液中汞具有一定吸附效果的新型磁珠材料,经过对磁珠粒径、磁珠用量以及不同汞浓度吸附去除效果的优化实验,发现粒径为1.0 μm的磁珠材料,在用量为5.0 μL/mL,处理汞浓度达10.0 μg/L的溶液时,对汞具有较好的吸附效果。
本实验研制的磁珠材料对水体中汞、砷、硒均有较好的吸附效果,其中汞元素主要通过与羧基微球上偶联的胸腺嘧啶稳定结合,砷、硒元素主要通过与羧基微球上的羧基稳定结合,由磁力架对此材料的吸附进而降低溶液中汞、砷、硒浓度。
