骨质疏松症对后入路腰椎椎体间融合术患者围手术期隐性失血的影响
2021-09-10李苏成傅栋铭李然周鸿猷茅於博杨惠林孟斌
李苏成 傅栋铭 李然 周鸿猷 茅於博 杨惠林 孟斌
骨质疏松症是目前被严重低估的疾病。由于其隐匿性,往往得不到充分诊断和治疗。骨质疏松症的特征是骨矿物质密度(bone mineral density,BMD)的减少,骨密度低于平均值2.5个标准差,以及骨代谢的失衡,骨折风险增加[1-2]。随着年龄的增长,除了骨质疏松症患病率的增加,老年患者往往伴有腰椎退行性病变的发生,如腰椎椎间盘突出症、腰椎椎管狭窄症、退行性腰椎滑脱症和退变性侧凸等[3]。经保守治疗无效后,临床上多采用后入路腰椎椎体间融合术(posterior lumbar interbody fusion,PLIF)治疗[4]。后入路腰椎椎体间融合术由于手术创伤较大,常伴有术中和术后的大量出血。虽然手术技术的优化和止血技术的发展,使得术中出血量大大减少,但是术后贫血仍是后入路腰椎椎体间融合术常见并发症之一,极大程度影响预后[5]。这往往是由于围手术期的隐性失血(hidden blood loss,HBL)造成的,有研究表明,患者性别、年龄、高血压、手术方式、手术时长等都对隐性失血量具有不同程度的影响[6-7]。然而,目前尚无报道骨质疏松症的严重程度对后入路腰椎椎体间融合术患者隐性失血的影响。本研究分析了后入路腰椎椎体间融合术患者隐性失血量,并探讨了骨质疏松症的程度对后入路腰椎椎体间融合术对患者围手术期失血量的影响。
资料与方法
一、资料
1.病例来源:2019年3月至2021年2月于苏州大学附属第一医院首次接受单节段后入路腰椎椎体间融合术治疗脊柱退行性病变女性患者的临床资料共213例。所有患者均由同一位手术医师完成。所有患者均借助骨密度测量仪进行腰椎骨密度测定。围手术期间均规范应用加速康复外科(enhanced recovery after surgery,ERAS)治疗理念。其中符合入选标准的患者共133例,年龄32~87(63.3±11.1)岁。骨密度正常组43例,骨密度T值为-0.126±0.637;骨量下降组44例,骨密度T值为-1.961±0.305;骨质疏松症组46例,骨密度T值为-3.583±0.868,各组骨密度之间差异有统计学意义(P<0.05)。所有女性患者的一般资料见表1。分析显示年龄在各组骨密度之间差异有统计学意义(P<0.05)。各组患者在身高、体重、BMI、手术时间和术前血糖等方面比较,差异无统计学意义。

表1 133例脊柱退行性病变女性患者3组基本情况对比
2.纳入与排除标准:(1)纳入标准:①女性患者;②保守治疗无效;③初次手术;④单节段后入路腰椎椎体间融合术患者;⑤病历资料完整。(2)排除标准:①男性患者;②多节段后入路腰椎椎体间融合术患者;③围手术期感染或严重凝血功能障碍、血液病患者;④合并有严重的内科疾病;⑤临床资料不完整者;⑥术后随访丢失。
二、方法
1.实验分组:所有患者骨密度评价指标参考WHO推荐骨质疏松诊断标准进行分组:T值((骨密度-骨峰值)/标准差):T值≥ -1.0为骨密度正常组;-2.5 2.数据收集:收集所有患者临床资料包括:年龄、身高、体重、身体质量指数((body mass index,BMI)、骨密度T值、术中出血量、手术时间、术前及术后第2天血红蛋白(hemoglobin,Hb)、红细胞压积(hematokrit,Hct)、术后引流量、围手术期输血量。 3.隐性失血量的计算:患者总血容量(patient blood volume,PBV)的计算:使用Nadler公式:PBV=K1×身高3(m)+K2×体重(kg)+K3。男性:K1=0.366 9,K2=0.032 19,K3=0.604 1;女性:K1=0.356 1,K2=0.033 08,K3=0.183 3[8]。 4.患者失血总量的计算:使用Gross方程:总失血量=PBV×(术前红细胞压积-术后红细胞压积)/平均红细胞压积×1000[9]。其中平均红细胞压积为术前红细胞压积和术后红细胞压积的平均值。 5.患者隐性失血量的计算方法:隐性失血量=失血总量-显性失血量+围手术期输血量[10]。其中显性失血量包括:术中失血量(吸引器吸引液体量-术中使用冲洗液量+纱布等术后称重增加的净重量)+术后伤口引流量-术中冲洗用水。 1.血液学指标:3组患者术前血浆白蛋白、术前红细胞压积和术前血红蛋白无统计学意义。骨密度对红细胞压积损失和血红蛋白损失的影响差异有统计学意义(P<0.05)。当患者骨密度T值越低,患者术后血液丢失度越严重(表2)。 表2 133例脊柱退行性病变女性患者3组血液学指标比较 2.骨密度T值、显性失血量、总失血量及隐性失血量:借助Nadler公式进一步分析患者的失血量,其中骨密度正常、骨量下降和骨质疏松症患者的隐性失血量差异有统计学意义(P<0.05)(表3)。 表3 3组患者骨密度T值、显性失血量、总失血量及隐性失血量比较 3.多元回归分析:多元回归分析显示,年龄、骨密度、手术时间、术前血红蛋白和术前红细胞压积对围手术期隐性失血量有统计学意义,是其独立危险因素(表4)。不同骨密度T值的隐性失血量,骨密度T值和隐性失血量呈负相关见图1。 表4 隐性失血相关因素的多元回归分析结果 图1 骨密度T值和隐性失血量的散点图 退行性节段椎体间融合术是一种有效的治疗手段,不仅可以稳定疼痛的病变节段,同时可对神经根进行减压,恢复腰椎前凸,达到矫正畸形的目的[11]。腰椎退变性疾病往往伴发骨质疏松症,尤其是绝经后女性,随着体内雌激素丢失,骨量丢失加快,腰椎退变程度也更为严重[12]。由于骨质疏松很少发生在皮质骨,因此椎板和关节突的骨密度相对较强,为椎弓根螺钉固定提供足够的应力[13]。故后入路腰椎椎体间融合术作为一种传统的腰椎入路成为大多数脊柱外科医生的首选[14]。 由于自体血回输及止血技术的发展,后入路腰椎椎体间融合术实际上术中失血量并不多,且术中与术后都会进行一定量的补液,故很多人认为术后贫血不会发生。可由于后入路腰椎椎体间融合术后血红蛋白指标仍会降低[5,15]。有研究证明,术后贫血将增加异基因输血率和术后感染率,显著降低身体的恢复功能,甚至引发其他严重心脑并发症的发生,最终导致病死[16]。术后贫血的频发,往往与忽略的隐性失血密切相关。隐性失血的概念首次由Sehat等[10]提出,主要指的是由于血液向间质组织外渗和溶血,最终导致血红蛋白水平降低。 随着患者进入老年期,各种因素导致骨小梁变薄、变细、断裂和吸收,数量减少,而骨小梁间的间隙增大[17];同时,骨皮质也将变薄,骨髓腔孔隙增多,严重时骨皮质薄如纸张,而松质骨消失殆尽,整个骨骼显得疏松、多大孔[18]。由于骨质疏松症主要发生在老年患者身上,老年人本身血管功能退化,更容易在应激状态下,血液供应失代偿,造成循环血量下降,进一步加重隐性失血[19]。这一点在本研究中也得到了证明,年龄是隐性失血的独立危险因素。 从手术本身考虑,由于后入路腰椎椎体间融合术在术中需切除椎板、小关节等骨性结构,同时对椎间盘、椎间盘上下终板进行彻底的刮除。这一系列手术操作势必将暴露大量的松质骨[20-21]。由于骨折后及进行手术时血管受损,血液将不断渗入松质骨,而骨质疏松症患者由于其松质骨稀疏,孔隙大且多,大量血液可由其渗透至周围组织[18]。 研究还显示手术时间延长是个独立的风险因素。本研究为减少误差,仅对单节段后入路腰椎椎体间融合术进行分析。但即使是处理单节段病变,每个患者的手术时间也不尽相同。若术中如遇到神经根粘连,硬膜破裂等复杂情况,手术时间都将延长。可以预见的是,多节段后入路腰椎椎体间融合术将花费更多的手术时间,造成更多的隐性失血量[22]。这就需要完善术前评估,对各种可以预见的情况提前进行处理,尽量减少手术时间,进而减少患者的围手术期隐性失血。 总之,当患有骨质疏松症患者进行后入路腰椎椎体间融合术时,应更加重视患者围手术期管理。年龄、骨密度、术前血红蛋白和术前红细胞压积是后入路腰椎椎体间融合术围手术期隐性失血的独立危险因素。对患有骨质疏松症的患者应及时进行围手术期血常规及术后引流的监测,预防术后贫血,加快患者术后康复。
结 果
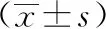


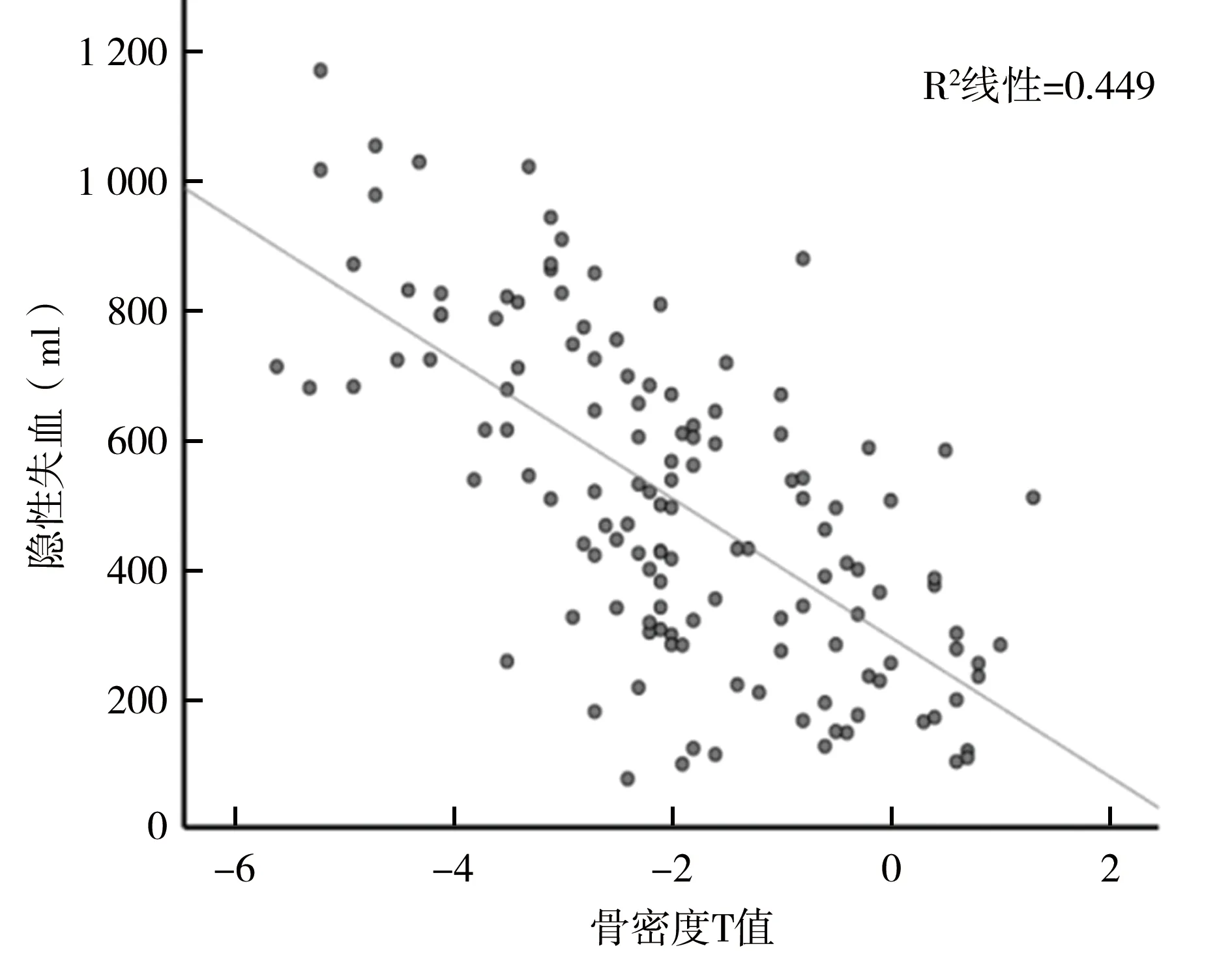
讨 论
